发烟硫酸中Ag2SO4催化瓦斯选择氧化制甲醇的影响因素及机理
朱丽华, 吴 扬, 徐 锋
(黑龙江科技大学 安全工程学院,哈尔滨 150022)
发烟硫酸中Ag2SO4催化瓦斯选择氧化制甲醇的影响因素及机理
朱丽华, 吴 扬, 徐 锋
(黑龙江科技大学 安全工程学院,哈尔滨 150022)
为考察反应温度、反应压力、反应时间和催化剂用量对瓦斯中甲烷转化率和甲醇选择性的影响,以Ag2SO4为催化剂,在质量分数20%的发烟硫酸中进行了低体积分数瓦斯选择氧化合成甲醇的实验,探讨发烟硫酸中低体积分数瓦斯选择氧化制甲醇的反应机理。实验结果表明:Ag2SO4催化低体积分数瓦斯选择氧化合成甲醇最优反应条件为反应温度180 ℃、反应压力4 MPa、反应时间2 h、Ag2SO4用量150 μmol。在此工艺条件下,瓦斯中甲烷的转化率为9.14%,甲醇的选择性为78.78%;低体积分数瓦斯中的甲烷在选择氧化反应中首先转化为硫酸单甲酯,进一步水解得到甲醇,反应遵循亲电取代机理。
瓦斯; 甲醇; Ag2SO4; 催化剂; 选择氧化; 发烟硫酸
0 引 言
煤矿瓦斯是一种与煤炭伴生的非常规天然气,其主要成分甲烷是优质的化工原料[1,2]。在当前安全生产形势严峻、石化资源日趋紧张的情况下,采用适当的技术手段将瓦斯,特别是低浓度瓦斯制成液态燃料甲醇十分必要[3]。1993年,Periana等[4]以浓硫酸为溶剂和氧化剂,HgSO4为催化剂,将甲烷转化为甲醇。该反应的中间产物为硫酸单甲酯,其水解后生成甲醇:1998年,Periana等[5]以发烟硫酸为溶剂,SO3为氧化剂,进行了由甲烷制甲醇的工作,并进一步提高了甲烷的转化率和甲醇的选择性。至此,人们对硫酸体系中甲烷低温转化制甲醇展开了广泛的研究,并取得了一系列进展[6-12]。以Pt(bpym)Cl2、Hg2SO4、Pd2SO4、碘化物等为催化剂,进行的甲烷液相转化研究获得了较大突破[5,13-16]。笔者借鉴上述研究,对低浓度瓦斯液相选择氧化制甲醇进行研究,考察发烟硫酸中Ag2SO4催化低浓度瓦斯选择氧化制甲醇的反应性能,探讨反应的催化机理,以期为低浓度瓦斯的化工利用提供借鉴。
1 实 验
1.1 试剂及装置
瓦斯气(φ(CH4)=25%,φ(O2)=5%,φ(N2)=70%)由哈尔滨市春霖气体经销有限公司配制;20%发烟硫酸(分析纯)由上海市外岗农场生产;Ag2SO4(分析纯)由天津市赢达稀贵化学试剂厂生产;NiSO4(分析纯)和CdSO4(分析纯)购自天津市致远化学试剂有限公司;ZrSO4(分析纯)和PbSO4(分析纯)分别由北京化学试剂厂和天津市光复精细化工研究所提供。
低体积分数瓦斯催化氧化反应在内衬四氟高压反应釜中进行,反应釜的有效体积为20 mL。
1.2 催化反应
向反应釜中按计量投入催化剂和发烟硫酸,封釜。反应釜经3次吹扫后,向其中充瓦斯气至相应实验压力,达到设定温度后搅拌,开始反应,到达设定的反应时间后自动停止加热和搅拌,反应结束。取出釜体冷却,取气样进行色谱分析;移出液样,加20倍体积的水于90 ℃下水解3 h,待冷却后,取水解样进行色谱分析。
1.3 产物分析方法
利用GC9790Ⅱ型气相色谱仪(浙江福立分析仪器有限公司)对气样进行分析。反应前后CH4及产物CO、CO2的含量由FID检测器检测;反应前后O2和N2的含量由TCD检测器检测;利用GC9790型气相色谱仪(浙江福立分析仪器有限公司)分析液体产物水解样。利用外标法定量各反应产物的含量,CH4转化率及主要产物的选择性经碳平衡后计算得到,公式如下:
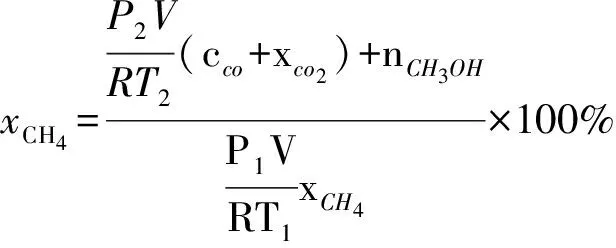

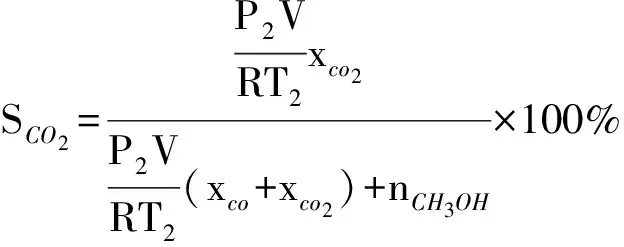
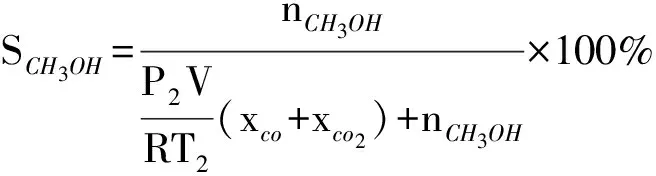
式中:p1——反应前气相压力,Pa;
p2——反应后气相压力,Pa;
V——釜内气相体积,m3;
T1——反应前温度,K;
T2——反应后温度,K;
R——气体常数,J·mol-1·K-1;
xCH4——反应气中CH4的摩尔分数;
xCO、xCO2——反应后气体中CO、CO2的摩尔分数;
nCH3OH——生产的CH3OH的量,mol。
2 结果与讨论
2.1 催化剂的选定
在发烟硫酸溶液中,对比了几种硫酸盐化合物对低体积分数瓦斯部分氧化的催化性能,结果如表1所示,其反应条件:p=3MPa,T=180 ℃,t=2h,Stirringrate300r/min。
由表1可看出,NiSO4、CdSO4和ZrSO4对低浓度瓦斯中的甲烷部分氧化反应均没有催化活性,而PbSO4和Ag2SO4有活性,但Ag2SO4的催化活性较PbSO4高,这可能是在硫酸体系中Ag2SO4的溶解度高于PbSO4的原因所致。由实验结果可知,低浓度瓦斯中氧含量在反应前后未变化,这说明氧气未参与甲烷的部分氧化反应。依据CH4在发烟硫酸体系中的研究,低体积分数瓦斯部分氧化中的氧化剂应该为SO3。

表1 硫酸盐化合物活化低浓度瓦斯的活性
2.2 反应温度对瓦斯催化氧化反应的影响
在Ag2SO4添加100 μmol、速率搅拌300 r/min、压力3 MPa、反应2 h的条件下,分析了瓦斯催化氧化反应中反应温度的影响,结果见图1。该实验的主要产物是硫酸单甲酯(水解后得甲醇)、CO和CO2。
从图1可以看出,在140 ℃的反应温度下,未发生瓦斯催化氧化反应。而当反应温度升高至160 ℃以上,瓦斯催化氧化反应开始发生,并且瓦斯中CH4的转化率随着反应温度的升高而增大。说明反应温度是瓦斯催化氧化反应的重要影响因素。在反应温度由160 ℃升高至200 ℃的过程中,CO的选择性变化不大,CO2的选择性略微增大,而甲醇的选择性逐渐减小。此结果说明高温在促进CH4活化的同时,也加快了它向CO2的过度氧化反应,使甲醇选择性降低。综合瓦斯中甲烷的转化率和甲醇的选择性,认为180 ℃是该反应的适宜温度。
2.3 催化剂用量对瓦斯催化氧化反应的影响
在压力3 MPa、反应温度180 ℃、搅拌速率300 r/min、反应2 h的条件下,分析了瓦斯催化氧化反应中催化剂用量的影响,结果见图2。图2显示,甲烷转化率随着Ag2SO4添加量的增加而逐渐增大,但当添加量超过150 μmol时,CH4转化率增大幅度放缓。Ag2SO4添加量对CO选择性的影响不显著。随着Ag2SO4添加量的增加,CO2选择性总体呈现减弱的趋势,而甲醇的选择性呈略微增大的趋势,说明Ag2SO4对目标产物甲醇的生成具有促进作用。

图2 催化剂用量对瓦斯催化氧化反应的影响
2.4 反应时间对瓦斯催化氧化反应的影响
在压力3 MPa、反应温度180 ℃,Ag2SO4添加量150 μmol、搅拌速率300 r/min的条件下,分析了瓦斯催化氧化反应中反应时间的影响,结果见图3。从图3中可以看出,CH4转化率、CO和CO2选择性随着反应时间的增加而逐渐增大,甲醇选择性随着反应时间的增加而逐渐减小。当反应时间超过2 h以后,CH4转化率增加放缓。这说明反应时间达2 h时,瓦斯催化氧化反应已基本停止。再延长反应时间,会加剧甲醇的继续氧化反应。
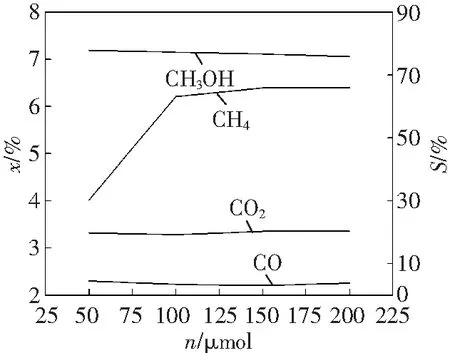
图3 反应时间对瓦斯催化氧化反应的影响
2.5 反应压力对瓦斯催化氧化反应的影响
在反应温度180 ℃、Ag2SO4添加量150 μmol、搅拌速率300 r/min、反应2 h的条件下,分析了瓦斯催化氧化反应中反应压力的影响。由图4可知,CO和CO2的选择性随着反应压力的升高逐渐减小,而甲醇的选择性和瓦斯中CH4的转化率随着反应压力的升高逐渐增大,在4 MPa时甲醇选择性达最大值78.78%。此后,甲醇选择性和CH4转化率增大速率都有所放缓。因为CH4催化氧化反应是在液相中进行,反应压力会影响液相中气相反应物的浓度以及气液相传质。反应压力升高,气相反应物向液相传递的动力得到增加,从而使得气相反应物在液相中的溶解度也增加,所以增加了瓦斯中CH4分子与Ag2SO4催化剂接触的机会,最终促进了催化反应的进行,当压力增大到一定数值时,溶解在发烟硫酸中的瓦斯达到饱和,之后再增大压力,CH4转化率提升不显著。
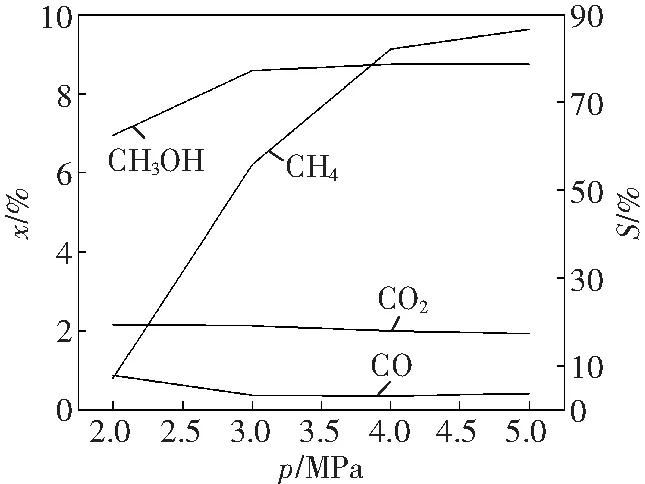
图4 反应压力对瓦斯催化氧化反应的影响
2.6 反应机理分析
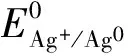
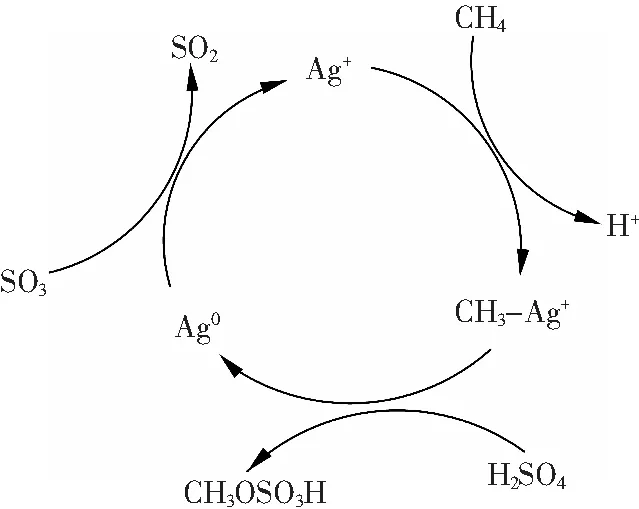
图5 发烟硫酸中Ag2SO4催化瓦斯选择氧化合成甲醇的机理
3 结束语
以Ag2SO4为催化剂,在发烟硫酸中进行了低浓度瓦斯选择氧化制甲醇的实验研究,发现对于该实验体系,反应温度180 ℃、Ag2SO4用量150 μmol、反应时间2 h、初始压力4 MPa是较适宜的反应条件。该条件下,瓦斯中甲烷的转化率为9.14%,甲醇的选择性为78.78%。发烟硫酸中Ag2SO4催化瓦斯选择氧化合成甲醇的机理为亲电取代反应机理。
[1] 徐 锋, 李 创, 朱丽华. 低温等离子体促进煤层甲烷活化转化[J]. 黑龙江科技大学学报, 2015, 25(6): 1-5.
[2] XU FENG,ZHU LIHUA. Synthesis of methanol from oxygen-containing coalbed methane and environmental benefit analysis[J]. Disa Adv, 2010, 3(4): 407-410.
[3] 朱丽华, 徐 锋. 瓦斯低温等离子体转化制甲醇的可行性分析[J]. 黑龙江科技学院学报, 2012, 22(2): 119-122.
[4] PERIANA R A, TAUBE D J, EVITT E R, et al. A mercury-catalyzed, high-yield system for the oxidation of methane to methanol[J].Science, 1993, 259(3): 340-343.
[5] PERIANA R A, TAUBE D J, GAMBLE S, et al. Platinum catalysts for the high-yield oxidation of methane to a methanol derivative[J]. Science, 1998, 280(3): 560-564.
[6] BJERRUM N J, XIAO G, HJULER A A. Process for the catalytic oxidation of hydrocarbons[P]. Danmark, WO, 1999: 5-20.
[7] 肖勇山, 陆润侠, 唐呈前, 等. 甲烷液相部分氧化制甲醇中溶剂介质的研究进展[J]. 化工进展, 2014, 33(10): 2598-2607.[8] 王维勋, 陈立宇, 徐 强, 等. 甲烷液相部分氧化制甲醇的研究进展[J]. 石油化工, 2014, 43(9): 1091-1097.
[9] BAO Z H, YANG Y, XU Y Y XU, et al. A review of the directoxidation of methane to methanol[J]. Chinese Journal of Catalysis, 2016, 37(8) : 1206-1215.
[10] 魏 新, 叶林敏, 祝明霞, 等. 发烟硫酸中Pd/C催化甲烷选择氧化制甲醇[J]. 催化学报, 2008, 29(8): 720-726.
[11] 徐 锋, 吴 扬, 朱丽华. Pd(bipy)Cl2催化瓦斯液相选择氧化制甲醇工艺[J]. 黑龙江科技大学学报, 2016, 26(4): 391-395.[12] 刘志林, 王维勋, 唐 城, 等. 低浓度煤层气在发烟硫酸中液相部分氧化的催化剂研究[J]. 燃料化学学报, 2012, 40(7): 838-842.
[13] PERIANA R A, MIRONOV O, TAUBE D J. Catalytic, oxidative condensation of CH4to CH3COOH in one step via CH activation[J]. Science, 2003, 301(4): 814-818.
[14] XIAO G, ZHU Y M, BIRCH H N. Iodine as catalyst for the direct oxidation of methane to methyl sulfates in oleum[J]. Appl
Catal:A, 2004, 261(1): 91-98.
[15] MICHALKIEWICZ B, KALUCKI K, SOSNICKI J G. Catalytic system containing metallic palladium in the process of methane partial oxidation[J]. J Catal, 2003, 215(1): 14-19.
[16] 陈立宇, 杨伯伦, 张秀成, 等. 甲烷液相部分氧化合成甲醇过程研究[J]. 高校化学工程学报, 2005, 19(1): 54-58.
[17] SHILOV A E, SHUL'PIN G B. Activation of C-H bonds by metal complexes [J]. Chem Rev, 1997, 97(8): 2879-2932.
[18] SEN A, BENVENTO M A, LIN M, et al. Activation of methane and ethane and their selective oxidation to the alcohols in protic media[J]. J Am Chem Soc, 1994, 116(3): 998-1003.
(编校 李德根)
Influencing factors and reaction mechanism for selective oxidation of coal mine gas to methanol in oleum over Ag2SO4catalyst
ZhuLihua,WuYang,XuFeng
(School of Safety Engineering, Heilongjiang University of Science & Technology, Harbin 150022, China)
This paper is devoted to exploring the effects of reaction temperature, reaction pressure, reaction time and catalyst dosage on the conversion of methane in gas and the yield of methanol. The exploration is achieved by carrying out selective oxidation of low-concentration coal mine gas to methanol in a concentration of 20% oleum using Ag2SO4catalyst; and investigating the reaction mechanism underlying the selective oxidation of low-concentration coal mine gas. The results demonstrate that the optimal reaction conditions determined for selective oxidation of low-concentration coal mine gas to methanol by Ag2SO4catalyst in oleum are the reaction temperature of 180 ℃, the reaction pressure of 4 MPa, the reaction time of 2 h, and the Ag2SO4dosage of 150 μmol; this technological condition affords the conversion ratio of methane in gas of 9.14% and the methanol selectivity of 78.78%;and the methane in low concentration gas starts by being transformed into methyl bisulfate which is then hydrolyzed into methanol, suggesting that the selective oxidation of low-concentration coal mine gas follows the mechanism behind electrophilic substitution.
coal mine gas; methanol; Ag2SO4; catalyst; selective oxidation; oleum
2016-10-16
国家自然科学基金项目(51374098);黑龙江省博士后科研启动基金项目(LBH-Q14143)
朱丽华(1979-),女,辽宁省沈阳人,讲师,硕士,研究方向:瓦斯转化及利用,E-mail:zhulihua79@163.com。
10.3969/j.issn.2095-7262.2016.06.009
TQ223.121; O643.32
2095-7262(2016)06-0631-04
:A

