三种呼吸系统兽药制剂中非法添加盐酸溴己新、吲哚美辛的HPLC-PDA检测方法的建立
王静文,龚旭昊,范强,万仁玲
(中国兽医药品监察所,北京 100081)
三种呼吸系统兽药制剂中非法添加盐酸溴己新、吲哚美辛的HPLC-PDA检测方法的建立
王静文,龚旭昊,范强*,万仁玲
(中国兽医药品监察所,北京 100081)
为检测麻杏石甘散、氟苯尼考注射液中非法添加的盐酸溴己新,甘草颗粒中非法添加的吲哚美辛,以十八烷基键合硅胶为填充剂,磷酸盐缓冲液-乙腈(20∶80)为流动相检测盐酸溴己新,以乙腈-0.1mol/L冰醋酸溶液(50∶50)为流动相检测吲哚美辛,流速为1.0 mL/min,波长扫描范围为200~400 nm,建立了相应的HPLC-PAD检测方法,并采用峰纯度检查和光谱相似度检查辅助对照品比对方法,对非法添加药物进行确证。结果显示,麻杏石甘散和氟苯尼考注射液中盐酸溴己新的回收率分别为94.8%和98.5%,甘草颗粒中吲哚美辛回收率为95.2%;盐酸溴己新线性方程为y=14780200x-16476,R=0.9999,吲哚美辛线性方程为y=10995430x+13033,R=0.9999;麻杏石甘散中盐酸溴己新检测限为83 mg/kg,氟苯尼考注射液中盐酸溴己新检测限为1.6 g/L,甘草颗粒中吲哚美辛检测限为1 g/kg。
盐酸溴己新;吲哚美辛;麻杏石甘散;氟苯尼考注射液;甘草颗粒
麻杏石甘散由麻黄、杏仁、石膏、甘草四味中药组成,具有清热,宣肺,平喘的功效,主治由细菌、病毒、支原体引起的畜禽呼吸道疾病[1]。甘草颗粒为甘草浸膏经加工制成的颗粒。具有祛痰止咳的功效,主治咳嗽[2]。氟苯尼考为酰胺醇类抗生素,用于治疗猪、鸡敏感菌所致的感染[3]。三种制剂均为《中国兽药典》2010年版收载,为兽药临床治疗呼吸系统疾病的常用药。盐酸溴己新为祛痰药,可直接作用于支气管腺体,促使粘液分泌细胞的溶酶体酶释出,裂解粘液中的粘多糖,使痰的粘稠度降低[4],吲哚美辛为非甾体解热镇痛药,通过抑制机体内前列腺素的合成而产生解热镇痛抗炎作用[5]。由于缺乏残留检测试验数据,为避免增加动物性食品中药物残留危害,农业部公告第560号于2005年废止了二者兽药地方标准。然而在进行兽药监督抽检工作中发现有在麻杏石甘散、氟苯尼考注射液中添加盐酸溴己新,在甘草颗粒中添加吲哚美辛的情况。目前尚未有针对上述制剂建立的盐酸溴己新、吲哚美辛HPLC-PDA非添检测方法,参考相关文献[6-13]并结合兽药中非法添加检测工作特点[14-15],建立了简便、快捷、可靠的检测方法。
1 仪器与材料
1.1 仪器 Waters e2695液相系统、2998 PDA二极管阵列检测器、Empower3色谱工作站软件(美国Waters 公司)、Mettler XS205型十万分之一天平(美国Mettler Toledo公司)、MiliQ纯水机、雷磁PHSJ-4A型pH 计。
1.2 试药与试剂 盐酸溴己新对照品(含量:99.9%,批号:100427-201102,中国食品药品检定研究院),吲哚美辛对照品(含量:99.9%,批号:100258-200904,中国食品药品检定研究院)供试品:麻杏石甘散空白样品(来源:实验室自制),麻杏石甘散阳性样品(批号:20140601),氟苯尼考注射液空白样品(批号:20140501),氟苯尼考注射液阳性样品(批号:14110501)甘草颗粒空白样品(批号:20160501)甘草颗粒阳性样品(批号:201601101)。乙腈(Merck,色谱纯,批号:1747130433),甲醇(Merck,色谱纯,批号:1748007433),磷酸二氢钾(Johnson Matthey,分析纯,批号:F21S033),氢氧化钠(国药集团化学试剂有限公司,分析纯,20150104),冰醋酸(国药集团化学试剂有限公司,分析纯,20140923),去离子水(MiliQ纯化系统制备的去离子水)。
2 方法与结果
2.1 色谱条件
2.1.1 盐酸溴己新色谱条件 色谱柱:资生堂 MG C18(4.6 mm×150 mm,5 μm),流动相:磷酸盐缓冲液(取磷酸二氢钾1.0 g,加900 mL水使溶解,用0.5 mol/L氢氧化钠溶液调节pH值至7.0,用水稀释至1000 mL,摇匀,即得)-乙腈(20∶80),流速:1.0 mL/min,柱温:40℃,进样量:10 μL,二极管阵列检测器(PDA,检测波长:200~400 nm,记录249 nm波长处的色谱图)。2.1.2 吲哚美辛色谱条件 色谱柱:资生堂MG C18(4.6 mm×250 mm,5 μm),流动相:乙腈-0.1 mol/L冰醋酸溶液(50∶50),流速:1.0 mL/min,柱温:25℃,进样量:10 μL,二极管阵列检测器(PDA,检测波长:200~400 nm,记录317 nm波长处的色谱图)。
2.2 溶液制备
2.2.1 麻杏石甘散样品溶液制备 取麻杏石甘散(空白样品为实验室自制)12.0 g,置具塞锥形瓶中,加甲醇200 mL,超声处理15 min,静置,滤过。
2.2.2 氟苯尼考注射液样品溶液制备 取氟苯尼考注射液(空白样品为已测得不含盐酸溴己新的氟苯尼考注射液)1.0 mL,置刻度管中,加甲醇稀释至10 mL,摇匀,滤过。
2.2.3 甘草颗粒样品溶液制备 取甘草颗粒(空白样品为已测得不含吲哚美辛的甘草颗粒)1.0 g,置具塞锥形瓶中,加甲醇100 mL,超声处理15 min,静置,滤过,取滤液5 mL置刻度管中,加甲醇至10 mL,摇匀,滤过。
2.2.4 盐酸溴己新对照品储备液 取盐酸溴己新对照品25 mg,精密称定,置25 mL量瓶中,加甲醇溶解并稀释至刻度,摇匀,置4 ℃冰箱保存。
2.2.5 吲哚美辛对照品储备液 取吲哚美辛对照品25 mg,精密称定,置25 mL量瓶中,加甲醇溶解并稀释至刻度,摇匀,置4 ℃冰箱保存。
2.3 方法学考察
2.3.1 专属性 通过麻杏石甘散空白试验、氟苯尼考注射液空白试验和甘草颗粒空白试验排除各制剂处方中主要成分对于被测物的干扰。精密量取盐酸溴己新对照品溶液(0.1 mg/mL)、麻杏石甘散空白溶液和氟苯尼考注射液空白溶液各10 μL,照2.1.1色谱条件,注入高效液相色谱仪,记录色谱图和光谱指数图,结果表明麻杏石甘散、氟苯尼考本底在盐酸溴己新出峰处无干扰(图1-图3)。精密量取吲哚美辛对照品溶液(0.1 mg/mL)、甘草颗粒空白溶液各10 μL,照2.1.2色谱条件,注入高效液相色谱仪,记录色谱图和光谱指数图,结果表明甘草颗粒本底在吲哚美辛出峰处无干扰(图4-图5)。
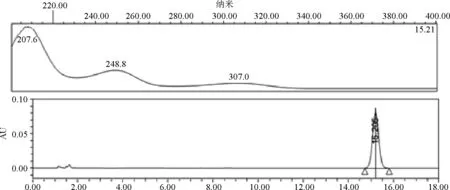
图1 盐酸溴己新对照品(0.1 mg/mL)光谱色谱图
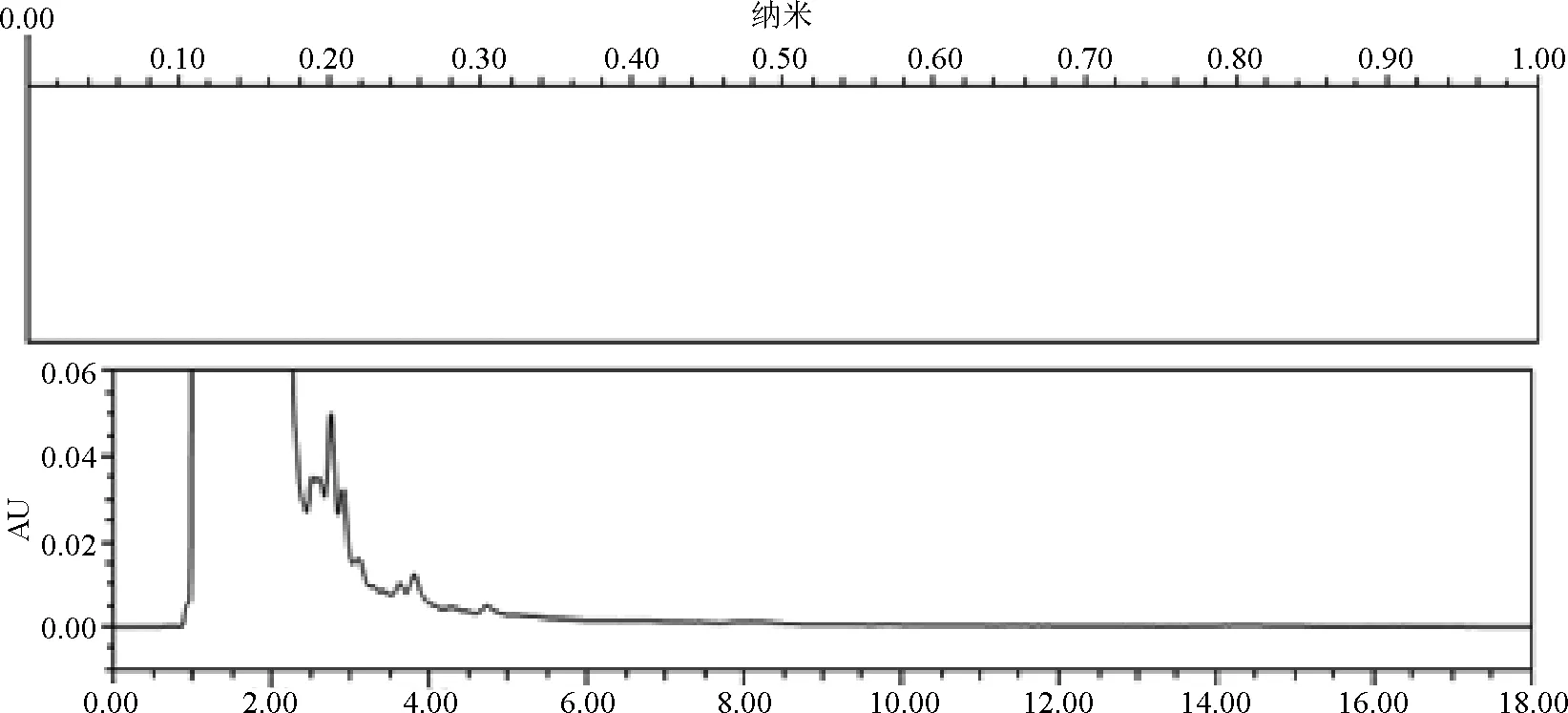
图2 麻杏石甘散空白溶液光谱色谱图
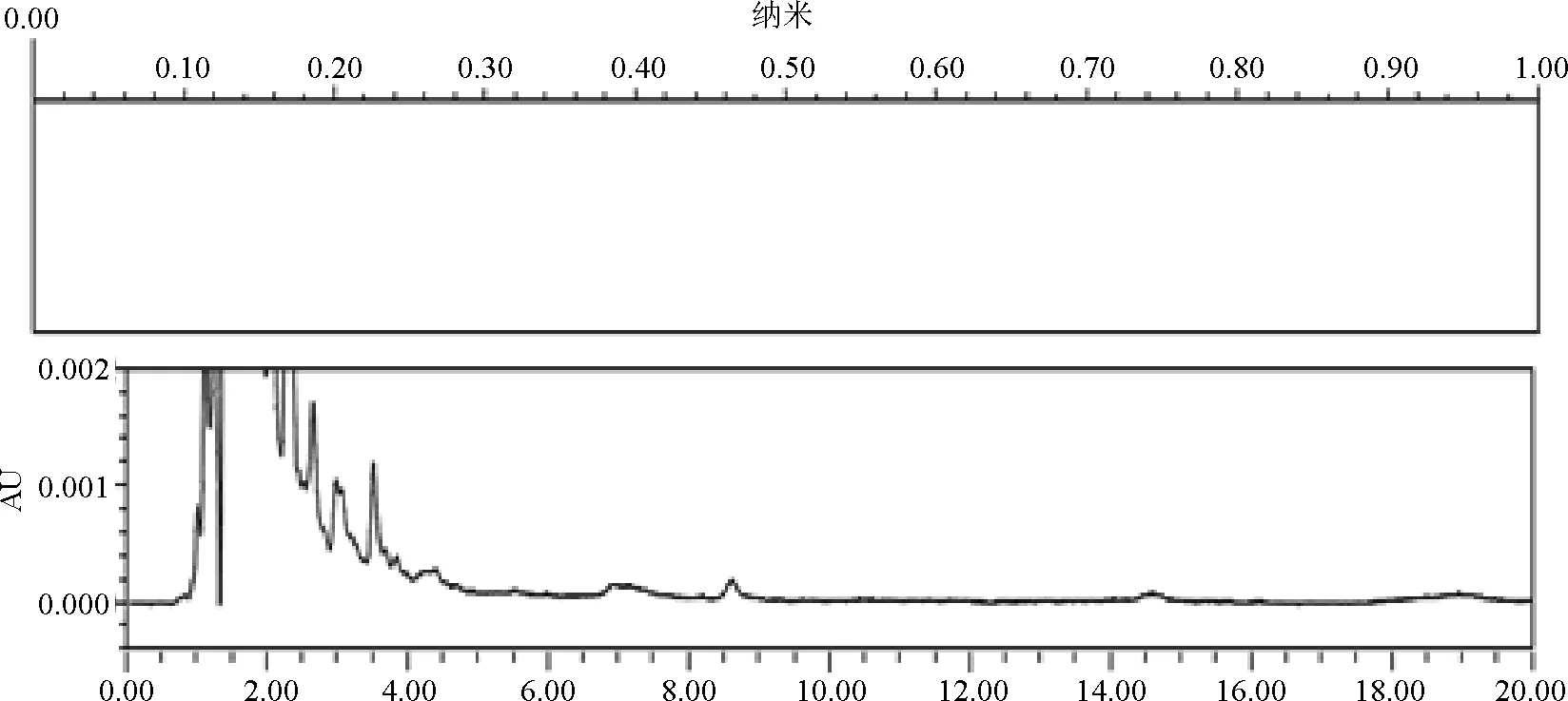
图3 氟苯尼考注射液空白溶液光谱色谱图
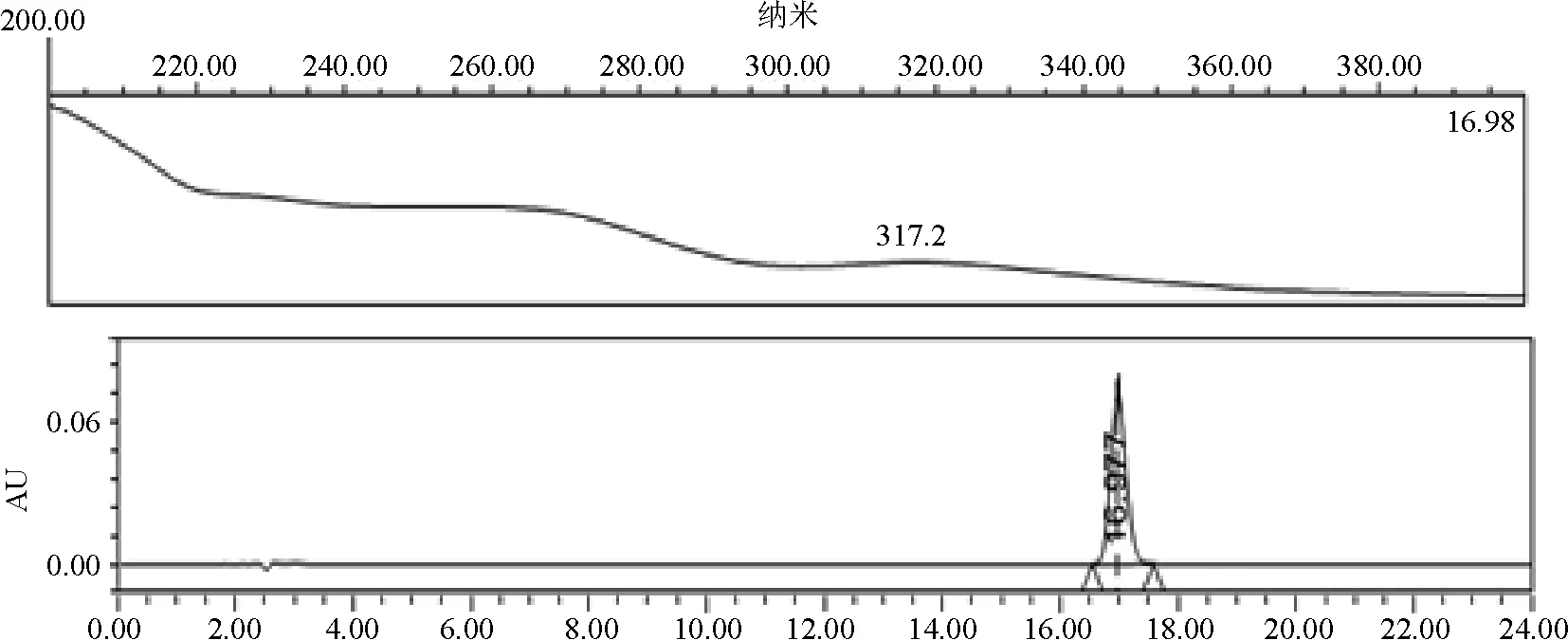
图4 吲哚美辛对照品(0.1 mg/mL)光谱色谱图
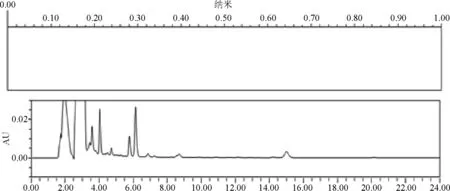
图5 甘草颗粒空白溶液光谱色谱图
2.3.2 线性 精密量取盐酸溴己新对照品储备液(1.0 mg/mL)1、3、5、7、9 mL置25 mL容量瓶中,加甲醇稀释至刻度,摇匀,得浓度为0.04、0.12、0.20、0.28、0.36 mg/mL的标准曲线溶液,照2.1.1色谱条件测定。按盐酸溴己新峰面积与对应的浓度作标准曲线,并计算回归方程和相关系数。盐酸溴己新回归方程为y=104780200x-16476,R=0.9999。表明盐酸溴己新在0.04~0.36 mg/mL浓度范围内,峰面积与浓度呈良好的线性关系;精密量取吲哚美辛对照品储备液(1.0 mg/mL)1、2、4、6、8 mL置25 mL容量瓶中,加甲醇稀释至刻度,摇匀,得浓度为0.04、0.08、0.16、0.24、0.32 mg/mL的标准曲线溶液,照2.1.2色谱条件测定。按吲哚美辛峰面积与对应的浓度作标准曲线,并计算回归方程和相关系数。吲哚美辛回归方程为y=10995430x+13033,R=0.9999。表明吲哚美辛在0.04~0.32 mg/mL浓度范围内,峰面积与浓度呈良好的线性关系。
2.3.3 检测限 所建方法以光谱图失真的最大浓度作为方法的检测限,并保证检测限浓度下样品与对照品溶液的保留时间一致(差异小于等于±5%),最大吸收波长一致(差异小于等于±2 nm),色谱峰的纯度角度小于纯度阈值,PDA匹配角度小于PDA匹配阈值。取麻杏石甘散空白样品12 g三份,置刻度管中,分别加入盐酸溴己新对照品溶液(1 mg/mL)适量(0.5、1.0、1.5 mL),加甲醇至200 mL,超声处理15min,静置,滤过;取氟苯尼考注射液空白样品1.0 mL三份,置刻度管中,分别加入盐酸溴己新对照品溶液(1.6 μg/mL)适量(0.5、1.0、1.5 mL),加甲醇至10 mL,摇匀,滤过。精密吸取上述检测限样品溶液各10 μL,注入液相色谱仪,照2.1.1色谱条件测定检测限,结果表明中间加入量为盐酸溴己新的检测限,该色谱条件下盐酸溴己新在麻杏石甘散样品和氟苯尼考注射液样品中的检出限分别为83 mg/kg和1.6 g/L。取甘草颗粒空白制剂1.0 g三份,置具塞锥形瓶中,分别加入吲哚美辛对照品溶液(1 mg/mL)适量(0.5、1.0、1.5 mL),加甲醇100 mL,超声处理15 min,静置,滤过,取滤液5 mL置刻度管中,加甲醇至10 mL,摇匀,滤过,精密吸取上述检测限样品溶液10 μL,照2.1.2色谱条件注入液相色谱仪,结果表明中间加入量为吲哚美辛的检测限,该色谱条件下吲哚美辛在甘草颗粒中的检出限为1.0 g/kg。检出限浓度下各化合物的纯度与光谱相似度结果见表1。
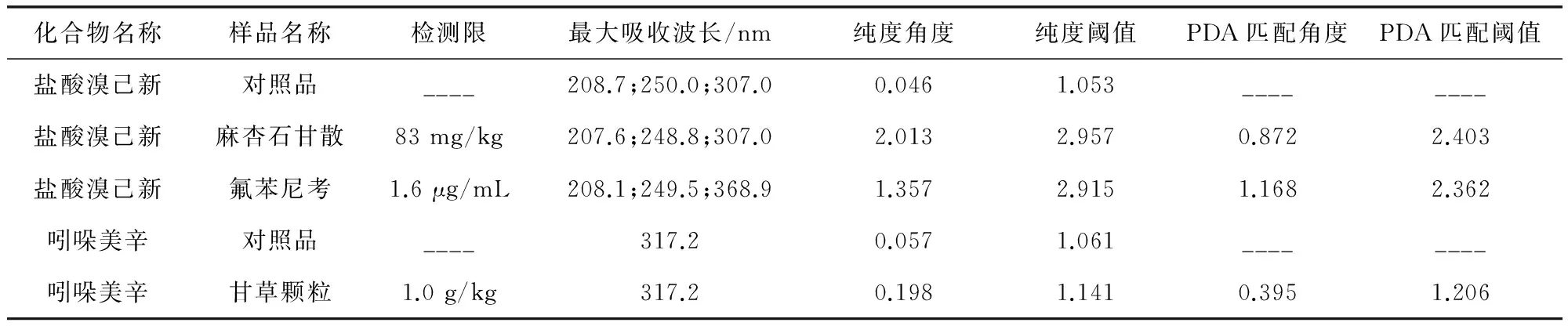
表1 检测限试验溶液峰纯度与光谱相似度结果表
2.3.4 准确度 以三种制剂的空白样品分别加盐酸溴己新、吲哚美辛对照品做回收率试验来考察方法的准确度。回收率试验溶液配制:精密称取麻杏石甘散空白样品12 g、盐酸溴己新对照品10 mg,置同一200 mL量瓶中,加入150 mL甲醇,超声处理15 min,静置,放冷后,用甲醇稀释至刻度,滤过;精密量取氟苯尼考空白样品1.0 mL、盐酸溴己新对照品溶液(16 μg/mL)1.0 mL,置同一10 mL量瓶中,加甲醇稀释至刻度,摇匀,滤过,平行配制上述试验溶液各6份。精密吸取上述试验溶液各10 μL,注入液相色谱仪,参照2.1.1色谱条件检测。精密称取甘草颗粒空白样品1.0 g、吲哚美辛对照品10 mg,置同一100 mL量瓶中,加入60 mL甲醇,超声处理15 min,静置,放冷后,用甲醇稀释至刻度,摇匀,精密量取5 mL置100 mL量瓶中,加甲醇稀释至刻度,摇匀,滤过,平行配制上述试验溶液6份。精密吸取上述试验溶液各10 μL,注入液相色谱仪,参照2.1.2色谱条件检测。结果显示:麻杏石甘散中盐酸溴己新回收率为94.8%,RSD为0.6%;氟苯尼考中盐酸溴己新回收率为98.5%,RSD为0.2%;甘草颗粒中吲哚美辛回收率为95.2%,RSD为0.4%。
2.3.5 耐用性 以各制剂的回收率试验溶液作为耐用性试验溶液。从柱温、流动相pH值、色谱柱三个方面考察盐酸溴己新检测方法的耐用性。调节柱温为30 ℃、35 ℃、40 ℃,结果表明:随着柱温升高,盐酸溴己新保留时间提前,时间相差近4 min;调节流动相pH值为6.0、7.0和8.0,结果表明:在所调节范围内,盐酸溴己新的保留时间差别不大;选择三款不同品牌色谱柱(资生堂 MG,150 mm×4.6 mm,5 μm;Waters Atlantis T3,250 mm×4.6 mm,5 μm;GRACE Alltima C18,250 mm×4.6 mm,5 μm),考察不同色谱柱对检测的影响,在所建检测方法条件下,三种品牌色谱柱所得色谱峰的理论塔板数、对称因子均符合规定,T3柱中,保留时间在28 min左右,资生堂 MG中,保留时间为15 min左右,本方法中,为节约分析时间,提高工作效率,建议使用短色谱柱。从柱温、色谱柱两个方面考察吲哚美辛检测方法的耐用性,调节调节柱温为25 ℃、30 ℃、35 ℃,结果显示:随着柱温升高,吲哚美辛保留时间略提前;选择三款不同品牌色谱柱(资生堂 MG,150 mm×4.6 mm,5 μm;资生堂®C18 4.6 mm×250 mm,5 μm;GRACE Alltima C18,250×4.6 mm,5 μm),考察不同色谱柱对检测的影响,在所建检测方法条件下,三种品牌色谱柱所得色谱峰的理论塔板数、对称因子均符合规定,方法耐用性良好。
2.4 样品测定结果 取麻杏石甘散阳性样品照2.2.1制备方法操作,氟苯尼考注射液阳性样品照2.2.2制备方法操作,照2.1.1色谱条件测定盐酸溴己新含量,结果为:麻杏石甘散中盐酸溴己新含量为0.43 g/kg,氟苯尼考注射液中盐酸溴己新的含量为6.36 g/L。取甘草颗粒阳性样品照2.2.3制备方法操作,照2.1.2色谱条件测定吲哚美辛含量,结果为:甘草颗粒中的吲哚美辛含量为17 g/kg。阳性样品检测结果见表2。
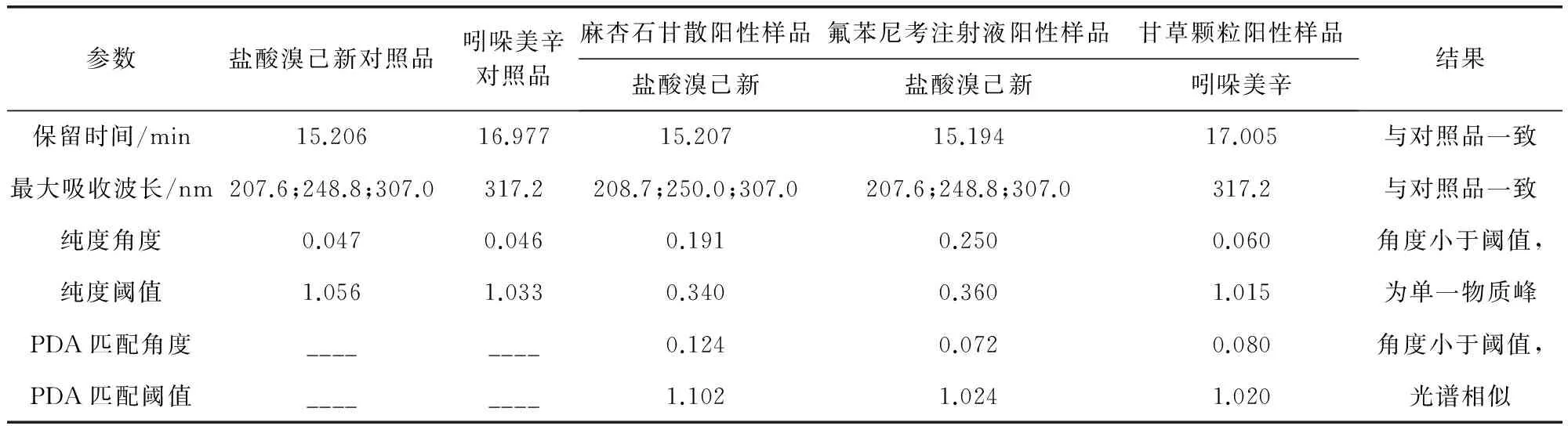
表2 阳性样品检测结果
3 讨 论
3.1 流动相的选择 试验中曾考察过0.1%磷酸-甲醇(30∶70)、0.12%磷酸二氢铵-乙腈(80∶20)、醋酸溶液(取冰醋酸50 mL加水930 mL,用三乙胺调节pH值至3.4)-甲醇(30∶70)[8-10]等不同的盐酸溴己新流动相系统,结果磷酸盐缓冲液(取磷酸二氢钾1.0 g,加900 mL水使溶解,用0.5 mol/L氢氧化钠溶液调节pH值至7.0,用水稀释至1000 mL)-乙腈(20∶80)为流动相时,盐酸溴己新的峰形好,麻杏石甘散和氟苯尼考本底中的化合物也不干扰测定。同时考察乙腈-0.1 mol/L冰醋酸(55∶45)、甲醇-0.5%磷酸(60∶40)、0.1 mol/L冰醋酸溶液-甲醇(20∶80)[11-13]等不同的吲哚美辛流动相系统,结果乙腈-0.1 mol/L冰醋酸溶液(50∶50)为流动相时,吲哚美辛的峰形好,甘草颗粒本底中的化合物不干扰测定。
3.2 测定用溶剂的选择 通过对盐酸溴己新和吲哚美辛在甲醇中的溶解性考察,发现在本方法浓度范围内,盐酸溴己新在甲醇中的溶解性良好。考虑到在非法添加高通量筛查工作中以甲醇作为溶剂具有普适性,结合优化的流动相种类、比例、柱温等色谱条件可以排除制剂中其他共提物的干扰,故选取甲醇作为检测用溶剂。
3.3 提取波长的选择 盐酸溴己新对照品在200~400 nm波长范围最大吸收波长为207.6、248.8、307.0 nm,麻杏石甘散中甘草酸铵、盐酸麻黄碱、盐酸伪麻黄碱等主要组份以及氟苯尼考在上述波长下对盐酸溴己新的检测均无干扰,故选取吸收系数最大的249 nm作为检测波长;吲哚美辛对照品在200~400 nm波长范围最大吸收波长为317.2 nm,甘草颗粒中甘草酸铵等组份在此波长下对检测无干扰,故选取317 nm作为检测波长。3.4 峰纯度和光谱相似度 峰纯度检查可以作为判断色谱峰是否为单一物质峰的重要依据,光谱相似度检查可以排除保留时间一致,但紫外光谱不同的化合物干扰,通过与对照品建立的标准物质谱库比较,Waters Empower工作站可以对峰纯度和光谱匹配度进行计算,当纯度角度小于纯度阈值时,可以判定为单一物质峰,当匹配角度小于匹配阈值时,可以判定光谱相似。在本文所建方法进行的各项检测中,都保证了目标峰的纯度角度小于纯度阈值,保证了目标峰与盐酸溴己新或吲哚美辛对照品光谱库比较时,PDA匹配角度小于PDA匹配阈值。
4 结 论
已发布的农业部公告中,呼吸系统用药中常见的非法添加物有烟酰胺、氨茶碱、甲氧氯普胺等[16-17],本文旨在对呼吸系统用药中新发现的盐酸溴己新和吲哚美辛两种非法添加药物建立检测方法,为以后的未知物监测提供信息。试验所建立的方法中各制剂的共提物组分对检测均无干扰,通过与对照品色谱峰的保留时间、最大吸收波长进行比对,以及峰纯度检测和光谱相似度检查来判定制剂中是否添加了盐酸溴己新和吲哚美辛,方法可靠、简便、重复性好,可广泛应用于兽药非法添加检测工作。
[1] 高艳艳,周德刚,李佑新.麻杏石甘制剂药理作用及其在兽医临床中的应用[J]. 中国兽药杂志,2012,46(10):54-57.
[2] 中国兽药典委员会.中华人民共和国兽药典2010年版二部[S]. 北京:中国农业出版社,2010:581-582.
[3] 中国兽药典委员会.中华人民共和国兽药典2010年版二部[S]. 北京:中国农业出版社,2010:159-160.
[4] A Boussairi, F Guyon. Liquid chromatographic analysis with electrochemical detection for Bromhexine Hydrochloride in human plasma[ J] .Chromatographic, 1987,23(9): 651- 652.
[5] 孔令春.吲哚美辛的临床应用进展[J].海峡药学,2006,18(2):116-118.
[6] 国家药典委员会.华人民共和国药典2015年版二部[S].北京:中国医药科技出版社,2015:1107-1108.
[7] 国家药典委员会.中华人民共和国药典2015年版二部[S].北京:中国医药科技出版社,2015:478-479.
[8] 刘淑华,赵志刚.HPLC 法测定盐酸溴己新及其片剂的含量[J].中国药事,2008,22(1):68-69.
[9] 孙莉.HPLC法测定盐酸溴己新注射液含量及有关物质[J].安徽医药,2008,12(2):121-122.
[10]岳昌林,毛黎静.反相高效液相色谱法测定注射用盐酸溴己新的含量及有关物质[J]中国现代应用药学杂志,2007,24(8):207-208.
[11]孙银华. HPLC法测定吲哚美辛片含量及有关物质[J].中国药事,2012,26(2):172-177.
[12]雷曙光,罗永煌,陈君.兽用吲哚美辛注射液的含量测定及热稳定性考察[J].西南大学学报(自然科学版),2011,33(9):172-176.
[13]周健鹏,唐素芳.RP-HPLC法测定吲哚美辛巴布膏的含量和有关物质[J].药物分析杂志,2014,34(7):1310-1317.
[14]郝利华,于晓辉,董玲玲,等. HPLC - PDA 法同时测定黄芪多糖注射液中非法添加的四种解热镇痛类药物[J].中国兽药杂志,2012,46( 8) : 28 -31.
[15]王静文,范强,龚旭昊,等.鱼腥草注射液中非法添加甲氧氯普胺的HPLC - PDA的检测方法的建立[J].中国兽药杂志,2016,50( 3) : 45- 48.
[16]中华人民共和国农业部公告第2508号. 氟苯尼考制剂中非法添加烟酰胺、氨茶碱检查方法[S].2014.
[17]中华人民共和国农业部公告第2278号. 鱼腥草注射液中非法添加甲氧氯普胺检查方法[S].2015.
(编辑:陈希)
Determination of Bromhexine Hydrochloride and Indometcain Illegally Added in Three Veterinary Preparations by HPLC-PDA
WANG Jing-wen, GONG Xu-hao, FAN Qiang*, WAN Ren-ling
(ChinaInstituteofVeterinaryDrugControl,Beijing100081,China)
Methods for the determination of bromhexine hydrochloride in Maxing Shigan power and florfenicol injectionas well as indometcain in Gancao Granule were developed by the high performance liquid chromatography with photo-diode array detector(HPLC-PDA).It was tested with C18 column, using phosphate buffer and acetonitrile(20∶80),0.1 mol/L acetic acid and acetonitrile(50∶50)as the mobile phases. The scanning wavelength was from 200 to 400 nm.Peak purity test and spectrum similarity test were used to identify bromhexine hydrochloride and indometcain. The mean recoveries of bromhexine hydrochloridein maxing shigan power and florfenicol injection were 94.8% and 98.5%. The mean recovery of indometcain in Gancao granule was 95.2%. The linear equations of bromhexine hydrochloride and indometcain werey=14780200x-16476(R=0.9999) andy=10995430x+13033(R=0.9999). The limit of detections of blomhexine hydrochloride in Maxing Shigan power and florfenicol injection were 83 mg/kg and 1.6 g/L. The limit of detection of indometcain in Gancao granule was 1 g/kg. In conclusion, the method is simple, accurate and reliable for the determination of bromhexine hydrochloride and indometcain in three veterinary preparations.
bromhexine hydrochloride; indometcain;Maxing Shigan power; florfenicol injection; Gancao granule
王静文,硕士研究生,从事药品检验及相关工作。
2016-08-15
A
1002-1280 (2016) 12-0045-06
S859.79

