PPARγ上调对PCOS患者卵巢颗粒细胞P450arom mRNA的表达及T转化效应的影响*
王碧君,郭艺红,张慧红,李 婧,杨新红
郑州大学第一附属医院生殖医学中心 郑州 450052
PPARγ上调对PCOS患者卵巢颗粒细胞P450arom mRNA的表达及T转化效应的影响*
王碧君,郭艺红#,张慧红,李婧,杨新红
郑州大学第一附属医院生殖医学中心 郑州 450052
关键词多囊卵巢综合征;卵巢颗粒细胞;过氧化物酶体增殖物激活受体γ;细胞色素P450芳香化酶;T转化效应
摘要目的:探讨PPARγ上调对PCOS患者卵巢颗粒细胞P450arom mRNA表达的调控作用及对T转化效应的影响。方法:提取10例雄激素正常的PCOS 患者(NA-PCOS组)、10例伴高雄激素血症的PCOS患者(HA-PCOS组)及10例仅因输卵管因素不孕患者(对照组)的卵巢颗粒细胞,分别给予0、1、10 nmol/L的PPARγ激动剂罗格列酮培养48 h后,采用RT-PCR测定PPARγ、P450arom mRNA的表达,采用 ELISA法测定培养液中E2值,计算T转化率。结果:PPARγ上调后,3组患者P450arom mRNA的表达均降低,T转化率下降,尤其是HA-PCOS组(P<0.05)。PPARγ上调(10 nmol/L罗格列酮处理)后,HA-PCOS组卵巢颗粒细胞中PPARγ mRNA的表达水平和T转化率负相关,P450arom mRNA的表达水平和T转化率正相关(r=-0.633、0.829,P<0.05)。结论:PPARγ可能通过抑制P450arom参与PCOS高雄激素血症的发生。
AbstractAim: To explore the effects of up-regulation of PPARγ on expression of P450arom mRNA and T transforming effects in the ovarian granulosa cells from patients with polycystic ovarian syndrome(PCOS). Methods: A total of 30 patients were included, with 10 in NA-PCOS group(PCOS with normal androgen),10 in HA-PCOS group(PCOS with hyperandrogenism) and 10 in control group. Granulosa cells were prepared and treated with 0,1,10 nmol/L rosiglitazone for 48 h.The expressions of PPARγ mRNA and P450arom mRNA were measured by RT-PCR. After intervention, the E2 value in broth was determined by ELISA and T transforming rate was calculated.Results: After the up-regulation of PPARγ, the expression of P450arom mRNA and the T transforming rate in the 3 groups were decreased,especially in the HA-PCOS group. In HA-PCOS group(being treated by 10 nmol/L rosiglitazone),the expression of PPARγ mRNA was negatively associated with T transforming rate,and the expression of P450arom mRNA was positively associated with T transforming rate(r=-0.633,0.829,P<0.05).Conclusion: PPARγ may participate in the pathogenesis of PCOS with high androgen level by down-regulating the expression of P450arom.
多囊卵巢综合征(polycystic ovarian syndrome,PCOS)是一种以卵泡发育障碍为主的病因复杂、表现异质的代谢紊乱综合征[1]。高雄激素血症是PCOS最主要的内分泌特征之一[2],对体外受精-胚胎移植妊娠结局有一定的负面影响[3]。细胞色素P450芳香化酶(cytochrome P450 aromatase,P450arom)是颗粒细胞中催化雄激素生成雌激素的关键酶,其活力受抑制导致雄激素转化障碍[4],是造成高雄激素血症的直接因子。过氧化物酶体增殖物激活受体γ(peroxisome proliferator activated receptor γ,PPARγ)是核受体超家族的成员,其表达量与PCOS患者卵泡液总睾酮、游离雄激素指数呈正相关[5]。二者在卵巢颗粒细胞中存在怎样的调控关系及如何影响T转化效应目前尚不清楚。作者观察了不同浓度的PPARγ激动剂罗格列酮对PCOS患者卵巢颗粒细胞P450arom mRNA 的表达及 T 转化效应的影响,为进一步深入研究 PPARγ对卵巢颗粒细胞 P450arom 的影响提供前期实验基础。
1对象与方法
1.1研究对象选择2013年11月至2014年2月在郑州大学第一附属医院生殖医学中心行体外受精-胚胎移植助孕的25~30岁的患者,按照设计要求分别选择雄激素正常的PCOS患者10例(NA-PCOS组),伴高雄激素血症的PCOS患者10例(HA-PCOS组)以及同期仅因输卵管因素导致不孕的患者10例(对照组)。PCOS的诊断按照2003年鹿特丹PCOS诊断标准。排除标准:有糖尿病家族史、遗传病史、免疫性不孕、卵巢缺如或腹盆腔手术史、畸形子宫以及内分泌疾病史者。该研究获郑州大学第一附属医院伦理委员会的批准,且所有受试对象均签署知情同意书。
1.2控制性超促排卵患者接受标准长方案促排卵治疗,采用郑州大学第一附属医院生殖医学中心常规方法受精,进行胚胎移植和黄体支持[6]。移植后剩余胚胎冷冻保存。
1.3标本收集及测定
1.3.1血样采集及性激素测定月经周期第2~4天,HCG注射当日晨抽血约4 mL,用电化学免疫发光法(德国2010自动化检测仪)以及试剂盒(GmbH,德国)测定血清 E2、 P及LH值。
1.3.2卵巢颗粒细胞的分离及罗格列酮干预处理
收集患者双侧卵巢直径≥14 mm的清亮、无血染的卵泡液,离心。PBS、淋巴细胞分离液(Ficoll)分别购于美国Hyclone公司和天津灏洋生物制剂公司。用M199细胞培养液调整卵巢颗粒细胞的密度为(2~4)×105mL-1,取96孔板,每孔加入0.5 mL;培养48 h加入1 μmol/L的雄烯二酮并分别加入终浓度为0、1、10 nmol/L的罗格列酮[7],培养24 h。PBS反复洗细胞3次,-84 ℃冻存。每个浓度及对照均设1个复孔,实验重复3次。
1.3.3RT-PCR测定卵巢颗粒细胞PPARγ mRNA和P450arom mRNA的表达用Trizol法(试剂购于美国Invitrogen公司)提取3组患者卵巢颗粒细胞的RNA,逆转录为cDNA;按照试剂盒(美国Promega公司)说明书进行RT-PCR操作。引物序列:PPARγ(274 bp)上游引物5’-CAGGAGCAGAGCAAAGA-3’,下游引物5’-GGACTCAGGGTGGTTCA-3’;P450arom(314 bp)上游引物5’-CAGCGGTCTCCCTTGATA-3’,下游引物5’-TCTTCTCGGCATTTCTCC-3’; GAPDH(580 bp)上游引物5’-GCACCGTCAAGGCT GAGAAC-3’, 下游引物5’-TGGTGAAGACGCCAGT GGA-3’。所用引物均由北京全式金生物技术有限公司合成。PCR反应条件:94 ℃ 2 min;94 ℃ 30 s,55 ℃ 30 s(P450arom为54 ℃),72 ℃ 2 min,共35个循环;72 ℃延伸6 min。阴性对照组均采用去RNase水代替cDNA。PCR产物行20 g/L琼脂糖凝胶电泳,使用D-140图像分析纪录系统、Quantity One软件进行半定量分析,以目的基因与内参GAPDH积分吸光度的比值作为目的基因的相对表达量。
1.3.4培养液中E2激素测定及T转化率计算罗格列酮干预24 h后,各样本取1 mL培养液,按照ELISA试剂盒(联世生物科技公司,中国)说明书测定E2值。T转化率=E2测定值/加入雄烯二酮值。
1.4统计学处理采用SPSS 15.0处理数据。采用单因素方差分析比较各组卵巢颗粒细胞PPARγ、P450arom mRNA及T转化率的差异,两两比较采用LSD-t检验;采用Spearman相关分析确定PPARγ、P450arom mRNA和T转化率的关系。检验水准α=0.05。
2结果
2.13组患者一般资料及血清性激素水平比较见表1。
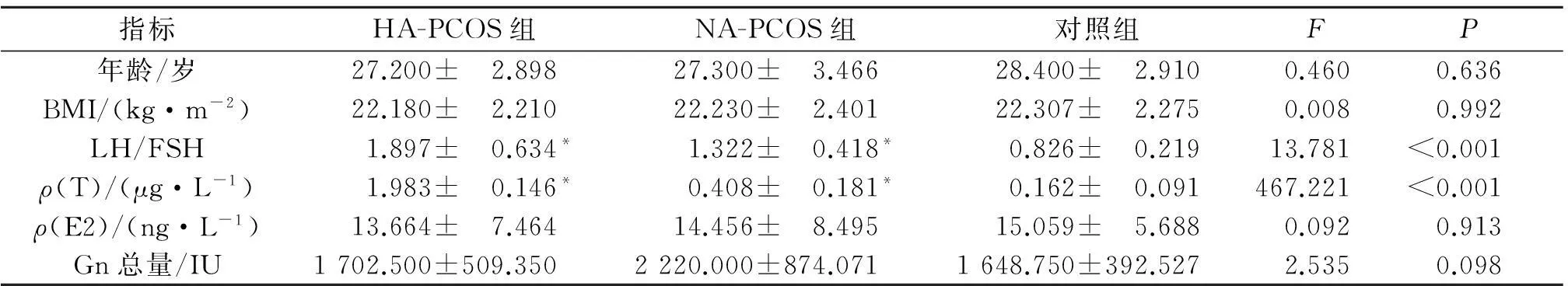
表1 3组患者一般资料及血清性激素水平比较(n=10)
*:与对照组比较,P<0.05。
2.23组患者卵巢颗粒细胞中PPARγ与 P450arom mRNA表达水平比较结果见图1、2和表2、3。由表2、3可知,未加罗格列酮时,与对照组相比,HA-PCOS组和NA-PCOS组患者卵巢颗粒细胞中PPARγ mRNA高表达、P450arom mRNA低表达。加入罗格列酮后,3组卵巢颗粒细胞中均出现PPARγ mRNA高表达、P450arom mRNA低表达,且在HA-PCOS组表现最明显。
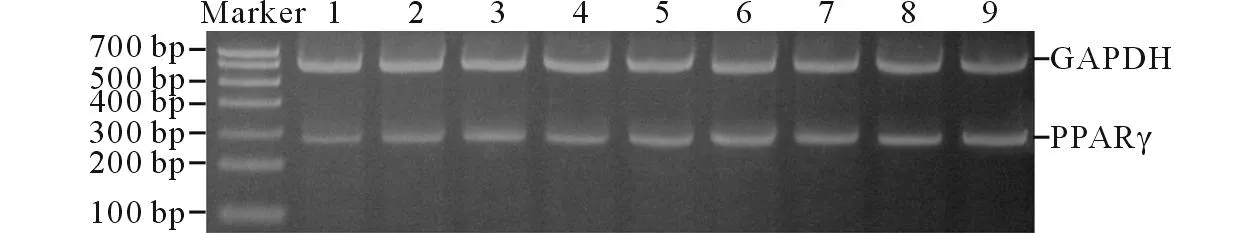
图1 不同浓度罗格列酮干预后3组患者卵巢颗粒细胞PPARγ mRNA RT-PCR结果
1~3:对照组;4~6:NA-PCOS组;7~9:HA-PCOS组;1、4、7:加入0 nmol/L 罗格列酮;2、5、8:加入1 nmol/L罗格列酮;3、6、9:加入10 nmol/L罗格列酮。
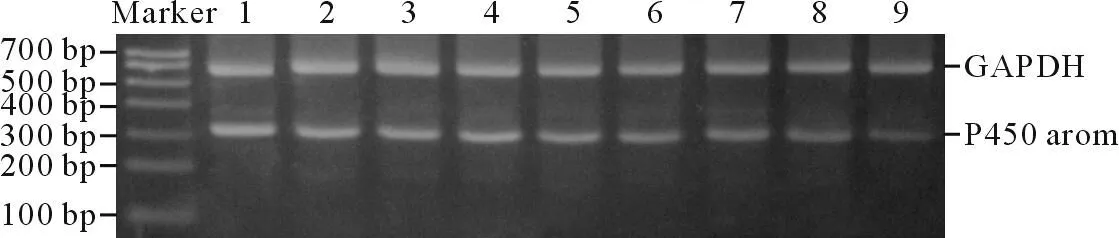
图2不同浓度罗格列酮干预后3组患者卵巢颗粒细胞P450arom mRNA RT-PCR结果
1~3:对照组;4~6:NA-PCOS组;7~9:HA-PCOS组;1、4、7:加入0 nmol/L 罗格列酮;2、5、8:加入1 nmol/L罗格列酮;3、6、9:加入10 nmol/L罗格列酮。
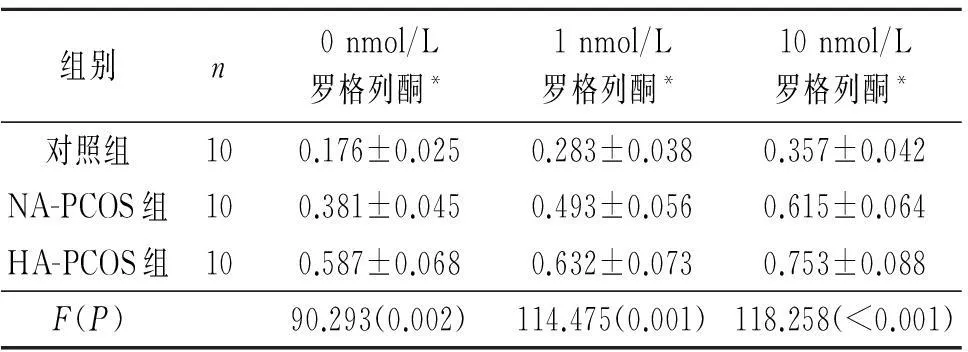
表2 3组患者卵巢颗粒
*:3组间两两比较,P均<0.05。
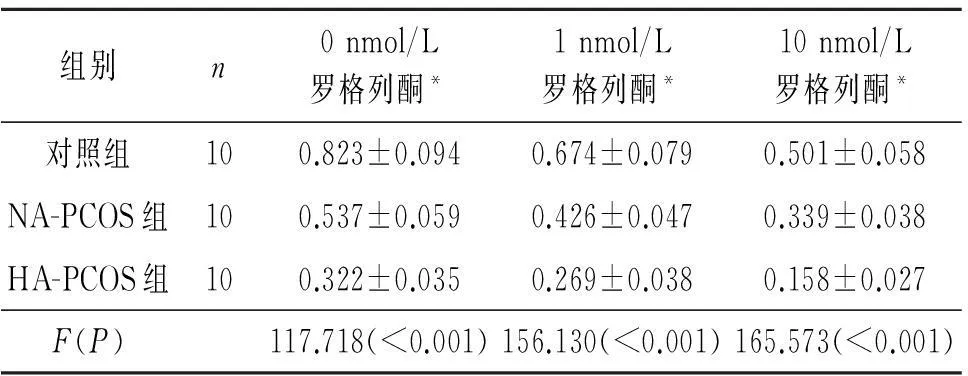
表3 3组患者卵巢颗粒
*:3组间两两比较,P均<0.05。
2.33组患者卵巢颗粒细胞 T 转化率下降幅度的比较见表4。

表4 3组患者卵巢颗粒细胞 T 转化率下降幅度
A:添加0 nmol/L罗格列酮与1 nmol/L罗格列酮时T转化率下降幅度;B:添加1 nmol/L罗格列酮与10 nmol/L罗格列酮时T转化率下降幅度;C:添加0 nmol/L罗格列酮与10 nmol/L罗格列酮 时T转化率下降幅度;*:与对照组相比,P<0.05。
2.43组患者卵巢颗粒细胞中P450arom、PPARγ mRNA的表达和T转化率的相关性分析见表5。

表5 3组患者卵巢颗粒细胞中PPARγ、
*:P<0.05;A:T转化率与PPARγ mRNA;B:T转化率与P450arom mRNA。
3讨论
高雄激素血症可导致PCOS患者排卵障碍,降低育龄期妇女妊娠率。目前,探索高雄激素血症的发病机制及临床治疗仍是PCOS相关研究的热点。有研究[8]显示女性P450arom基因多态性和PCOS发病相关。但PCOS患者体内P450arom表达水平尚有争议,部分学者认为PCOS患者高雄激素状态是因为P450arom底物发生了变化,P450arom活性仍正常甚至亢进,多数学者认为PCOS患者体内P450arom表达或活性降低[9-10]。该研究结果显示伴或不伴高雄激素血症PCOS患者的卵巢颗粒细胞中P450arom mRNA水平均低于对照组,与大部分学者的研究结果相同,此外,作者还发现HA-PCOS组P450arom mRNA的表达低于NA-PCOS组,提示P450arom mRNA低表达可能参与PCOS高雄激素血症的发生。
既往研究[5]多认为PCOS患者卵巢颗粒细胞中PPARγ呈高表达,但2013年胡卫红等[7]研究发现
PCOS患者卵巢颗粒细胞中PPARγ mRNA含量较低,但其组间样本量差异较大可能影响其结果。该研究结果显示PCOS患者卵巢颗粒细胞中PPARγ mRNA表达高于对照组,并且PPARγ mRNA在HA-PCOS组内表达更高,提示它与PCOS高雄激素血症的发生相关。
Faut等[11]学者认为PPARγ与窦卵泡凋亡相关,通过影响卵泡生长影响妊娠结局;而P450arom的芳香化作用发生异常会导致卵泡中的T/E2升高影响卵泡发育[12]。有学者[13-14]行聚类分析发现PPARγ合成异常与PCOS和高雄激素血症发生相关。作者所在的课题组前期研究(未发表)表明,PCOS患者卵巢颗粒细胞PPARγ mRNA表达水平高于对照组, 且与卵泡液雄激素水平呈正相关,与P450arom呈负相关。该研究结果显示: HA-PCOS组和NA-PCOS组卵巢颗粒细胞P450arom mRNA的表达和T转化率存在差异;PPARγ上调后,HA-PCOS组P450arom mRNA表达降低和T转化效应下降变化更明显。相关性分析结果显示,加入10 nmol/L罗格列酮的HA-PCOS组卵巢颗粒细胞中PPARγ mRNA的表达水平和T转化率负相关,P450arom mRNA的表达水平和T转化率正相关,提示PPARγ可能通过抑制P450arom参与PCOS高雄激素血症的发生。该研究为探索PCOS高雄激素血症的发生机制奠定了基础,并为其治疗提供了理论依据。
参考文献
[1]易思思,陈薪,刘玉东,等.多囊卵巢综合征患者反复种植失败后成功妊娠3例及其文献复习[J].南方医科大学学报,2014,34(9):1329
[2]王丽,吕淑兰,曹缵孙.青春期与育龄期多囊卵巢综合征患者的临床对照研究[J].西安交通大学学报:医学版,2010,31(6):745
[3]Lebbe M,Woodruff TK.Involvement of androgens in ovarian health and disease[J].Mol Hum Reprod,2013,19(12):828
[4]García Barrado MJ,Blanco EJ,Carretero Hernández M,et al.Local transformations of androgens into estradiol by aromatase P450 is involved in the regulation of prolactin and the proliferation of pituitary prolactin-positive cells[J].PLoS One,2014,9(6):e101403
[5]王芳芳,曲凡,黄荷凤,等.多囊卵巢综合征患者卵巢局部高雄与颗粒细胞PPARγ的表达[C].中国杭州生殖健康学术论坛暨浙江省计划生育学与生殖医学分会学术年会,2009.
[6]孙莹璞,苏迎春,郭艺红,等.体外受精-胚胎移植技术在常规超排卵304个治疗周期中的应用[J].郑州大学学报:医学版,2002,37(1):1
[7]胡卫红,陈琳,同军,等.PPARγ mRNA在卵巢颗粒细胞的表达调节及与多囊卵巢综合征的相关性[J].北京大学学报:医学版,2013,45(6):859
[8]Hao CF,Zhang N,Qu Q,et al.Evaluation of the association between the CYP19 Tetranucleotide(TTTA)n polymorphism and polycystic ovarian syndrome(PCOS) in Han Chinese women[J].Neuro Endocrinol Lett,2010,31(3):370
[9]Barroso G,Menocal G,Felix H,et al.Comparison of the efficacy of the aromatase inhibitor letrozole and clomiphene citrate as adjuvants to recombinant follicle-stimulating hormone in controlled ovarian hyperstimulation:a prospective,randomized,blinded clinical trial[J].Fertil Steril,2006,86(5):1428
[10]Maliqueo M,Sun M,Johansson J,et al.Continuous administration of a P450 aromatase inhibitor induces polycystic ovary syndrome with a metabolic and endocrine phenotype in female rats at adult age[J].Endocrinology,2013,154(1):434
[11]Faut M,Elia EM,Parborell F,et al.Peroxisome proliferator-activated receptor gamma and early folliculogenesis during an acute hyperandrogenism condition[J].Fertil Steril,2011,95(1):333
[12]Lazaros L,Xita N,Hatzi E,et al.CYP19 gene variants affect the assisted reproduction outcome of women with polycystic ovary syndrome[J].Gynecol Endocrinol,2013,29(5):478
[13]San-Millán JL,Escobar-Morreale HF.The role of genetic variation in peroxisome proliferator-activated receptors in the polycystic ovary syndrome(PCOS):an original case-control study followed by systematic review and meta-analysis of existing evidence[J].Clin Endocrinol(Oxf),2010,72(3):383
[14]Koika V,Marioli DJ,Saltamavros AD,et al.Association of the Pro12Ala polymorphism in peroxisome proliferator-activated receptor gamma2 with decreased basic metabolic rate in women with polycystic ovary syndrome[J].Eur J Endocrinol,2009,161(2):317
*卫生部医药卫生科技发展研究课题W2012FZ065
Effects of up-regulation of PPARγ on expression of P450arom mRNA and T transforming effects in ovarian granulosa cells from patients with PCOS
WANGBijun,GUOYihong,ZHANGHuihong,LIJing,YANGXinhong
ReproductiveMedicineCenter,theFirstAffiliatedHospital,ZhengzhouUniversity,Zhengzhou450052
Key wordspolycystic ovarian syndrome;ovarian granulosa cell;peroxisome proliferator activated receptor γ;cytochrome P450 aromatase;T transforming effect
doi:10.13705/j.issn.1671-6825.2015.06.016
中图分类号R711.6
通信作者#,女,1968年1月生,博士,主任医师,教授,研究方向:生殖医学,E-mail:13613863710@163.com

