基于预混辅料的拉莫三嗪口腔崩解片的制备
·实验研究·
基于预混辅料的拉莫三嗪口腔崩解片的制备
查静,王铁杰,王思明,涂家生
(中国药科大学药剂教研室,江苏 南京 210009)
摘要:目的由预混辅料入手,制备拉莫三嗪口腔崩解片。方法以异麦芽酮糖醇、微晶纤维素和交联聚维酮为主要辅料,使用湿法制粒的方法制备预混辅料,并测定了预混辅料产品的粉体学性质。选用拉莫三嗪为主药,与预混辅料及少量崩解剂、润滑剂和矫味剂,通过粉末直压的方法制备拉莫三嗪口腔崩解片,并对拉莫三嗪口腔崩解片进行基本的体外评价。结果通过单因素考察和正交试验,预混辅料的最终处方组成为:异麦芽酮糖醇与微晶纤维素的比例为3∶4,加入8%交联聚维酮。拉莫三嗪口腔崩解片的最优处方组成(按1 000片计)为:25 g 拉莫三嗪,137 g预混辅料,14.4 g低取代羟丙基纤维素,1.8 g硬脂酸镁,1.8 g矫味剂。拉莫三嗪口腔崩解片的崩解时限为35 s,且在5 min内溶出完全。结论根据试验,制备的预混辅料的性质优良,口腔崩解片的崩解时限、口感和溶出度等均符合规定。
关键词:预混辅料;口腔崩解片;拉莫三嗪
基金项目:深圳市战略新兴产业发展专项资金项目(No.JCYJ20130402144215892)
作者简介:查静,女,研究方向:药物新制剂和新技术,E-mail:zj20150501@163.com
通讯作者:涂家生,男,教授,博士生导师,研究方向:药物新制剂和新技术,Tel:13605159819,E-mail:jiashengtu@cpu.edu.cn
中图分类号:R944.4文献标识码:A
Preparation of Lamotrigine Orally Disintegrating Tablets based on the co-processed exicipient
ZHAJing,WANGTie-jie,WANGSi-ming,TUJia-sheng
(DepartmentofPharmaceutics,ChinaPharmaceuticalUniversity,Nanjing210009,China)
Abstract:ObjectiveTo prepare Lamotrigine Orally Disintegrating Tablets (ODTs) based on the co-processed excipients.MethodsFirstly,to prepare the co-processed excipient consisting of isomalt,microcrystalline cellulose and crospovidone by wet granulation method.Afterwards,Lamotrigine ODTs was directly compressed after mixing the co-processed excipient with a small amount of disintegrant,taste-masked agents and magnesium stearate,and the formula optimization was conducted.Finally,the micromeritic properties of co-processed excipient and the disintegration time of Lamotrigine ODTs with the optimal formula were investigated.ResultsThe desirable co-processed excipient composed of isomalt/microcrystalline cellulose at a ratio of 3∶4 and 8% crospovidone.And the components of the optimal formula of Lamotrigine ODTs(in 1 000) included 25 g lamotrigine,137 g co-processed excipient,14.4 g low-substituted hydroxypropyl cellulose,1.8 g magnesium stearate,1.8 g taste-masked agents.From the in-vitro study,the disintegration and dissolution time of Lmotrigine ODTs were within 35 seconds and 5 minutes,respectively.ConclusionAccording to the experiments,the micromeritic properties of co-processed excipients was good and the disintegration time,the dissolution time and the taste of ODTs were eligible.
Key words:Co-processed exicipient;Orally disintegrating tablets;Lamotrigine
口腔崩解片(orally disintegrating tablet,ODT)是近年来发展起来的一种新型速释制剂,其特点是药物置于舌面后,不需用水或只需少量水,也无需咀嚼,就能迅速崩解,借助吞咽动作入胃起效。与普通片剂相比,迅速崩解后药物通过黏膜吸收起效。该剂型尤其适合于一些老年人、儿童、精神病患者、吞咽有困难的患者及卧床体位难变动(如外科术后)患者用药,在口腔内迅速崩解而溶解,有起效快、生物利用度高等特点[1~3]。
拉莫三嗪是一种苯三嗪类的广谱抗癫痫药,是用于治疗癫痫局限性发作的辅助药物,主要作用于电压依赖性钠通道,对反复放电有抑制作用,也可能作用于谷氨酸相关神经递质,可抑制谷氨酸和天冬氨酸的抗癫痫药,能稳定突触前膜,抑制谷氨酸和天冬氨酸的释放[4]。主要用于治疗顽固性癫痫,目前国内仍然只有普通片这一种剂型,很难满足市场的需求,因此拉莫三嗪口腔崩解片的开发具有很高的实用价值和经济价值。
1仪器与试药
1.1仪器电子天平(FA1004);BZJ-360MⅡ 旋转压片机(上海立森机械仪器有限公司);752紫外可见分光光度计(上海精密科学仪器有限公司);BHX型电热恒温鼓风干燥箱(南京科尔仪器设备有限公司)。
1.2试药异麦芽酮糖醇(广西维科特生物技术有限公司,批号:1105227);微晶纤维素 pH301(日本旭化成);微晶纤维素 pH302(日本旭化成);微晶纤维素pH200(日本旭化成);硬脂酸镁(安徽山河药用辅料股份有限公司);交联聚维酮(安徽山河药用辅料股份有限公司);羧甲基淀粉钠(安徽山河药用辅料);低取代羟丙基纤维素(安徽山河药用辅料股份有限公司);拉莫三嗪(广州亿邦医药科技有限公司)。
2方法
2.1预混辅料及口腔崩解片的制备[5]预混辅料的制备:将一定量的异麦芽酮糖醇加入少量水中,在80 ℃水浴中溶解成过饱和溶液,作为粘合剂。另取一定量过筛后的微晶纤维素和交联聚维酮,混合均匀。将上述粘合剂逐滴缓慢加入,边加边搅拌进行湿法制粒,然后加入适量的水,使制得的颗粒握之成团,触之即散。最后,将制粒后的颗粒过筛,后于60 ℃下干燥90 min,即得。
口腔崩解片的制备:取过筛后的拉莫三嗪原料药25 mg,与一定量的预混辅料和少量外加崩解剂,矫味剂和润滑剂混合均匀,使用旋转压片机,粉末直压制成口腔崩解片。
2.2口腔崩解片体外崩解时限测定[6]测定方法如下:于恒流泵中固定一根内径约为4 mm的橡胶管,橡胶管一端置于恒温水浴中,设置恒温水浴的温度,使得橡胶管另一端(即出水端)的水温为37 ℃,调节恒流泵以控制水滴速度 (以2 mL·min-1为宜 ),同时水滴距片剂垂直距离约为1~2 cm。将片剂置于筛网上,使橡胶管中的水恰能滴到片剂上,开始计时,当片剂溶解并从筛网中全部漏下这段时间记为崩解时间。
2.3口腔崩解片口腔内崩解时限测定及口感评价[7]6名健康志愿者,用水清洁口腔,随机取药片置于舌面,不用水,也不咀嚼,允许舌适当上下运动,用秒表记录下药片在口腔中完全崩解所需时间,即为口腔崩解时间。然后将药粉吐出并漱口,立即记录口感。是否有苦感,甜度是否合适,崩解后有无砂砾感和残存片心等。
2.4处方设计
2.4.1填充剂种类的筛选选用MCC pH301、MCC pH302、MCC pH200 3种粒径不同的微晶纤维素进行考察,以口腔崩解片的崩解时限和口感作为指标,对结果进行分析比较。
2.4.2填充剂用量的筛选本试验中主要以Isomalt和MCC 都作为填充剂,选用不同比例的Isomalt/MCC进行考察,以口腔崩解片的崩解时限和口感作为指标,对结果进行分析比较。
2.4.3湿法制粒崩解剂类型的筛选选用PVPP、L-HPC和CMS-Na 3种崩解剂进行考察,用量均定为5%。以口腔崩解片的崩解时限和口感作为指标,对结果进行分析比较。
2.4.4湿法制粒过筛目数的选择湿法制粒时,选择24目、30目和40目筛制粒,以口腔崩解片的崩解时限和口感作为指标,对结果进行分析比较。
2.4.5外加崩解剂种类的选择选用PVPP、L-HPC和CMS-Na 3种崩解剂进行考察,用量均定为5%。以口腔崩解片的崩解时限和口感作为指标,对结果进行分析比较。
2.4.6片剂硬度的筛选根据预试验,设计各处方的片剂硬度分别为1.5、2.0、2.5、3.0、4.0 kg,考察各片剂的崩解时限。
2.5处方优化采用正交试验设计进行处方优化。选择Isomalt∶MCC的比例(A),PVPP的量(B)和L-HPC的量(C)为3个因素,采用3因素3水平正交试验(见表1),以片剂崩解时限为主要考察指标,结合口感评价优化处方。
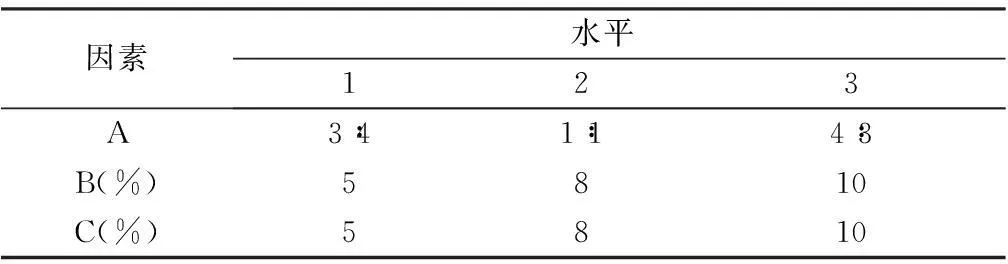
表1 正交试验因素水平表
2.6预混辅料的性质测定[8,9]
2.6.1外观形态及粒径采用扫描电镜(型号:SU8010 Semi-In-Lens FE-SEM)观察预混辅料的形态。采用马尔文激光粒度测定仪测定预混辅料的粒径。
2.6.2吸湿性临界相对湿度的测定:取样品6份,每份约1 g,置于恒重的称量瓶中,精密称定,打开称量瓶盖,分别放入不同湿度的玻璃干燥器中,在25 ℃恒温放置48 h,取出称量瓶,加盖后精密称定,计算样品的水分含量。以吸湿率为纵坐标,相对湿度为横坐标作曲线。
2.6.3休止角固定漏斗法:将3只玻璃漏斗串联并固定于水平放置的坐标纸上5.0 cm左右的高度处。小心地将物料沿漏斗壁倒入最上的漏斗中,直到坐标纸上形成的堆积圆锥体尖端接触到漏斗口为止,测定圆锥直径,以锥体高度(H)与圆锥半径(R)比作为正切值计算休止角(α),计算公式如下。测定3次,取平均值。
α=arctg(H/R)
2.6.4松密度、振实密度、Carr′s指数及Hausner比值量筒干燥后称重(M0),置漏斗颈下,量筒顶距漏斗5 cm,使漏斗和量筒同心,将样品沿漏斗壁旋转倒入漏斗中,使样品连续流出,刮刀轻轻夷平粉末顶部,不压实,精密称定质量(M1)并记录未处理的外观体积(V0)。平行测定3次,计算松密度(ρb)。
ρb=(M1-M0)/V0
将上述量筒从距离桌面高度2 cm处自由下落,重复500次,记录振实后粉末体积(Vt),平行测定3次,计算振实密度(ρt)。
ρt=(M1-M0)/Vt
根据下式计算Hausner 比值和Carr′s指数。
Hausner 比值=ρt/ρb
Carr′s指数=(ρt-ρb)/ρt×100%
2.6.6抗张强度采用压片机将预混辅料在不同压力下压成直径为9 mm的片剂,放置 24 h 后,测定片剂的硬度 (fc,单位kg) 和尺寸 (直径 d 和厚度 h,单位cm), 利用下式计算抗张强度 (σT,MPa)。结果见图4。
σT=2 fc/πhd
2.6.7弹性复原率粉末的塑性在片剂成型过程中起重要的作用,但它只能反映一种材料保持一定形状的能力,还不能确切地表明该粉末一定能结合成硬度高的压实体。因此还要结合考察粉末的结合力,可以用弹性复原率(Elastic recovery,ER)来表示。
具体试验方法:采用压片机将预混辅料在某一压力下压成直径为9 mm的片剂,分别测量受压时的片厚(H0,单位cm)及解除压力放置 24 h 后的片厚(Ht,单位cm),利用下式计算弹性复原率。
ER=(H0-Ht)/H0×100%
2.7拉莫三嗪口腔崩解片的溶出度实验[6]测定波长的选择:精密称取拉莫三嗪原料药,用0.1 mol·L-1盐酸制成20 μg·mL-1拉莫三嗪溶液。采用紫外-可见分光光度计[《中国药典》2010年版(二部)附录ⅣA],在200~800 nm的波长范围内进行扫描。
溶出度测定:参照美国药典,取本品,按溶出度测定法[《中国药典》2010年版(二部)附录 Ⅹ C 第一法(转篮法)],以0.1 mol·L-1盐酸900 mL为溶出介质,转速为100 rpm,依法操作,分别于1、3、5、10、20、30 min,取溶液5 mL,滤过,照紫外-可见分光光度法[《中国药典》2010年版(二部)附录Ⅳ A],在267 nm波长处测定吸光度。
3结果与讨论
3.1处方设计
3.1.1填充剂种类的筛选填充剂种类对片剂崩解时限的影响结果见表2。结果表明,以MCC pH302制得的崩解片崩解时限较短,且口感良好。

表2 填充剂种类对片剂崩解时限的影响
3.1.2填充剂用量的筛选填充剂用量对片剂崩解时限的影响结果见表3。结果表明,当Isomalt和MCC的比例为1∶1时崩解时限较短,且口感良好。
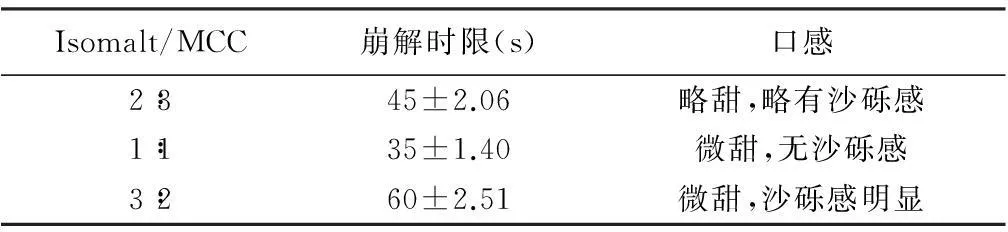
表3 填充剂用量对片剂崩解时限的影响
3.1.3湿法制粒崩解剂类型的筛选湿法制粒崩解剂类型对片剂崩解时限的影响结果见表4。结果表明,在湿法制粒的过程中,用PVPP作为崩解剂制得的崩解片崩解时限较短。
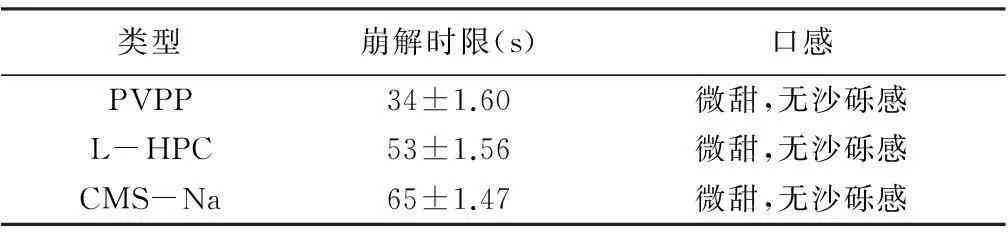
表4 湿法制粒崩解剂类型对片剂崩解时限的影响
3.1.4湿法制粒过筛目数的选择过筛目数对片剂崩解时限的影响结果见表5。结果表明,湿法制粒后过30目筛,制得的崩解片崩解时限较短,口感良好。

表5 过筛目数对片剂崩解时限的影响
3.1.5外加崩解剂种类的选择外加崩解剂类型对片剂崩解时限的影响结果见表6。结果表明,用PVPP和L-HPC制得的崩解片崩解时限相近,用L-HPC时崩解时限略短,这可能是由于湿法制粒时已使用PVPP作为崩解剂,使用PVPP的总量过多,使崩解时限增加,因此综合考虑后选择L-HPC作为外加崩解剂。
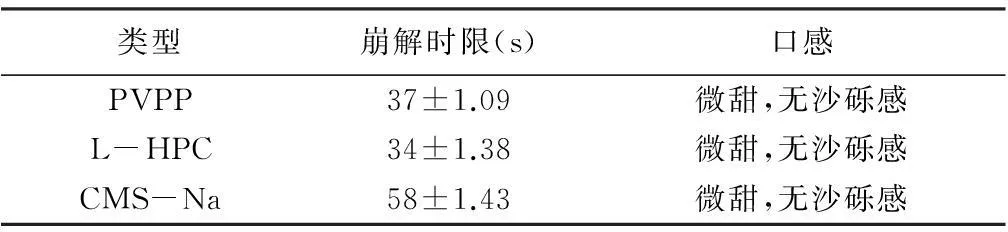
表6 外加崩解剂类型对片剂崩解时限的影响
3.1.6片剂硬度的筛选硬度对片剂崩解时限的影响结果见表7。结果表明,随着片剂硬度的增大,其崩解时限明显延长,说明片剂硬度对口腔崩解片的质量有较大的影响。但当片剂硬度较低时,片剂较为松散,易碎,不便于储存和运输,因此,综合考虑多种因素,选择硬度为2.0~2.5 kg较为合适。
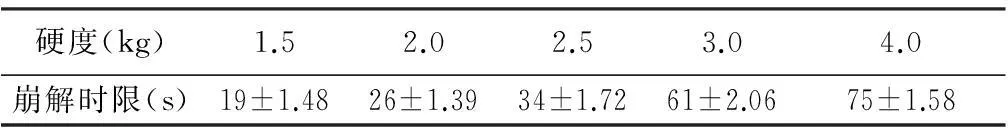
表7 硬度对片剂崩解时限的影响
3.2处方优化处方优化的结果见表8。
结果显示,预混辅料的处方组成为:异麦芽酮糖醇和微晶纤维素的比例3∶4,加入的交联聚维酮的量为8%。拉莫三嗪口腔崩解片的最终处方(按1 000片计)见表9。
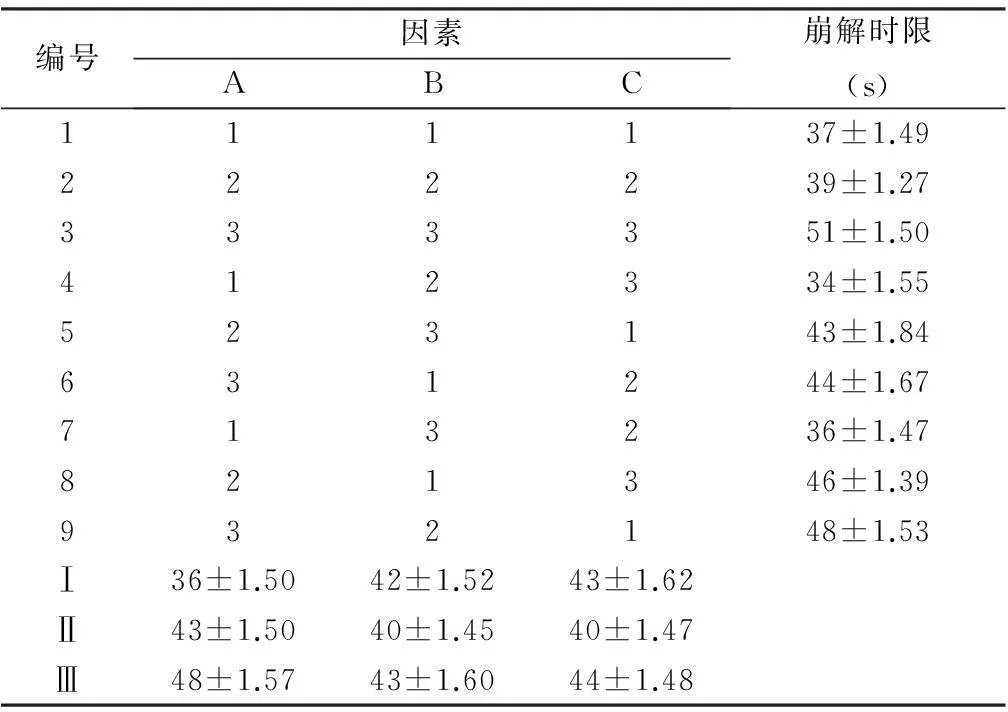
表8 正交试验设计和结果

表9 拉莫三嗪口腔崩解片的最终处方(按1 000片计)
3.3预混辅料的性质测定
3.3.1外观形态及粒径外观形态见扫描电镜图,如图1。粒径分布图见图2。

图1 预混辅料的扫描电镜图
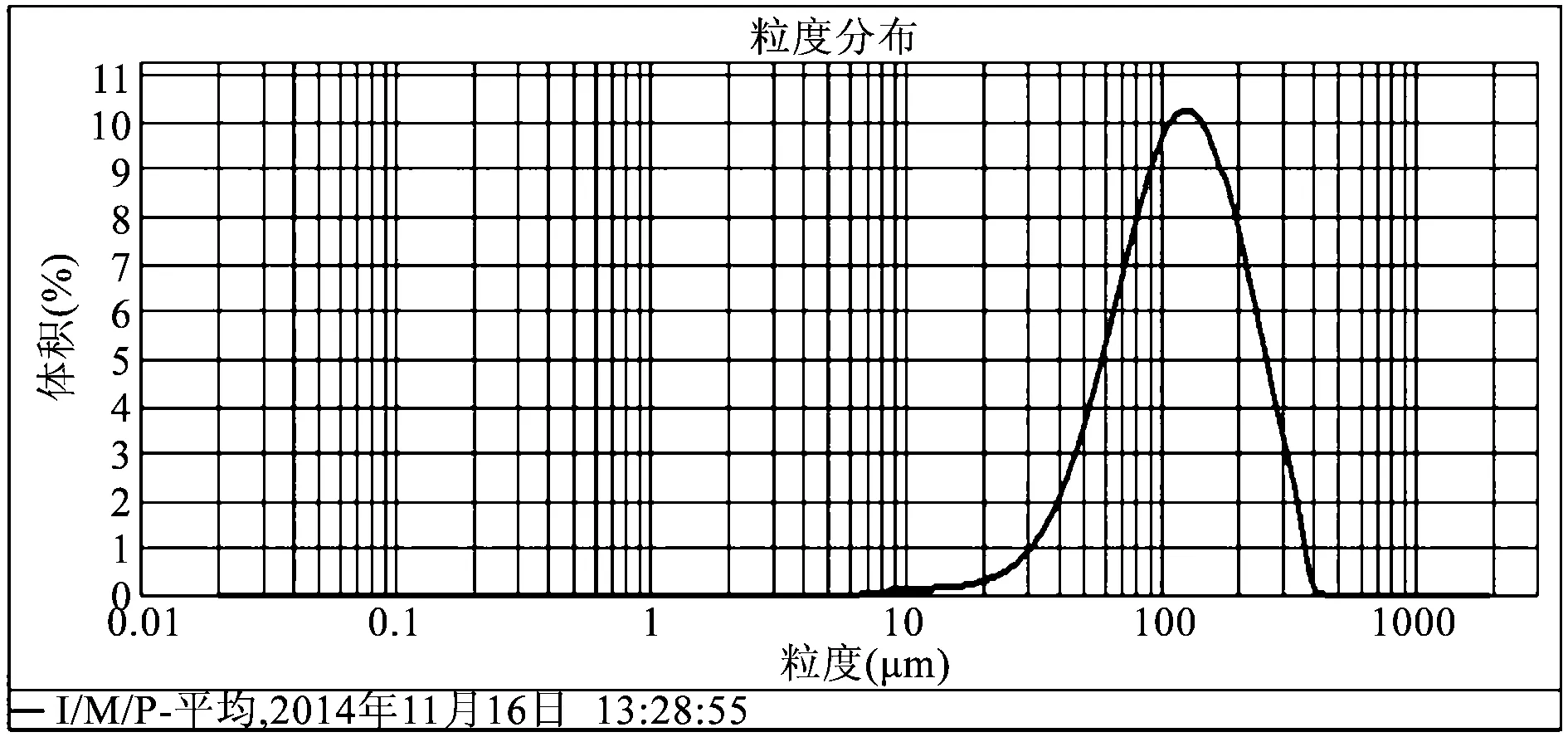
图2 预混辅料粒径分布图
从图中可以看出,预混辅料由多种物质聚集而成,是块状结构。激光粒度测定仪的测定结果显示预混辅料的平均粒径为133 μm,这既能保证预混辅料的流动性符合粉末直压的要求,也能确保压片后的口崩片口感良好。
3.3.2吸湿性预混辅料吸湿性结果见图3。结果显示,预混辅料临界相对湿度约为75%,便于压片和储存。
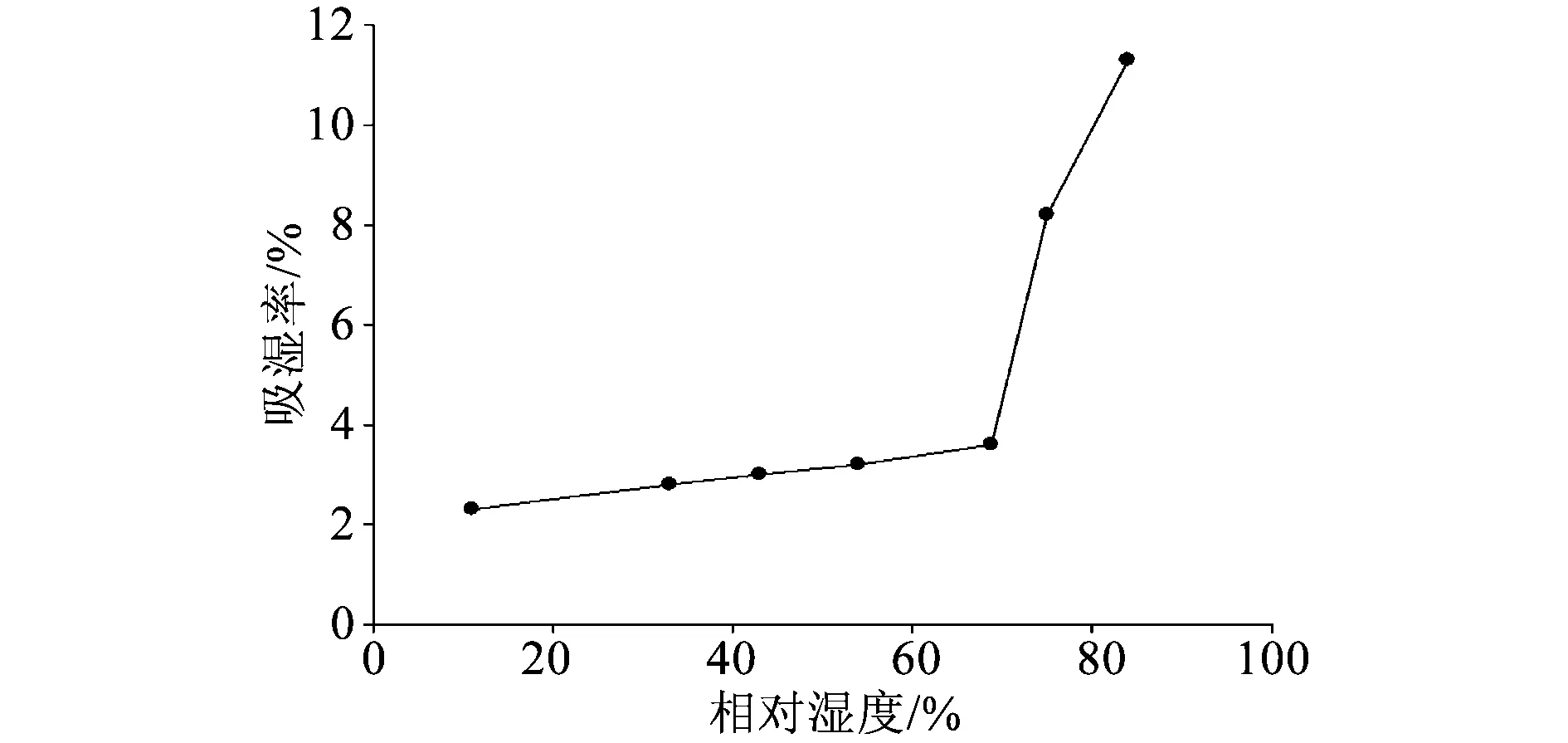
图3 预混辅料相对湿度-吸湿率图
3.3.3休止角、松密度、振实密度、Carr′s指数及Hausner比值休止角、松密度、振实密度、Carr′s指数及Hausner比值结果见表10。预混辅料的休止角、卡尔指数和Hausner比值等的结果表明,预混辅料的流动性良好,满足粉末直压的要求。将自制的预混辅料作为主要辅料,与少量外加崩解剂、矫味剂、润滑剂和主药混合均匀,可通过粉末直压的方法制备口腔崩解片。
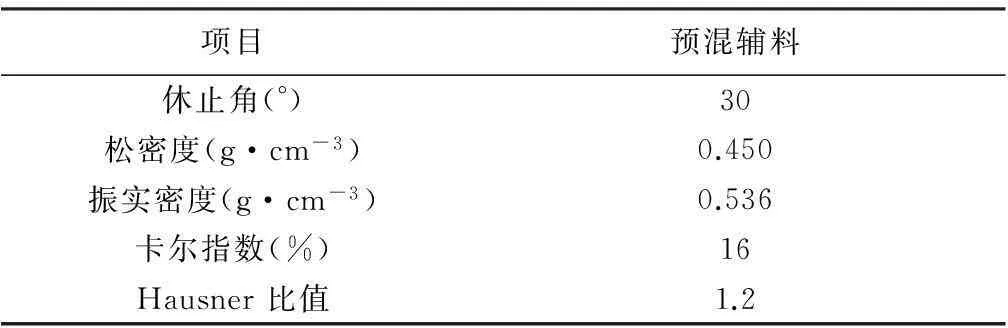
表10 预混辅料流动性测定结果
3.3.4抗张强度预混辅料的硬度与抗张强度关系见图4。抗张强度是粉末可压性和成形性的一种衡量指标。粉末在一定压片力下成形后,抗张强度的大小可以体现粉末的成形性。抗张强度越大,成形性越好。从图中可见,预混辅料的抗张强度随片剂硬度的增加而增大。因此,综合考虑抗张强度和崩解时限,选择片剂的硬度为2.5 kg较合理。
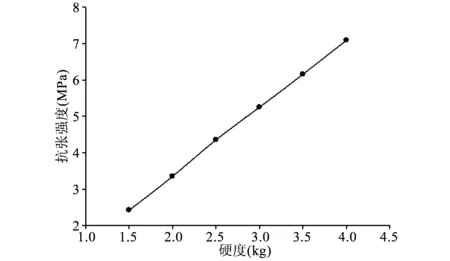
图4 预混辅料的硬度—抗张强度曲线图
3.3.5弹性复原率预混辅料的弹性变形率和硬度之间的关系见图5。弹性复原率是指片剂从模孔中移出后,由于内应力的作用而发生的弹性膨胀。如果在压力解除后,片剂产生较大的弹性复原率,就会发生裂片等现象。图5结果显示,预混辅料的弹性变形率较小,压实性较好。
3.4拉莫三嗪口腔崩解片的体外评价
3.4.1拉莫三嗪口腔崩解片的体外和口腔内的崩解时限经测定,拉莫三嗪口腔崩解片的体外崩解时限为(33.3±1.20)s,6名受试者口腔内崩解时限为(36.1±1.52)s,且无1例超过60 s,口感良好,无片心。
3.4.2溶出度根据扫描图谱显示拉莫三嗪在267 nm 和222 nm波长处有最大吸收。另取处方量的辅料溶解过滤后同法测定,结果显示辅料在267 nm 波长处无干扰。因此选用 267 nm为测定波长。扫描图见图6。溶出曲线见图7,样品在5 min内能完全溶出。

图5 预混辅料的弹性变形率和硬度之间的关系

图6 空白辅料(A)和拉莫三嗪(B)的紫外扫描图谱
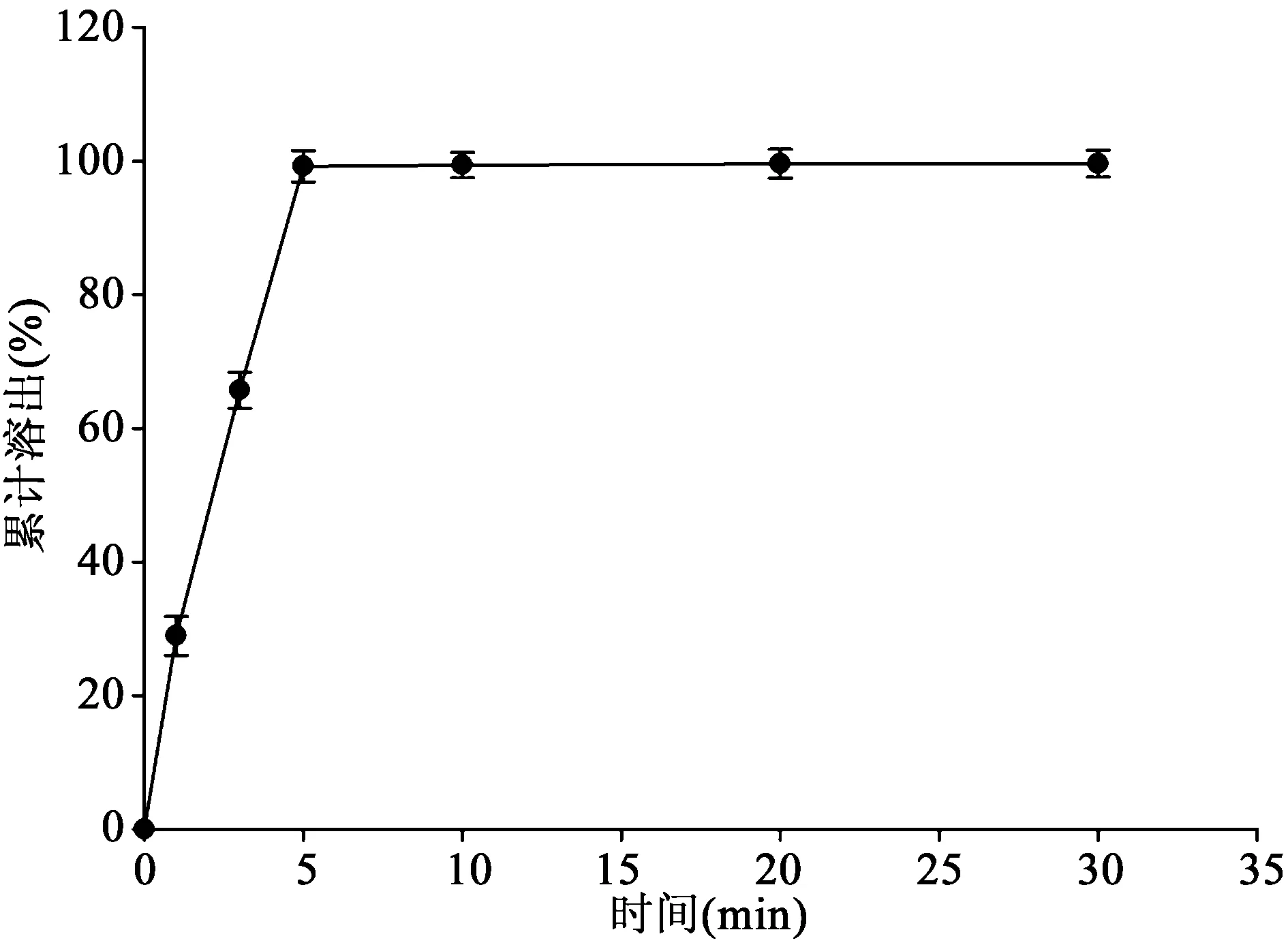
图7 拉莫三嗪口腔崩解片累积溶出曲线
4小结
预混辅料,系指将两种或多种单一辅料按适当的比例,通过一定生产工艺均匀混
合在一起,产生的功能协同作用且表现均一的新辅料。本文通过工艺简单,成本低廉的湿法制粒制备了预混辅料,并对自制的预混辅料进行了性质测定,结果表明,预混辅料的流动性、可压性、吸湿性和崩解性等性质优良,满足粉末直压的要求。
预混辅料的发展使口腔崩解片的开发成为可能。本文利用自制的预混辅料制备了拉莫三嗪口腔崩解片,通过单因素试验,处方主药为拉莫三嗪,辅料由Isomalt、MCC、PVPP、L-HPC、硬脂酸镁等组成,硬度为2.0~2.5 kg。另外,对拉莫三嗪口腔崩解片进行了初步体外评价:崩解时限和溶出度测定,结果显示制备的口腔崩解片符合规定,可为这类精神病患者的药物服用提供方便。
参考文献:
[1] 咸银库,周毅生.口腔崩解片的研究进展[J].广东药学院学报,2006,22(6):694-696.
[2] Goel H,Rai P,Rana V,et al.Orally disintegrating systems:innovations in formulation and technology[J].Recent Pat Drug Deliv and Formul,2008,2(3):258-274.
[3] 姚西玲.盐酸美金刚口腔崩解片的制备[J].齐鲁药事,2011,30(8):440-441.
[4] 陈司汉,邓俊丰,江晓玲.HPLC法测定拉莫三嗪片的含量[J].北方药学,2014,11(7):2-3.
[5] Daraghmeh N,Rashid I,Al Omari MM,et al.Preparation and characterization of a novel co-processed excipient of chitin and crystalline mannitol[J].AAPS PharmSciTech,2010,11(4):1558-1571.
[6] 姚方耀,刘欢,刘衡,等.口腔崩解片体外崩解评价方法探讨[J].中国药学杂志,2007,42(4):276-279.
[7] 毛叶萌.阿普唑仑口腔崩解片的研制[D].复旦大学,2008.
[8] 张益兰,田超,胡丹蓉,等.直接压片辅料LubriTose AN 的粉体学评价[J].药学学报,2012,47(5):640-645.
[9] 陈盛君,朱家壁,祁小乐.粉末直接压片常用辅料的粉体学性质评价[J].中国医药工业杂志,2013,44(10):1010-1013.

