盐酸米安色林片的处方研究
盐酸米安色林片的处方研究
李宁,张玉美,聂昌盛
(山东仁和堂药业有限公司,山东 临沂 276600)
摘要:目的研究盐酸米安色林片处方。方法盐酸米安色林为水溶性药物,采用微晶纤维素,淀粉,聚维酮K30等辅料,选择最合理处方。结果盐酸米安色林片中淀粉占48%,微晶纤维素占18%,羧甲基淀粉钠3%,聚维酮K30适量。结论此处方合理、稳定,片剂质量符合要求。
关键词:盐酸米安色林片;研究;处方筛选;质量检验
作者简介:李宁,男,研究方向:药物制剂,E-mail:lining696@sina.com
中图分类号:R944.4文献标识码:A
Prescription research of Mianserin Hydrochloride Tablets
LINing,ZHANGYu-mei,NIEChang-sheng
(ShandongRenhetangPharmaceuticalCo.,Ltd.,Linyi276600,China)
Abstract:ObjectiveTo study the prescription of Mianserin Hydrochloride Tablets.MethodsMianserin hydrochloride is water-soluble drugs,using microcrystalline cellulose,starch,povidone K30 as adjuncts,chose the most reasonable prescription.ResultsMianserin Hydrochloride Tablets were composed of starch 48%,18% microcrystalline cellulose,3% sodium carboxymethyl starch,povidone K30 for moderation.ConclusionThis prescription was reasonable,stable,and the tablet quality met the requirements.
Key words:Mianserin Hydrochloride Tablets;research;Prescription screening;Quality inspection
盐酸米安色林(Mianserin Hydrochloride)是由荷兰欧加农(Organon)公司开发1985年上市的新一代四环类抗抑郁药,其抗抑郁作用可与目前已有的各种抗抑郁药相媲美,但在治疗剂量时抗胆碱能的副作用极低,对心血管系统也无明显影响,长期使用不损伤心肌收缩力和心肌内传导,具有广泛药物相容性[1~6]。本文对其片剂的处方进一步改进,主要研究其制备方法、脆碎度、溶出度及在高温高湿储存条件下是否稳定。采用多种处方组合形式进行处方筛选,找出最佳处方,为该药能够具有更加稳定的产品质量,更好地发挥疗效提供理论依据。
1盐酸米安色林片的制备
1.1设备仪器与试剂
1.1.1设备仪器颗粒机(型号:YK-160D,丹东市制药设备厂);循环烘箱(型号:CT-C-II,南京长鑫干燥设备厂);压片机(型号:ZP-437,北京翰林科技公司);高效包衣机(型号:BGB-150C,浙江小伦);紫外分光光度计(型号:UV2800,上海舜宇恒平);溶出度仪(型号:RCZ-8M,天津市天大天发);分析天平(型号:DV215CD,奥斯豪仪器);脆碎度仪(型号:WB-2000XG,北京国立)。
1.1.2试剂盐酸米安色林(批号:140301,公司自产),淀粉(批号:140201)、微晶纤维素(批号:140203)、羧甲基淀粉钠(批号:131201)均购自于曲阜天利药用辅料公司;聚维酮K30(批号:140301,湖北葛店人福药用辅料公司),其他试剂均为分析纯。
1.1.3制备
1.1.3.1片芯处方盐酸米安色林30 g,淀粉48 g,微晶纤维素18 g,羧甲淀粉钠3 g,10%聚维酮K30 28 g,硬脂酸镁适量,制成1 000片。
1.1.3.2薄膜衣处方(每1 kg片芯包衣液用量) 薄膜包衣预混辅料15 g ,乙醇(75%)300 mL溶解后可用。
1.1.3.3处方依据本品主药为盐酸米安色林,为一水溶性药物。处方设计时,主要考虑片剂的可压性、溶出度和脆碎度。初筛的5组处方见表1。
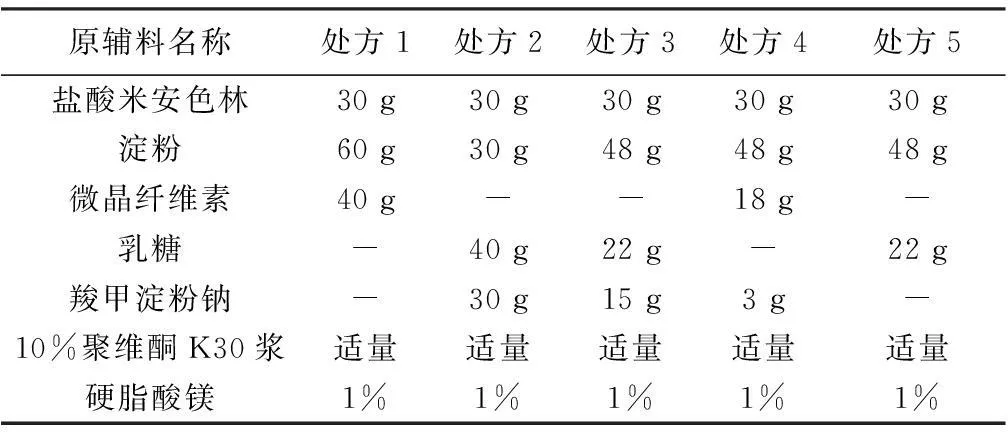
表1 盐酸米安色林片处方筛选(1 000片用量)
1.1.3.4制备按上述5组处方分别称取,过80目筛,加入适量聚维酮K30浆,20目筛制粒,55~60 ℃烘干,水分3.0%,20目筛整粒,加适量硬脂酸镁,压片,包薄膜衣即得。
2有关质量研究[7,8]
2.1经观察处方1片剂色泽差,应淘汰。处方2、3、4、5外观合格,均留作进一步试验。
2.2脆碎度、溶出度试验结果试验结果见表2。
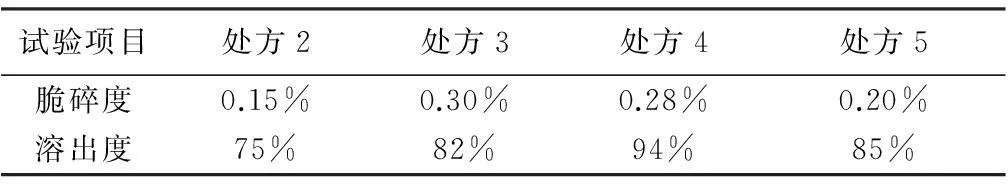
表2 处方2、3、4、5试验结果
试验结果表明,处方4脆碎度合格,溶出度优于处方2和处方3、5,处方2和处方3、5应淘汰,留处方4做进一步试验。
2.3强光照射试验 将初筛选处方4样品置药物稳定性检查仪中,以(4 500±500)Lx光照度照射,分别于第5、10天取样,按考察项目检查和测定,并与0 d的结果进行比较,观察样品在强光照射下的稳定性,试验结果见表3。
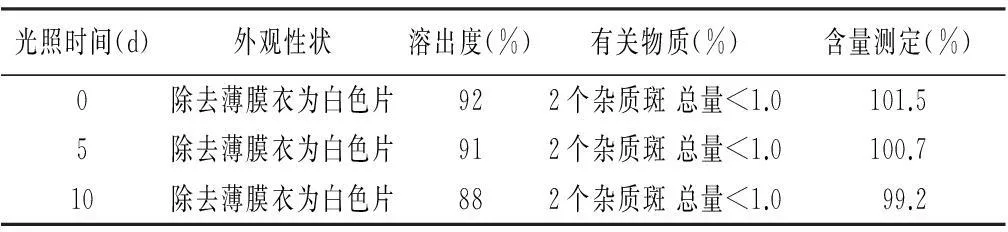
表3 强光照射试验[(4 500±500)Lx]结果(处方4)
2.4高温试验将初筛选处方4样品置恒温箱中,60 ℃放置,分别于第5、10天取样,按考察项目检查和测定,并与0 d的结果进行比较,观察样品在高温条件下的稳定性,试验结果见表4。
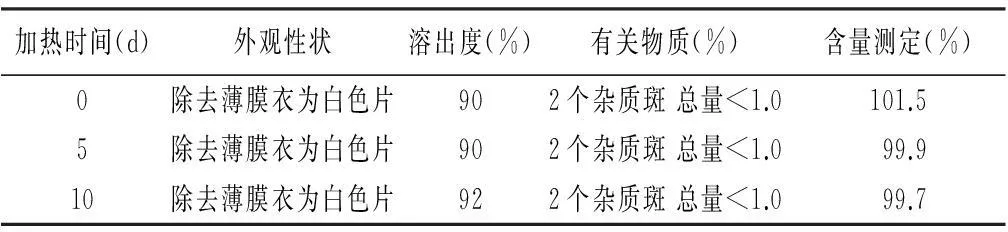
表4 高温试验(60 ℃)结果(处方4)
2.5高湿度试验将初筛选的处方4样品置恒湿密闭容器中,样品开口在25 ℃分别于相对湿度90%±5%条件下放置,分别于第5、10天取样,按考察项目检查和测定,并与0 d的结果进行比较,观察样品在高湿度条件下的稳定性,试验结果见表5。

表5 高湿度试验(90%±5%)结果(处方4)
试验结果表明,样品在强光照射、高温试验、高湿条件下,除高湿度试验水分变化较大外,样品的溶出度、有关物质及含量与0 d样品相比较变化较小,该处方产品质量稳定可控,因此选用处方4作为米安色林片的生产处方。
3总结
盐酸米安色林为一水溶性药物,处方设计中曾试用淀粉,微晶纤维素、乳糖、羧甲淀粉钠、硬脂酸镁等辅料,以不同量组方、以溶出度、脆碎度、外观成本作为指标。比较后筛选出上述处方,制成的片剂剂型大小合适,外观平整光滑,成本低,硬度、崩解较好,质量稳定。
本处方经回收率、含量、溶出度、有关物质检测,认为处方组成合理、工艺可行、质量可靠。并可以大大降低生产成本,创造更多的企业价值。通过对其处方工艺的优化,使产品质量得到进一步提升,让患者安心用药,体现公司的更多社会责任。
参考文献:
[1]国家食品药品监督管理局.化学药品稳定性技术研究指导原则[S].国食药监注[2005]106号,2005-3-18.
[2]王来海,曾宪奎,原海燕.盐酸米安色林片[J].中国新药杂志,2002,11(11):891-892.
[3]龚亚林,田小芹.抗抑郁药的临床综述[J].中国药师,2004,7(2):149-151.
[4]季建林.抗抑郁药临床治疗的选择[J].临床药物治疗杂志,2012,10(2):23-26.
[5]张光勇,周小东.米安舍林治疗老年抑郁症对照研究[J].临床精神医学杂志,2000,10(5):268-269.
[6]李亚玲,漆文烨.米安色林与舍曲林治疗老年抑郁症的对照研究[J].医药导报,2011,30(11):1460-1461.
[7]朱丽,贾首时,张连成.盐酸米安色林片的HPLC法测定[J].中国医药工业杂志,2014,45(6):570-572.
[8]孙丽丽,司天梅.HPLC法测定血浆中米安色林的浓度[J].中国新药杂志,2002,11(9):714-716.

