与睡眠相关的脑结构(二)——与睡眠时相有关的神经结构
与睡眠相关的脑结构(二)——与睡眠时相有关的神经结构
段莹耿新玲吴建永高和
引言——1950年代的两个里程碑
人类对睡眠和失眠的兴趣可以追溯到古代,在中医理论对失眠也有自己的理论体系,不过在20世纪40年代以前人们都认为睡眠是由疲劳引起的脑活动减少。那时的脑科学认为疲劳可以导致大脑对感觉信息的反应降低,从而导致睡眠。
理解睡眠的第一个里程碑是在20世纪40年代末期,意大利生理学家莫如滋(Giuseppe Moruzzi)的工作:他在动物实验中发现,破坏了脑干网状结构(brain stem reticular formation)之后,动物就会陷入持续的脑电睡眠状态。然而,如果破坏了所有感觉信息传入大脑的通路并不能影响清醒和睡眠。这个突破性的发现说明,脑干网状结构的活动可维持前脑(即大脑)的清醒。大约10年之后,他的实验室又传出了另一个惊人发现:在脑桥的水平切断脑干,动物就会进入持续的不眠状态[1]。这些实验证明,睡眠是一个主动过程,脑干网状结构是控制这一过程的关键环节。上半部网状结构(桥脑之上)持续活动可以维持大脑的清醒状态,而网状结构的桥脑以下部分则能抑制其上半部的活动。因此如果去掉整个脑干,动物则长睡不醒;如果只去掉下半部脑干,其上半部就过于兴奋,出现持续不眠的状态。莫如滋作为一个著名的生理学家,他的故事请见参考文献[2]。
第二个里程碑是2世纪50年代在睡眠脑电研究中的发现。芝加哥大学的研究生,尤金·阿瑟林斯基(Eugene Aserinsky)发现了整夜睡眠是由非快速眼动睡眠(NREM)和快速眼动睡眠(REM)两个时相交替组成的[3]。这个发现是在他们的导师,著名睡眠学者内森·克雷曼(Nathaniel Kleitman)的指导下,利用脑电记录实现的。
所谓脑电就是大脑活动时头皮外面记录到的微小电信号。这种信号非常小,电压只有手机电池的十万分之一左右,但是在清醒和睡眠期间的表现却很不一样。人类脑电在20世界20年代由德国心理学家汉斯·伯格(Hans Berger)发现。伯格发现人在清醒时,睁眼和闭眼状态下的脑电波形差别很大[4]。几年后科学家们将脑电监测用于睡眠研究。可是,在20世纪30年代,哈佛大学开展的睡眠脑电研究只记录了睡眠开始的几十分钟,并没有延续到快速眼动睡眠的时段,因此使快速动眼睡眠的发现推迟了20年左右。现在看来造成推迟的原因可能有两个:理念上,当时人们认为睡眠是被动的休息,不存在复杂的时相结构;技术上,当时脑电都是记录在纸带上的,整夜的监测可以有几千米长。可能为了节约,多数研究者都没有进行长时间的脑电监测。同样,也没有人花时间仔细看那些堆积如山的纸带。
而阿瑟林斯基的里程碑式工作源于他的出发点不同。刚开始做博士论文的时候,导师克雷曼让他观察入睡的眨眼行为,但他做了几个月毫无进展。迫于毕业找个工作养家糊口,他提了一个新计划——研究睡眠者整夜眼球的活动。这个计划过于冒险,不适于有毕业压力的研究生,但他非常热爱科学,经常彻夜不眠地观察睡眠者,见到熟睡的人眼球会有激烈活动这一现象并觉得非常有意思。也许这个发现能够让他得到可以发表的实验结果。导师同意了他的冒险计划,并提议让他用一台记录仪把数据记下来,避免只用眼观手记的主观办法。阿瑟林斯基由此发明了把脑电电极放在眼睛附近来记录眼动的方法。他的第一个被试者是自己的儿子阿萌,他很快就发现当阿萌进入熟睡后眼球呈周期性地激烈活动,而且每几个小时会重复一次。这个惊人的发现引起了导师克雷曼的注意。他先找来自己的女儿重复了实验,进而找来更多的成年被试者。结果无一例外,人进入熟睡后的1 h左右眼睛虽然紧闭,但眼球会快速地活动。更加惊人的是,如果在此时叫醒被试者,他们都会说当时正在做梦。阿瑟林斯基的工作最终以1篇高质量文章在《科学(Science)》杂志上发表[3]。这个跨时代的发现让阿瑟林斯基和克雷曼成为现代睡眠科学的开创者。可惜阿瑟林斯基刚得到博士学位就找到工作离开了睡眠领域。他的故事详见参考文献[5]。
20世纪50年代的两个里程碑清楚地提示,睡眠不是一个单一的休息状态,而是具有复杂的时相结构的。清醒和睡眠之间的转化以及睡眠之中各时相的转化并不是受皮层控制,却是由皮层下的脑结构控制。后来的研究证明,大脑是泡在含有各种“佐料”的汤里的。一种“佐料”使大脑清醒,另一种使之睡眠。不同的“佐料”决定了皮层是清醒、深睡还是做梦。这些“佐料”就是神经递质,是由皮层下不同核团中的细胞来产生的。与清醒和睡眠有关的神经递质系统主要有五种:分别是乙酰胆碱(acetylcholine)、去甲肾上腺素(Norepinephrine,NE)、五羟色胺(serotonin,5-HT)、多巴胺(dopamine)和组胺(histamine)。下面先介绍睡眠的时相分期,再介绍操纵这些时相分期的五个神经递质系统。
1睡眠的多导记录分期
从阿瑟林斯基和他的师弟在克来曼的工作开始,人们逐渐了解一整夜的睡眠包含着几个睡眠周期。而每个周期又可以根据脑电特征分成非快速眼动睡眠(NREM睡眠)和快速动眼睡眠(REM睡眠)两类,其中后者是做梦的时段。早期的睡眠监测只包括1对脑电导联(C3-m2或C4-M1)、左右眼动和颏肌电信号。1968年《人类睡眠分期标准术语和判读手册》出版[6]。我们习惯称之为“R&K标准”,该标准将NREM睡眠分为S1期、S2期、S3期、S4期和REM期。其中S1期和S2期为浅睡眠,S3期和S4期为深睡眠,REM期即为会做梦的REM睡眠。
1972年,斯坦福睡眠实验室在监测脑电、眼动和颏肌电的基础上,增加了心电和呼吸的同步监测,并由Jerome Holland在1974年将此技术命名为多导睡眠监测(polysomnography,PSG)[7]。时至今日,PSG仍是睡眠医学的重要研究手段,也是一些睡眠疾病诊断所需的“金标准”。随着数字化技术的发展,传统走纸式PSG逐步被数字化PSG所取代,而PSG监测也增加了很多可扩展的参数。此时,《R&K分期》的使用也遇到了更多的问题和争议。2007年,美国睡眠医学会组织各领域专家在充分回顾以往研究的基础上出版了《AASM睡眠及其相关事件判读手册:规则、术语和技术规范》(The AASM Manual for the Scoring of Sleep and Associated Events:Rules,Terminology and Technical Specifications1sted)[8]。我们习惯称之为《AASM判读手册》,2012年和2014年该手册分别进行了规则更新[9-10]。这是现代多导睡眠监测技术的首部规范,也是目前睡眠分期的国际标准。手册将判读睡眠分期所需的脑电监测增加至2对额部导联、2对中央导联和2对枕部导联。由于脑电导联的变化,睡眠分期也进行了更改:原NREM睡眠中的3期和4期合并为N3期,即NREM睡眠包括N1期、N2期和N3期,REM睡眠为R期,清醒期为W期。
睡眠分期,其实就是根据脑电、眼动和颏肌电这3类信号中的不同特征波来判定的。从监测起始处,每30 s为一帧,逐帧判读睡眠分期。
W期的脑电频率较快,安静闭眼时枕部导联出现8~13 Hz的α节律;可以见到快速眼球运动或眨眼;颏肌电波幅较高。如图1、图2所示。

图1 W期:脑电(黑色)可见α节律,两眼动导联(蓝色)也拾取到α节律;颏肌电(红色)波幅较高,通常高于睡眠期的肌电水平

图2 W期,可见快速眼球运动(蓝色),颏肌电波幅较高(红色)
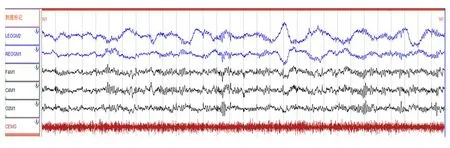
图3 N1期,可见缓慢眼球运动(蓝色);脑电为低电压混合频率,还可见散在α波
N1期的脑电以低电压混合频率(LAMF)为主。低电压是指脑电波的波幅较低,混合频率是指频率范围在4~7 Hz之间。N1期可以出现缓慢眼球运动,也可以没有眼球运动。颏肌电通常较W期有所降低。如图3所示。
N2期的特征性脑电波为K复合波和梭形波,二者可单独出现,也可出现在同一帧中;有时可见缓慢眼球运动,多数情况无明显眼球运动;颏肌电波幅通常较W期低,有时可达到R期肌电水平。如图4。
N3期的脑电特征波为慢波。顾名思义,这种脑电波频率较慢,在0.5~2 Hz范围内;同时波幅较高,通常>75 μv。如图5。
R期的脑电以低电压混合频率为主,有时会出现散在的α波。R期的特点是在眼动导联出现快眼动,肌电波幅达到整夜睡眠的最低水平。如图6。
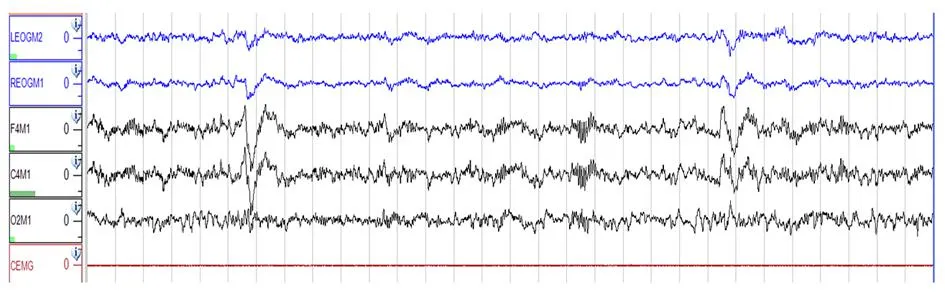
图4 N2期,无明显眼球运动(蓝色);脑电(黑色)可见K复合波和梭形波;颏肌电波幅很低

图5 N3期,无明显眼球运动(蓝色),眼动导联拾取到了很多脑电的慢波活动;脑电(黑色)可见0.5~2 Hz、高波幅的慢波;颏肌电波幅较低
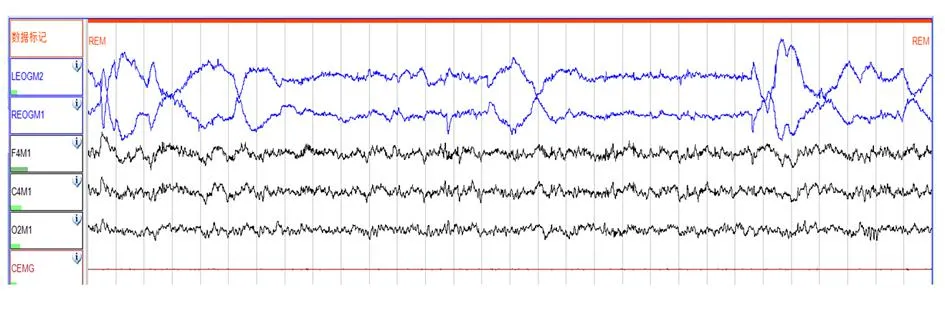
图6 R期,快速眼球运动(蓝色);脑电(黑色)为低电压混合频率;颏肌电波幅非常低
在一整夜的睡眠中,睡眠期并不是绝对地按照“W期-N1期-N2期-N3期-R期”这样的规律变化的。各睡眠期之间是可以互相转化的,可以由W期直接进入N2期,或者由N2期直接进入R期。正常成人除了W期直接转为R期和W期直接转为N3期很少见以外,其他各期之间均能见到互相转化,具体规则见《AASM判读手册》[9-10]。
然而,无论具体的睡眠期怎样转变,从整夜的趋势来看,睡眠是呈现周期性变化的。一个睡眠周期是由NREM睡眠和REM睡眠组成。正常成人先出现NREM睡眠,再出现REM睡眠。一个晚上有3~5个这样的NREM/REM睡眠周期,周期长度约90~100 min[11]。
2控制睡眠-清醒节律的五大神经递质系统
1930年Von Economo在其发表的一篇文章中提到,对因昏睡性脑炎去世的患者进行尸检后发现,凡是下丘脑后部和中脑喙部(rostral midbrain)受损的患者都存在嗜睡,而那些下丘脑前部受损的患者则存在持续性失眠。因此,他认为下丘脑和中脑连接处附近区域含有促进清醒的神经元,下丘脑前部含有促进睡眠的神经元[12-13]。而进一步研究莫如滋的“脑干上行激动系统”(asending activating reticular system)发现,维持清醒这一理论并没有那么简单。在慢性实验中,如果用神经毒素选择性地破坏脑干里的神经细胞却不破坏经过脑干的远程联系,动物虽然会立即进入昏迷状态,可是过一段时间就会从这种状态中恢复清醒。可见还有另外的维持清醒的神经结构。
大脑中特定区域的神经结构需要通过各自相应的神经递质才能实现他们对睡眠和清醒的调控。神经系统的组成有些类似于我们现实社会的公司一样,从员工到老板有着各自的级别和职能。神经系统的基本单位是“神经元”,它就像公司中的员工一样,也同样有高低级别之分。工作中,上司的指令可以通过邮件、电话等方式传递给下一级员工。神经系统的信息(神经冲动)则通过“神经递质”(neurotransmitter)从上一级神经元传递至下一级神经元。不过,中枢神经系统内冲动是单向传递的,即传入神经元传向中继神经元,中继神经元再传向传出神经元。两个神经元相联系的部分称为突触(synapse)。突触前部是发射的神经细胞,突触后部是接收的神经细胞。神经递质由突触前的神经细胞释放至突触间隙,被突触后神经细胞的相应受体摄取,再进入突触后神经细胞,引起突触后神经细胞的电位变化。有的神经递质是兴奋性的,会促进突触后神经元的活动;有的神经递质则是抑制性的,抑制突触后神经元的活动。以下神经递质对于人类维持睡眠和清醒有着重要作用。
2.1五羟色胺(5HT)含有五羟色胺的神经元位于中脑的中缝背核。5HT在醒睡调节中的主要作用是促进清醒[14]。释放5HT的神经元在清醒时兴奋性最高,NREM睡眠时兴奋性减低,REM睡眠时兴奋性最低[15]。除了促进清醒之外,5HT还有很多其他作用。这是因为能够摄取5HT的受体种类很多,目前发现的至少有14种[16]。某些心理疾病和精神疾病的患者需要服用五羟色胺再摄取抑制剂(SSRI)或五羟色胺去甲肾上腺素再摄取抑制剂(SNRI)时,会出现失眠的问题。
2.2去甲肾上腺素(NE)释放NE的神经元主要位于蓝斑(LC)区。NE在醒睡调节中主要起到兴奋性作用,即促进清醒。NE能神经元的兴奋性在清醒时最高,NREM睡眠时较低,而REM睡眠时不兴奋[17]。因此,如果患者服用作用于NE受体的药物,如β受体阻滞剂,可能会影响睡眠质量。
2.3组胺含有组胺的神经元主要位于下丘脑后部的结节乳头核(TMN)。其兴奋性在清醒时最高,NREM睡眠时减低,REM睡眠时消失[18]。可见组胺也是一种促进清醒的神经递质。常用于治疗过敏性疾病的抗组胺药,由于拮抗了突触后神经元“摄取”组胺,因此服药期间易产生困倦感或易瞌睡的现象。
2.4乙酰胆碱胆碱能神经元位于中脑背侧和脑桥的特定区域,是背侧网状激活系统的主要组成部分。这部分的神经元分为2类。一类在清醒和REM睡眠时兴奋,而另一类仅在REM睡眠时兴奋[19-20]。由于这两类神经元的兴奋性受特定睡眠分期的影响,就像有着特定“开关”一样,因此将这两类神经元称为“清醒/REM-on”神经元和“REM-on”神经元。前者只在清醒和REM睡眠时兴奋,NREM睡眠时不兴奋;后者仅在REM睡眠时高度兴奋,其余时段不兴奋[21]。由此可见,乙酰胆碱对醒睡调节的主要作用是促进REM睡眠,也有促清醒的作用。服用胆碱酯酶抑制剂的患者,由于乙酰胆碱分解减少,累积增加,可出现夜间觉醒增多的现象[22]。
2.5多巴胺(DA)释放多巴胺的神经元多位于中脑黑质和腹侧被盖区。DA的释放在睡眠期间内无明显变化,但清醒时很多脑区释放DA明显增多[23]。DA维持清醒的作用机制尚不清楚。帕金森患者由于DA减少,白天可出现过度困倦的症状[24]。
这些神经递质的作用类似“开关”,通过调节皮层和丘脑的神经群体兴奋性实现清醒和不同睡眠状态的转换。除了这些神经递质以外,清醒与睡眠还受到自身昼夜节律的调节,也就是常说的“生物钟”。诸多因素会生物钟对清醒和睡眠的调节,如光照、活动、旅行等。与人体生物钟有关的神经结构将在下一节进行介绍。
(未完待续)
参考文献
[1]Moruzzi G,Magoun HW.Brain stem reticular formation and activation of the EEG[J].Electroencephalogr Clin Neurophysiol,1949,1(4):455-473.
[2]Levi-Montalcini R,Piccolino M,Wade NJ.Giuseppe Moruzzi:A tribute to a“formidable”scientist and a“formidable”man[J].Brain Res Rev,2011 Jan 7,66(1-2):256-269.
[3]Aserinski E.,Kleitman N.,Regularly occurring periods of eye motility,and concomitant phenomena,during sleep[J].Science,1953 Sep 4,118(3062):273-274.
[4]Millett,D.Hans Berger:From Psychic Energy to the EEG[J].Perspectives in Biology and Medicine,2001 Volume 44,Number 4,pp.522-542 The Johns Hopkins University Press.
[5]Rock A.,The Mind at Night:The New Science of How and Why We Dream[M].2004.,Basic Books,Perseus Books Group.中译版:吴妍儀译,梦的科学:解析睡眠中的大脑 2007,台北市猫头鹰书房出版.
[6]Rechtschaffen A,Kales A,eds.A Manual of Standardized Terminology,Techniques,and Scoring System for Sleep Stages of Human Subjects[M].US Department of Health,Education,and Welfare Public Health Service-NIH/NIND.1968.
[7]Meir H.Kryger,Thomas Roth,William C.Dement[M].Principles and practice of sleep medicine 5th ed.P11.
[8]C Iber,S Ancoli-Israel,A Chesson,SF Quan.The AASM Manual for the Scoring of Sleep and Associated Events[M].Westchester,IL:American Academy of Sleep Medicine,2007.
[9]Berry RB,Brooks R,Gamaldo CE,Harding SM,Marcus CL and Vaughn BV for the American Academy of Sleep Medicine[M].The AASM Manual for the Scoring of Sleep and Associated Events:Rules,Terminology and Technical Specifications,Version 2.0.www.aasmnet.org.Darien,Illinois:American Academy of Sleep Medicine,2012.
[10]Berry RB,Brooks R,Gamaldo CE,Harding SM,Lloyd RM,Marcus CL and Vaughn BV for the American Academy of Sleep Medicine[M].The AASM Manual for the Scoring of Sleep and Associated Events:Rules,Terminology and Technical Specifications,Version 2.1.www.aasmnet.Org.Darien,Illinois:American Academy of Sleep Medicine,2014.
[11]Berry RB.fundamentals of sleep medicine[M].IL:Saunders of Elsevier Inc,2012:74.
[12]Von Economo C:Sleep as a problem of localization[J].J Nerv Ment Dis,1930,71:249-259.
[13]Reid A,McCall S,Henry JM,Taubenberger K:Experimenting on the past:the enigma of von Economo 's encephalitis lethargica[J].J Neuropathol Exp Neurol,2001,60:663-670.
[14]Ursin R.Serotonin and sleep[J].Sleep Med Rev,2002,6:57-69.
[15]Espana RA,Scammell TE:Sleep neurobiology for the clinician[J].Sleep,2004,27:811-820.
[16]Meir H.Kryger,Thomas Roth,William C.Dement[M].Principles and practice of sleep medicine 5th ed.P78.
[17]Saper CB,Chou TC,Scammell TE:The sleep switch:hypothalamic control of sleep and wakefulness[J].Trends Neurosci,2001,24:726-731.
[18]Espana RA,Scammell TE:Sleep neurobiology for the clinician[J].Sleep,2004,27:811-820.
[19]Siegel JM:Th e neurobiology of sleep[J].Semin Neurol,2009,29:277-296.5.
[20]McCarley RW:Neurobiology of REM and NREM sleep[J].Sleep Med,2007,8:302-330.
[21]Th akkar MM,Strecker RE,McCarley RW:Behavioral state control through diff erential serotonergic inhibition in the mesopontine cholinergic nuclei:a simultaneous unit recording and microdialysis study[J].J Neurosci,1998,18:5490-5497.
[22]Karczmar AG,Longo A,de Carolis S.A pharmacological model of paradoxical sleep:the role of cholinergic and monoaminergic neurons[J].Physiol Behav,1970,5:175-182.
[23]Berry RB.fundamentals of sleep medicine[M].IL:Saunders of Elsevier Inc,2012:74.
[24]Rye DB,Biwise DL,Dihenia B,et al.Daytime sleepiness in Parkinson’s disease[J].J Sleep Res,2000,9:63-69.

·信息·
欢迎订阅2016年《世界睡眠医学杂志》
《世界睡眠医学杂志》(ISSN 2095-7130、CN 10-1207/R)是经国家新闻出版广电总局批准,由国家中医药管理局主管、世界中医药学会联合会主办的睡眠医学专业学术期刊,是目前国内第一本睡眠医学学术期刊。《世界睡眠医学杂志》的办刊宗旨是发展传统与现代睡眠医学、促进睡眠医学领域国内外信息交流和传播,为宣传和普及科学睡眠知识提供平台,为医学科研和临床应用服务。本刊将及时刊登睡眠医学的基础研究、临床研究的新成果、新经验、新技术和新动态,重视所刊出内容的科学性、先进性、实用性和可读性。
本刊期望业内同仁及各界人士关注《世界睡眠医学杂志》,并欢迎踊跃投稿。详情请参照本刊网站内稿约。
网址:http://www.sjsmyxzz.com:8080; QQ:2867653989
《世界睡眠医学杂志》为大16开本,双月刊,全年6期;每期定价19.00,全年定价114.00元。
邮局汇款方式
地址:北京市西城区广安门内广义街5号广益大厦A座406
邮编:100053
联系人:《世界睡眠医学杂志》编辑部李薇
·病例介绍·
作者单位:262200山东省诸城市精神卫生中心(丁树栋);262200山东省诸城市和平药店总店(管恩兰)
通信作者:管恩兰,Email:yixuekepu@126.com

