山楂叶总黄酮对酒精性肝损伤小鼠肝细胞凋亡的影响
山楂叶总黄酮对酒精性肝损伤小鼠肝细胞凋亡的影响
李素婷吴淑彦1杜超陈龙
(承德医学院生化教研室,河北承德067000)
摘要〔〕目的研究山楂叶总黄酮(FMCL)对酒精性肝损伤小鼠肝细胞凋亡的影响并探讨其机制。方法昆明种小鼠60只随机分为正常组、模型组、FMCL低、高剂量组和维生素E阳性对照组。采用白酒灌胃制备急性肝损伤模型,造模同时按剂量(40、80 mg/kg)每天给予FMCL保护,10 d后处死小鼠,TUNEL法检测肝细胞凋亡情况,HE染色观察肝组织病理学变化,比色法检测肝组织丙二醛(MDA)、超氧化物歧化酶(SOD)、还原型谷胱甘肽(GSH)水平。结果和模型组比较,FMCL明显降低酒精性肝损伤小鼠肝细胞凋亡指数,TUNEL染色阳性细胞数明显减少(P<0.01),肝细胞脂肪变性、炎症坏死等病理改变明显好转;模型组小鼠肝组织MDA含量明显升高,SOD、GSH活性明显降低,给予FMCL保护后,MDA含量明显降低,SOD、GSH活性明显提高(P<0.05,P<0.01)。结论FMCL对酒精性肝损伤小鼠肝细胞凋亡具有一定的抑制作用,其机制与抑制酒精介导的脂质过氧化有关。
关键词〔〕山楂叶总黄酮;酒精性肝损伤;肝细胞凋亡;脂质过氧化
中图分类号〔〕R285.5〔文献标识码〕A〔
基金项目:河北省科学技术研究与发展计划项目(12276104D-93)
1新乐市医院消化科
第一作者:李素婷(1963-),女,医学硕士,教授,硕士生导师,主要从事中药对肝损伤保护作用及其分子机制的研究。
肝脏是酒精代谢的主要器官,过度饮酒会引起酒精性肝损伤。研究表明,酒精引起的氧化应激介导的肝细胞凋亡在酒精性肝损伤的发生、发展中发挥重要的作用〔1〕。抑制肝细胞凋亡有利于酒精性肝损伤的防治,也是抗酒精性肝纤维化一种治疗方法。山楂叶总黄酮(FMCL)是从山楂叶中提取的黄酮类化合物,含有黄酮苷、荭草素、葡荆牡黄酮等多种抗氧化成分,具有很强的清除自由基抗脂质过氧化作用〔2〕,对大鼠脑缺血再灌注后细胞凋亡具有保护作用〔3〕。本研究观察FMCL对酒精所致小鼠急性肝损伤肝细胞凋亡的保护作用及其机制。
1材料与方法
1.1动物、药品及仪器昆明种小鼠,雄性,清洁级,体重(22±2)g,石家庄实验动物管理中心提供。FMCL(纯度为80%):北京中医药大学馈赠,临用前以蒸馏水配置,4℃保存;56°红星二锅头白酒:北京红星酿酒厂生产; 丙二醛(MDA)、超氧化物歧化酶(SOD)、还原型谷胱甘肽(GSH),购于南京建成生物工程研究所;TUNEL细胞凋亡原位检测试剂盒,由南京凯基生物科技发展有限公司提供;Olympus显微镜和组织切片机:德国Leica公司。
1.2动物造模与药物处理〔4〕将60只昆明种小鼠随机分为5组,分别为正常组、模型组、FMCL小剂量(40 mg/kg)组、FMCL大剂量(80 mg/kg)组和维生素E(100 mg/kg)阳性对照组。正常组每天给予蒸馏水0.4 ml灌胃,模型组和给药组按8 ml/kg灌胃给予56°红星二锅头白酒,2次/d,连续10 d造模结束。自造模第1天起,FMCL组和维生素E组按剂量每天中午灌胃给药1次,正常组和模型组同时灌服等体积蒸馏水,实验期间各组小鼠自由饮水、进食。最后一次灌胃结束,禁食不禁水14 h,断头处死小鼠。
1.3TUNEL法检测肝细胞凋亡情况TUNEL法按试剂盒说明书进行操作。凋亡的肝细胞多表现为胞膜完整、核改变,细胞核呈棕黄色染色或细胞质因核DNA逸出而呈阳性染色者为凋亡细胞,肝细胞凋亡小体也呈阳性着色。每例标本选5个高倍视野(400倍)观察凋亡细胞,计数不少于500个细胞,观察并计数阳性凋亡细胞核数占该视野肝细胞核总数的比例,取均值以百分数表示,以凋亡指数(AI)反映肝细胞凋亡情况。
1.4肝组织病理学学观察取小鼠肝左叶,置10%中性甲醛溶液中固定,常规石蜡包埋、切片机切片,HE染色,光镜下观察肝组织脂肪变性和炎症、坏死等病理改变。
1.5肝组织MDA、SOD、GSH水平的检测取小鼠肝左叶,以生理盐水制备成10%的肝匀浆,比色法检测肝匀浆MDA含量和SOD、GSH活性。
1.6统计学处理采用SPSS17.0软件进行t检验。
2结果
2.1FMCL对酒精引起小鼠肝细胞凋亡的保护作用正常组小鼠肝组织无或偶见肝细胞凋亡〔(2.92±0.88)%〕;模型组小鼠肝组织中可见大量棕黄色、棕褐色凋亡细胞核,肝细胞AI比正常组明显升高〔(11.41±1.13)%,P<0.01〕;FMCL小、大剂量组肝细胞凋亡阳性细胞数目明显减少,染色强度减弱,AI明显降低〔(9.78±2.43)%、(7.96±1.84)%,P<0.01,P<0.05〕,并呈现剂量依赖关系,表明FMCL能明显抑制酒精诱发的肝细胞凋亡,维生素E阳性对照组肝细胞AI为(7.64±2.23)%,较模型组明显改善(P<0.01)。见图1。
2.2FMCL对酒精引起小鼠肝组织病理学改变的保护作用各组小鼠肝组织切片HE染色后在光学显微镜下观察:正常组,肝小叶结构清晰,肝细胞呈索状排列,肝细胞无明显病变;模型组,肝组织结构紊乱,肝小叶界限模糊,肝细胞明显肿胀,胞质疏松化弥漫存在,并伴有肝细胞核浓缩、核碎裂,肝组织内有炎症细胞浸润;FMCL各剂量组,肝细胞胞质疏松化明显减轻,细胞轻度肿胀,未见明显的脂肪变性和炎症细胞浸润;维生素E阳性对照组,可见少量肝细胞胞质疏松化,肝细胞炎症反应明显减轻,肝细胞结构基本正常。见图2。
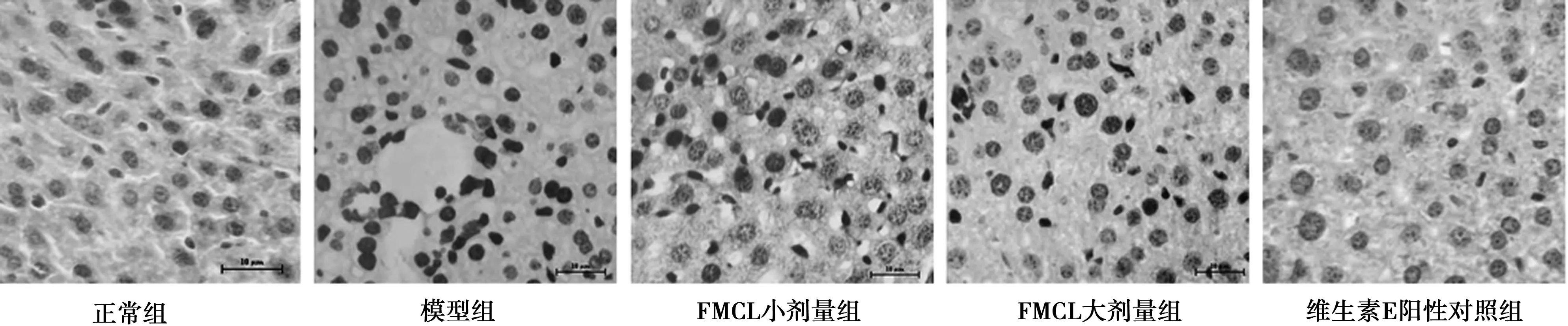
图1 FMCL对酒精性肝损伤小鼠肝细胞凋亡的影响(TUNEL,×400)

图2 FMCL对酒精性肝损伤小鼠肝细胞病理改变的影响(HE,×400)
2.3FMCL对酒精引起小鼠脂质过氧化的保护作用见表1。与正常组比较,模型组小鼠肝组织中MDA含量明显升高,SOD、GSH活性明显降低,表明急性酒精性肝损伤伴有显著的脂质过氧化反应;而给予FMCL保护后,肝组织MDA含量明显降低,SOD、GSH活性明显升高,表明FMCL可提高内源性抗氧化剂的活性,具有明显的清除自由基,抗脂质过氧化作用。
表1 FMCL对肝组织MDA含量及SOD、GSH
与正常组比较:1)P<0.01,与模型组比较:2)P<0.05,3)P<0.01
3讨论
细胞凋亡又称程序化细胞死亡(PCD),是细胞在一定的生理或病理信号刺激下遵循自身程序,由基因控制的自主性死亡方式。凋亡与增殖的动态平衡是维系正常组织自稳态的一个基本过程。近年来研究发现细胞凋亡与各种肝脏疾病的发生密切相关,肝细胞的异常凋亡在酒精性肝病的发生与发展中起重要作用〔5〕。而促氧化物增多和抗氧化物减少造成的氧化应激是酒精性肝病肝细胞凋亡的主要机制之一〔6〕。
酒精介导的肝细胞凋亡在酒精性肝损伤的发病机制中扮演重要角色〔7〕。长期或大量饮酒时,酒精在肝微粒体经细胞色素P4502E1代谢时产生大量活性氧自由基(如O2-·、OH-·、C2H5O-·和C2H5OH-·等),活性氧介导脂质过氧化连锁反应,产生大量脂质过氧化终产物MDA,对肝细胞产生毒性,引起肝细胞凋亡。酒精在肝内代谢及活性氧的产生主要在线粒体,线粒体DNA对氧自由基攻击高度敏感,可引起线粒体DNA广泛缺失而形成线粒体DNA微环,并破碎成数百个微环碎片,是肝细胞发生凋亡的前提。活性氧还能改变线粒体膜渗透性,通过释放凋亡相关蛋白细胞色素C和其他凋亡相关因子,活化Caspase蛋白与凋亡效应分子结合,诱导肝细胞发生凋亡。活性氧亦可活化NF-κB等信号通路,通过上调P53、Bax及Caspase-3等促凋亡因子基因的表达,介导肝细胞凋亡〔8,9〕。肝细胞凋亡可直接导致大量肝细胞的减少,并可激活肝组织炎症和(或)坏死,最终导致肝功能严重损伤〔10〕。
正常肝组织内存在多种抗氧化物质,其中以SOD和GSH在抵抗酒精所致的肝损伤中起关键作用。SOD能有效清除自由基,保护细胞不受自由基侵害。GSH是肝细胞内游离存在的小分子抗氧化剂,能直接和氧自由基起反应,并作为谷胱甘肽过氧化物酶的特异性底物,还原体内已生成的自由基〔11〕。许多研究证实GSH等内源性抗氧化剂能够对抗乙醇引起的肝细胞凋亡〔12,13〕。但是,当产生的活性氧自由基超过SOD、GSH等抗氧化因子的清除能力时,便可由氧应激损伤线粒体或活化促凋亡因子基因的表达,诱导肝细胞凋亡。因此,提高内源性抗氧化剂含量,清除自由基,抑制氧应激介导的肝细胞凋亡,是防治酒精性肝损伤的关键所在。
本研究结果表明小鼠急性酒精性肝损伤的形成是由于肝细胞异常凋亡所致,FMCL通过抑制肝细胞凋亡起到保肝护肝作用。FMCL能明显降低酒精介导的脂质过氧化产物MDA含量的升高,明显提高内源性抗氧化剂SOD、GSH的活性,具有较强的清除自由基的抗氧化能力。表明FMCL通过提高内源性抗氧化剂水平,抑制了氧化应激诱导的肝细胞异常凋亡,这可能是FMCL对酒精性肝损伤起保护作用的重要机制之一。
参考文献4
1程凤丹,刘红云,刘丽君,等.两个时间段的急性酒精性肝损伤与肝细胞凋亡〔J〕.广东医学,2010;31(13):1641-3.
2刘寿先,徐金彰.山楂叶总黄酮对小鼠的抗氧化作用〔J〕.咸阳学院学报(医学版),2006;20(6):477-9.
3纪影实,曲极冰,李红,等.山楂叶总黄酮对大鼠脑缺血再灌注后细胞凋亡的保护作用〔J〕.吉林大学学报,2008;34(4):590-3.
4赵敏,迟丽萍,王凤岩,等.小鼠急性酒精性肝损伤模型的建立及应用〔J〕.华南预防医学,2005;3(1):14-7.
5Schattenberg JM,Galle PR,Schuchmann M.Apoptosis in liver disease〔J〕.Liver Int,2006;26(8):904-11.
6朱传龙,高人焘,李宜.凋亡及其调控基因bcl-2家族在肝脏损伤中的作用〔J〕.使用肝脏杂志,2008;11(6):206-9.
7Slomiany A,Piotrowski E,Grabska M,etal.Chronic ethanol-initiated apoptosis in hepatocytes is induced by changes in membrane biogenesis and intracellular transport〔J〕.Alcohol Clin Exp Res,1999;23(2):334.
8安红姬,金武丕.乙醇诱发肝细胞凋亡的发病机制〔J〕.吉林医学,2007;28(8):1155-7.
9张志勇,金武丕,徐晓俊.核转录因子-κB与酒精性肝病的研究进展〔J〕.临床肝胆病杂志,2010;26(3):269-71.
10肖卫东.细胞凋亡及其相关因素在酒精性肝病中的作用〔J〕.国外医学临床生化与检验分册,2002;23(3):161-3.
11柳海艳,种赣生,李怡文,等.醇提和水提葛花枳椇子及其配伍对酒精性肝损伤大鼠肝脏抗氧化功能的影响〔J〕.中华中医药杂志,2012;27(4):1181-4.
12Masalkar PD,Abhang SA.Oxidative stress and antioxidant status in patients with alcoholic liver disease〔J〕.Clin Chim Acta,2005;355(1-2):61-5.
13Woo SH,Park IC,Park MJ,etal.Arsenic trioxide induces apoptosis through a reactive oxygen species-dependent pathway and loss of mitochondria embrane potential in HeLa cells〔J〕.Int J Oncol,2002;21(1):57.
〔2013-09-28修回〕
(编辑赵慧玲/曹梦园)

