艾迪注射液联合多西他赛、卡铂化疗方案对非小细胞肺癌的近期疗效及血清SIL-2R、CEA、VEGF水平的影响
艾迪注射液联合多西他赛、卡铂化疗方案对非小细胞肺癌的近期疗效及血清SIL-2R、CEA、VEGF水平的影响
胡其艳漆辉雄
作者单位:441000 湖北省襄阳市中心医院
【摘要】目的探讨艾迪注射液联合多西他赛、卡铂方案对非小细胞肺癌的临床疗效及作用机制。方法将70例非小细胞肺癌患者随机分为观察组35例和对照组35例。对照组采用多西他赛、卡铂方案,观察组在对照组基础上联合艾迪注射液。比较2组患者临床疗效、生存质量、不良反应发生情况,并记录2组患者治疗前后血清可溶性白介素2受体(SIL-2R)、癌胚抗原(CEA)和血管内皮生长因子(VEGF)水平。结果观察组总有效率为31.43%,临床受益率为94.29%;对照组总有效率为28.57%,临床受益率为85.71%。组间临床疗效相比,差异无统计学意义(χ2=0.195,P=0.659);观察组临床受益率显著高于对照组(χ2=4.089,P=0.043)。观察组生理功能、情感功能、社会功能得分显著提高,疲劳,疼痛,恶心呕吐得分显著优于对照组(P<0.05);治疗后2组患者血清SIL-2R、CEA、VEGF水平均显著降低(P<0.05),其中观察组SIL-2R、CEA、VEGF水平显著低于对照组(P<0.05)。2组患者主要不良反应包括骨髓抑制(白细胞减少、血小板减少)、消化道反应(恶心、呕吐、腹泻)和口腔黏膜炎等,其中观察组血小板减少发生率显著低于对照组(χ2=8.363,P=0.004)。结论艾迪注射液能够提高非小细胞肺癌患者生存质量,降低不良反应发生,可以作为非小细胞肺癌化疗的一种重要辅助用药。
【关键词】艾迪注射液;化疗;非小细胞肺癌;肿瘤标志物
通讯作者:漆辉雄
DOI:10.3969/j.issn.1001-5930.2015.10.013
中图分类号:R734.2
收稿日期(2014-12-22修回日期 2015-03-25)
Clinical Efficacy and Serum SIL-2R、CEA、VEGF Level Changes of Addie Injection
Combined with Docetaxel and Carboplatin for NSCLC
HUQiyan,QIHuixiong.TheCentralHospitalofXiangyang,Xiangyang,441000
Abstract【】ObjectiveTo explore the the clinical efficacy and serum SIL-2R,CEA,VEGF level changes of addie injection combined with docetaxel and carboplatin for non-small cell lung cancer (NSCLC).Methods70 cases of NSCLC were randomly divided into the experimental group and the control group,each with 35 cases.The control group received docetaxel and carboplatin,the experimental group received addie injection based on the control group.Clinical efficacy,quality of life and adverse reactions of the 2 groups were compared,and serum SIL-2R,CEA,VEGF levels of the 2 groups before and after treatment were recorded.Results In the experimental group,the total effective rate was 31.43%,the clinical benefit rate was 94.29%; in the control group,the total effective rate was 28.57%,the clinical benefit rate was 85.71%,there had no significant difference in clinical efficacy between the 2 groups (χ2=0.195,P=0.659),the clinical benefit rate of the experimental group was significantly higher than that of the control group (χ2=4.089,P=0.043).Serum SIL-2R,CEA,VEGF levels of the 2 groups after treatment were significantly lower,and those of the experimental group were significantly lower than those of the control group(P<0.05).Physiological function,emotional function and social function scores in the experimental group after treatment improved significantly,fatigue,pain,nausea and vomiting in the experimental group were superior to the control group (P<0.05); main adverse reactions of the 2 groups were bone marrow suppression (leukopenia,thrombocytopenia),gastrointestinal reactions (nausea,vomiting,diarrhea)and oral mucositis.Thrombocytopenia in the experiment group was significantly lower than that of the control group (χ2=8.363,P=0.004).ConclusionAddie injection for NSCLC can improve quality of life,reduce adverse reactions,and it can be used as an important adjuvant chemotherapy for NSCLC.
【Key words】Addie injection;Chemotherapy;Non-small cell lung cancer(NSCLC);Tumor markers
(ThePracticalJournalofCancer,2015,30:1469~1472)
肺癌是临床上常见的恶性肿瘤,其中非小细胞肺癌(non-small-cell carcinoma)占肺癌发病率的70%~80%[1]。由于患者就诊时往往进入晚期而丧失最佳手术时机,因而放化疗成为NSCLC治疗的主要方式。但是放化疗的毒副作用较大,患者常因无法耐受而放弃治疗,如何减少放化疗的毒副作用、提高疗效成为临床肿瘤治疗的热点。大量研究显示[2],中医药在改善肿瘤患者体征、提高患者生活质量方面具有显著作用,已成为肿瘤辅助治疗的主要手段。本研究对NSCLC患者采用艾迪注射液联合多西他赛、卡铂化疗方案治疗,并分析SIL-2R、CEA、VEGF变化水平,探讨艾迪注射液对NSCLC的疗效及作用机制。
1材料与方法
1.1一般资料
将2010年7月至2013年7月在我院住院治疗的NSCLC患者70例作为研究对象,男性41例,女性29例;年龄34~76岁,平均(52.6±7.3)岁;其中鳞癌31例,腺癌28例,腺鳞癌8例,大细胞癌3例;初治51例,复治19例;按照TMN分期:ⅢB期37例,Ⅳ期33例。纳入标准:①符合NSCLC诊断标准[3],并经细胞学、病理学证实;②具有明确可测量病灶;③功能状态评分(KPS评分)≥60分;④预计生存期≥3个月;⑤无相关化疗禁忌证;⑥取得患者或家属同意,并签署知情同意书。排除标准:①肝、肾功能异常;②对化疗药物无法耐受者;③预计生存期<3个月;④其他不符合条件者。将70例患者按照随机数字表法分为观察组35例和对照组35例,2组患者性别、年龄、病理分期等一般资料差异无统计学意义(P>0.05),具有可比性。
1.2方法
对照组采用多西他赛、卡铂方案:静脉滴注多西他赛(扬子江药业集团有限公司,0.5 ml:20 mg)75 mg×m-2,第1天,每次1 h;卡铂AUC=5 mg×ml-1×min-1,第2天,静脉滴注;连续治疗3 w为1个周期。治疗期间常规给予昂丹司琼、托拉司琼止吐。观察组在对照组基础上联合艾迪注射液(贵州益佰制药股份有限公司,10 ml/支)50 ml溶于250 ml生理盐水中静脉滴注,每日1次,连用2 w,治疗3 w为1个周期。2组患者均完成2个周期化疗,2个周期后进行评价。
1.3观察指标
⑴采用WHO实体瘤客观疗效标准[4]将疗效分为:完全缓解(CR):所有可见病变完全消失并至少维持4周以上;部分缓解(PR):肿瘤病灶的最大径及其最大垂直径的乘积减少50%以上,维持4周以上;稳定(SD):肿瘤病灶两径乘积缩小<25%,或增大<25%,无新病灶出现;病变进展(PD):肿瘤病灶两径乘积增大>25%,或出现新病灶;其中总缓解率=CR+PR;临床获益率=CR+PR+SD。⑵采用欧洲癌症治疗研究组(EORTC)制定的肿瘤生存质量调查表[5](QLQ-C30)对患者生存质量进行评价,该量表由30个问题构成,分别从5种功能(生理、日常生活、认知、情感和社会功能),3种症状(疲劳、疼痛、恶心呕吐)对患者的生存质量进行测量,其中功能量表得分越高代表患者生存质量越高,症状量表得分越高代表患者生存质量越低。⑶取患者静脉血3 ml,高速离心分离血清后,于-80 ℃冰箱中保存待检。采用酶联免疫吸附试验(ELISA)对患者血清可溶性白介素2受体(SIL-2R)、癌胚抗原(CEA)和血管内皮生长因子(VEGF)进行检测,相关试剂盒由上海超研生物科技有限公司提供;操作参考试剂盒说明书。⑷记录2组患者不良反应。
1.4统计学方法
数据采用SPSS 17.0统计学软件包进行统计分析,计量资料以(±s)表示,率的比较采用χ2检验,组间比较采用t检验,多组间比较采用秩和检验分析样本间的差异,以P<0.05为差异有统计学意义。
2结果
2.12组患者近期疗效比较
观察组总有效率为31.43%,临床获益率为94.29%;对照组总有效率为28.57%,临床获益率为85.71%。2组间临床疗效相比差异无统计学意义(χ2=0.195,P=0.659),观察组临床获益率显著高于对照组(χ2=4.089,P=0.043),见表1。
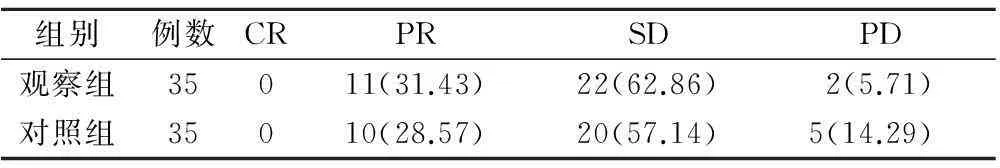
表1 2组患者近期疗效比较(例,%)
2.22组患者治疗前后生存质量评分比较
治疗后2组患者生理功能、情感功能、社会功能得分显著提高,疲劳,疼痛,恶心呕吐得分显著降低(P<0.05),其中观察组各项目得分显著优于对照组(P<0.05),见表2。
表2 2组患者治疗前后生存质量评分比较(分, ± s)
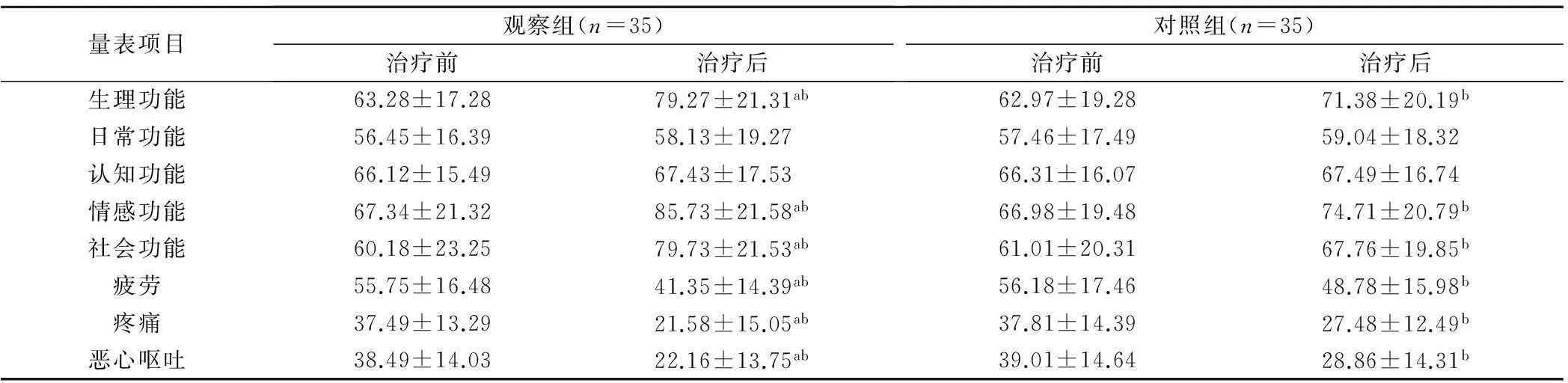
表2 2组患者治疗前后生存质量评分比较(分, ± s)
量表项目观察组(n=35)治疗前治疗后对照组(n=35)治疗前治疗后生理功能63.28±17.2879.27±21.31ab62.97±19.2871.38±20.19b日常功能56.45±16.3958.13±19.2757.46±17.4959.04±18.32认知功能66.12±15.4967.43±17.5366.31±16.0767.49±16.74情感功能67.34±21.3285.73±21.58ab66.98±19.4874.71±20.79b社会功能60.18±23.2579.73±21.53ab61.01±20.3167.76±19.85b疲劳55.75±16.4841.35±14.39ab56.18±17.4648.78±15.98b疼痛37.49±13.2921.58±15.05ab37.81±14.3927.48±12.49b恶心呕吐38.49±14.0322.16±13.75ab39.01±14.6428.86±14.31b
注:b为与治疗前相比,P<0.05;a为与对照组比较,P<0.05。
2.32组患者治疗前后血清SIL-2R、CEA、VEGF比较
治疗后2组患者血清SIL-2R、CEA、VEGF水平均显著降低(P<0.05),其中观察组SIL-2R、CEA、VEGF水平显著低于对照组(P<0.05),见表3。
表3 2组患者治疗前后血清SIL-2R、CEA、VEGF比较( ± s)

表3 2组患者治疗前后血清SIL-2R、CEA、VEGF比较( ± s)
组别时段SIL-2R/(U·ml-1)CEA/(ng·ml-1)VEGF/(ng·ml-1)观察组(n=35)治疗前617.3±131.534.71±12.190.36±0.07治疗后279.7±67.3ab3.76±1.07ab0.23±0.02ab对照组(n=35)治疗前627.1±172.835.81±11.530.35±0.08治疗后368.4±81.5b10.37±7.69b0.29±0.04b
注:b为与治疗前相比,P<0.05;a为与对照组比较,P<0.05。
2.42组患者不良反应发生情况比较
2组患者主要不良反应包括骨髓抑制(白细胞减少、血小板减少)、消化道反应(恶心、呕吐、腹泻)和口腔黏膜炎等,其中观察组血小板减少发生率显著低于对照组(χ2=8.363,P=0.004),见表4。
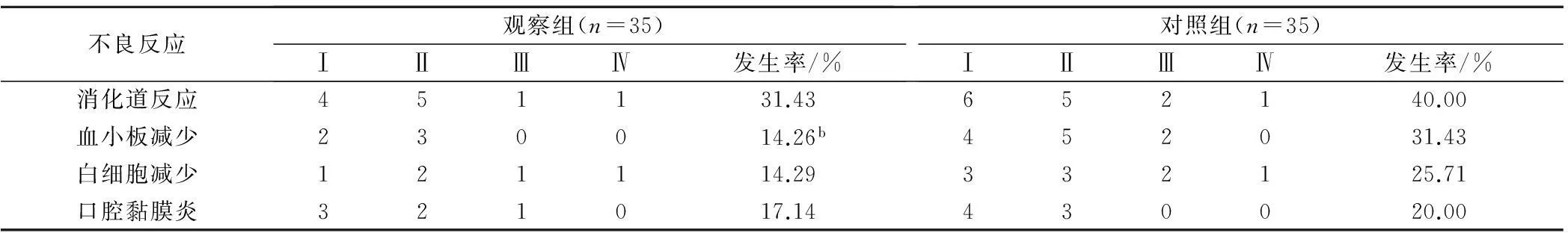
表4 2组患者不良反应发生情况比较/例
注:b为与对照组相比,P<0.05。
3讨论
约有70%以上非小细胞肺癌患者就诊时已是中晚期,丧失了最佳手术时机,放化疗则成为主要治疗手段。大量研究证实[6],以卡铂或顺铂为主的化疗方案能够显著改善NSCLC患者病情、提高生活质量。但是铂类药物虽然抗癌活性强,但是毒副作用依然明显,主要包括胃肠道反应及肾毒性,因此常与其他药物联合使用。多西他赛对于多种肿瘤均有较强的治疗作用,如乳腺癌、肺癌、食管癌等。研究显示[7]多西他赛单药治疗NSCLC的总有效率为21%~40%,而与铂类联合化疗有效率则显著提高至35%~59%。但是两种药物杀伤癌细胞的同时对正常机体细胞、组织也有一定影响,导致患者免疫功能下降、生活质量降低;部分患者甚至无法耐受而停止治疗,使其丧失最后治疗机会。寻找一种既能提高疗效,又能降低不良反应的药物是目前治疗肿瘤的热点之一。
艾迪注射液是利用现代技术将黄芪、刺五加、人参、斑蝥中的活性成分提取精制而成的抗肿瘤药。基础研究表明[8],艾迪注射液主要含有人参多糖、皂苷、黄芪多糖等成分,具有提高机体免疫力、促进肿瘤细胞凋亡、逆转化疗药物耐药性、保护骨髓等作用。严虹霞等[9]证实,艾迪注射液中多糖成分能够激活人体自然杀伤细胞、巨噬细胞的活性,诱导肿瘤坏死因子、干扰素的产生,提高机体免疫功能,起到杀灭肿瘤细胞的作用。张金梅等[10]也发现,斑蝥中的去甲斑蝥素能够抑制细胞蛋白质的合成,降低癌细胞的浸润转移。潘琪等[11]在实验中发现,去甲斑蝥素能够刺激骨髓造血干细胞的成熟分化,具有一定的升高白细胞作用。
本研究结果显示虽然观察组与对照组总有效率相比无显著差异,但观察组临床获益率显著高于对照组,说明艾迪注射液能够与化疗药物起到协同治疗的作用,共同提高患者的疗效。本研究中,治疗后观察组生理功能、情感功能、社会功能得分显著提高,疲劳,疼痛,恶心呕吐得分显著降低,且显著优于对照组,说明艾迪注射液具有改善NSCLC患者生存质量的作用,这对提高患者治疗依从性、缓解患者病痛具有重要意义。此外观察组血小板减少发生率也显著低于对照组,进一步证实了艾迪注射液治疗NSCLC的安全性。
肿瘤标志物不仅可以用作诊断肿瘤,还能作为肿瘤预后的一项敏感评价指标。SIL-2R是存在于血清和尿液中的P55蛋白,由活化的淋巴细胞表面脱落;SIL-2R能够作为IL-2的载体,并与IL-2结合延长其半衰期。因此SIL-2R可以反映出机体的免疫状态;Kanazawa等[12]亦证实肺癌患者血清SIL-2R显著升高,并认为SIL-2R可以作为肺癌增殖活性的标志。VEGF能够诱导血管形成,是一种特异性较强的血管生长因子。Zhang等[13]证实,肺癌组织中VEGF呈现高表达,且与肿瘤血管计数正相关。Farhat等[14]也发现,多种实体瘤及转移的癌症患者血清VEGF浓度显著升高。CEA是一种广谱性肿瘤标志物,它能向人们反映出多种肿瘤的存在,对大肠癌、乳腺癌和肺癌的疗效判断、病情发展、监测和预后估计是一个较好的肿瘤标志物。本研究提示艾迪注射液治疗NSCLC的作用机制可能与提高机体免疫力、抑制肿瘤血管形成、促进肿瘤细胞凋亡有关。
综上所述,艾迪注射液能够提高非小细胞肺癌患者生存质量,降低不良反应发生,可以作为NSCLC化疗的一种重要辅助用药。
参考文献
[1]Koo CW,Miller WT,Kucharczuk JC.Focal ground-glass opacities in non-small cell lung carcinoma resection patients〔J〕.Eur J Radiol,2012,81(1):139-145.
[2]庄静,孙长岗,梁艳,等.肿瘤干细胞学说及相关性中药作用机理的研究〔J〕.世界中西医结合杂志,2013,8(3):275-278.
[3]Machtay M,Bae K,Movsas B,et al.Higher biologically effective dose of radiotherapy is associated with improved outcomes for locally advanced non-small cell lung carcinoma treated with chemoradiation: An analysis of the radiation therapy oncology group〔J〕.Int J Radiat Oncol Biol Phys,2012,82(1):425-434.
[4]杨旭,许光,雷振,等.RECIST1.1与WHO、RECIST1.0标准评价周边型肺癌疗效比较〔J〕.中国医学影像学杂志,2012,20(5):355-358,362.
[5]Kim EJ,Ko SK,Kang HY.Mapping the cancer-specific EORTC QLQ-C30 and EORTC QLQ-BR23 to the generic EQ-5D in metastatic breast cancer patients〔J〕.Qual Life Res,2012,21(7):1193-1203.
[6]田艳,田中,吴柯,等.恩度联合含铂类化疗药物治疗晚期非小细胞肺癌的疗效及安全性的Meta分析〔J〕.重庆医科大学学报,2012,37(2):151-157.
[7]Atmaca A,Al-Batran SE,Werner D,et al.Arandomisedmulticentre phase Ⅱ study with cisplatin/docetaxelvsoxaliplatin/docetaxel as first-line therapy in patients with advanced or metastatic non-small cell lung cancer〔J〕.Br J Cancer,2013,108(2):265-270.
[8]李涛,王涛,张锡朋,等.艾迪注射液对结肠癌裸鼠移植瘤生长的抑制作用及对COX-2、VEGF、MMP-9蛋白表达的影响〔J〕.中国老年学杂志,2013,33(16):3911-3912.
[9]严虹霞,杨广文,刘如良,等.艾迪注射液联合化疗对肺癌患者免疫功能的影响〔J〕.中国药物与临床,2012,12(9):1123-1124.
[10]张金梅,吴杰,常城,等.去甲斑蝥素对肝癌细胞增殖和凋亡的影响〔J〕.中国肿瘤生物治疗杂志,2011,18(1):33-37.
[11]潘琪,高志棣,周强,等.去甲斑蝥素的抗肿瘤作用机制及临床应用进展〔J〕.齐鲁医学杂志,2012,27(6):555-556,559.
[12]Kanazawa S,Yamaguchi K,Kinoshita Y,et al.Elevation of soluble interleukin-2 receptor in patients with non-small cell lung cancer treated with gefitinib〔J〕.J Cancer Res Clin Oncol,2006,132(11):719-725.
[13]Zhang H,Yun S,Batuwangala TD,et al.A dual-targeting antibody against EGFR-VEGF for lung and head and neck cancer treatment〔J〕.Int J Cancer,2012,131(4):956-969.
[14]Farhat FS,Tfayli A,FakhruddinN,et al.Expression,prognostic and predictive impact of VEGF and bFGF in non-small cell lung cancer〔J〕.Crit Rev Oncol Hematol,2012,84(2):149-160.
(编辑:甘艳)

