心尖轴流泵的结构和性能的比较
李国荣,朱晓东,陈海丰,田步升,彭远仪
心尖轴流泵的结构和性能的比较
李国荣,朱晓东,陈海丰,田步升,彭远仪
目的:比较不同结构心尖轴流泵的流体力学及溶血特性差异。方法:在体外模拟循环台上测试外形尺寸相似的4种不同结构的轴流泵(包括单滑动面球支点、双滑动面球支点心尖轴流泵及保留后导叶和无后导叶的全悬浮心尖轴流泵)的流体力学和溶血特性。结果:单滑动面球支点心尖轴流泵和双滑动面球支点心尖轴流泵的流体力学特性及溶血特性相似,均可在11 000 r/min条件下产生100 mmHg(1 mmHg=133.32 Pa)的压力输出和5 L/min的流量输出,标准溶血指数(normalized index of hemolysis,NIH)分别为0.023和0.025 g/100 L。在产生相同压力和流量输出条件下,两型全悬浮心尖轴流泵转速明显增加,保留后导叶的全悬浮心尖轴流泵和无后导叶的全悬浮心尖轴流泵转速分别为17 000和23 000 r/min,NIH分别为0.072和0.13 g/100 L。结论:单滑动面球支点心尖轴流泵结构简单、效率高、溶血强度低,可作为心尖轴流泵的结构选择;双滑动面球支点心尖轴流泵结构优势尚需在长时间体内植入实验中证实。悬浮心尖轴流泵体积较小,但效率较低,溶血作用强,保留后导叶可明显提高悬浮心尖轴流泵效率,降低溶血强度。
血泵;心室辅助;悬浮轴流泵;人工心脏
0 引言
近年来,以旋转叶轮式血泵(rotary blood pump)为基础的植入式心脏辅助装置在临床中的应用取得了很大成功。旋转叶轮式血泵主要包括轴流泵和离心血泵,与早期的搏动血泵式心脏辅助装置不同,旋转叶轮式血泵输出持续性血流,具有体积小、结构简单和能量转化效率较高等优点,目前国内外不少研究者正致力于旋转叶轮式血泵的研发[1-4]。
心脏辅助装置的体内植入方式对并发症及治疗效果均有重要的意义。由于旋转叶轮式血泵的体积小,所以可提供多种体内植入方式供选择,便于临床应用。比如,轴流泵和离心血泵不仅可按传统的方式植入到胸腔外的上腹壁内,还可直接植入到胸腔内、心包腔内甚至心室腔内。去除血泵的入口引流管道,不仅可减少体内异物,缩小血液与异物的接触面积,而且可直接引流心室腔,减小入口阻力,是较好的植入方式。国外的 Jarvik 2000[5]轴流泵及 HeartWare HVAD[6]离心血泵均采用这种连接方式,但仍需进一步改进。Jarvik 2000轴流泵将泵体全部植入心室腔内,心室内异物较多,增加了心室内血栓形成的危险。而HeartWare HVAD离心血泵的泵体完全位于心包腔内,对体形较小的患者来说植入难度较大。我们曾经提出心尖轴流泵[7-9],仅将一部分泵体置于心室腔内,其余部分位于心包腔(如图1所示)。这种植入方式既去除了入口引流管道,又减少了心室腔内异物,还可避免对胸腔内器官的压迫和粘连。
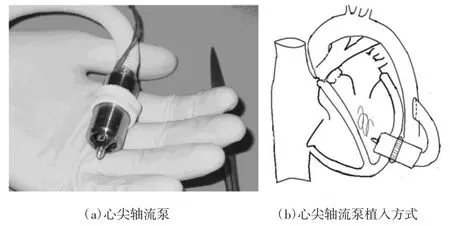
图1 心尖轴流泵及其植入方式示意图
由于心尖轴流泵植入位置特殊,因此对体积要求较为苛刻。从理论上看,减小泵体积和提高血泵性能是优化设计时需要仔细权衡的矛盾。轴流泵体积减小后叶轮的转速必须相应增加才能维持足够的流量和压力输出。但较高的叶轮转速将增大轴承的机械摩擦,且叶轮对血细胞的损伤也有加重的趋势。我们在心尖轴流泵研制的优化过程中曾采用不同的叶轮支撑技术,以满足较高叶轮转速的要求。早期的心尖轴流泵采用机械轴承,近期则采用全悬浮技术。本文旨在比较研究应用不同的支撑技术时心尖轴流泵的流体力学和溶血特性的差异,为心尖轴流泵的进一步优化提供基础。
1 材料和方法
心尖轴流泵的基本结构已在先前的文献[10-12]中描述,本文用于比较的各种心尖轴流泵的结构尺寸相近。轴流泵筒内径12 mm;叶轮外径11.8 mm;转子由钕铁硼永磁材料制成,直径7.5 mm,长19 mm,充磁后最大表磁为435 mT。电动机定子外径18 mm,采用三相空心杯式绕组;电动机最大外径18.8 mm,长度65~70 mm,总质量95~120 g。
1.1 机械轴支撑的心尖轴流泵
轴流泵的轴承工作时浸泡在血液中,对其基本要求是在高速运行时不对血液成分造成强烈破坏,也不被血液蛋白沉积物阻塞。常见的滚珠轴承显然不适合轴流泵选用,最常采用的是滑动轴承,比如美国的MicroMed DeBakey VAD[3]、HeartMateⅡ[4]、Jarvik 2000[5]等轴流泵均采用滑动轴承作为旋转叶轮的支撑装置。滑动轴承又可有多种结构形式,我们在早期的研究中观察到常用的“轴套-轴杆”式滑动轴承性能不佳,血液中的蛋白沉积物容易使轴承堵塞,增大阻力和能量消耗,有时甚至可造成叶轮停转。“球-窝”式滑动轴承较适合轴流泵,最早为美国的“Heart-MateⅡ”轴流泵所采用。在“球-窝”式滑动轴承基础上,我们提出了“球支点”轴承,以期获得更佳的效果。“球支点”轴承是一种简化的“球-窝”式滑动轴承,球支点在高速旋转时有“钻头”样效应,有利于随时清除沉积在滑动面上的血液蛋白,故可防止摩擦阻力的不断增加和叶轮停转。滑动轴承的重要缺点是机械磨损和局部产热。由于直接的机械滑动摩擦可使滑动面形状改变,并使间隙性能下降,达到一定程度时使支撑作用失效。机械摩擦在局部产生的热量可使血液接触面温度升高,可加速血小板和凝血相关因子的激活,在局部形成血栓生长点。因此,尽可能降低滑动轴承的局部摩擦是关键技术之一,特别是对于叶轮转速极高的心尖轴流泵来说更是如此。可将“球支点”轴承设计为“单滑面球支点”和“双滑面球支点”轴承,采用其中的双滑面球支点可使滑动面的相对运动速度降低,进一步减小轴承局部的摩擦效应。图2为我们采用的2种“球支点”轴承结构示意图。
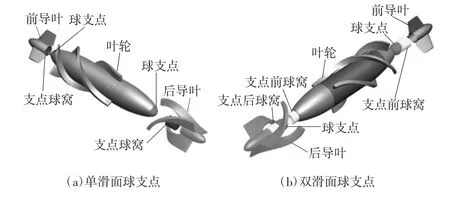
图2 “球支点”轴承结构示意图
对于单滑面球支点,互相滑动的球形面相对运动速度较大。由于球支点跟随叶轮高速转动,所以滑动面间的相对运动速度等于叶轮的转动速度。而对于双滑面球支点,球支点面相对于支点后球窝和支点前球窝的接触面都可以自由滑动,所以在力学条件对称的情况下球支点的转速为叶轮转速的1/2,即球支点对于支点前球窝或支点后球窝的球面滑动速度仅为叶轮转速的1/2。因此可减少滑动面的磨损并减少局部产热,进一步改善“球-窝”式滑动轴承的机械性能和生理相容性。
1.2 全悬浮心尖轴流泵
采用磁力或流体动力使轴流泵叶轮在流体中悬浮旋转,可完全去除机械轴承,被推崇为“第三代”血泵。此类血泵没有机械摩擦磨损,可完全消除局部产热,防止血栓形成,且寿命不受限制,是较理想的血泵结构。但悬浮血泵有其固有的缺点,比如采用全磁悬浮技术时泵体积不易缩小,且能量消耗较大。“磁-液”联合悬浮技术虽可使泵体积减小,且可避免大幅度增加能量消耗,但需设置狭窄的流体动力悬浮间隙,对血细胞的剪切破坏较严重。因此,尽可能减低溶血是采用此类悬浮方式需要认真解决的困难。
在叶轮悬浮条件下,后导叶的机械支持作用已不再需要,去除后导叶可进一步简化泵内结构,有利于进一步缩小泵体积,还可能降低泵内血栓形成的几率。因此,我们早期设计的全悬浮心尖轴流泵无后导叶,结构类似于美国的HeartWare MVAD[13]微型轴流泵。但我们后来的研究发现:去除后导叶不仅降低了心尖轴流泵的流体效率,而且大幅度增加了机械溶血作用。为克服这些缺点,我们在全悬浮心尖轴流泵的尾端设置了无机械支撑作用的后导叶,其结构如图3所示。
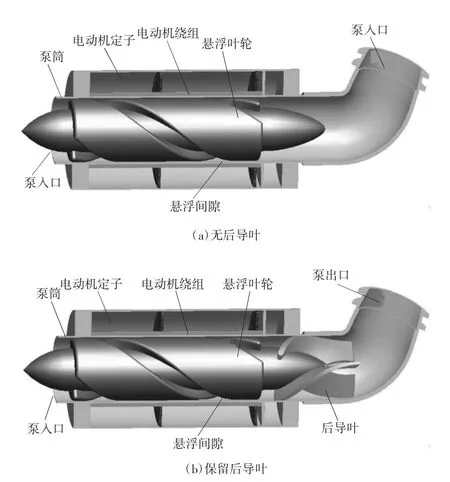
图3 全悬浮心尖轴流泵结构示意图
全悬浮心尖轴流泵叶轮的径向位置由流体动力控制,即当叶轮高速旋转时在叶轮叶片外周圆弧面与轴流泵泵筒内面之间的间隙内可形成流体动压,使叶轮与轴流泵泵筒脱离机械接触,从而产生流体动压悬浮(液悬浮)作用,叶轮的轴向约束力则由磁场产生[14]。
2 体外比较测试
在模拟循环台上分别比较单滑面球支点、双滑面球支点心尖轴流泵及保留后导叶、无后导叶的全悬浮心尖轴流泵的流体力学性能。模拟循环台根据HU Q H等[15]的报道设计,由储液罐、血泵、阻力调节器、流量计串联组成。各组件用内径12 mm的有机玻璃管顺序连接,在血泵的出口和阻力调节器之间的管道中设置压力传感器,测定泵的输出压力和流量。在测定血泵流体力学特性时采用30%甘油水溶液作为循环介质,以使其黏滞度接近于血液。通过调节储液罐中液面高度调节泵的入口压力,通过调节轴流泵的输入电压改变被测泵的转速,通过调节阻力阀改变泵输出流量和压力比。通过仔细调节阻力阀和泵转速,可使泵输出稳定在5 L/min流量和100 mmHg(1 mmHg=133.322 Pa)输出压水平,这一输出接近于实际心脏辅助时的要求。溶血实验采用新鲜牛血作为循环介质,采集血液时加入枸橼酸钠抗凝剂抗凝,根据红细胞压积测定值用适量生理盐水稀释,将红细胞比容(hematocrit,HCT)调节至0.30左右。取1 ml血样后将其完全溶血(超声法溶血),再用牛血浆稀释成不同游离血红蛋白浓度的溶液并标定,作为比对用基准样本。将制备好的总容积为5 L的新鲜牛血装入模拟循环管道,用恒温水浴浸没以保持血液温度在35~37℃之间。充分排出循环管道中空气后,开启被测轴流泵并将其输出压力调节到100 mmHg,流量调节到5 L/min。定时采集循环管路中的血液样本约5 ml,离心后取血浆,通过与基准样本的颜色比较确定血浆中游离血红蛋白浓度,并计算溶血强度。每标本测定3次,取平均值。溶血强度由溶血指数(normalized index of hemolysis,NIH)反映,NIH参照T Tsukiya[16]等的方法由下列公式计算:
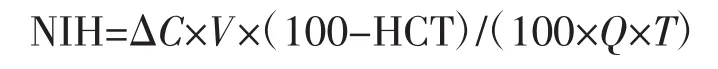
式中,V是循环管路中的血液总量,Q为泵流量,T为运行时间,HCT是红细胞比容,ΔC为血浆中游离血红蛋白浓度改变量。
3 结果
4种不同结构的心尖轴流泵具有不同的流体力学输出特性。双滑面球支点心尖轴流泵与单滑面球支点心尖轴流泵输出特性差异极轻微。2种悬浮心尖轴流泵的流体力学特性明显不同于球支点心尖轴流泵,且去除后导叶的悬浮心尖轴流泵流体效率最低。在输出压力恒定为100 mmHg条件下,各心尖轴流泵的“转速-流量”关系如图4所示。
由图4的曲线可知,在相同的输出压力条件下,各型心尖轴流泵的输出流量与转速之间大体呈现正比关系。但悬浮心尖轴流泵需要在较高的转速条件下才能达到与球支点心尖轴流泵相似的输出流量。2种球支点心尖轴流泵均可在11 000 r/min的转速条件下达到5 L/min的输出流量。悬浮心尖轴流泵的转速明显增加,有后导叶的悬浮心尖轴流泵在约17 000 r/min的转速条件下达到5 L/min流量,而无后导叶的悬浮心尖轴流泵需要在23 000 r/min的转速条件下才能达到类似流量,比球支点心尖轴流泵转速提高约一倍。随着泵转速的增加,电动机的输入电流和电压也相应增加。通过输入电压和电流可计算各型心尖轴流泵的输入功率,各泵的流体输出功率则由输出压力和流量的乘积估算。在100mmHg输出压力和5 L/min输出流量条件下,泵的流体输出功率为1.2 W。本文的研究发现,心尖轴流泵的溶血特性与泵的效率有密切关系,效率较高的心尖轴流泵溶血作用较轻微。悬浮心尖轴流泵的溶血强度比球支点心尖轴流泵明显增加,各型心尖轴流泵的标准溶血指数(NIH)及效率见表1。
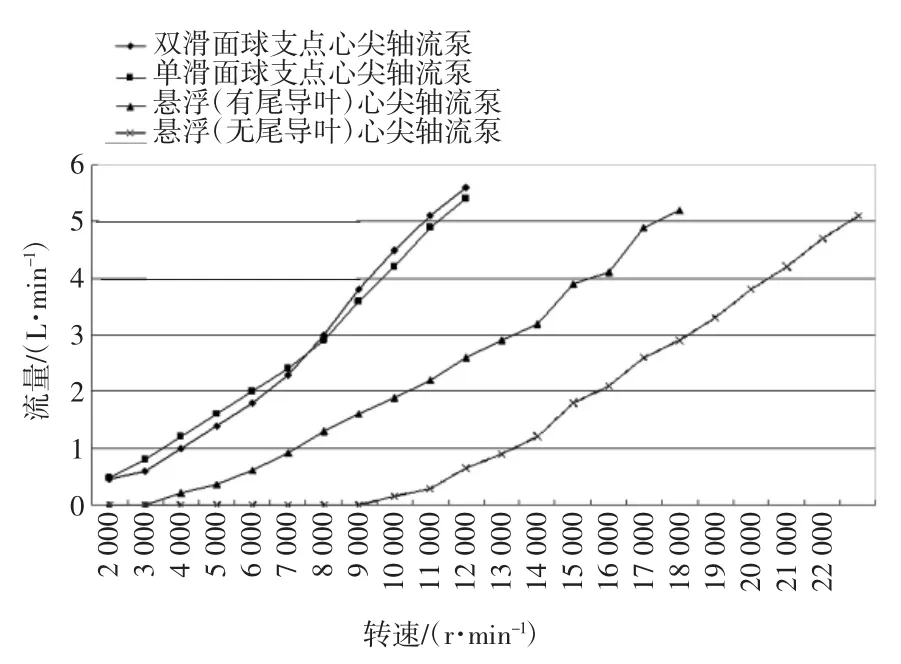
图4 各型轴流泵转速-流量关系示意图
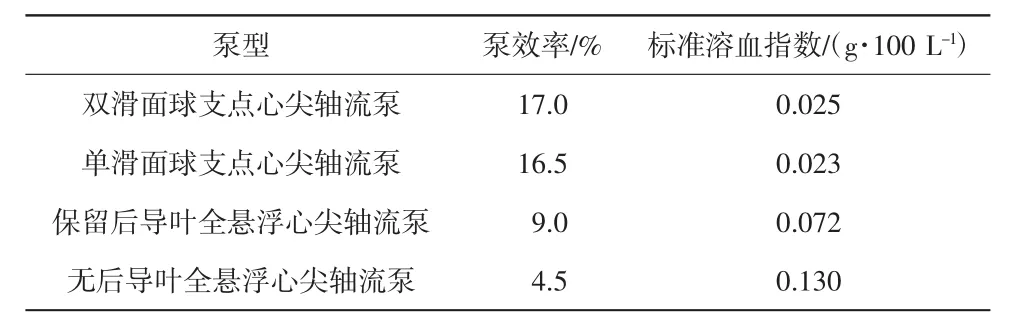
表1 各型轴流泵泵效率及溶血强度
4 讨论
作为植入体内的心脏辅助装置,血泵的植入位置、与心脏大血管的连接方式是非常重要的考虑因素。目前,临床常用的植入方法是将泵体放置到患者上腹壁内,在腹直肌的前或后创建囊袋来容纳泵体。早期应用于临床的HeartMate和Novacar搏动泵均采用此种植入方式。目前,新发展起来的持续流血泵也大多继承了这种植入方式,如HeartMateⅡ和BerlinHeart incor等。此种植入方式的缺点是手术创伤较大,容易产生出血、感染等并发症。此外,连接泵入口的管道容易产生移位变形,导致引流不畅甚至入口端负压,成为血栓形成的易发部位。近几年发展起来的持续流血泵,由于体积较小所以可以直接植入到心包腔甚至心室腔内,这样可以去除入口引流管道,避免传统植入方法的诸多缺点,比如Jarvik 2000轴流泵和HeartWare HVAD离心泵。值得一提的是,美国研究者新近研制的HeartWare MVAD是一种体积极小的磁-液悬浮轴流泵,植入方法也与Jarvik 2000轴流泵类似。未来发展的微型化血泵都极有可能采用心室内或心包腔内的植入方式。虽然心包或心室内植入血泵的方式有很多优点,但最大的困难是泵体积要求微型化,特别是对身材较小的患者来说更是受到限制。我们设计的心尖微型轴流泵部分泵体放置在心室腔内,部分泵体位于心包腔内,虽然可在一定程度上缓解植入位置对泵体积的限制,但仍然需要在设计时考虑缩小泵体积的问题。轴流泵的前、后导叶可使泵长度增加,在优化微型轴流泵结构时需要仔细设计。我们曾经观察过去除前导叶对轴流泵流体力学特性的影响[17],发现在没有前导叶的条件下轴流泵的流体效率仅轻微下降,可作为心尖轴流泵改进时的备选结构;但后导叶对轴流泵的效率有重要意义,不应去除。
美国的HeartWare MVAD微型轴流泵同时去除了前、后导叶,大大缩小了泵体积,特别有利于心尖部位的植入,且该装置目前已有动物实验成功的报道[18]。但我们在本文的实验观察中发现,去除后导叶不仅使轴流泵流体效率严重下降,而且溶血强度也大幅度增加,这些缺点可能在长期应用时导致较严重并发症,所以在我们设计的心尖轴流泵中采用了去除前导叶、保留后导叶的结构,这是我们与Heart Ware MVAD微型轴流泵的重要差别。
悬浮轴流泵的叶轮设计与机械轴支撑的轴流泵叶轮设计有较大区别。悬浮叶轮的外周面面积直接关系到径向悬浮动压的大小,一般来说,叶轮的外周面面积越大旋转时产生的流体悬浮力也越大。在一定悬浮间隙条件下,叶轮外周面面积关系到叶轮悬浮状态的稳定性,较大的流体悬浮力可使叶轮处于较稳定的悬浮状态。因此,在设计悬浮叶轮时总是趋向于采用较宽的叶轮叶片。
虽然加宽叶片可实现叶轮稳定悬浮,但也相应地减小叶片间流道的过流面积,减小泵的输出流量。因此,在悬浮轴流泵采用的宽叶轮叶片条件下,必须增加转速才能获得较大的流量,这是悬浮轴流泵要求较高工作转速的原因。对于无后导叶的悬浮轴流泵来说,除上述叶轮结构因素外,没有后导叶的整流作用,泵出口处的流体旋转分量不能转变为直流分量,造成机械能损耗,这是转速增加的另一个重要原因。我们的实验观察到悬浮轴流泵的溶血强度明显增加,可能是叶轮转速较高所致。在特定的悬浮间隙条件下,悬浮间隙中剪切力随叶轮转速增大,使血细胞损伤加重。影响溶血的因素较多,如在悬浮状态不稳定时,悬浮间隙不均匀也可引起溶血增加,对剪切区域总体积、血细胞的剪切暴露时间等也有重要影响。因此,仔细选择叶轮叶片宽度以求获得最佳的悬浮间隙,尽可能减小泵转速是下一步改进设计的重要内容。本文的对比观察表明:保留后导叶与无后导叶的悬浮心尖轴流泵相比,虽然叶轮几何形状相同,但效率特性和溶血特性均有很大的改善。保留后导叶可使轴流泵总体效率提高将近40%,溶血强度下降为原来的1/2,而在泵外径不变情况下长度仅增加30%左右。因此,保留后导叶可作为心尖轴流泵较好的结构选择。
在研制可长期应用的植入式血泵时,泵结构的不断改进和优化是必经的过程。在相同条件下进行体外比较测试是评估血泵性能的基本研究方法。在相同的测试平台上比较测试,各种不同结构轴流泵的特性可获得正确评估,为优化结构、分析动物实验结果提供基础。本文的研究采用相同的测试装置同时比较了4种不同结构的心尖轴流泵的流体力学特性和溶血特性,可以排除不同研究条件和实验环境差异可能导致的误差,揭示轴流泵结构和性能之间的关系。本文的研究结果显示:球支点心尖轴流泵总体性能优于悬浮心尖轴流泵。这也提示有机械支点的第二代血泵仍然会成为今后很长一段时间内临床应用的主流。但在有机械轴支点的条件下,加工和装配过程中的微小误差均会导致机械支点的迅速磨损。我们的研究发现:球支点滑动轴承有较好的配合性能,球型旋转支点和静止的球窝配合,允许相对运动的2个球型面之间有轻微的轴偏移,防止滑动面磨损加重。另外,在滑动面上沉积的血液蛋白也可在球型旋转支点的“钻头”样作用下被清除,防止滑动阻力增加甚至堵塞。双滑面球支点摩擦面间相对运动速度较低,可有更好的抗磨损作用,由于局部产热小也可有更好的防止血栓特性。
5 结论
单滑动面球支点心尖轴流泵结构简单、效率高、溶血强度低,适合于心尖轴流泵的结构选择;双滑动面球支点心尖轴流泵的结构优势尚需在长时间体内植入实验中证实。悬浮心尖轴流泵体积较小,但效率较低,溶血作用强,保留后导叶可明显提高悬浮心尖轴流泵效率,降低溶血强度。
[1]Butler K,Thomas D,Antaki J,et al.Development of he Nimbus/ Pittsburgh axial flow left ventricular assist system[J].Artif Organs,1997,21:602-610.
[2]Kirklin J K,Naftel D C,Pagani F D,et al.Long-term mechanical circulatory support(destination therapy):on track to compete with heart transplantation[J].J Thorac Cardiovasc Surg,2012,144:584-603.
[3]DeBakey M E,Teitel E R.Use of the MicroMed DeBakey VAD for the treatment of end-stage heart failure[J].Expert Rev Med Devices,2005,2:137-140.
[4]Granfeldt H,Peterzén B,Hübbert L,et al.A single center experience with the HeartMateⅡleft ventricular assist device(LVAD)[J].Scand Cardiovasc J,2009,43:360-365.
[5]Westaby S,Katsumata T,Evans R,et al.The Jarvik 2000 Oxford system:increasing the scope of mechanical circulatory support[J].J Thorac Cardiovasc Surg,1997,114:467-474.
[6]Formica F.HeartWare LVAD is a promising device for patients with end-stage heart failure[J].Ann Thorac Surg,2012,94(6):2 180-2 181.
[7]李国荣,朱晓东,田步升,等.微型心尖轴流泵的结构及流体力学特性研究[J].医疗卫生装备,2008,29(5):3-5.
[8]郝宗超,田步升,象天工,等.“晓东-国荣”心尖轴流泵的手术植入方法—动物实验研究[J].医药与保健,2009,17(5):21-23.
[9]李国荣,朱晓东,郝宗超,等.心尖轴流泵的解剖相容性及对心肌损伤的动物实验观察[J].医疗卫生装备,2010,31(3):20-22.
[10]李国荣,朱晓东,彭远仪,等.微型轴流泵式心脏辅助装置的研制:流体力学特性分析[J].中国医疗器械信息,2007,13(8):36-39.
[11]彭远仪,郝宗超,田步升,等.“晓东-国荣”型轴流泵的流体力学特性研究[J].中外健康文摘,2008(3):66-68.
[12]李国荣,田步升,朱晓东,等.植入式轴流泵心脏辅助装置的动物体内植入实验[J].中外健康文摘,2008(2):58-60.
[13]Mark S S,Michael A S.HeartWare miniature axial-flow ventricular assist device design and initial feasibility test[J].Tex Heart Inst J,2009,36:12-16.
[14]李国荣,朱晓东,田步升,等.全悬浮心尖轴流泵左心辅助装置[J].医疗卫生装备,2013,34(10):21-24.
[15]HU Q H,LI J Y,ZHANG M Y.Effects of fluid viscoelasticity on the performance of an axial blood pump model[J].ASAIO J,2012,58:32-39.
[16]Tsukiya T,Taenaka Y,Tatsumi E,et al.Performance of a newly developed implantable centrifugal blood pump[J].ASAIO J,2001,47:559-562.
[17]李国荣,朱晓东,彭远仪,等.前导叶对轴流泵式心脏辅助装置流体力学特性的影响及改进意义[J].医疗卫生装备,2007,28(8):5-7.
[18]McGee E Jr,Chorpenning K,Brown M C,et al.In vivo evaluation of the HeartWare MVADPump[J].J HeartLungTransplant,2014,33:366-371.
(收稿:2014-12-13 修回:2015-03-26)
Comparative study of miniature apex axial flow blood pumps with different structures
LI Guo-rong1,ZHU Xiao-dong1,CHEN Hai-feng2,TIAN Bu-sheng2,PENG Yuan-yi2
(1.Fuwai Heart Hospital&Cardiovascular Institute,Chinese Academy of Medical Sciences,Beijing 100037,China; 2.Jiuan Artificial Heart Science and Technology Development Co.,Ltd.,Changzhi 046000,Shanxi Province,China)
ObjectiveTo compare the hydrodynamics and hemolytic characteristics of four types of miniature apex axial flow pumps.MethodsFour types of axial flow pumps with similar boundary dimensions were fabricated,including two axial flow pumps with mechanical contacting bearings and two suspending axial flow pumps.The mechanical contacting bearing was designed as pivot ball bearing with either double sliding surface or single sliding surface,while the suspending axial flow pumps were constructed as one with either a tail flow straighter or without it.The four prototypes of axial flow pumps were tested on a mock circle for the hydrodynamic and hemolytic characteristics.ResultsThe two prototypes of axial flow pumps with mechanical contacting bearings were similar in performance,and both could yield a flow rate of 5 L/min at 100 mmHg pressure with a rotating speed of 11 000 r/min.The normalized index of hemolysis (NIH)was 0.025 g/100 L for the pump of pivot ball bearing with double sliding surface,and 0.023 g/100 L for that with single sliding surface.For producing same hydrodynamic output of 5 L/min at 100 mmHg pressure,the two prototypes of suspending axial flow pumps needed a much higher rotational speed,which reached 17 000 and 23 000 r/min for the suspending axial flow pump with or without a tail flow straighter respectively,correspondently the NIH reached 0.072 g/100 L for the former and 0.13 g/100 L for the latter,significantly higher than the axial flow pump with mechanical contact bearing.ConclusionThe axial flow pump with pivot ball bearing has high efficiency and low NIH,suitable as an apex axial flow blood pump.The tail flow straighter is necessary for the suspending axial flow to achieve high hydrodynamic and hemolysis performance.[Chinese Medical Equipment Journal,2015,36(7):4-8]
blood pump;ventricular assist device;suspending axial flow pump;artificial heart
R318.6;TH778
A
]1003-8868(2015)07-0004-05
10.7687/J.ISSN1003-8868.2015.07.004
李国荣(1957—),男,博士,副教授,硕士研究生导师,主要从事心血管外科、人工心脏及辅助循环方面的研究工作,E-mail:Li-Guorong@ 263.net。
100037北京,中国医学科学院阜外心血管病医院(李国荣,朱晓东);046000山西长治,长治市久安人工心脏科技开发公司(陈海丰,田步升,彭远仪)

