晚期非小细胞肺癌患者外周血游离DNA中EGFR突变与靶向药物一线治疗疗效的相关性
张世强,张旭东,王保庆,王海清(徐州医学院第二附属医院放疗三科,徐州 006;徐州医学院第二附属医院肿瘤内科;徐州医学院第二附属医院呼吸内科;通讯作者,E-mail:zxdmail8@sohu.com)
肺癌是世界上发病率及死亡率较高的恶性肿瘤,其中非小细胞肺癌(NSCLC)在肺癌中约占85%,大部分患者确诊时已处于晚期,对于中晚期肺癌患者的治疗目前仍以姑息性化疗为主,改善症状。但第三代化疗药物的临床应用未能明显改善患者的预后,大部分患者经过化疗治疗后1年的生存率仍维持在约35%-40%左右[1-3],而且化疗药物的毒副反应极大降低了患者的生活质量。随着医学技术的发展,目前靶向药物如吉非替尼、厄洛替尼已广泛用于肺癌的临床治疗,取得较好的临床疗效,而且成为肺癌综合治疗领域的研究热点。
靶向药物在NSCLC患者治疗中的疗效已获得国内外肿瘤专家的认可,其疗效与肺癌细胞EGFR基因第19和21外显子突变状态有着密切的关系,是临床应用靶向药物治疗的重要依据。由于大部分肺癌患者确诊时已处于肿瘤晚期,无法获得足够用于检测EGFR基因突变的肺癌组织标本。目前已有大量的研究证实[4-6],外周血游离DNA中EGFR基因突变状态与肿瘤组织中的EGFR基因突变状态具有高度的相关性,且外周血取材方便,故本研究的目的是通过检测外周血游离DNA中EGFR基因突变状态,探讨其指导晚期NSCLC患者口服吉非替尼作为一线治疗的临床意义。
1 材料与方法
1.1 材料与试剂
入组的31例患者来自于我院2012-09~2014-10收治的晚期NSCLC患者,均有细胞病理学诊断证据,入组的患者KPS评分大于60分;其中男性17例,女性14例;年龄56-78岁,平均63.5岁;组织学类型为鳞癌10例,腺癌17例,腺鳞癌4例。患者均有影像学检查证实合并有骨、肾上腺、肝脏或肺等脏器单发或多发转移灶,所有患者治疗前均放弃放化疗治疗,并签署治疗知情同意书。
1.2 方法
1.2.1 治疗方法 入选患者均选取靶向药物吉非替尼治疗,治疗前晨取患者静脉血2 ml,枸橼酸钠抗凝处理,-70℃低温冰箱保存。所有患者口服吉非替尼250 mg/次,1次/d,直到肿瘤进展或患者不能耐受药物不良反应而终止治疗。服药时间最短1个月,最长13个月。所有患者吉非替尼治疗期间不采用其他的抗肿瘤治疗。
1.2.2 外周血游离DNA的提取 采集患者治疗前外周静脉血4 ml,室温放置2 h后用低温高速离心机将静脉血离心(20 ℃,3 000 r/min,10 min),弃下液,取上层液血浆1 ml放置入2 ml冻存试管,血清DNA以磁珠法全血基因组DNA抽提试剂盒(美国Omega公司生产)抽提,按说明书所述的方法抽提血清DNA。
1.2.3 外周血游离DNA中EGFR基因突变的检测 DNA抽提完成后进行PCR扩增目的片段EGFR,EGFR外显子19上游引物:5'-AACGTCTTCTCCCTTCTCTCTCTGTCA-3',下游引物:5'-C CACACAGCA AAGCAGAAACT-3',产物大小为150 bp;EGFR外显子21上游引物:5'-TCTTCTCGTTTT CAGGGC ATG-3',下游引物:5'-GGCTGACCTAAAGCCACCTC-3',产物大小为196 bp;PCR扩增体系设计为 20 μl,模板 1 μl。扩增外显子为 l9、2l外显子。扩增步骤:①95℃,5 min变性;②95℃30 s,57 ℃30 s,72 ℃ 45 s,40 个循环;③72 ℃ 延伸7 min。扩增产物经1.6%琼脂糖凝胶电泳100 V 30 min后EB染色摄片。对观察到阳性扩增条带的样本分离纯化后进行基因测序,测序引物采用各外显子的上游引物。
1.2.4 疗效评价标准 根据WHO疗效评价标准,口服吉非替尼疗效分为完全缓解(CR)、部分缓解(PR)、稳定(SD)和进展(PD),CR和PR要在距离首次评价至少4周后再次确认,计算有效率(RR)和疾病控制率(DCR)。定期复查胸部CT、头颅CT、腹部B超及全身同位素骨扫描,进行疗效判定。吉非替尼治疗开始后前3个月每月随访评估疗效,以后每2个月评估1次。随访终止时间2015-02-01。
1.3 统计学处理
应用SPSS 10.0软件进行统计分析,检验水准α=0.05(双侧),采用确切概率法对计数资料进行检验,比较两组患者吉非替尼治疗后的RR、DCR,采用Kaplan-Meier分析两组患者PFS差异,均以P<0.05为差异有统计学意义。
2 结果
2.1 EGFR基因突变与吉非替尼疗效关系
31例患者采样时首次接受吉非替尼治疗,治疗前均未接受放化疗,应用RT-PCR方法检测出的外周血游离DNA中EGFR突变率为41.9%(13/31),患者根据检测结果分组,EGFR野生型患者18例(其中有10例患者虽然未检测到EGFR基因突变,经患者要求并签署知情同意书后给予吉非替尼治疗,作为对照组),突变型患者13例。评估吉非替尼对晚期NSCLC患者治疗结果显示,EGFR突变型患者的有效率为 61.5%(8/13),疾病控制率为69.2%(9/13);EGFR野生型患者的客观缓解率为10.0%(1/10),疾 病 控 制 率 为 10.0%(1/10)。EGFR基因突变型患者疗效优于野生型,对两组患者治疗效果进行统计学分析表明差异具有显著性(P<0.05,见表1),提示外周血游离DNA检测EGFR基因突变结果可以作为临床应用靶向药物治疗的重要依据。
2.2 预后
根据随访计划,EGFR基因突变组患者中位无进展生存时间(PFS)为14个月,1年生存率为75.0%,2年生存率为30.7%;而EGFR基因野生组患者中位无进展生存时间(PFS)为7.5个月,1年生存率为20.0%,2年生存率为0,两组间生存率及PFS比较差异具有统计学意义(P=0.004 2,见图1),提示根据外周血EGFR基因突变状况指导临床靶向药物治疗,可以明显改善患者的预后。
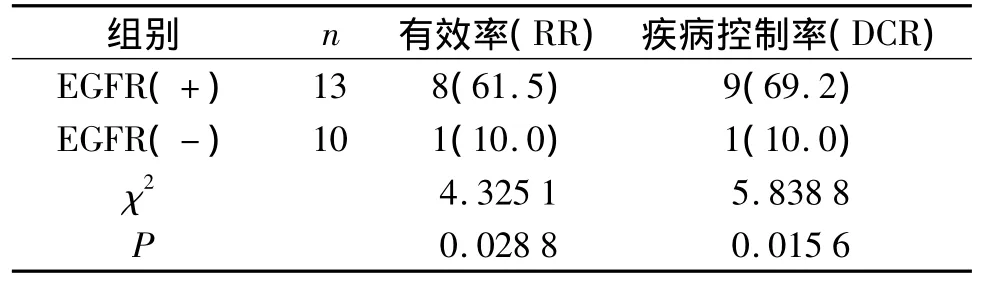
表1 EGFR突变组与野生组RR、DCR的比较 例(%)Table 1 Comparison of RR,DCR between wild type and mutation group cases(%)
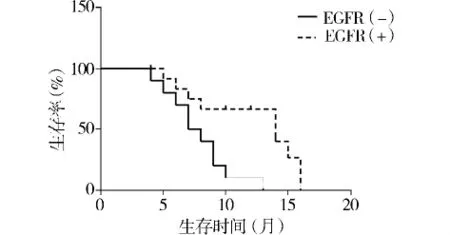
图1 Kaplan-Meier分析两组患者PFS生存曲线Figure 1 Kaplan-Meier survival curves of progression-free survival of patients with or without EGFR mutations
2.3 吉非替尼治疗的不良反应
吉非替尼出现不良反应主要有皮疹、腹泻、转氨酶升高、恶心、呕吐、白细胞减少及间质性肺疾病等。入组患者中最常见为痤疮样皮疹,发生率为39.1%(9/23),皮疹表现为Ⅰ-Ⅱ度;其次为皮肤瘙痒,发生率为13.0%(3/23),均为Ⅰ度,给予抗组胺药物治疗后症状缓解,入组患者中口服吉非替尼后未出现腹泻、转氨酶升高、恶心、呕吐、白细胞减少或间质性肺疾病等不良反应,无因不良反应而导致药物减量或停药者。
3 讨论
表皮生长因子受体(EGFR)是目前抗癌药物研究领域中最受瞩目的靶点分子之一,其主要通过特异地、竞争性地与EGFR激酶功能区的ATP结合位点结合,抑制其激酶活性从而阻断和癌细胞增殖、转移等相关的信号传导。与传统的化疗药物相比,靶向药物克服了一般化疗药物常见的毒副作用,尤其是骨髓抑制作用及胃肠道反应。目前临床应用的EGFR抑制剂主要包括吉非替尼、厄洛替尼,主要用于非小细胞肺癌患者的治疗[7-9],而EGFR基因的突变状态是厄洛替尼及吉非替尼疗效的有效预测指标,大量的临床研究表明[10-12],对于存在EGFR基因突变的肺癌患者,尤其对于亚洲、女性及不吸烟的肺腺癌患者,吉非替尼及厄洛替尼在肺癌的治疗中显示出良好的临床疗效,且不良反应轻。
现有EGFR基因的检测均需采用手术切除或活检肿瘤组织,而对于不具备手术指征的中晚期NSCLC患者而言,临床由于缺乏足够的组织标本而无法检测患者EGFR基因的突变状态。肿瘤患者血清游离DNA的来源主要是肿瘤组织中癌细胞凋亡后,癌细胞内的DNA释放入人体外周血或癌细胞在体内循环中坏死、凋亡,其中的DNA释放到外周血。经癌组织来源的循环DNA,其遗传特性与肿瘤基因组DNA相同[13,14]。因而通过检测血清游离 DNA中的EGFR基因,可以间接反映肿瘤组织EGFR基因的突变情况,从而为临床应用靶向药物治疗提供依据。
近年来,国内已有利用外周血检测EGFR突变指导靶向药物治疗的报道,周小昀等[15]应用EGFRTKIs治疗的有效率高达83%,而马玲等[16]应用EGFR-TKIs治疗有效率为55.6%。在本组研究中,31例患者应用RT-PCR方法检测出的外周血游离DNA中EGFR突变率为41.9%,入组的患者中有10例未检测到EGFR基因突变接受了吉非替尼治疗,有EGFR基因突变的13例患者均接受吉非替尼治疗,治疗结果显示,EGFR突变型患者的有效率为61.5%,疾病控制率为69.2%,PFS为14个月,1年生存率为75.0%,2年生存率为30.7%;而EGFR野生型患者的客观缓解率为10.0%,疾病控制率为10.0%,PFS为7.5个月,1年生存率为20.0%,2年生存率为0,再次表明外周血EGFR基因突变型患者接受吉非替尼治疗其疗效优于野生型,可以明显改善患者的预后,本研究中接受吉非替尼治疗的有效率与已有的报道存在一定的差异,考虑与入组患者的例数较少、实验方法及病例病理分型不同等因素有关。另外,EGFR野生型患者中出现1例吉非替尼治疗有效,考虑可能与采样的外周血中提取到的游离的DNA较少,导致EGFR基因检测结果出现假阴性。在所有接受吉非替尼治疗的患者中最常见的不良反应为痤疮样皮疹,其次为皮肤瘙痒,症状较轻,给予对症治疗后症状均可缓解,无因不良反应而导致药物减量或停药者。
本研究结果表明,外周血游离DNA中EGFR基因突变检测结果可以为肺癌患者靶向治疗提供指导作用,对于无法获取组织学检测的肺癌患者具有重要的意义,而且采集患者外周血比较方便,患者痛苦少易于接受,该项技术值得临床推广。
[1]Ozkaya S,Findik S,Atici AG,et al.Cisplatin-based chemotherapy in elderly patients with advanced stage(ⅢB and IV)non-small cell lung cancer patients[J].Neoplasma,2011,58(4):348-351.
[2]康艳虹,马为.非小细胞肺癌患者的预后因素分析[J].广东医学,2014,35(4):524-527.
[3]Kaira K,Takahashi T,Murakami H,et al.Long-term survivors of more than 5 years in advanced non-small cell lung cancer[J].Lung Cancer,2010,67(1):120-123.
[4]郭琛,郭其森,曾洪生,等.非小细胞肺癌患者肿瘤组织与外周血中EGFR表达相关性研究[J].中国肺癌杂志,2010,13(12):1107-1112.
[5]赵宇,郭惠琴.检测非小细胞肺癌患者的血清循环EGFR基因突变研究进展[J].癌症进展,2012,10(1):6-9.
[6]赵瑾,彭群新,杨炳华,等.应用HRM法检测肺癌患者循环DNA中表皮生长因子受体基因突[J].中华医学杂志,2011,91(10):674-678.
[7]Cho SH,Park LC,Ji JH,et al.Efficacy of EGFR tyrosine kinase inhibitors for non-adenocarcinoma NSCLC patients with EGFR mutation[J].Cancer Chemother Pharmacol,2012,70(2):315-320.
[8]Petrelli F,Borgonovo K,Cabiddu M,et al.Efficacy of EGFR tyrosine kinase inhibitors in patients with EGFR-mutated non-smallcell lung cancer:a meta-analysis of 13 randomized trials[J].Clin Lung Cancer,2011,13(2):107-114.
[9]Lim SH,Lee JY,Sun JM,et al.Comparison of clinical outcomes following gefitinib and erlotinib treatment in non-small-cell lung cancer patients harboring an epidermal growth factor receptor mutation in either exon 19 or 21[J].J Thorac Oncol,2014,9(4):506-511.
[10]Fukuoka M,Wu YL,Thongprasert S,et al.Biomarker analyses and final overall survival results from a phaseⅢ,randomized,open-label,first-line study of gefitinib versus carboplatin/paclitaxel in clinically selected patients with advanced non-small-cell lung cancer in Asia(IPASS)[J].J Clin Oncol,2011,29(21):2866-2874.
[11]Wu YL,Chu DT,Han B,et al.Phase Ⅲ,randomized,open-label,first-line study in Asia of gefitinib versus carboplatin/paclitaxel in clinically selected patients with advanced non-small-cell lung cancer:evaluation of patients recruited from mainland China[J].Asia Pac J Clin Oncol,2012,8(3):232-243.
[12]Saito H,Murakami S,Kondo T,et al.Effectiveness of erlotinib in advanced non-small cell lung cancer in cases of gefitinib resistance after treatment of more than 6 months[J].Onkologie,2012,35(1-2):18-22.
[13]Paci M,Maramotti S,Bellesia E,et al.Circulating plasma DNA as diagnostic biomarker in non-small cell lung cancer[J].Lung Cancer,2009,64(1):92-97.
[14]He C,Liu M,Zhou C,et al.Detection of epidermal growth factor receptor mutations in plasma by mutant-enriched PCR assay for prediction of the response to gefitinib in patients with non-smallcell lung cancer[J].Int J Cancer,2009,125(10):2393-2399.
[15]周小昀,李龙芸,崔巍,等.检测肺癌患者血清游离DNA的EGFR基因点突变与EGFR-TKI疗效的相关性分析[J].癌症进展,2011,9(1):13-18.
[16]马玲,刘莉,张涛,等.晚期NSCLC患者血清EGFR基因测定及意义[J].中国肺癌杂志,2013,16(6):303-307.

