HPLC法测定双氢青蒿素哌喹片中双氢青蒿素的含量Δ
周 琳(重庆市食品药品检验检测研究院/重庆市药物过程与质量控制工程技术研究中心,重庆 401121)
双氢青蒿素哌喹片为双氢青蒿素和磷酸哌喹的复方制剂。双氢青蒿素为青蒿素衍生物[1-2],是青蒿素体内活性物质,对疟原虫无性体有较强杀灭作用,能迅速杀灭疟原虫,控制疾病症状。双氢青蒿素和磷酸哌喹合用具有协同作用,可延缓疟原虫耐药性的产生[3]。《中国药典》2010年版第一增补本收载了双氢青蒿素哌喹片,并采用高效液相色谱(HPLC)法测定双氢青蒿素的含量,但该方法不能有效排除磷酸哌喹的影响。本文参考《国际药典》2011 V2.2版中双氢青蒿素的含量测定方法[4],对现行标准中的测定方法进行了改进。
1 材料
2695型HPLC仪,包括2998型二极管阵列检测器和Empower工作站(美国Waters公司);KQ5200型超声波清洗器(昆山市超声仪器有限公司,功率:200 W,频率:40 kHz);ME215S型十万分之一天平(德国Sartorius公司)。
双氢青蒿素对照品(中国食品药品检定研究院,批号:100184-201202,纯度:99.94%),青蒿素对照品(中国食品药品检定研究院,批号:100202-201004,纯度:100%);双氢青蒿素哌喹片(华立岩康制药有限公司,批号:011110、010212、010512);乙腈为色谱纯;其他试剂均为分析纯;水为纯化水。
2 方法与结果
2.1 色谱条件
色谱柱:Waters YMC-Pack ODS-AQ(250 mm×4.6 mm,5 μm);流动相:乙腈(A)-水(B),梯度洗脱(洗脱程序见表1);流速:1.0 ml/min;柱温:30 ℃;检测波长:216 nm;进样量:20 μl。
2.2 溶液的制备
2.2.1 对照品溶液 取双氢青蒿素对照品约25 mg,精密称定,置于25 ml量瓶中,加乙腈-水(60∶40,V/V)适量,超声处理10 min使溶解,放冷,用乙腈-水(60∶40,V/V)稀释至刻度,摇匀,即得。
2.2.2 供试品溶液 临用新制。取本品10片,精密称定,研细,取粉末适量(相当于双氢青蒿素约25 mg),精密称定,置于25 ml量瓶中,加乙腈-水(60∶40,V/V)适量,超声处理10 min使溶解,冷却,用乙腈-水(60∶40,V/V)稀释至刻度,摇匀,离心,取上清液作为供试品溶液。
2.2.3 空白溶液 按处方比例配制无双氢青蒿素的阴性对照品,精密称取相当于双氢青蒿素约25 mg的粉末,置于25 ml量瓶中,加乙腈-水(60∶40,V/V)适量,超声处理10 min使溶解,冷却,用乙腈-水(60∶40,V/V)稀释至刻度,摇匀,离心,取上清液作为空白溶液。
2.3 系统适用性试验
取双氢青蒿素、青蒿素对照品各适量,精密称定,加乙腈-水(80∶20,V/V)超声处理10 min,并稀释制成每1 ml中含双氢青蒿素和青蒿素各1 mg的系统适用性溶液。精密吸取20 μl注入HPLC仪,按“2.1”项下色谱条件进样测定,记录色谱图。结果,双氢青蒿素(呈两个色谱峰)第一个色谱峰与青蒿素峰相比,相对保留时间为0.6;各组分峰之间的分离度>2.0;理论板数以β-双氢青蒿素峰计算>3 000。色谱见图1。
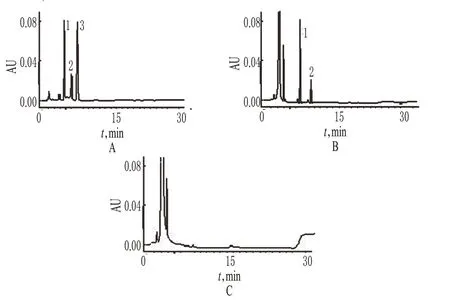
图1 高效液相色谱图Fig 1 HPLC chromatograms
2.4 空白干扰试验
分别精密吸取“2.2”项下对照品溶液、供试品溶液、空白溶液各20 μl,按“2.1”项下色谱条件进样测定,记录色谱图。按外标法计算供试品溶液中双氢青蒿素的含量,色谱见图1。结果表明,空白溶液无干扰。
2.5 线性关系考察
精密称取双氢青蒿素对照品0.482 5 g,置于200 ml量瓶中,加乙腈-水(60∶40,V/V)适量,超声处理10 min使溶解,置37℃水浴中保温1 h,冷却后用流动相稀释至刻度,摇匀,制成质量浓度为2.412 mg/ml的双氢青蒿素标准溶液。精密量取双氢青蒿素标准溶液适量,用乙腈-水(60∶40,V/V)稀释并制成双氢青蒿素质量浓度分别为1.930、0.965 0、0.482 5、0.096 50、0.048 25、0.009 650 mg/ml的标准溶液。按“2.1”项下色谱条件分别进样20 μl测定,记录色谱图。以质量浓度(x)为横坐标、双氢青蒿素两个峰面积之和(y)为纵坐标,绘制标准曲线,得回归方程为y=3.086 8×107x+28.833(r=0.999 9)。结果表明,双氢青蒿素的质量浓度在0.009 650~1.930 mg/ml范围内与峰面积呈良好线性关系。
2.6 双氢青蒿素双峰转换
精密称取双氢青蒿素原料10.00 mg,精密加入乙腈-水(60∶40,V/V)10 ml,超声处理10 min使溶解,连续进样30次(每次运行时间14 min,等度)。结果,峰面积之和的RSD为0.80%,表明双氢青蒿素溶液在6 h内两峰面积间的比例变化较大,但两峰面积之和基本一致,对测定结果无影响。
2.7 定量限与检测限
精密称取双氢青蒿素对照品20.04 mg,置于100 ml量瓶中,加乙腈-水(60∶40,V/V)适量,超声处理10 min使溶解,并稀释至刻度,摇匀;再精密量取1.0 ml,置于100 ml量瓶中,加乙腈-水(60∶40,V/V)稀释至刻度,摇匀,即得供试品溶液。按“2.1”项下色谱条件进样5 μl测定,记录色谱图。按信噪比为10计算定量限、以信噪比为3计算检测限。结果,α-双氢青蒿素的定量限、检测限分别为1.78、0.533 ng;β-双氢青蒿素的定量限、检测限分别为7.39、2.22 ng。
2.8 精密度试验
精密吸取“2.2.2”项下供试品溶液20 μl,按“2.1”项下色谱条件连续进样6次,记录色谱图,按外标法以双氢青蒿素两个峰面积之和计算。结果,RSD为0.21%,表明仪器精密度良好。
2.9 稳定性试验
精密吸取“2.2.2”项下供试品溶液适量,在室温下放置0、1.5、3、4.5、6.5、8.5、10.5、14.5 h时按“2.1”项下色谱条件分别进样20µl,以双氢青蒿素两个峰面积之和计算。结果,RSD为0.31%,说明供试品溶液在14.5 h内稳定性良好。
2.10 重复性试验
取同一批样品(批号:011110)适量,按“2.2”项下方法制备供试品溶液6份,按“2.1”项下色谱条件进样,记录色谱图,按外标法以双氢青蒿素两个峰面积之和计算。结果,RSD为0.5%,表明本方法重复性良好。
2.11 加样回收率试验
精密称取同一批样品(批号:011110)适量,共9份,每3份为一组,分别精密加入相当于双氢青蒿素对照品质量浓度80%、100%、120%的溶液各适量,按“2.2”项下方法制成供试品溶液,再按“2.1”项下色谱条件进样测定,记录色谱图,并计算加样回收率,结果见表2。

表2 加样回收率试验结果(n=9)Tab 2 Results of recovery tests(n=9)
2.12 样品含量测定
取3批样品及双氢青蒿素对照品各适量,按照“2.2”项下方法配制供试品和对照品溶液,按“2.1”项下色谱条件进样测定,记录色谱图,按外标法计算样品含量,结果以标示量的百分含量表示,详见表3。

表3 样品含量测定结果(n=3)Tab 3 Results of content determination of samples(n=3)
3 讨论
双氢青蒿素哌喹片现行质量标准收载于《中国药典》2010年版第一增补本[5]中,其双氢青蒿素含量测定方法为HPLC法,检测波长为210 nm,本文参照国际药典2011 V2.2版[4]将检测波长改为216 nm,既能保证双氢青蒿素含量测定的灵敏度,同时又能相对减少末端吸收的影响。
现行质量标准流动相为乙腈-水(60∶40,V/V),等度洗脱。本试验中发现,等度洗脱时磷酸哌喹的保留时间较长,不易洗脱,而且磷酸哌喹的色谱峰会影响双氢青蒿素的色谱峰,出现峰重叠等现象。因此,本文采用乙腈和水的梯度洗脱方式,将磷酸哌喹洗脱,避免其对双氢青蒿素含量测定的影响。
综上所述,本方法准确、简便、快速,可用于双氢青蒿素哌喹片中双氢青蒿素的含量测定。
[1]韦国峰,何有成,黄祖良.双氢青蒿素的制备及其含量测定[J].右江民族医学院学报,2001,23(5):691.
[2]王满元.青蒿素类药物的发展历史[J].自然杂志,2012,34(1):44.
[3]韩涛,代勇.简述使用青蒿素联合西药疟疾的研究进展[J].当代医药论丛,2015,13(6):10.
[4]World Health Organization.The international pharmacopoeiaFourth Edition Second Supplement[EB/OL].(2011)[2013-07-25].http://apps.who.int/phint/en/p/docf/.
[5]国家药典委员会.中华人民共和国药典:第一增补本[S].2010年版.北京:中国医药科技出版社,2010:271.

