超声波/H2O2协同降解水中三唑磷的研究
张媛媛,陈忠正,罗文超,路海燕,李 斌,殷 桃
(华南农业大学食品学院,广东广州510642)
超声波/H2O2协同降解水中三唑磷的研究
张媛媛,陈忠正,罗文超,路海燕,李斌*,殷桃
(华南农业大学食品学院,广东广州510642)
研究了超声波/H2O2联合处理对水模拟体系中有机磷农药三唑磷的去除效果,并分析了超声功率、农药初始浓度和溶液初始pH对三唑磷降解的影响。结果表明,超声波/H2O2联合处理对水模拟体系中的三唑磷具有良好的降解效果。在本实验研究条件下,与单独超声和H2O2处理相比,超声波/H2O2联合处理对三唑磷具有明显的协同降解作用;在超声功率为475~850 W时,三唑磷的降解率随功率的上升而显著增加;在农药浓度为2~20 mg/L的范围内,降低农药初始浓度有利于提高三唑磷的降解率;pH对三唑磷的降解有显著影响,且碱性条件更有利于三唑磷的降解。当溶液pH为9、三唑磷初始浓度为2.46 mg/L、H2O2添加浓度为2.5 g/L时,采用300 W的超声波处理90 min,三唑磷的降解率高达79.2%。动力学分析的结果表明,一级动力学模型能很好模拟超声波/H2O2联合处理作用下三唑磷的降解。
超声波,H2O2,三唑磷,动力学
三唑磷是一种中等毒性的有机磷农药,其化学名称为O,O-二乙基-O-1-苯基-1,2,4-三唑-3-基硫代磷酸酯。三唑磷具有广谱杀虫、杀螨作用,并兼有一定的杀线虫作用[1]。自20世纪70年代起,三唑磷即被用于防治棉花、玉米、稻谷和蔬菜等农作物害虫。近年来,随着甲胺磷、甲拌磷、对硫磷等高毒农药的禁用,三唑磷在农业生产中的应用越来越广泛。但是,三唑磷具有生殖毒性、神经毒性,对血液、肝脏和脑组织等亦有氧化损伤作用[2-3]。因此,控制三唑磷在农产品以及食品中的残留对于保证食品安全、保护消费者健康具有重要意义。
超声波是频率高于16 kHz的机械波,因其具有对食品的品质影响小,能够更好的保持食品的营养成分以及风味等优点[4-5],已被美国食品药品监督管理局推荐为可替代热杀菌的食品非热杀菌技术[6]。近年来,该技术在污染物降解领域也受到广泛关注[7-8]。过氧化氢(H2O2)是经典的化工产品,因其分解产物无害,现广泛应用于纺织、造纸、环保和农业等领域;食品级H2O2已作为消毒剂用于乳品及饮料等食品的无菌包装,还在啤酒、饮用水、水产保鲜等食品加工过程中得到了应用。在污染物控制方面,H2O2处理对部分农药和生物毒素等具有良好的去除作用[9-10]。本文采用磷酸盐缓冲液建立水模拟体系,研究超声波/ H2O2联合处理对水模拟体系中三唑磷的降解效果,分析超声功率、三唑磷初始浓度和溶液pH对其降解效果的影响,并探究其降解动力学,以期为采用超声波/H2O2清洗技术控制水果、蔬菜等农产品中的农药残留提供理论依据,并对拓宽超声波技术的应用范围、有效提高食品安全性提供一定的科学意义和实用价值。
1 材料与方法
1.1材料与仪器
三唑磷标准品纯度≥98.0%,德国Dr.Ehrenstorfer公司;乙腈色谱纯,韩国Honeywell Burdick&Jackson公司;Na2HPO4·2H2O、KH2PO4·2H2O、H2O2(质量分数为30%)、氢氧化钠、磷酸分析纯试剂。
Scientz-IID型超声波细胞粉碎机宁波新芝生物科技股份有限公司;Milli-Q超纯水机美国Millipore公司;Agilent 1200型高效液相色谱仪(配有多波G1315C/D,G1365C/D二极管阵列检测器和B.04.01色谱工作站)、ZORBAX-XDB C18色谱柱(5 μm×4.6 mm(i.d)×250 mm)、Eclipse XDB-C18保护柱美国Agilent公司。
1.2实验方法
1.2.1标准溶液的配制称取三唑磷标准品10 mg(精确到0.0010 g)于10 mL容量瓶,用乙腈溶解定容,配制成1000 mg/L的标准储备液,-18℃下避光保存。将标准储备液用乙腈稀释成0.5、1.0、2.0、5.0、8.0 mg/L的系列标准工作溶液用于制作标准曲线。
1.2.2样品制备采用Na2HPO4·2H2O和KH2PO4·2H2O配制pH为7的磷酸盐缓冲液,用磷酸和氢氧化钠溶液调节至指定pH。向上述磷酸盐缓冲液中添加一定量浓度为1000 mg/L的三唑磷储备液,混匀后即得三唑磷水模拟体系,用于后续实验。
1.2.3添加回收率与精密度准确量取50、100、200、300、400、500 μL浓度为1000 mg/L的三唑磷储备液,采用1.2.2中所制得的磷酸盐缓冲液分别定容至100 mL,得到浓度为0.5、1.0、2.0、3.0、4.0、5.0 mg/L的三唑磷水溶液,每个浓度分别添加6份,涡旋混匀后放置过夜12 h,然后按照1.2.4进行提取和检测,并计算添加回收率和相对标准偏差。
1.2.4超声波/H2O2联合处理准确量取100 mL 1.2.2中制备的三唑磷水模拟体系溶液于容积为150 mL的冷阱中(冷阱连接于20℃恒温循环器上以保持处理过程中温度恒定),加入适量的H2O2后在设定的超声功率下进行超声波处理,每隔一定时间取样,样品采用终止剂Na2SO3去除剩余的H2O2。处理后的样品于4℃下保存,并在48 h内分析完毕。
1.2.4.1不同处理条件的影响在三唑磷浓度为2.46 mg/L、pH为5的条件下,研究超声波(850 W)、H2O2(2.5 g/L)和超声波/H2O2联合处理(超声功率:850 W;H2O2添加浓度:2.5 g/L)对三唑磷的降解率。
1.2.4.2超声功率的影响在三唑磷浓度为2.46 mg/L、pH为5、H2O2添加浓度为2.5 g/L条件下,分别分析超声功率为475、650、850 W时三唑磷的降解率。
1.2.4.3农药初始浓度的影响在超声功率为850 W、pH为5、H2O2添加浓度为2.5 g/L条件下,分别分析三唑磷初始浓度为2.46、10.20、19.82 mg/L时三唑磷的降解率。
1.2.4.4溶液pH的影响为避免大功率超声波可能掩盖pH对三唑磷降解率的影响,采用低功率超声(300 W)处理、三唑磷添加浓度为2.46 mg/L、H2O2添加浓度为2.5 g/L的水溶液,分析pH为3、5、7、9时三唑磷的降解率。
1.2.5分析方法
1.2.5.1样品前处理取1.2.3处理后的三唑磷溶液2 mL于15 mL离心管中,加入4 mL乙酸乙酯,涡旋振荡30 s后,5000 r/min离心3 min;将乙酸乙酯相转移至20 mL样品瓶中,下层水相再分别用4 mL乙酸乙酯萃取2次,重复上述操作,合并乙酸乙酯相,氮吹干后用乙腈定容至1 mL,用0.22 μm的针式过滤器过滤后转移至样品瓶中待HPLC分析。
1.2.5.2HPLC检测条件采用Agilent 1200高效液相色谱仪测定三唑磷浓度。色谱条件为:色谱柱:Agilent ZORBAX-XDB C18(5 μm×4.6 mm(i.d)× 250 mm);柱温:40℃;流动相:乙腈/超纯水=80/20;流速:1.0 mL/min;进样体积:10 μL;检测波长:245 nm。
1.2.6数据分析三唑磷的降解率采用公式:降解率(%)=(C0-Ct)/C0×100计算,其中t表示时间,C0和Ct分别表示农药的初始浓度和t时刻的浓度。
一级动力学模型是一个广泛应用于描述农药在自然环境中降解的数学模型[11-12]。其表达式为:Ct=C0e-kt,将两边取自然对数,该公式可换化为:ln(Ct/C0)=-kt。
半衰期t1/2是研究一级动力学中的重要参数,它指某种特定物质的浓度经过某种反应降低到初始浓度一半时所消耗的时间,其计算公式为:t1/2=ln2/(10k)。
本研究所有实验均重复三次,采用Origin 9.0制图并对实验数据进行方差分析,显著水平p为0.05,当p<0.05时,表示差异显著。
2 结果与讨论
2.1三唑磷分析方法的回收率和精密度
三唑磷的定性分析采用与标准品出峰时间比较的方法,其定量分析采用外标法。实验结果表明,在0.5~8.0 mg/L的浓度范围内,三唑磷的响应值与浓度呈良好的线性关系(R2>0.99);当水体系中三唑磷浓度为0.5~5.0 mg/L时,其回收率为89.6%~94.5%,相对标准偏差为1.9%~7.6%。方法的精密度达到农药残留分析的要求,检测方法准确可靠[13]。
2.2不同实验条件下三唑磷的降解
不同实验条件下三唑磷的降解效果如图1所示。从图1可以看出,三种处理对三唑磷均具有显著降解作用。与单独超声、H2O2处理相比,超声/H2O2联合处理对三唑磷具有明显的协同降解作用。以处理时间90 min为例,单独超声波和H2O2作用下三唑磷的降解率分别为22.8%和15.0%,而采用超声/H2O2联合处理时,三唑磷的降解率提高到35.6%。这与Yavuz等采用超声波/H2O2降解耐碱红时的结果类似[14]。超声/H2O2联合处理对三唑磷的降解作用与空化效应以及由此产生的羟自由基有关。研究表明[15],在超声过程中,有大量空化气泡形成,空化气泡会在极短时间内崩溃破裂;在气泡破裂的过程中,空化气泡及其周围极小空间范围内出现热点(Hot spot),产生1900~5200℃的高温和超过50 MPa的高压[15],这种极端条件造成体系中的水分子发生热分解作用,产生活性极强的羟自由基[16];同时,超声波作用下H2O2也会分解生成羟自由基;羟自由基所具有的强氧化性促进了三唑磷的降解。
从图1中还可以看出,在三种处理条件下,三唑磷的降解率均随着处理时间的延长而显著提高。分别采用超声波、H2O2和超声波/H2O2联合处理时,处理90 min时三唑磷的降解率分别是处理30 min时的3.8、3.3和2.1倍。尤其值得注意的是,采用超声波和超声/H2O2处理时,随处理时间的延长,三唑磷的降解率均呈持续上升趋势;而采用H2O2处理60 min后,三唑磷的降解率则上升缓慢,这和Kang等[17]采用γ射线/H2O2降解壳聚糖时的规律一致。其原因可能是:采用超声波和超声/H2O2联合处理时,参与降解反应的羟自由基随着超声处理时间的延长而不断生成,进而促进三唑磷降解反应的持续进行[16];采用单独H2O2处理时,H2O2随着反应的进行而不断被消耗,造成三唑磷的降解速度下降。

图1 不同实验条件对三唑磷降解率的影响Fig.1 Effect of experimental conditions on the degradation of triazophos
2.3超声功率对三唑磷降解效果的影响
超声功率是影响污染物降解的重要参数之一。如图2所示,超声功率对三唑磷的降解有显著影响(p<0.05);且随着超声功率的增加,三唑磷的降解率上升。以处理时间45 min为例,采用功率为850 W的超声波处理时,三唑磷的降解率为21.5%,分别是采用650 W和475 W处理时的1.6和2.1倍。在Schramm& Hua[18]报道的超声波降解敌敌畏的研究中也有类似规律。超声功率的提高对三唑磷降解的促进作用和空化效应有关。当超声功率提高时,输入处理体系中的总能量增加,从而提高了空化效应,引起空化气泡的增加以及更高浓度羟自由基的产生[19];更高浓度的羟自由基可以与更多的三唑磷分子反应,从而提高其降解率;此外,高功率下超声所带来的更强烈的机械效应如搅拌和振荡等[20]也有利于三唑磷的降解。
2.4农药初始浓度对三唑磷降解效果的影响
如图3所示,三唑磷的降解率随初始浓度的增加而降低。以处理时间60 min为例,当初始浓度为2.46 mg/L时,三唑磷的降解率为27.0%;当初始浓度提高到19.82 mg/L时,三唑磷降解率降低至9.7%。这和Singla等采用超声波降解马休黄染料时的结果一致[21]。尽管初始浓度为19.82 mg/L时三唑磷的降解率低,但其降解量(192.3 μg)却显著高于低浓度时(2.46 mg/L)的降解量(66.4 μg)。这种现象和超声过程中羟自由基的形成有关。Tauber等[22]提出,羟自由基不仅能够参与污染物的降解反应,且羟自由基可重新结合生成H2O2;在特定的超声条件下,羟自由基的生成浓度是一定的,当三唑磷浓度较低时,羟自由基以合成H2O2为主;随着三唑磷初始浓度的增加,更多的羟自由基会攻击三唑磷分子,引起更多三唑磷分子的降解。
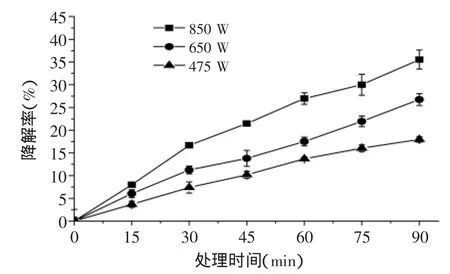
图2 超声功率对超声/H2O2降解三唑磷的影响Fig.2 Effect of ultrasonic power on the degradation of triazophos by ultrasonic/H2O2system
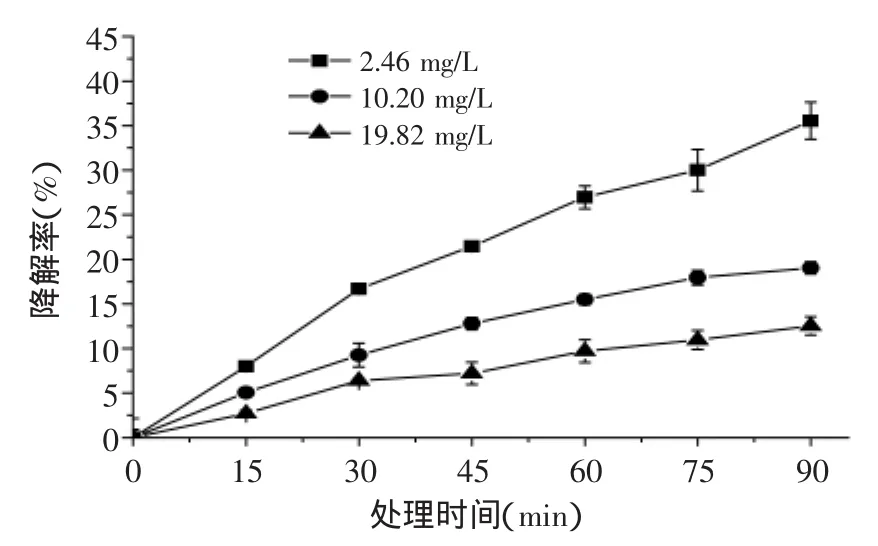
图3 初始浓度对超声/H2O2降解三唑磷的影响Fig.3 Effect of initial concentration of triazophos on the degradation by ultrasonic/H2O2system
2.5pH对三唑磷降解效果的影响

图4 pH对超声/H2O2降解三唑磷的影响Fig.4 Effect of pH on the degradation of triazophos by ultrasonic/H2O2system
不同pH下三唑磷的降解效果如图4所示。方差分析表明,在pH3~7的范围内,溶液pH对三唑磷的降解率无显著影响;当pH从7~9时,三唑磷的降解率显著上升;当pH为9时,处理90 min后三唑磷的降解率达到最高值79.2%。已有研究表明,三唑磷在酸性环境中较为稳定(pH=4~7时,半衰期为17.2~31.2 d),而在碱性环境中极易发生分解(pH=8~10时,半衰期为1.3~7.5 d)[23]。由此可见,采用超声/H2O2处理时,三唑磷在不同pH下的稳定性与其性质紧密相关。该现象也提示:采用超声/H2O2去除三唑磷时,可适当增加体系pH,以提高降解效率。
2.6三唑磷降解动力学
表1~表3分别为不同超声波功率、农药初始浓度和溶液pH时三唑磷的降解动力学参数。从表中可以看出,除pH为9时外,各模型的相关系数R2均大于0.94,p值均小于0.001,说明一级动力学模型能很好的拟合超声/H2O2作用下三唑磷的降解规律。事实上,一级动力学可描述超声波处理中多种污染物的降解过程[7,24],本研究也得到了相近的结果。
从表1和2可以看出,在不同超声波功率和农药初始浓度下,三唑磷的降解速率常数和半衰期有明显变化,规律如下:k850W>k650W>k475W,k2.46mg/L>k10.20mg/L>k19.82 mg/L;t1/2 475 W>t1/2 650 W>t1/2 850 W,t1/2 19.82 mg/L>t1/2 10.20 mg/L>t1/22.46mg/L,说明功率的上升和农药初始浓度的下降有利于提高农药的降解速率,这和图2、图3的降解率数据一致。从表3可以看出,pH为3~7时,k值的变化幅度较小,说明pH对三唑磷的降解无显著影响;当pH值从7升至9时,k值显著提高,说明碱性条件有利于三唑磷的降解,这和图4所得的降解率数据一致。

表1 不同超声功率时水模拟体系中三唑磷的一级动力学模型参数Table 1 Kineticparameterscalculatedbyfirst-orderkineticmodel for the degradation of triazophos in aqueous solution under different ultrasonic power
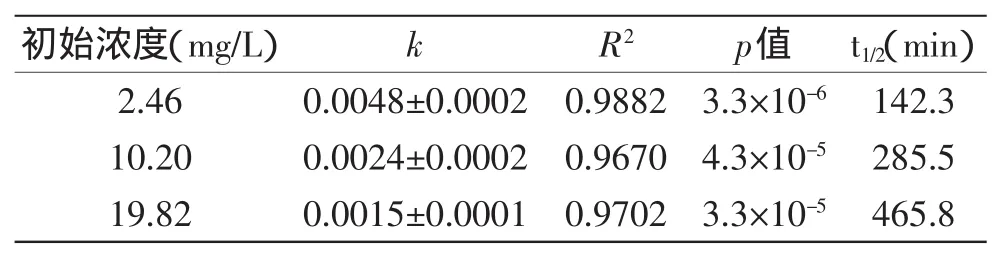
表2 不同农药初始浓度时水模拟体系中三唑磷的一级动力学模型参数Table 2 Kinetic parameters calculated by first-order kinetic model of triazophos in aqueous solution with different initial concentrations

表3 不同pH时水模拟体系中三唑磷的一级动力学模型参数Table 3 Kinetic parameters calculated by first-order kinetic model of triazophos in aqueous solution at different pH values
3 结论
3.1超声波/H2O2联合处理对水模拟体系中的三唑磷具有良好的降解效果。与单独超声、H2O2处理相比,超声波/H2O2联合处理能更有效地降解水模拟体系中的三唑磷,且处理时间越长,农药的降解率越高。
3.2在本研究条件下,采用超声波/H2O2联合处理时,三唑磷的降解率随超声功率的提高而显著增加;在农药浓度为2~20 mg/L的范围内,降低农药初始浓度能提高三唑磷的降解率;pH对三唑磷的降解率有显著影响,且碱性条件更有利于三唑磷的降解。当溶液pH为9,H2O2添加浓度为2.5 g/L,农药初始浓度为2.46 mg/L时,采用300 W的超声波处理90 min后三唑磷的降解率高达79.2%。
3.3动力学分析的结果表明,一级动力学模型能很好地拟合水模拟体系中三唑磷在超声/H2O2作用下的降解规律。
[1]Tomlin C D S.The pesticide manual:A world compendium[M].Farnham,U.K.:British Crop Protection Council Publications,2006:925-926.
[2]董竞武,杨隽,洪新宇,等.三唑磷原药的大鼠两代繁殖毒性研究[J].癌变畸变突变,2003,24(6):448-451.
[3]Jain S,Ahmed R S,Arora V K,et al.Biochemical and histopathological studies to assess chronic toxicity of triazophos in blood,liver and brain tissue of rats[J].Pesticide Biochemistry and Physiology,2011,100(2):182-186.
[4]Aadil R M,Zeng X-A,Han Z,et al.Effects of ultrasound treatments on quality of grapefruit juice[J].Food Chemistry,2013,141(3):3201-3206.
[5]Ferrario M,Alzamora S M,Guerrero S.Study of the inactivation of spoilage microorganisms in apple juice by pulsed light and ultrasound[J].Food Microbiology,2015,46:635-642.
[6]U.S.Food and Drug Administration.Kinetics of microbial inactivationforalternativefoodprocessingtechnologies--Ultrasound[EB/OL].http://www.fda.gov/food/foodscienceresearch/ safepracticesforfoodprocesses/ucm100158.htm,2014-12-18/2015-03-02.
[7]Matouq M,Al-Anber Z,Susumu N,et al.The kinetic of dyes degradation resulted from food industry in wastewater using high frequency of ultrasound[J].Separation and Purification Technology,2014,135:42-47.
[8]Sutar R S,Rathod V K.Ultrasound assisted enzyme catalyzed degradationofCetirizinedihydrochloride[J].Ultrasonics Sonochemistry,2015,24:80-86.
[9]Orr P T,Jones G J,Hamilton G R.Removal of saxitoxins from drinking water by granular activated carbon,ozone and hydrogen peroxide-implications for compliance with the Australiandrinking water guidelines[J].Water Research,2004,38(20):4455-4461.
[10]袁小强,万茵,刘成梅,等.H2O2降解草甘膦条件的响应面法优化[J].农药,2014,53(11):792-795.
[11]Cengiz M F,Certel M,Göçmen H.Residue contents of DDVP(Dichlorvos)and diazinon applied on cucumbers grown in greenhouses and their reduction by duration of a pre-harvest interval and post-harvest culinary applications[J].Food Chemistry,2006,98(1):127-135.
[12]El Beit I O D,Wheelock J V,Cotton D E.Factors influencing the degradation of dimethoate in soils and solutions[J].International Journal of Environmental Studies,1978,11(4):253-260.
[13]Putnam R A,Nelson J O,Clark J M.The persistence and degradation of chlorothalonil and chlorpyrifos in a cranberry bog[J].Journal of Agricultural and Food Chemistry,2003,51(1):170-176.
[14]Yavuz Y,Koparal A S,Artık A,et al.Degradation of C.I. Basic Red 29 solution by combined ultrasound and Co2+-H2O2system[J].Desalination,2009,249(2):828-831.
[15]Suslick K S.Sonochemistry[J].Science,1990,247(4949):1439-1445.
[16]Makino K,Mossoba M M,Riesz P.Chemical effects of ultrasound on aqueous solutions.Formation of hydroxyl radicals and hydrogen atoms[J].The Journal of Physical Chemistry,1983,87(8):1369-1377.
[17]Kang B,Dai Y-d,Zhang H-q,et al.Synergetic degradation of chitosan with gamma radiation and hydrogen peroxide[J]. Polymer Degradation and Stability,2007,92(3):359-362.
[18]Schramm J D,Hua I.Ultrasonic irradiation of dichlorvos:Decomposition mechanism[J].Water Research,2001,35(3):665-674.
[19]Dükkanci M,Gündüz G.Ultrasonic degradation of oxalic acid in aqueous solutions[J].Ultrasonics Sonochemistry,2006,13(6):517-522.
[20]Zhang Y,Xiao Z,Chen F,et al.Degradation behavior and products of malathion and chlorpyrifos spiked in apple juice by ultrasonic treatment[J].Ultrasonics Sonochemistry,2010,17:72-77.
[21]Singla R,Grieser F,Ashokkumar M.Sonochemical degradation ofmartiusyellowdyeinaqueoussolution[J].Ultrasonics Sonochemistry,2009,16(1):28-34.
[22]Tauber A,Schuchmann H-P,von Sonntag C.Sonolysis of aqueous 4-nitrophenol at low and high pH[J].Ultrasonics Sonochemistry,2000,7(1):45-52.
[23]Kunde L,Dongxing Y,Yongzhi D,et al.Hydrolytic products and kinetics of triazophos in buffered and alkaline solutions with different values of pH[J].Journal of Agricultural and Food Chemistry,2004,52(17):5404-5411.
[24]Zhang Y,Zhang Z,Chen F,et al.Effect of sonication on eliminating of phorate in apple juice[J].Ultrasonics Sonochemistry,2012,19(1):43-48.
Degradation of triazophos in aqueous solution by ultrasonic/H2O2system
ZHANG Yuan-yuan,CHEN Zhong-zheng,LUO Wen-chao,LU Hai-yan,LI Bin*,YIN Tao
(College of Food Science,South China Agricultural University,Guangzhou 510642,China)
This study focused on the degradation of one of organophosphorus pesticides triazophos by an ultrasonic/H2O2system and the factors including ultrasonic power,initial concentration of triazophos and pH value of aqueous solution on the degradation were investigated.Results indicated that the ultrasonic/H2O2system was effective in the degradation of triazophos in aqueous solution and had a noticeable synergetic effect in the removal of triazophos compared with the single treatment of ultrasonic and H2O2.Furthermore,the degradation efficiency of triazophos was significantly improved as ultrasonic power increased from 475 W to 850 W.In addition,the degradation efficiency declined as the initial concentration of triazophos increased from 2 mg/L to 20 mg/L under ultrasonic/H2O2treatment.It was also found that the degradation of triazophos was strongly pH-dependent and alkalinity condition favored the degradation.The degradation efficiency was 79.2% when the ultrasonic treatment was operated at 300 W for 90 min with pH value of 9 with the concentrations of triazophos and H2O2at 2.46 mg/L and 2.5 g/L,respectively.The degradation kinetics of triazophos was fitted to the first-order kinetics model well.
ultrasonic;hydrogen peroxide;triazophos;degradation kinetics
TS201.2
B
1002-0306(2015)16-0248-05
10.13386/j.issn1002-0306.2015.16.042
2015-03-09
张媛媛(1983-),女,博士,副教授,研究方向:食品安全与污染物控制,E-mail:zhangyy@scau.edu.cn。
李斌(1960-),女,博士,教授,研究方向:食品化学与营养,E-mail:bli@scau.edu.cn。
农业部现代农业产业技术体系专项资金(CARS-23);国家自然科学基金(31201450);华南农业大学校长基金。

