一种底泥释放气体收集装置的设计
胡茂俊等

摘要:针对底泥温室气体排放和反硝化气态脱氮的原位研究亟需有效、便捷收集底泥释放气体方法的现状,自主研发了一种可连续、自动、有效收集底泥释放气体的装置。本文对该装置的结构和功能进行了详细的描述,并利用该装置研究了江苏省农业科学院富营养化水塘中泥水界面释放气体速率及各种气体组分(N2、N2O、CH4、CO2、O2)的释放情况。结果表明,该装置成功实现了原位定量研究底泥产生并释放气体的速率以及各气体组分的释放速率。该技术为利用N2直接测定法原位研究底泥的反硝化脱氮过程,以及底泥释放温室气体规律提供了可靠的方法。
关键词:底泥;反硝化;温室气体;气体收集装置;气体释放;原位研究
中图分类号: X52文献标志码: A文章编号:1002-1302(2015)09-0418-04
自从1776年Alessandro Volta使用倒置漏斗收集水体沼气以来[1],类似的装置常被用于采集水体、底泥释放的冒泡气体(gas bubbles)[2-3],尤其在近年对水体、底泥温室气体释放的研究中发挥着重要作用[4-6]。倒置漏斗式集气装置在使用过程中不断得到改进。1989年,Chanton等描述了一种利用漂浮在水面的锥形装置测定潮汐河口释放冒泡气体通量的方法,该装置通过长5~10 m、直径0.358 cm的聚乙烯管将注射器连接到采气装置顶部,定期手动采集所收集的气体样品。1992年,Sorrell等在落基山科罗拉多河用漂浮的密封塑料装置测量冒泡CH4释放过程,在每个采样周期,该装置均为密封,气样通过隔垫用配有三通的玻璃注射器抽取[3]。1994年,Keller等在巴拿马市加通湖的另一个研究项目中应用了类似装置收集冒泡CH4气体,并在装置的边缘安装了锚以限制其在水中四处飘动,该方法使得倒置漏斗集气装置固定漂浮于底泥上方,免去了人工将倒置漏斗控制在采样点的过程,可以实现多点同时采样;此外,为了取样方便,在该装置的顶端通过鲁尔接口和注射器与聚乙烯采气试管相连[4]。
在对底泥温室气体排放和反硝化脱氮的规模化原位研究中,亟需有效、便捷、自动收集底泥释放气体的装置,并能对收集气体样品中反硝化脱氮气态终产物N2进行精确定量测定的方法。在科学研究中,结果的获取在很大程度上依赖于研究方法和工具。针对此现状,本文主要介绍一种底泥释放气体连续自动收集装置的结构和使用方法,该装置根据排水集气原理并结合倒置漏斗方法进行设计,适用于直接测定所收集气体中的硝化、反硝化脱氮终产物N2,温室气体CH4、CO2、N2O,以及反映底泥新陈代谢(光合作用和呼吸作用)情况的O2含量,并揭示了富营养化水体底泥释放气体(N2、CH4、CO2、N2O)的规律及特征。
1材料与方法
1.1基本原理
通过悬挂在水面之下、底泥之上5 cm的气体收集罩,收集底泥产生并释放到水体中的气体。当集气罩内积聚的气体形成一定压力时,在压力差的作用下,收集的气体通过进气管自动被吸入预先充满水的集气瓶,相应体积集气瓶中的水通过排水管排入水体,从而可连续、自动收集底泥中释放的气体。
1.2底泥释放气体采集装置描述
图1为连续自动收集底泥释放气体装置的系统结构。该装置适用于自然水体底泥释放气体的直接收集,包括方形浮球支架、连接杆、固定旋钮、集气瓶、阀门、进气管、排水管、排气管、集气罩等。方形浮球支架上顶部有1块有孔硬质板,孔位于硬质板中部,允许连接杆通过;孔上方有固定旋钮,用于固定连接杆,连接杆有刻度。方形浮球支架的硬质板下方有小钩,用来悬挂集气瓶,集气瓶的瓶口处有进气管和排水管。集气罩顶端有排气孔,排气孔通过排气管与悬挂在浮球支架上的集气瓶的进气管连接,连接处位于水面上且有三通阀。集气罩罩体外面附着有支架,支架上方有固定旋钮,固定旋钮可以与连接杆的下端相连并固定,集气罩下方边缘处有摄像头支架,用来放置水下摄像头。集气罩底边附着有垂直向下的刻度尺,并在刻度尺上涂有反光漆以提高水下能见度。
本装置各个组件间连接牢固,组装与拆卸均方便快捷,尤其适合于水面行船作业。集气罩底边上的摄像头可以将集气罩底边以及所附属的刻度尺的图像传输到电脑上,通过摄影图像的指引调节连接杆长度,可将装置正确放置于底泥上方5 cm处,从而实现释放气体的定位直接收集。该装置应用性广,可实现野外自然水体不同环境下底泥释放气体的研究。
在放置底泥释放气体采集罩时,注意保证采气装置的底部与水底之间有5 cm距离,以免装置摇晃对底泥产生干扰。开始连接采气装置时,如图1所示,首先将浮球支架放置于水面上,将连接杆与浮球支架连接,连接杆末端位于水面上,旋
紧固定旋钮1对连接杆进行初步固定。然后将集气罩放入水下,把集气罩上方的固定旋钮2与连接杆底端连接并旋紧固定。集气罩上方排气孔上连接气路管,气路管末端连接三通阀并一直位于水面上,气路管长度与水柱深度一致。然后将水下摄像头放置于集气罩底边的摄像头支架上,并通过电脑捕获水下图片。此时,一边将浮球支架上的固定旋钮缓慢松开,一边抓紧连接杆,缓慢向下移动,通过电脑捕获水下图像和连接杆上的刻度指示将集气罩正确放置于底泥上方5 cm处,将浮球支架上的固定旋钮旋紧,连接杆不再上下移动。最后将集气瓶悬挂于浮球支架上,进气管与排气管相连,排水管打开放入水中,并确保管路中没有气泡,最后打开三通阀。
1.3试验方案
在江苏省农业科学院内2#蓄水塘布置上述采气装置,进行底泥释放气体样品的采集,采样装置分布于蓄水塘中心,用尼龙绳将采气装置栓于塘中的毛竹桩上,固定在一定范围之内。采样时间为2012年8月30日至9月1日,采样的同时采用多功能水质测定仪对泥水界面的溶氧值和温度进行测定。在采样点布置采气装置的时间为试验开始当日08:00。布置采气装置时,将集气罩完全浸没于水中,距底泥5 cm左右,使气罩和进气管中空气全部排出,并将准备好的装满水的集气瓶倒挂于浮球支架顶端。然后,将集气瓶与集气罩之间的出气管与进气管连通。将出水管的尾端浸没于水中。注意准备过程中确保集气瓶与相关管道中无任何细小的气泡。记录集气瓶初始重量。18:00左右将集气瓶从浮球支架上取下,替换新集气瓶,分别收集白天、夜晚水体释放的气体。集气瓶用天平称重,计算产气量。集气瓶中的气体直接用气相色谱仪测定N2、O2、N2O、CH4、CO2气体浓度。endprint
1.4收集气体的成分分析
集气瓶中收集的气体样品采用气相色谱仪(SHIMADZU,GC2010)进行分析。气体测定采用阀进样方式,阀进样系统配有1 mL的定量管,并采用十通进样阀自动进样。填充柱为Porapak Q柱(2 m×2 mm)、Porapak Q柱(3 m×2 mm)和Porapak QS柱(6 m×2 mm),测定样品时柱温保持70 ℃。N2、CH4、O2、CO2检测采用热导检测器(TCD),检测器温度200 ℃,高纯H2作为载气,流速为 8 mL/min,电流70 mA。N2O检测采用ECD检测器,检测器温度为300 ℃,电流为1.0 nA,尾吹气为5% CH4/Ar,流量为30.0 mL/min。以上气体的浓度采用峰面积外标法定量。
1.5气体通量计算
收集的气体体积(mL)、气体释放速率[底泥单位面积单位时间内释放气体的总量,mL/(m2 ·h)]、气体释放通量[底泥单位面积单位时间内释放某种气体的量,mg/(m2 ·h)],计算方法详见文献[1]。
2结果与分析
2.1水体释放气体样品的N2、O2、N2O、CH4、CO2浓度
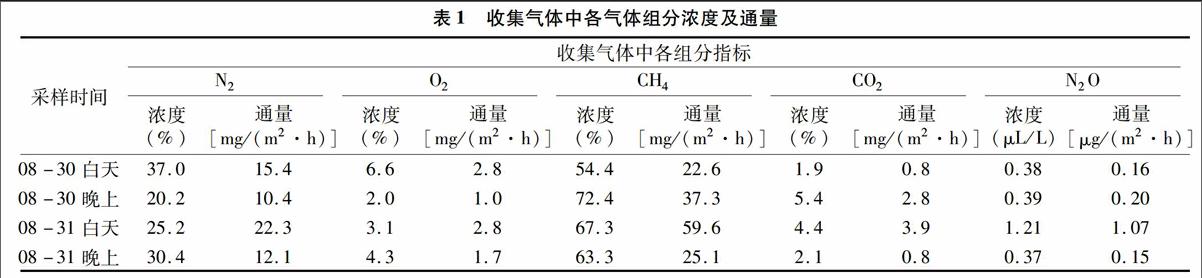
该试验采用一套采气装置,在8月30—31日连续2 d分别收集白天和晚上底泥产生的气体,采集的气体直接用气相色谱仪测定各种组分的浓度,结果见表1。表1收集气体中各气体组分浓度及通量2.2底泥释放气体速率
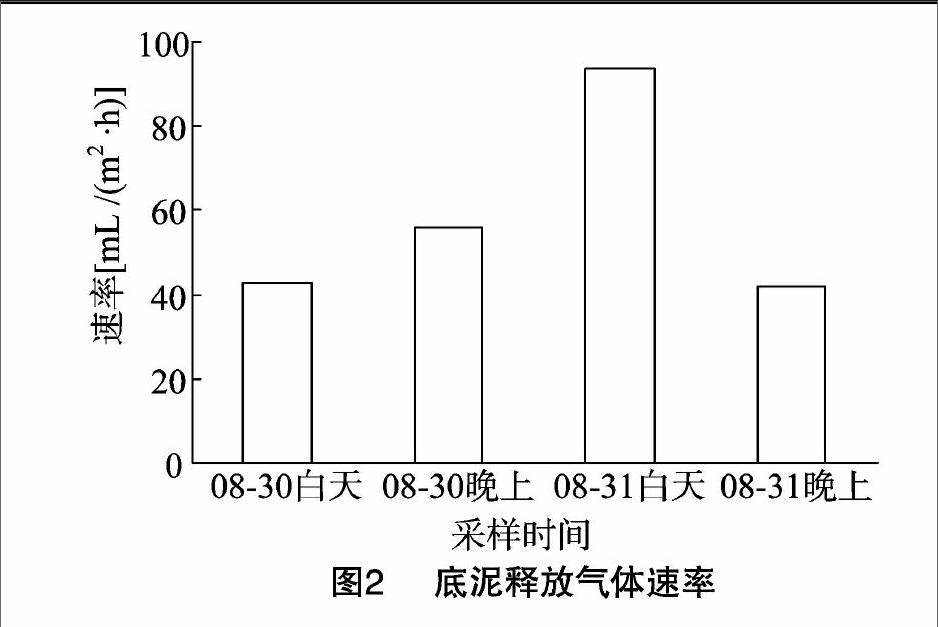
如图2所示,江苏省农业科学院富营养化蓄水塘底泥8月30日白天(08:00—18:00)释放气体的速率为 42.91 mL/(m2 ·h),30日夜间(18:00—08:00)释放气体的速率为55.82 mL/(m2 ·h),31日白天(08:00—18:00)释放气体的速率为93.76 mL/(m2 ·h),31日夜间(18:00—08:00)释放气体的速率为 42.12 mL/(m2 ·h)。
2.3底泥释放气体中N2通量
如表1所示,江苏省农业科学院富营养化蓄水塘底泥白天(08:00—18:00)释放N2的通量为15.4、22.3 mg/(m2·h), 明显
高于夜间(18:00—08:00)的10.4、12.1 mg/(m2·h)。
2.4底泥释放气体中O2通量
如表1所示,江苏省农业科学院富营养化蓄水塘底泥白天(08:00—18:00)释放O2的通量为2.8、2.8 mg/(m2 ·h),明显高于夜间(18:00—08:00)的10、1.7 mg/(m2 ·h)。
2.5底泥释放气体中CH4通量
如表1所示,江苏省农业科学院富营养化蓄水塘底泥白天(08:00—18:00)释放CH4的通量为22.6、59.6 mg/(m2 ·h),夜间(18:00—08:00)释放CH4的通量为37.3、25.1 mg/(m2 ·h)。
2.6底泥释放气体中CO2通量
如表1所示,江苏省农业科学院富营养化蓄水塘底泥白天(08:00—18:00)释放CO2的通量为0.8、3.9 mg/(m2 ·h),夜间(18:00—08:00)释放CO2的通量为2.8、0.8 mg/(m2 ·h)。
2.7底泥释放气体中N2O通量
该试验采用一套采气装置,在8月30-31日连续2天分别收集白天和晚上底泥产生的气体,测定气体样品中N2O浓度并计算N2O通量。如表1所示,发现江苏省农业科学院富营养化蓄水塘底泥白天(08:00—18:00)释放N2O的通量为0.16、1.07 μg/(m2·h);夜间(18:00—08:00)释放N2O的通量为0.20、0.15 μg/(m2·h)。
3讨论
已有研究中,直接收集底泥释放气体主要采用倒置漏斗法。使用简单的倒置漏斗装置采集气体时,需要在每个采样点人工将漏斗或漏斗形状的采样装置倒置在底泥上方,并等待一定量气体进入倒置漏斗后引入集气容器中[2-3]。这种采样方式耗时、费力,在进行大范围采样研究过程中工作量过大。虽然不断对倒置漏斗装置进行改进,达到了原位收集底泥释放冒泡气体的目的,但仍不能同步进行气体收集和气体采样[7-9],因此不能完全解决大范围采样过程中工作量较大、采样不及时、容易引入误差等问题。使用本文描述的装置,达到了原位、连续、自动收集底泥释放冒泡气体的目的,无需在每个采样点上等待整个气体采集过程的完成,也无需手动抽取收集的气体,实现了气体的自动收集与采集,方便简单,且可同时进行多点采样,减少不同采样点因采样时间的不同步造成的结果差异,适用于较大尺度的底泥释放气体原位收集。本文描述的装置还可以根据水体释放气体的速度调节采样时间,既适用于研究产气量大、产气速度快的底泥,也适用于有冒泡气体产生但产气缓慢的底泥。本文描述的装置还适用于收集特定时间段水体释放的气体,例如研究水体昼夜释放气体的规律特性。由于本方法可连续自动采集收取的气体,因而还可以精确定量一定面积一定时间内底泥释放气体的总量。
倒置漏斗法在采集气体时因需要人为抽取气体,在采气过程中增加了与空气接触的机会,而本方法直接采用排水集气原理自动将收集到的底泥释放气体吸入集气瓶,最大程度地保证了采集的气体样品均来自于底泥释放的气体,而不受空气污染,适用于底泥释放N2的原位研究。准确收集水体、土壤及底泥硝化、反硝化脱氮释放N2的方法一直是国内外共同面临的难题。这主要是由于N2在空气中的本底值极高,强烈干扰着脱氮过程产生的N2的收集和测定,使得以往关于水体脱氮的研究只能借助间接测定的方法,并不能对水体向大气释放的氮量做出直接测定和比较精确的定量化评估[10]。本文描述的装置利用倒置漏斗方法的同时结合排水集气原理,达到了定量收集、测定底泥释放气体中硝化、反硝化脱氮产物N2的目的,在原位研究反硝化脱氮方面取得了重要的突破。endprint
本试验详尽测定了底泥释放气体的组成成分,包括N2、CH4、CO2、N2O、O2。以往的研究虽然收集了底泥气体,但并未对收集气体中的成分做详尽分析,仅重点关注了CH4的含量。本研究的测定结果表明所收集气体的主要组成成分为CH4(24.3~32.3 mmol/L)、N2(9.0~16.5 mmol/L)、O2(0.9~2.9 mmol/L)。这与以往认为水体冒泡气体以CH4为主的观点不尽相同。以往传统的气体采集装置和方法不能解决同时直接测定上述气体的问题,本文描述的采气装置在该方面也取得了突破,避免了采用不同方法造成的取样及测定误差。CH4、N2O、CO2等温室气体排放能够引起全球范围内温度持续变暖,引起了世界各国的关注。其中CH4是全球变暖研究中最受重视的温室气体之一[11-12]。从CH4的产生机制来看,主要由厌氧发酵产生,水体生态系统(如湖泊、水库、池塘等)底泥长期处在淹水状态下,且含有丰富的有机质、养分和大量的微生物,完全符合CH4的产生条件[13-14]。同时,由于水体的富营养化程度不断加剧,底泥中聚集了丰富的氮、磷营养盐,底泥中的生物硝化、反硝化脱氮作用强烈。本方法可用于直接收集并测定底泥释放气体的研究,有助于全面掌握底泥对于温室气体排放的贡献,对于底泥中生物脱氮过程的研究具有实际应用价值。
本装置在使用过程中须注意:在采样点布置装置时,要提前测量水体的深度,以此来确定连接杆放置到水下的大致深度,并在放置过程中时刻观察刻度尺,以确定不扰动底泥。在放置好浮球支架系统后要将集气罩完全浸没于水下,排除集气罩内的空气,并赶出采气装置系统内(包括集气罩、进气管、排水管等)各部分的细微气泡。准备集气瓶时应确定集气瓶充满水,无细小气泡。在连接集气瓶与进气管时需排除连接处的细小气泡。在收采气瓶时应让进气管中自动充满水,确保气瓶中气体不与空气接触。集气瓶收好气后应倒置以贮存气体,并及时测定。测定气体样品时,要注意保持气体样品的进样过程不被空气污染,保证不让空气进入气相色谱的进样系统。
中国的天然湿地系统的CH4释放量为2.46~30 mg/(m2·h) [15-18],本试验中测得的CH4释放通量为22.6~59.6 mg/(m2·h),远远高于湿地系统的CH4释放通量,这可能是因为湿地CH4释放具有很大的时空变异性[19],有关湿地释放CH4的研究多集中在低温地区[20-21],而本试验在亚热带地区夏季进行,是CH4释放最强烈的阶段;本研究中的富营养化水塘水力停留时间较长,且无外界扰动,底泥有机质丰富,这些都有利于厌氧环境的发酵及CH4释放过程。释放的CH4通过气泡扩散方式向大气中释放。我国湖泊的CH4释放通量0.01~1.12 mg/(m2 ·h)[22-23],也低于本试验数据,因为地表淹水过深时CH4不仅可以在水体中向各个方向扩散,还会在以气泡或扩散形式穿越水层时被氧化,水层越深CH4损失量越大[18],以往底泥释放气体的收集方法多漂浮在水面上,而本试验装置直接在底泥上方收集底泥产生的CH4,避免了CH4在水层上升时大量损失,有利于研究底泥释放CH4的潜力。
N2O是仅次于CO2和CH4的温室气体,其增温潜势是CO2的300倍左右[24-27]。研究表明,湖泊排放N2O的通量为16~28 μg/(m2 ·h)[28-30],远远高于本试验测定值,这可能是因为本试验研究的富营养化水塘长期淹水处于厌氧环境,有利于N2O进一步被还原为N2,向大气排放的N2O比较少[24,31-32],因此N2O含量较低。
参考文献:
[1]Gao Y,Liu X H,Yi N,et al. Estimation of N2 and N2O ebullition from eutrophic water using an improved bubble trap device[J]. Ecological Engineering,2013,57(4):403-412.
[2]Chanton J P,Marten C S,Kelley C A. Gas transport from methane-saturated,tidal freshwater and wetland sediment[J]. Limnology and Oceanography,1989,34(5):807-819.
[3]Sorrell K B,Boon P I. Biogeochemistry of billabong sediments. Ⅱ. Seasonal variations in methane production[J]. Freshwater Biology,1992,27(3):435-445.
[4]Keller M,Stallard R F. Methane emission by bubbling from Gatun Lake,Panama[J]. Journal of Geophysical Research,1994,99(D4):8307-8319.
[5]Bastviken D,Cole J,Pace M,et al. Methane emissions from lakes:dependence of lake characteristics,two regional assessments,and a global estimate[J]. Global Biogeochemical Cycles,2004,18(4):4009-4020.
[6]Delsontro T,Mcginnis D F,Sobek S,et al. Extreme methane emissions from a Swiss hydropower reservoir:contribution from bubbling sediments[J]. Environmental Science & Technology,2010,44(7):2419-2425.endprint
[7]王东启,陈振楼,王军,等. 夏季长江口潮间带CH4、CO2和N2O通量特征[J]. 地球化学,2007,36(1):78-88.
[8]胡启武,朱丽丽,幸瑞新,等. 鄱阳湖苔草湿地甲烷释放特征[J]. 生态学报,2011,31(17):4851-4857.
[9]沙晨燕. 季节性人工河滨湿地甲烷排放[J]. 生态环境学报,2012,21(7):1271-1276.
[10]胡玲珍,陈振楼. 反硝化实验方法研究综述[J]. 环境科学动态,2003(3):27-29.
[11]王明星. 中国稻田甲烷排放[M]. 北京:科学出版社,2001:1-4.
[12]张秀云,梁霞,何池全. 大型丝状藻类对城市河流甲烷排放的影响研究进展[J]. 应用生态学报,2013,24(5):1291-1299.
[13]周启星,朱荫湄. 西湖底泥不同供氧条件下有机质降解及CO2与CH4释放速率的模拟研究[J]. 环境科学学报,1999,19(1):11-15.
[14]李婷婷,张稳. 自然湿地甲烷排放模拟研究——模型的灵敏度分析与应用[J]. 气候与环境研究,2010,15(3):257-268.
[15]王德宣,丁维新,王毅勇. 若尔盖高原与三江平原沼泽湿地CH4排放差异的主要环境影响因素[J]. 湿地科学,2003,1(1):63-67.
[16]Hirota M,Tang Y H,Hu Q W,et al. Methane emissions from different vegetation zones in a Qinghai-Tibetan Plateau wetland[J]. Soil Biology and Biochemistry,2004,36(5):737-748.
[17]黄国宏,肖笃宁,李玉祥,等. 芦苇湿地温室气体甲烷(CH4)排放研究[J]. 生态学报,2001,21(9):1494-1497.
[18]陈槐,周舜,吴宁,等. 湿地甲烷的产生、氧化及排放通量研究进展[J]. 应用与环境生物学报,2006,12(5):726-733.
[19]Kayranli B,Scholz M,Mustafa A,et al. Carbon storage and fluxes within freshwater wetlands:a critical review[J]. Wetlands,2010,30(1):111-124.
[20]Song C C,Xu X F,Tian H Q,et al. Ecosystem-atmosphere exchange of CH4 and N2O and ecosystem respiration in wetlands in the Sanjiang Plain,Northeastern China[J]. Global Change Biology,2009,15(3):692-705.
[21]Long K D,Flanagan L B,Cai T B. Diurnal and seasonal variation in methane emissions in a northern Canadian peatland measured by eddy covariance[J]. Global Change Biology,2010,16(9):2420-2435.
[22]彭世彰,侯会静,徐俊增,等. 节水灌溉对稻田N2O季节排放特征的影响[J]. 农业工程学报,2011,27(8):14-18.
[23]陈永根,白晓华,李香华,等. 中国8大湖泊冬季水-气界面甲烷通量初步研究[J]. 湖泊科学,2007,19(1):11-17.
[24]王洪君,王为东,卢金伟,等. 太湖湖滨带秋、冬季CH4排放特征及其影响因素初步研究[J]. 湿地科学,2006,4(1):21-28.
[25]秦晓波,李玉娥,刘克樱,等. 不同施肥处理稻田甲烷和氧化亚氮排放特征[J]. 农业工程学报,2006,22(7):143-148.
[26]巩有奎,王赛,彭永臻,等. 生活污水不同生物脱氮过程中N2O产量及控制[J]. 化工学报,2010,61(5):1286-1292.
[27]朱波,易丽霞,胡跃高,等. 黑麦草鲜草翻压还田对双季稻CH4与N2O排放的影响[J]. 农业工程学报,2011,27(12):241-245.
[28]王仕禄,刘丛强,万国江,等. 贵州百花湖分层晚期有机质降解过程与溶解N2O循环[J]. 第四纪研究,2004,24(5):569-577.
[29]万晓红,周怀东,王雨春,等. 白洋淀湖泊湿地氧化亚氮的排放通量初探[J]. 生态环境,2008,17(5):1732-1738.
[30]王洪君,王为东,卢金伟,等. 湖滨带温室气体氧化亚氮(N2O)排放研究[J]. 生态环境,2006,15(2):270-275.
[31]李旭东,王昶,李琳. 湖泊湿地水陆交错带脱氮作用中N2O产生机理研究[J]. 时代报告:下半月,2012(2):302-303.
[32]邹建文,黄耀,宗良纲,等. 稻田CO2、CH4和N2O排放及其影响因素[J]. 环境科学学报,2003,23(6):758-764.endprint

