吡喃阿霉素治疗非霍奇金淋巴瘤的临床效果
胡秀娟 唐超莉 何春萍
(广西崇左市人民医院,广西 崇左 532200)
吡喃阿霉素治疗非霍奇金淋巴瘤的临床效果
胡秀娟 唐超莉 何春萍
(广西崇左市人民医院,广西 崇左 532200)
目的 探讨吡喃阿霉素治疗非霍奇金淋巴瘤的临床效果。方法 选择60例初治的非霍奇金淋巴瘤患者,分为观察组和对照组。观察组和对照组分别采用含吡喃阿霉素和阿霉素的方案化疗。评定两组临床效果。观察不良反应发生情况。结果 观察组化疗后临床效果评定的总有效率为66.7%;对照组化疗后临床效果评定的总有效率为66.7%;观察组的有效率和对照组有效率比较,差异无统计学意义(P>0.05)。不良反应(白细胞减少、血小板减少、贫血、消化道反应、肝功能损伤、脱发、心电图改变)中观察组在消化道反应、脱发、心电图改变发生率小于对照组,差异有统计学意义(P<0.05)。结论 吡喃阿霉素治疗非霍奇金淋巴瘤的临床效果和阿霉素治疗非霍奇金淋巴瘤的临床效果近似,但前者不良反应发生率低于后者,值得临床借鉴。
吡喃阿霉素;阿霉素;非霍奇金淋巴瘤
淋巴瘤是淋巴结或淋巴结外的相关淋巴组织发生的恶性肿瘤,按组织病理学改变,分非霍奇金淋巴瘤和霍奇金淋巴瘤。非霍奇金淋巴瘤较霍奇金淋巴瘤发病率高,呈逐年上升趋势,且恶性度高,是我国常见的恶性肿瘤类型,好发于青壮年人群。治疗淋巴瘤的化疗药物中,阿霉素较为常用。阿霉素和吡喃阿霉素均为蒽环类抗肿瘤药物。吡柔比星(吡喃阿霉素,pirarubicin,THP)是阿霉素(ADM)的一个四氢吡喃衍生物,临床前研究显示,由于化学结构和立体构型的改变,其抗肿瘤活性优于或相当于ADM,大量临床研究表明THP的心脏毒性和脱发等不良反应较ADM低[1]。本文选择我院收治的初治非霍奇金淋巴瘤患者,观察吡喃阿霉素和阿霉素在治疗此类患者中的临床疗效和不良反应。报道如下。
1 资料与方法
1.1 一般资料:入选的60例初治的非霍奇金淋巴瘤患者均为我院2003年5月至2014年5月期间病例(所选患者均经病理组织学检查证实),上述患者分为观察组和对照组。每组病例分别为15例。观察组的男性和女性病例分别为18例和14例。对照组中男性患者和女性患者分别为20例和10例。观察组的平均年龄为(42.3±5.1)岁(最小和最大年龄分别为22岁和66岁);对照组的平均年龄分别为(43.9±4.6)岁(最小和最大年龄分别为23岁和62岁)。观察组和对照组患者均为初治患者。观察组中Ⅳ期、Ⅱ~Ⅲ期和Ⅰ期患者分别为6例、20例和4例。对照组中Ⅳ期、Ⅱ~Ⅲ期和Ⅰ期患者分别为6例、18例和6例。两组患者的性别、年龄、恶性程度方面比较,差异无统计学意义(P>0.05),具有可比性。
1.2 方法:观察组患者均采用含吡喃阿霉素方案治疗。对照组患者均采用含阿霉素方案治疗。化疗方案采用吡喃阿霉素40 mg/m2(或阿霉素40 mg/m2)、环磷酰胺750 mg/m2、长春新碱1.4 mg/m2,第1天静脉注射。强的松100 mg,第1~5天为口服。以上方案3周为一个疗程。
1.3 疗效评定[2]和不良反应。按照实体瘤疗效评价标准:患者的病灶完全消失,且1个月后复查提示肿瘤完全消失,为完全缓解;测量的肿瘤病灶最大直径和最大垂直直径乘积和治疗前比较缩小超过50%以上,其他肿瘤病灶并没有增大,上述情况持续超过1个月,为部分缓解;肿瘤病灶的最大垂直直径和最大直径乘积和治疗前比较减少没有超过50%或增大但低于25%,为稳定;肿瘤病灶的最大垂直直径和最大直径乘积增大超过25%,或发现有新的病灶出现,为进展。有效率=(完全缓解例数+部分缓解例数)/总例数×100%。观察两组患者治疗过程中出现的不良反应(白细胞减少、血小板减少、贫血、消化道反应、肝功能损伤、脱发、心电图改变)。
1.4 统计学处理:在统计学软件SPSS17.0下对所得的化疗效果评定结果、不良反应发生情况等方面数据进行统计学分析,率的比较采用卡方检验,均数比较采用t检验,P<0.05,显示差异有统计学意义。
2 结 果
2.1 两组化疗后临床效果评定结果比较:观察组化疗后临床效果评定的总有效率为66.7%;对照组化疗后临床效果评定的总有效率为66.7%;观察组的有效率和对照组有效率比较,差异无统计学意义(P>0.05)。见表1。
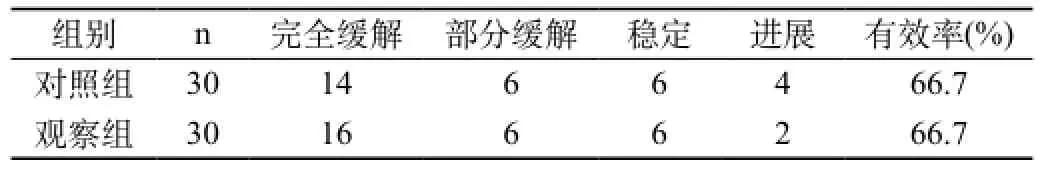
表1 两组化疗效果评定结果比较
2.2 两组不良反应发生情况比较:白细胞减少例数在观察组和对照组中均为6例(发生率为20.0%),差异无统计学意义(P>0.05)。血小板减少在观察组和对照组中例数分别为3例(发生率10%)和4例(13.33%),差异无统计学意义(P>0.05)。贫血在观察组和对照组中均为8例(发生率26.67%),差异无统计学意义(P>0.05)。肝功能损害在观察组和对照组中例数分别为4例(发生率13.33%)和5例(16.67%),差异无统计学意义(P>0.05)。观察组中消化道反应(主要表现为恶心、呕吐)共8例(发生率为26.67%),对照组中共15例(发生率为50%),观察组消化道反应发生率低于对照组,差异有统计学意义(P<0.05)。观察组中脱发共4例(发生率为13.33%),对照组中共10例(发生率为33.33%),观察组脱发发生率低于对照组,差异有统计学意义(P<0.05)。观察组中心电图异常共2例(发生率为6.7%),对照组中肝功能损伤共7例(发生率为23.33%),观察组心电图异常发生率低于对照组,差异有统计学意义(P<0.05)。见表2。

表2 两组患者不良反应发生情况比较[n(%)]
3 讨 论
非霍奇金淋巴瘤(non-Hodgkin's lymphoma,NHL)是一种常见的恶性肿瘤,且发病率呈快速上升趋势。 联合化疗仍是 NHL的主要治疗手段,CHOP方案是已被公认的初治 NHL 患者的一线化疗方案[3]。近年来,美罗华联合 CHOP方案的免疫化疗能显著提高B细胞NHL 患者的近期疗效和远期生存率。长期的临床使用中发现,CHOP方案中的主要药物ADM存在较严重的心脏毒性和脱发,寻找疗效与ADM相当,不良反应更低的蒽环类药物成为治疗的主要目标。吡柔比星(吡喃阿霉素)是阿霉素的衍生物,属于新一代蒽环类抗肿瘤药物,吡柔比星能够快速进入肿瘤细胞内,对肿瘤细胞的RNA聚合酶活性产生抑制作用,或者嵌入到肿瘤细胞DNA双链间,对细胞周期中的G2期产生阻断作用,使核酸合成被阻滞,从而导致肿瘤细胞死亡而产生抗肿瘤作用[4-5]。研究表明,吡喃阿霉素对耐阿霉素的肿瘤细胞也产生抑制和杀灭效果[6-8]。吡柔比星是继阿霉素和表阿霉的新一代 葸环类抗肿瘤药物,其心脏毒性及脱发等不良反应较阿霉素及表阿霉素少且程度较轻,以THP为主的CHOP化疗方案是目前治疗非霍奇金淋巴瘤安全性较好的化疗药物[9]。
本文中,观察组和对照组分别应用含吡柔比星和阿霉素的方案化疗,观察组的治疗后疗效评定结果总有效率和对照组总有效率比较,二者差异无统计学意义,说明吡喃阿霉素和阿霉素在治疗淋巴瘤中的疗效近似,均对淋巴瘤细胞产生抑制及杀灭作用;但观察组的不良反应(消化道反应、脱发、心电图改变)发生率低于对照组,说明吡柔比星在治疗淋巴瘤的过程中产生不良反应较阿霉素少。所以,吡柔比星治疗淋巴瘤的临床效果和阿霉素治疗淋巴瘤的临床效果近似,但前者不良反应发生率低于后者。
近年来,用吡喃阿霉素(THP)代替阿霉素,组成CEOP或CTOP方案已广泛应用于临床,其有效率与CHOP方案相当,甚至高于CHOP方案,而不良反应低于CHOP方案。本文病例观察发现吡柔比星为主CHOP方案较以阿霉素为主的CHOP方案疗效相同,但脱发、心脏毒性发生率小于以阿霉素为主的CHOP方案,值得临床借鉴。本病例观察还发现,吡柔比星为主CHOP方案在消化道反应上有更低的发生率,但此结论尚需开展更多高质量及大样本的病例观察。
[1] Tone H,Kurebe M,Takeuchi T,et al.Experimental studies on (2''R)-4'-O-Tetrahydropyranyladriamycin (THP)[M]//Kuemmerle HP.Advanced in experimental and clinical chemotherapy.15th International Congress of chemotherapy.Landsbeg/Lech:Ecomed,1998:1-9.
[2] 吴少华,王华庆,钱正子,等.吉西他滨 长春瑞滨联合吡喃阿霉素方案治疗复发难治T细胞淋巴瘤疗效分析[J].中国肿瘤临床,2014,6(10):647-650.
[3] Morel P,Munck JN,Coiffier B,et al.Comparison of two high-dose cyclophosphamide,doxorubicin,vincristine,and prednisone derived regimens in patients aged under 60 years with low-intermediate risk aggressive lymphoma: a final analysis of the multicenter LNH93-2 protocol[J].Leuk Lymphoma,2010,51(9):1668-1677.
[4] 马鸿雁.淋巴瘤治疗方法研究及效果分析[J].中国实用医药,2014,5(21):155-156.
[5] 傅鸿亮,江伟民,陈春明.吡喃阿霉素与阿霉素治疗非霍奇金淋巴瘤的临床观察[J].海峡药学,2010,7(12):116-117.
[6] 韩利杰,赵晓武,董秀娟,等.CTOP与CHOP治疗非霍奇金淋巴瘤的疗效及心脏毒性临床观察[J].临床荟萃,2011,11(03):208-211.
[7] 马军,沈志祥,秦叔逵.防治蒽环类抗肿瘤药物心脏毒性的中国专家共识(2011版)[J].临床肿瘤学杂志,2011,3(12):1122-1129.
[8] Yao HC,Xu EJ,Zeng WY,et al.Determination of doxorubicin in pharmaceutical preparation and rat plasma with luminol-K 3 Fe(CN) 6 chemiluminescence system[J].J Food Drug Anal,2013,213(2):336-339.
[9] 张之南,沈悌.血液病诊断及疗效标准[M].3版.北京:科学出版社,2007:220-227.
Clinical Effect of Non-Hodgkin's Lymphoma Treated by Pirarubicin
HU Xiu-juan, TANG Chao-li, HE Chun-ping
(Chongzuo People’s Hospital, Chongzuo 532200, China)
Objective Explore the clinical effect of pirarubicin in treatment of non Hodgkin's lymphoma. Methods 60 cases of initial treatment of non Hodgkin's lymphoma patients,divided into observation group and control group. The observation group and the control group respectively by chemotherapy with Tetrahydropyranyl adriamycin and adriamycin. Evaluation of two groups of clinical effect. Observation of adverse reactions occur. Results In the observation group assessment of clinical effect after chemotherapy the total efficiency of 66.7%; control efficacy was evaluated after chemotherapy group the total effective rate was 66.7%; the observation group and the control group with efficiency efficiency comparison, no significant difference (P>0.05). Adverse drug reaction (change the leukopenia, thrombocytopenia,anemia, gastrointestinal reaction, liver function damage, hair loss, ECG)in the observation group in the digestive tract reaction, hair loss, the change rate of ECG was less than the control group, the difference was statistically significant (P<0.05). Conclusion Similar clinical effect of clinical effect and doxorubicin treatment conclusions pirarubicin in treatment of non Hodgkin lymphoma and non Hodgkin's lymphoma, but the incidence rate of adverse reaction is lower than that of the latter, worthy of clinical reference.
Pirarubicin; Adriamycin; Non Hodgkin's lymphoma
R733
B
1671-8194(2015)15-0013-02

