乙酰氨基阿维菌素的合成工艺
温赛 陈长京

摘要: 乙酰氨基阿维菌素是一种高效广谱驱虫兽药。本研究以阿维菌素经AVMB1C5—OH保护反应、C4″—OH氧化反应的产物(4″-氧-5-O-烯丙氧甲酰基阿维菌素B1)作为起始原料,在反应器中连续进行氨化反应、还原反应、解C5的保护基反应,将所得反应液进行过滤、萃取,得到的有机液相直接进行乙酰化反应,再通过结晶、干燥后得到乙酰氨基阿维菌素成品。该路线与现有工艺比较,减少了工艺步骤,更换了氨化反应催化剂,优化了合成条件,使总收率提高4 6~6 8百分点,形成了一条适宜工业化生产的合成工艺路线。
关键词: 阿维菌素;乙酰氨基阿维菌素;合成工艺
中图分类号:O629 9;S859 79+5 文献标志码:A
文章编号:1002-1302(2015)08-0216-03
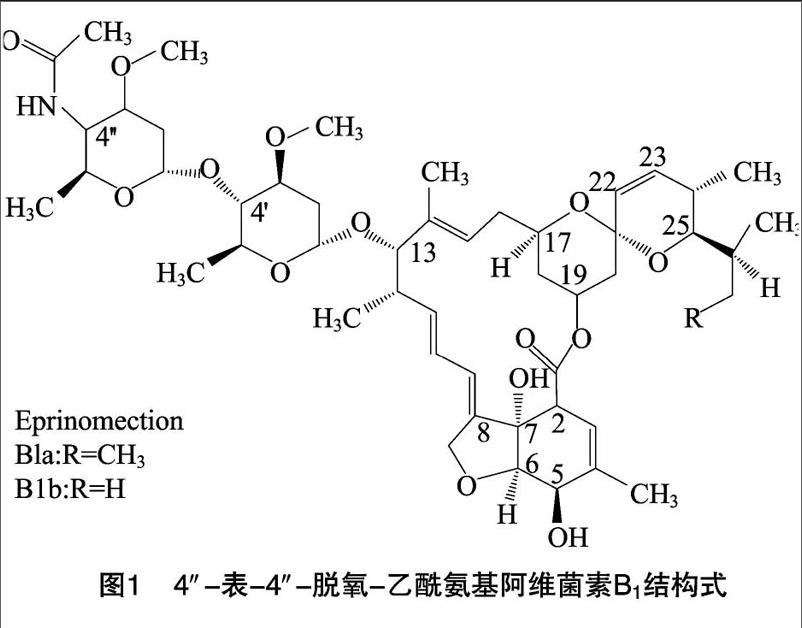
乙酰氨基阿维菌素(eprinomectin,4″-表-4″-脱氧-乙酰氨基阿维菌素B1,结构式见图1)是一种高效、广谱、低残留的兽用驱虫药物,是美国食品药品监督管理局(FDA)和欧盟批准的唯一应用于泌乳奶牛不需弃奶的广谱驱虫药,其制剂已在美国、欧盟、新西兰等国批准上市。中国农业部于2006年批准为二类新兽药,填补了我国奶牛寄生虫病防治药物的一项空白,也是防治家畜体内外各种寄生虫的首选药剂 [1-3]。
[ (W13][TPWS1 tif]
目前,制备乙酰氨基阿维菌素的路线有2种,第1种是糖苷法,但该方法工艺复杂,反应流程过长,收率较低;第2种是直接合成法 [3-4],工艺路线是以阿维菌素B1(avermectin B1,简写为AVMB1,结构式见图2)为起始原料,经过7个步骤[(1)AVMB1C5—OH保护反应→(2)C4″—OH的氧化反应→(3)AVMB1C4″[FY=,1]O的亚氨化反应、还原反应→(4)解C5的保护基反应→(5)氨基AVMB1的洗提、纯化,得到干基中间体→(6)氨基AVMB1乙酰化反应→(7)乙酰氨基阿维菌素经过结晶]得到成品。其中步骤(3)以氯化锌作催化剂,该步反应收率较低,需要探索新的催化剂,且反应物经过了过滤、液相分离、减压脱溶等处理后才可进行步骤(4),操作繁琐。此外,需对步骤(5)反应产物采用硅胶吸附洗脱,分离纯化为固体中间体,再进入步骤(6)的乙酰化反应,但是硅胶吸附洗脱工艺在工业生产中效率低,难以实行。
[ (W12][TPWS2 tif]
本试验针对文献路线存在的不足进行了优化。以步骤(1)(2)的反应产物(即4″-氧-5-O-烯丙氧甲酰基阿维菌素B1)为研究起点,对后续合成工艺主要进行了3项改进:第一,将步骤(3)(4)合并,连续进行合成反应;第二,对步骤(3)的AVMB1C4″[FY=,1]O氨化反应,采用新催化剂三氟乙酸锌代替氯化锌 [4-6],收率达到89 5%,比文献[4]提高了4 5百分点;第三,优化步骤(5),省略了硅胶吸附洗脱进行分离纯化这个工业化难以实现的方法,并省略了脱溶操作,而以液态中间体进行步骤(6)。
1 材料与方法
1 1 材料与试剂
氧化物(4″-氧-5-O-烯丙氧甲酰基阿维菌素B1),自制。六甲基二硅氮烷(hexamethyldisilazane,HMDS),[(CH3)3Si]2NH,市售工业品,含量≥99%,相对密度0 77。三氟乙酸锌[zinc trifluoroacetate,(CF3COO)2Zn],市售工业品,使用时配制成浓度为15%的乙酸异丙酯溶液。乙酸异丙酯(CH3COOC3H7),市售工业品,水分≤0 05%。硼氢化钠(NaBH4),市售工业品,含量≥99%。无水乙醇,C2H5OH,市售工业品,水分≤0 05%。四(三苯基膦)钯,Pd[P(C6H5)3]4,市售工业品,钯含量≥9 9%。乙酸(CH3COOH),市售工业品,含量≥99%。氢氧化钠(NaOH),市售工业品。乙酸酐[(CH3CO)2O],市售工业品,含量≥98%。乙腈(CH3CN),市售工业品,含量≥98%。
1 2 试验设备
FC204型电子分析天平、R200 旋转蒸发器、HHS-4s 型电子恒温不锈钢水浴锅、CL-200集热式恒温磁力搅拌器、DLSB-5/20型低温冷却液循环泵、SHB-ⅣA 型循环水式多用真空泵、L-7000高效液相色谱仪。
1 3 氨化反应
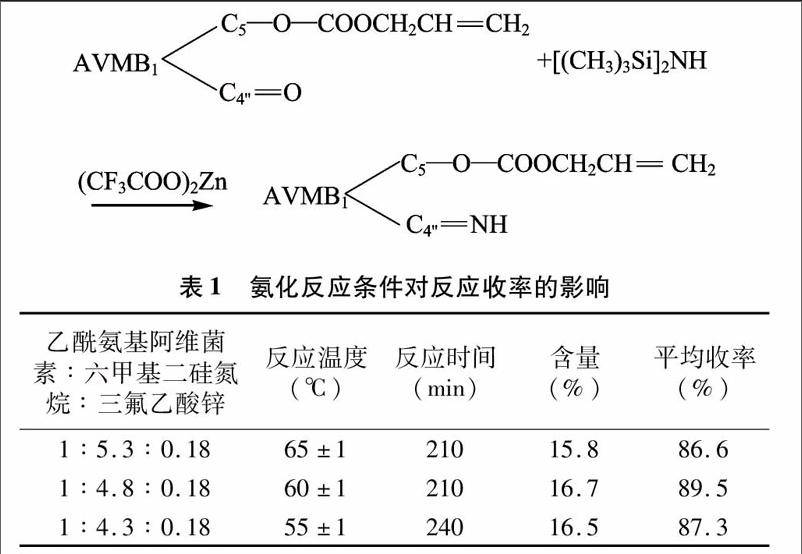
称量阿维菌素经AVMB1C5—OH保护反应、C4″—OH氧化反应的产物(4″-氧-5-O-烯丙氧甲酰基阿维菌素B1,简称为氧化物)97 5 g,配制成25%乙酸异丙酯溶液390 mL,投入干燥四颈烧瓶中。按表1比例投入六甲基二硅氮烷、三氟乙酸锌(乙酸异丙酯溶液,浓度15%),按不同反应温度和不同反应时间进行试验,完成后取样,分析后移入冰液中降温。C4″[FY=,1]O被氨加成,氨来自六甲基二硅氮烷,生成亚胺。
反应式:
1 4 还原反应
连续以上氨化反应,将氨化反应的物料温度降低到0~5 ℃ 时,在氮气保护下,按表2加入一定量硼氢化钠,缓慢滴加定量无水乙醇,约1 h加完,30 min后取样,分析合格。该反应以NaBH4/EtOH为还原剂,利用硼氢化钠和无水乙醇反应生成的 [H],将C4″[FY=,1]NH的亚胺双键还原为氨基,生成C4″—NH2 [5-6]。
反应式:
1 5 解保护反应
连续以上还原反应,温度保持在-2~0 ℃,在氮气保护下,加入催化剂四(三苯基膦)钯少量,先一次加入一定量硼氢化钠,再缓慢加入定量无水乙醇,约30 min加完,取样,以HPLC分析无C5保护物为合格。之后,在0 ℃以下滴加乙酸溶液消耗过量的硼氢化钠,以终止反应,调节反应液pH值至6 0,再滴加5 mol/L NaOH溶液,中和过量的乙酸,调节反应液pH值至8 0。过滤得到含有氨基AVMB1的物料,滤液静止分层,水相用乙酸异丙酯萃取2次,合并有机相,直接用于乙酰化。解保护用Pd催化剂,硼氢化钠和乙醇氢解,脱掉5位保护基团。
反应式:
1 6 乙酰化反应
将以上有机相投入干燥四口烧瓶中,漏斗中加入乙酸酐与无水乙酸异丙酯溶液,待反应液冷却到0 ℃以下时开始滴加,保持(0±2) ℃反应,保温15 min后取样,HPLC分析合格,用饱和NaHCO3液终止反应,调pH值至8 0,静置分层,水相用含水异丙酯溶液洗提2次,合并有机相,蒸干即制得乙酰氨基AVMB1粗品。
反应式:
1 7 结晶
在四颈烧瓶中,加入粗品乙酰氨基AVMB1,加入工业乙腈,水浴加热,直至粗品乙酰氨基AVMB1全部溶解,热过滤,转入另一四颈烧瓶中缓慢降温析晶,约2 h,继续降温至 35 ℃,维持析晶温度下陈化1 h,抽滤,滤饼用冷乙腈洗2次,晶体真空干燥。
结晶条件:乙酰氨基AVMB1粗品 ∶ 乙腈=1 g ∶ 3 2 mL,析晶温度下限:35 ℃。
2 结果与分析
2 1 氨化反应
在氨化反应中,氨化剂用量对反应结果有直接影响,同时反应温度也有较大影响。温度较高时,收率降低;温度较低时,尽管延长了反应时间但收率仍偏低,反应不完全(表1)。综合考虑,最佳反应条件是:投料比为乙酰氨基阿维菌素 ∶ 六甲基二硅氮烷 ∶ 三氟乙酸锌=1 ∶ 4 8 ∶ 0 18,反应温度为(60±1) ℃,反应时间≥210 min。
文献[4,7]中的氨化反应均以氯化锌作催化剂,投料比为乙酰氨基阿维菌素 ∶ 氯化锌=1 ∶ 0 48,收率为85%。本研究以三氟乙酸锌代替了氯化锌,投料比为乙酰氨基阿维菌素 ∶ 三氟乙酸锌=1 ∶ 0 18,收率为89 5%。可见,三氟乙酸锌的催化活性优于氯化锌。
2 2 还原反应
由表2可见,在还原反应中,当投料比为乙酰氨基阿维菌素 ∶ 硼氢化钠 ∶ 无水乙醇=1 ∶ 3 ∶ 40时,反应收率较低;当投料比为1 ∶ 2 ∶ 47时,反应收率较高。这说明还原反应是温和反应,不宜过快,降低硼氢化钠的用量,有利于减缓反应速度,减少副产物的生成,提高还原反应产物的含量和收率。
为了清晰验证反应温度的影响,单独进行比较试验。分别在20、0 ℃下加入70 mL无水乙醇,缓慢加入2 0 g NaBH4,约40 min加完,进行氨化反应和还原反应。由表3可知,在20 ℃时还原时间短,反应速度快,但是所得到的还原产物的含量和收率低。低温(0 ℃)虽然延长了还原反应时间,但副反应少,使含量和收率提高。综合考虑,还原反应温度选择在0 ℃左右为宜。
综合考虑,还原反应最佳条件是:投料比为乙酰氨基阿维菌素 ∶ 硼氢化钠 ∶ 无水乙醇=1 ∶ 2 ∶ 47,反应温度0 ℃左右,反应时间120 min。
2 3 解保护反应
解保护反应平稳,收率(相对氧化物)达到了74 2%,最佳条件:投料比乙酰氨基阿维菌素 ∶ 硼氢化钠 ∶ 无水乙醇=1 ∶ 1 ∶ 26,反应温度-5~0 ℃,反应时间60 min。
2 4 乙酰化反应
在乙酰化反应中,乙酸酐作为酰化剂,与氨(胺)形成酰胺,乙酸酐投料应过量。为筛选出适宜量,本研究将有机相调整为氨基AVMB1含量52 4%,氨基AVMB1 ∶ 乙酸酐摩尔比分别为1 ∶ 1 5、1 ∶ 1 3。结果表明,氨基AVMB1 ∶ 乙酸酐=1 ∶ 1 5 适宜,收率达到96 4%,高于1 ∶ 1 3时的收率95 4%。
2 5 结晶
在乙酰化反应物的结晶过程中,利用乙酰氨基阿维菌素相对于其他杂质在乙腈中的溶解度随温度变化较大的高选择性,分离出乙酰氨基阿维菌素。即先将粗品乙酰氨基阿维菌素溶解于热的乙腈中,再缓慢降温,使精品乙酰氨基阿维菌素析出。该创新有效缩短了工艺流程。
3 结论
文献报道中,氨化反应与还原反应为1步进行,解保护为1步进行,解保护反应液再经过过滤、萃取、脱溶,得到干基,且2步衔接需要物料转移,必有物料损失而未计入。本研究将氨化、还原、解保护合并进行是可行的,基于体系中始终存在乙酸异丙酯,能溶解氨化、还原、解保护各中间目标产物,具备了与其他原料进行液-液相反应的条件,尽管各反应物质的浓度有所降低不利于相互接触,但结果表明这3个合成反应较易进行,可通过延长反应时间、增加次要原料比例来改善。另外,合并步骤后的收率为74 2%,尽管比文献降低了,但由于在3个合成反应完成后,再对混合液进行过滤以除去固体物质,分离水相转移出系统,最大限度地把目标产物保留在系统内,从而保证总收率高于文献值。
本研究以4″-氧-5-O-烯丙氧甲酰基阿维菌素B1为起始原料,在一个反应器中连续进行AVMB1C4″[FY=,1]O的氨化反应、AVMB1C4″—NH2还原反应、C5—O—COOCH2CH[FY=,1]CH2的解保护反应。所得反应物料进行过滤、萃取,将液态有机相直接用于乙酰化反应,反应所得有机相蒸干得乙酰氨基AVMB1粗品,再经结晶得到乙酰氨基阿维菌素,反应总收率比文献值分别提高了4 6、6 8百分点(表4)。该方法缩短了工艺流程,操作方便,过程易控,所用原料易购,收率较高,产品纯度达到92%,是较理想的合成方法。
参考文献:
[1] Pitterna T,Cassayre J,Hüter O F,et al New ventures in the chemistry of avermectins[J] Bioorganic & Medicinal Chemistry,2009,17 (12):4085-4095
[2]冒玉娟,陈晓兰,赵 丽 乙酰氨基阿维菌素在动物医学中的研究进展[J] 畜牧与饲料科学,2013,34 (7/8):86-88
[3]陈俊辑,刘志滨,孙 哲,等 乙酰氨基阿维菌素对奶牛内寄生虫的驱虫效果[J] 中国动物保健,2014,1 (16):25-28
[4]赵永华 [HJ2 2mm]乙酰氨基阿维菌素的试验开发[D] 北京:北京化工大学,2003
[5]Cvetovich R Process for the preparation of 4′-amino avermectin compounds:USA, 5362863[P] 1994-11-08
[6]Mrozik H 4-deoxy-4-methylamino avermectin B1a/B1b:Europe,0301806 (A2)[P] 1989-02-01
[7]Fisher M,Mrozik H Avermectin derivatives:Europe, 0379341[P] 1990-07-25

