注射用盐酸川芎嗪与复方氨基酸(18AA)注射液配伍稳定性观察
马超
注射用盐酸川芎嗪与复方氨基酸(18AA)注射液配伍稳定性观察
马超
目的 对川芎嗪与复方氨基酸(18AA)注射液配伍稳定性进行实验研究。方法 模拟临床浓度和使用方法,实验研究两种药物配伍后,外观、pH值变化、配伍后的含量变化。结果 配伍后各项结果均无明显变化。结论该两种药物可配伍。
川芎嗪;复方氨基酸(18AA)注射液;配伍稳定性
川芎嗪治疗心脑血管病疗效显著[1]。而复方氨基酸(18AA)注射液为18种氨基酸与山梨醇配制而成的灭菌水溶液,用于大面积创伤、严重感染、消化系统功能障碍、营养恶化及免疫功能下降患者的营养支持,临床治疗中常常需要心血管药物与复方氨基酸注射液同时配伍使用。为保证临床安全,笔者对川芎嗪与复方氨基酸(18AA)注射液配伍稳定性进行了观察,现报告如下。
1 仪器与试药
1.1 仪器 Waters510型高效液相色谱仪(美国Waters);Waters486紫外检测器;N2000色谱工作站(江西创新信息工程有限公司);KQ-100E数控超声波清洗器(南通市精工仪器有限公司);pHS-3C酸度计(上海雷磁仪器厂)。
1.2 试药 川芎嗪对照品(中国药品生物制品检定所提供,批号:200351-201406);复方氨基酸(18AA)注射液(500 mL,四川科伦,pH5.6,批号51550);注射用盐酸川芎嗪(湖南中南科伦药业,规格:40 mg,批号30251,pH2.70);甲醇、乙腈为色谱纯;磷酸为分析纯;水为纯化水。
2 方法与结果
2.1 配伍后外观、不溶性微粒及pH值变化观察 根据临床用法与用量配制药液:川芎嗪40 mg溶于复方氨基酸(18AA)注射液500 mL中,制得药液,在室温条件下,分别在0,1,2,4,6h按中国药典[2]进行目视观察及不溶性微粒检查,同时测定溶液的pH值,每个样本连测3次,取平均值。结果:混合液在整个观察期间内透明澄清,无颜色变化,均未见结晶、沉淀,外观无任何变化。pH值的变化见表1。
2.2 含量变化考察
2.2.1 溶液配制 (1)对照品溶液:取盐酸川芎嗪对照品40 mg,置于250 ml量瓶中,加水溶解并稀释至刻度。(2)空白样品溶液:取复方氨基酸(18AA)注射液为空白溶液。(3)样品溶液:以复方氨基酸(18AA)注射液为溶媒模拟临床实际应用,将注射用盐酸川芎嗪80 mg注射液加入500 ml中,精密配制溶液。
2.2.2 含量测定条件[3]
2.2.2.1 色谱条件 色谱柱:ODS C18柱(150 mm×4.6 mm,5 μm);流动相:甲醇-乙腈-水-磷酸(250:30:250: 0.2);流速:1 ml/min;检测波长:254 nm;温度:25℃;进样量: 20 μL;AUFS:0.02。
2.2.2.2 系统适应性试验 分别取对照品溶液、供试品溶液、空白样品溶液各20 μL进样,以川芎嗪的峰记,色谱柱的理论塔板数为1 900,分离度为2.5。
2.2.2.3 线性关系考察 精密吸取对照品溶液适量,加灭菌注射用水分别配成系列浓度的川芎嗪溶液。按色谱条件测定,记录峰面积,以质量浓度(X)为横坐标,以峰面积(Y)为纵坐标,经回归计算,线性关系良好,其线性关系范围分别为14 ~324 μg/ml,回归方程为 Y=0.840X+8.65×522(r= 0.9995,n=6)。
2.2.2.4 精密度试验 分别精密吸取川芎嗪对照品1.0,1.5,2.0 ml。置于5 ml量瓶中各3份,流动相定容,配成低、中、高3个浓度,按上述色谱条件连续进行测定6次,峰面积积分RSD结果分别为0.66%、0.71%、0.77%。
2.2.2.5 回收率试验 取复方氨基酸(18AA)注射液5 ml 10份,置于10 ml量瓶中,其中9份加入川芎嗪对照品溶液0.5,1.0,1.5 ml各3份,所有10份溶液均加水至10 ml,精密量取2~50 ml量瓶中,用流动相稀释至50 ml摇匀。在上述色谱条件下分别测定,取平均值,计算回收率,结果两种药液3个浓度的平均回收率和RSD分别为99.98%和1.15%、100.04% 和99.0%、100.06%和1.06%。
2.2.3 含量测定 分别精密取“2.1”项下溶液于室温下放置,用流动相稀释1倍后得浓度约为0.3 mg/ml的配伍液按0,1,2,4,6 h分别取适量样品测定,按色谱条件,进行测定。将峰面积代入回归方程,计算各时间点溶媒中川芎嗪的含量。以配伍即刻(0 h)的含量为100%,计算各时间点的川芎嗪的相对含量,每一样品进样3针取平均值,结果见表1。
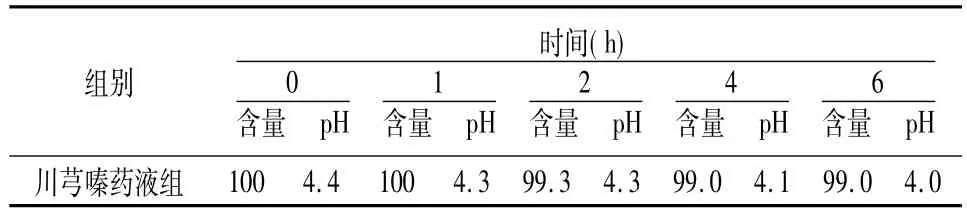
表1 含量测定及pH测定结果(20±1℃,n=3)
3 讨论
本研究根据临床常用量进行配伍实验,在(20±1)℃、自然光照射下观察到配伍后外观、pH均符合药典相关规定,配伍后6 h内药物含量变化极小,提示临床混合配伍未见化学反应和结构改变,但注射用盐酸川芎嗪pH为2.8左右,与复方氨基酸(18AA)注射液配伍后,pH值较低(pH4.4),对血管壁有一定刺激,应缓慢静滴。两种药液在6 h内可以配伍使用,但本研究仅考察了在常温下6 h内的稳定性,对其在非常温下及更长时间内的配伍尚待作进一步考察。
[1] 郭 军,孟 华,王骊丽,等.川芎嗪的药动-药效学研究近况[J].南京中医药大学学报(自然科学版),2002,18(5):318.
[2] 国家药典委员会.中华人民共和国药典(二部)[S].北京:化学工业出版社,2000.附录68-69.
[3] 夏赛忠.高效液相色谱法测定盐酸川芎嗪氯化钠注射液的含量及有关物质[J].中国药业,2010,19(7):34-36.
10.14126/j.cnki.1008-7044.2015.06.048
R94
A
1008-7044(2015)06-0597-02
江西省赣州市人民医院药剂科,341100
马 超(1984-),男,江西赣州市人,主管药师,研究生。
2015-04-14)

