表面增强拉曼光谱法定量检测食品中香豆素
黄梅英等
摘要 建立了食品中香豆素的表面增强拉曼光谱定量分析法。以粒径约为55 nm的金纳米粒子为拉曼活性基底,以pH=5.0 HClKCl溶液为溶剂,釆用便携式拉曼仪进行分析。通过实验优化得到最佳测定条件(金纳米溶胶浓缩倍数为50倍,激光照射时间为5 s,金纳米溶胶与溶液的混合比例为1∶1),建立了食品中游离香豆素直接检测方法,方法在1.0~100.0 mg/L的浓度范围内具有良好的线性,检出限为0.91 mg/L。将建立的分析方法用于蔬果、糖果、糕点等实际样品中香豆素的检测(样品前处理过程:称取10 g样品于烧杯中,加入50 mL溶剂,超声提取0.5 h后, 定容至100 mL,摇匀后过滤,取10 mL定容至100 mL,摇匀得到样品处理液),香豆素含量在0.61~5.52 g/kg之间;样品的加标回收率为75.12%~103.2%,相对标准偏差为0.6%~14%。结果表明, 本方法快速准确、操作简单,可用于水果、糖果、糕点中香豆素的快速检测。
关键词;表面增强拉曼光谱;定量分析; 金纳米粒子; 快速检测; 香豆素; 食品。
1引言
香豆素(Coumarin)化学名称为12苯并吡喃酮,在酸性条件下稳定存在,碱性条件下易开环。香豆素是一种天然植物次生产品,广泛存在于自然界的一种内酯类化合物,具有高毒性,于1820年发现于黑香豆中,主要以游离状态和苷的形式存在于植物中[1]。香豆素是一种重要的香料,被广泛用作香料香精,也用作饮料、食品、香烟等的增香剂。常香兰素作为调料共同用于糕点、糖果中,或作为天然香料添加到烟草中[2~6]。动物实验证实香豆素具有致癌性,因此有些国家制定了摄取的安全剂量。欧洲理事会在1988年规定香豆素在食品中的限量为2 mg/kg,澳大利亚对酒精中香豆素的限量为10 mg/kg,欧洲食品安全局规定在食品中的添加限量在5~50 mg/kg之间[7,8]。
研究香豆素在体内的含量达到一定量时具有生理毒性,通过长期的动物实验发现具有肝毒性[2],主要是由于代谢的途径导致P450(细胞色素P)及其依赖性酶的减少导致肝毒性。由于香豆素的潜在的不良反应,美国于2011年禁止在食品中添加由香豆属类植物中提取的香豆素[9]。
目前,香豆素检测方法有酶联免疫法[10]高效液相色谱检测[11~13]、液相色谱质谱联用[14]、荧光光谱法[18~22]以及毛细管电泳法[23]等。酶联免疫法只是诊断的辅助手段,易出现假阳性;色谱法和色谱质谱联用法操作过程繁琐、耗时长, 常用到有毒有害的有机溶剂;荧光光谱法干扰大、灵敏度较低;毛细管电泳法重现性差。因此,建立香豆素的方便快捷,选择性高的检测方法具有重要意义。近年来表面增强拉曼光谱(Surfaceenhanced raman spectroscopy, SERS)作为一种新型有效的指纹光谱技术,具有方便快速、检测成本低、分析速度快、便携性强等优点,在食品安全、毒品检测领域显示出巨大的应用潜力[24,25]。利用贵金属纳米粒子的SERS效应,可以将拉曼信号的灵敏度提高104~1014个数量级。本研究建立了食品中香豆素的表面增强拉曼光谱快速检测分析方法, 与传统检测方法相比,本方法具有快速、灵敏、准确等特点,具有良好的应用前景。
2实验部分
2.1仪器与试剂
Delta Nu Inspector便携式拉曼仪(功率为120 MW, 美国DeltaNu公司); A TG16离心机(湘仪仪器有限公司); FA1604分析天平(上海天平仪器厂); 搅拌器(Midea MJ250BP02A); B广泛试纸(114,上海三爱思试剂有限公司); 超声波清洗机(SCIENTZ SB5200D, 宁波新芝生物科技股份有限公司)。 金纳米粒子溶液(由厦门大学提供,其浓度约为2.94×10
Symbolm@@ 4 mol/L,金纳米粒子半径约为55 nm); HCl(分析纯,36%~38%,广州化学试剂二厂); KCl(分析纯, 广州化学试剂); 香豆素(阿拉丁试剂); 王水(自配); H2SO430%H2O2溶液(3∶1, V/V); 纯水(怡宝纯净水)。苹果购于附近的水果市场; 西红柿购于附近的菜市场、燕麦、糕点和糖果均购于超市。
2.2分析方法
2.2.1样品制备标准溶液的配制:准确称取0.1000 g香豆素标准品于烧杯中, 用HClKCl混合溶液(pH 5.0)溶解并定容至100 mL,得到1000 mg/L香豆素储备液。取适量香豆素储备液,用HClKCl混合溶液逐级稀释成0.0 , 1.0, 2.0, 5.0, 10, 20, 50, 100, 200, 300, 400和500 mg/L的标准工作溶液,密封、避光保存备用。
样品处理:将样品除去非食用部分后磨碎,准确称取10 g样品于烧杯中,加入50 mL HClKCl混合液,超声浸泡0.5 h后,用HClKCl混合液定容至100 mL,摇匀后过滤,取10 mL滤液用HClKCl混合溶液定容至100 mL,摇匀后直接进行SERS检测。
通过公式(1)计算出样品的香豆素含量:
ω=CmV/ms(1)
ω为质量含量 (g/kg), Cm为质量浓度 (g/L), V为溶液体积(L), ms为样品量(kg)。
2.2.2SERS检测取2.0 μL一定浓缩倍数的金纳米粒子于硅片光滑面上,加入量香豆素标准溶液充分混合后,进行调焦后获得拉曼光谱,并对数据进行处理。
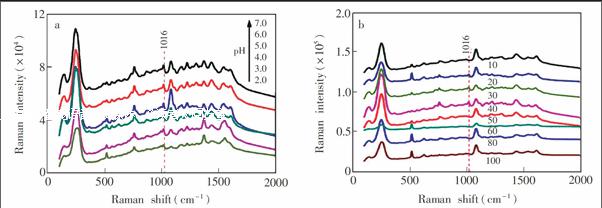
以HClKCl混合溶液(pH 5.0)为溶剂,不同金纳米粒子的浓缩倍数下进行检测。金的浓缩倍数影响金纳米粒子间的距离,影响物质与金纳米粒子间的相互作用,会引起拉曼响应信号的变化。当浓缩倍数为50倍时,香豆素的SERS响应较好(图3b),故浓缩倍数选择50倍。
3.2.3激光照射时间
激光的作用是提供能量使分子获得能量从而产生电子的跃迁,适当增加激光照射时间能够提高能量,发生跃迁的电子增加,响应信号增强,但过长的照射时间会破坏分子的结构,因此需要在适当的时间下进行测定。在不同的激光照射时间进行香豆素的SERS检测发现,激光照射时间对香豆素的SERS响应信号有较大影响,随激光照射时间的延长,香豆素SERS信号呈现逐渐增强的趋势,当照射时间过长,高浓度香豆素的拉曼响应信号容易溢出(图4)。因此,激光照射时间选择5 s。
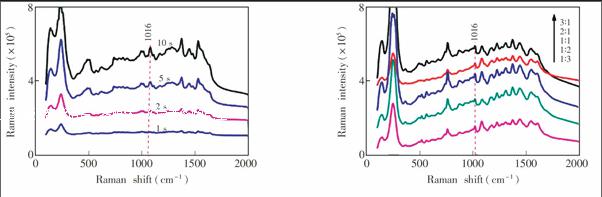
3.2.4混合比例金纳米粒子用量的增加使物质与金纳米粒子结合更充分,拉曼响应信号有一定程度的增强,当金纳米粒子用量增加到一定程度时, 可能会对物质形成比较厚的包裹层,降低物质拉曼信号的检测。选择合适的比例有利于物质的检测。分别将待测液与金纳米粒子以不同体积比混合均匀后检测,1016 cm
Symbolm@@ 1处峰的强度呈现先增后减的趋势,当体积比为1∶1时得到的峰面积最大,增强效果最明显。因此,选择待测液与金纳米粒子的体积混合比例为1∶1作为最佳体积混合比,结果见图5。
通过实验条件的优化,选择以为溶剂,浓缩倍数为50倍的金纳米粒子为增强基底,激光照射时间为5 s,待测液与金纳米粒子的体积比为1∶1作为香豆素检测的最佳实验条件。
选择激发光光源波长为785 nm,积分时间为5 s,平等测定3次取平均值,激光功率High,测定模式为Software,分辨率选择Low,每测定一次扣除一次暗电流。
3.3标准曲线
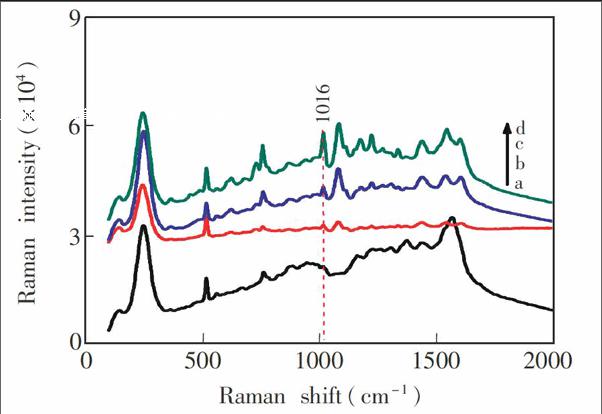
配制香豆素系列标准工作溶液,在优化的实验条件下进行SERS检测,结果见图6。在1.0~100 mg/L范围内,香豆素在1016 cm
Symbolm@@ 1处的拉曼光谱峰面积(y)与香豆素的质量浓度呈良好的线性关系,线性方程为y=1354+1945x,线性相关系数(R2)为0.9987。
对1.0 mg/L香豆素标准溶液测定15次,以3倍信噪比计算得到检出限为0.91 mg/L。
苹果、燕麦、西红柿、1号糖果和2号糖果中香豆素含量分别为0.82, 0.80, 0.61, 5.52和1.51 g/kg,糕点中均未检出1号糖果中香豆素含量超出标准,其样品香豆素含量均符合标准(European Council, 1988,≤2.0 g/kg)\[5\];样品加标回收率为75.1%~103.2%,相对标准偏差RSD为0.6%~14.0%,表明方法准确度高,精密度好,结果可靠。
4结论
采用表面增强拉曼光谱法建立了食品中香豆素的定量检测方法,方法在1.0~100.0 mg/L的浓度范围内具有良好的线性,其线性相关系数为0.9987,检出限为0.91 mg/L。苹果、燕麦、西红柿、1号糖果、2号糖果中香豆素的含量分别为0.82, 0.80, 0.61, 5.52和1.51 g/kg,两种糕点样品中未检出,1号糖果香豆素含量超出标准(European Council, 1988, ≤2.0 g/kg),样品回收率为75.1%~103.2%,相对标准偏差为为0.6%~14%。方法具有样品用量少、成本低、环境友好、快速简便等优点,适合于食品中香豆素快速检测。
Reference
1Raters M, Matissek R. European Food Research and Technology, 2008, 227(2): 637-642
2Wang Y, Avula B, Nanayakkara N P D, Zhao J P, Khan I A. J. Agr. Food Chem., 2013, 61(18): 4470-4476
3Stanfill S B, Calafat A M, Brown C R, Polzin G M, Chiang J M, Watson C H, Ashley D L. Food Chem. Toxicol, 2003, 41(2): 303-317
4Bettero A, Benassi C A. Journal of Pharmaceutical and Biomedical Analysis, 1983,2(1): 229-233
5Sproll C, Ruge W, Andlauer C, Godelmann R, Lachenmeier D. Food Chemistry, 2008, 109(2): 462-469
6Woehrlin F, Fry H, Abraham K, PreissWeigert, Angelika. J. Agr. Food Chem., 2010, 58(19): 10568-10575
7WU XinHua, ZHURuiZhi, LU SheMing, WANG Kai, MENG ZhaoYu, MOU DingRong, MIU MingMing. Physical and chemical inspection (Chemical volume), 2009, (12): 1404-1409
吴新华, 朱瑞芝, 路舍铭, 王 凯, 孟昭宇, 牟定荣, 缪明明. 理化检测(化学分册), 2009, (12): 1407-1409
8HAN Yi, ZHANG ChengMing ,YU Kun, MENG Xia, CHEN YongKuan, MIU MingMing. Flavour Fragrance Cosmetics February, 2013, (1): 45-49
韩 熠, 张承明, 喻 坤, 孟 霞, 陈永宽, 缪明明. 香料香精化妆品, 2013, (1): 45-49
9Wang Y H, Avula B, Nanayakkara, N P Dhammika, Zhao J P, Khan, Ikhlas A. Journal of Agricultural and Food Chemistry, 2013, 61(18): 4470-4476
10St Cklein W F M, Scheller F W, Abuknesha R. Sensors & Actuators: B. 1995, 24(1): 80-84
11Gutierrez M C, Parry A, Tena M, Jorrin J, Edwards R. Phytochemistry, 1995, 38(5): 1185-1191
12YANG YingLai,YANG Tao,YANG YuHua,GUO Long, LIU XiaoHua, LI YingDong, FENG ShiLan. Chinese J. Anal. Chem., 2013, 41(11): 1744-1748
杨英来, 杨 涛, 杨玉华, 郭 龙, 刘小花, 李应东, 封士兰. 分析化学, 2013, 41(11): 1744-1748
13LI LiHua, XUE Xue, PENG Chao ,BAI XiaoHong. Chinese J. Anal. Chem., 2013, 41(3): 337-343
李利华, 薛 雪, 彭 超, 白小红. 分析化学, 2013, 41(3): 337-343
14Eeva M, Rauha J P, Vuorela P, Vuorela H. Phytochem. Anal., 2004, 15, 167-174
15Raters M, Matissek R. European Food Research and Technology, 2008, 227(2): 637-642
16De Jager L S, Perfetti G A, Diachenko G W. Food Chem., 2008, 107(4): 1701-1709
17Yeh T, Lin C, Chang S. J. Agr.Food Chem., 2014, 62(7): 1706-1712
18Kalita P, Kumar R. Microporous and Mesoporous Materials, 2012, 149(1): 1-9
19Li W, Sun W, Yu X, Du L P, Li M Y. Journal of Fluorescence, 2013, 23(1): 181-186
20Shiraishi Y, Sumiya S, Manabe K, Hirai T. ACS Applied Materials & Interfaces, 2011, 3(12): 4649-4656
21Wu Z, Li Z, Yang L, Han J H, Han S F. Chemical Communications, 2012, 48(81): 10120-10122
22Yuan L, Lin W, Song J. Chemical Communications, 2010, 46(42): 7930-7932
23Wang W, Tang J, Wang S, Zhou L, Hu Z D. J. Chromatogr. A, 2007, 1148(1): 108-114
24CHEN YongJian, FENG ShangYuan, GUO XiaoLin, XI GangQin, WANG Jing, CHEN Rong. Spectroscopy and Spectral Analysis, 2012, 32(10): 2702-2705
陈永坚, 冯尚源, 郭小林, 席刚琴, 王 静, 陈 荣. 光谱学与光谱分析, 2012, 32(10): 2702-2705
25WANG Lei, GUO ShuXia, DAI YinZhen, YANG LiangBao, LIU GuoKun. Chinese J. Anal. Chem., 2015, 43(1): 33-39
王 磊, 郭淑霞, 戴吟臻, 杨良保, 刘国坤. 分析化学, 2015, 43(1): 33-39
AbstractA method was established for the determination of coumarin in various foods by surfaceenhanced Raman spectroscopy in a hydrochloric acidpotassium chloride solution (pH=5. 0) with 55 nm Au nanoparticles as Raman substrate. Under the optimal experiment conditions such as concentrated gold sol with concentration multiple of 50, 5 s of laser irradiation time and 1∶1 mixing ratio of gold sol and solution, the method was used for the direct determination of coumarin. The method had a good linearity between the peak intensity and the courmain concentration in the range of 1.00-100.0 mg/L, and the detection limit was 0.91 mg/L. For the determination of real samples of courmain in vegetables, fruits, sweets and pastries, 10 g of sample was added in 50 mL of hydrochloric acidpotassium chloride solution in a beaker, and then ultrasonically extracted for 0. 5 h. After transferred into a 100mL flask, the sample solution was filtered and 10 mL of supernatant was taken and diluted to 100 mL for the further analysis. The concentration of courmain was determined to be 0. 61-5.52 g/kg. The relative standard deviations were 0.6%-14.0%. The spiked recoveries of these samples ranged from 75.1% to 103.2%. This method is simple, and has wide linear range and high accuracy.
KeywordsSurfaceenhanced Raman spectroscopy; Quantitative analysis; Gold nanoparticles; Rapid detection; Coumarin; Foods
(Received 11 December 2014; accepted 12 April 2015)
This work was supported by the Major Scientific Instruments and Equipment Development Projects of China (No.2011YQ03012409) and the National Natural Science Foundation of China (Nos.21277176,21275168, 21127008)
中国化学会第二届全国质谱分析学术报告会(第一轮通知)
为促进我国质谱分析及相关研究的快速发展,增进质谱研究与应用领域科技人员的学术交流与合作,由中国化学会及国家自然科学基金委主办,中国化学会质谱分析专业委员会与浙江大学承办的“中国化学会第二届全国质谱分析学术报告会”将于2015年10月16日~19日在浙江大学紫金港校区召开。
本次会议将邀请多位院士和质谱专家参会并作特邀报告。会议热诚邀请全国从事质谱研究与应用、及相关仪器研究与开发等领域的广大学者、研究生、相关单位代表及仪器厂商参会。
一、征文内容:
应征的论文是未曾发表的质谱分析研究成果,涉及如下方面: 1 环境分析; 2 生命分析; 3 食品分析; 4 石油化工; 5 医药卫生; 6 公共安全; 7 天然物及烟草; 8 裂解机理、方法; 9 新材料、新能源; 10 样品前处理方法; 11 仪器研制与新技术; 12 其它。
征集的论文将被分为大会报告、邀请报告、口头报告和墙报四种形式交流。大会将设优秀青年报告奖和优秀墙报奖。
二、征文格式与要求:
1. 请在会议网站(http://www.mschina.org/)下载论文模板,严格按论文模板编辑,在线注册投稿。请务必提供稿件联系人、电话、通讯地址和Email。
2. 论文提交截止日期为2015年8月15日。
三、会议联系人
柴云峰,电话: 0571-87951285,Email: hplcms@zju.edu.cn
潘远江,电话: 0571-87951629,Email: fticrms@zju.edu.cn
通讯地址:浙江大学玉泉校区化学系735室,310027。
有关会议的详细介绍、组织机构、征文格式、日程安排、宾馆住宿等相关信息,请登录会议网址(http://www.mschina.org/) 查询。
中国化学会质谱分析专业委员会
浙江大学化学系

