心房颤动患者冠状动脉支架置入术后三联抗栓对比二联抗栓治疗的安全性和疗效分析
陆文彬 陈立娟 鞠成伟 朱建 傅聪 姚玉宇 马根山
目前,对于经皮冠状动脉介入治疗(percutaneous coronary intervention,PCI)术后的冠心病或急性冠状动脉综合征患者,双联抗血小板治疗,即阿司匹林联合氯吡格雷双重抗血小板治疗,是预防血栓事件及不良预后的金标准[1]。这类患者中约有5%合并持续性或永久性心房颤动(AF)[2],AF显著增加了患者的血栓风险,导致包括卒中在内的多种严重并发症[3]。对于非瓣膜性AF 具有中、高血栓风险的患者,需要药效更强的三联抗栓治疗(维生素K 拮抗剂+ 阿司匹林+ 氯吡格雷),2010年/2012 年欧洲心脏病协会(ESC)AF 治疗指南[4-5]推荐,对这些患者需联合口服抗凝药物行抗栓治疗,以减少卒中风险。然而,有研究报道双重抗血小板治疗联合抗凝药物可能增加AF 患者的出血风险[6-7]。AF 患者在PCI 术后如何进行更优化的抗栓治疗仍然是一个重要的临床问题,目前关于三联抗栓对比二联抗栓的研究分析数据较少。本研究拟分析AF 患者冠状动脉支架置入术后三联抗栓治疗对比二联抗栓治疗在出血及主要不良心血管事件方面的差异,以期为AF 患者在行支架置入术后的抗栓治疗提供更多临床证据。
1 对象与方法
1.1 研究对象
选取2007 年6 月至2012 年6 月在东南大学附属中大医院心内科确诊为持续性或永久性AF[部分患者术前根据CHADS2评分已使用华法林抗凝治疗,但是所有患者的国际标准化比值(INR)都是控制在标准范围内,即INR2.0 ~3.0]并行冠状动脉新一代药物洗脱支架置入术的患者228 例(包含稳定性冠心病及急性冠状动脉综合征患者),根据支架置入术后患者口服抗栓药物种类(根据评估患者当时血栓栓塞及出血风险非随机分组)分为三联抗栓组(TT 组,120 例)和二联抗栓组(DT 组,108 例)。持续性或者永久性AF 的的诊断至少符合以下一条[8-9]:(1)持续>7 d,不能自行复律,治疗后可转复,但反复发作,常需要电复律;(2)复律失败或复律后24 h 内又复发,不能维持窦性心律或无复律适应证的AF。所有患者均合并冠心病,并在住院期间行经皮冠状动脉支架置入术。排除标准:慢性感染性疾病、恶性肿瘤、严重肝肾功能损害[转氨酶≥2倍正常值、肾小球滤过率(eGFR)≤30 ml/min]、活动性出血及凝血功能障碍、30 d 内行外科大手术、年龄<18 岁或者>80 岁、30 d 内参与其他药物研究、存在免疫缺陷疾病以及临床预期寿命<1 年的患者。
1.2 方法
两组患者均在冠状动脉支架置入术后6 ~12 h内开始行不同的抗栓治疗方案。三联抗栓用药方案为华法林(2.5 mg 起始,维持INR 2.0 ~3.0)、阿司匹林(100 mg/d)、氯吡格雷(75 mg/d),根据支架的洗脱药物不同,治疗时间为3 ~6 个月不等(西罗莫司洗脱支架至少3 个月,紫杉醇洗脱支架至少6 个月),其后根据2010 年/2012 年ESC AF 治疗指南[4-5]改为双联抗栓治疗(华法林+阿司匹林或氯吡格雷),12 个月后若病情稳定改为华法林单药治疗。二联抗栓用药方案为华法林(2.5 mg 起始,维持INR 2.0 ~3.0)、氯吡格雷(75 mg/d)治疗12 个月。根据患者病情及临床医师建议,允许患者短期使用血小板糖蛋白Ⅱb/Ⅲa 抑制剂及肝素治疗。研究方案取得东南大学附属中大医院的伦理委员会批准后,开始收集患者的临床资料(包括年龄、病史、生活方式及本次疾病的病例资料等)和所有患者入院前后1 个月内的合并用药,记录分析所有患者的HAS-BLED[10]以及CHA2DS2-VASc 评分[11],并分析其与出血及不良心血管事件的相关性。
1.3 随访和相关定义
所有患者随访360 d,主要研究终点为两组患者早期(90 d 内)及晚期(90 ~360 d)的总出血(包含主要出血、次要出血及微小出血)及主要出血事件发生率,出血的评定采用TIMI 出血标准和分类方法[12]。主要出血:颅内出血,或临床出血征象不显著伴随血红蛋白下降>5 g/dl;次要出血:包括影像观察在内的任何临床上显著的出血征象伴随血红蛋白下降3 ~5 g/dl;微小出血:包括影像学在内任何临床可见的出血征象伴随血红蛋白下降<3 g/dl。主要不良心血管事件:再次PCI,支架内血栓,再发心肌梗死,非出血性卒中,短暂性脑缺血发作(TIA),心脏缺血性或血管栓塞原因相关的死亡。
1.4 统计学分析
应用SPSS 19.0 统计软件,计量资料以均数±标准差表示,两组间比较采用t 检验,多组数据比较采用单因素方差分析,分类资料采用χ2检验或Fisher 精确概率检验比较。比较两组患者出血事件及不良心血管事件发生率及因素分析采用Mantel-Cox 检验和Kaplan-Meier 生存曲线。以双侧P <0.05 为差异有统计学意义。
2 结果
2.1 两组患者一般资料比较
两组患者的年龄、性别、出血史、缺血及卒中史、吸烟、心力衰竭、高血压病、糖尿病、左心室射血分数、低密度脂蛋白(LDL)、三酰甘油、口服用药等临床资料比较,差异均无统计学意义(均P >0.05,表1)。HAS-BLED 评分TT 组为(2.03 ±0.74)分,DT组为(1.91 ±0.66)分,两组比较,差异无统计学意义(P=0.202);CHA2DS2-VASc 评分TT 组(2.81 ±0.65)分,DT 组(2.20 ±0.44)分(P=0.014,图1)。
2.2 两组患者早期出血发生率比较
随访90 d 时,总出血发生率TT 组18.3%,DT组6.5%,两组比较,差异有统计学意义(P =0.007,图2A)。其中,TT 组严重的颅内出血1 例,其余均为不同程度的牙龈出血、鼻出血或消化道出血;DT组未发生严重出血事件(如颅内出血)。与DT 组相比,尽管主要出血事件发生率TT 组增多,但是差异无统计学意义(6.70% 比3.70%,P = 0.317,图2B)。Kaplan-Meier 生存分析进一步证实,TT 组和DT 组无出血事件生存率比较,差异有统计学意义(81.7%比93.5%,P =0.001,图2C),无主要出血事件生存率比较,差异无统计学意义(93.3% 比96.3%,P=0.313,图2D)。使用Cox 回归模型排除年龄≥65 岁、性别、高血压病、既往出血史、血小板糖蛋白Ⅱb/Ⅲa 抑制剂的使用、三支病变血管、HASBLED 评分≥3 分等混杂因素后分析发现,TT 组出血发生率仍显著增加(P <0.001),同时高HAS-BLED评分(HR 5.74,95% CI 2.53 ~12.99,P <0.001)、三支血管病变(HR 4.27,95% CI 1.00 ~18.20,P =0.05)均与患者的早期总出血事件显著相关。
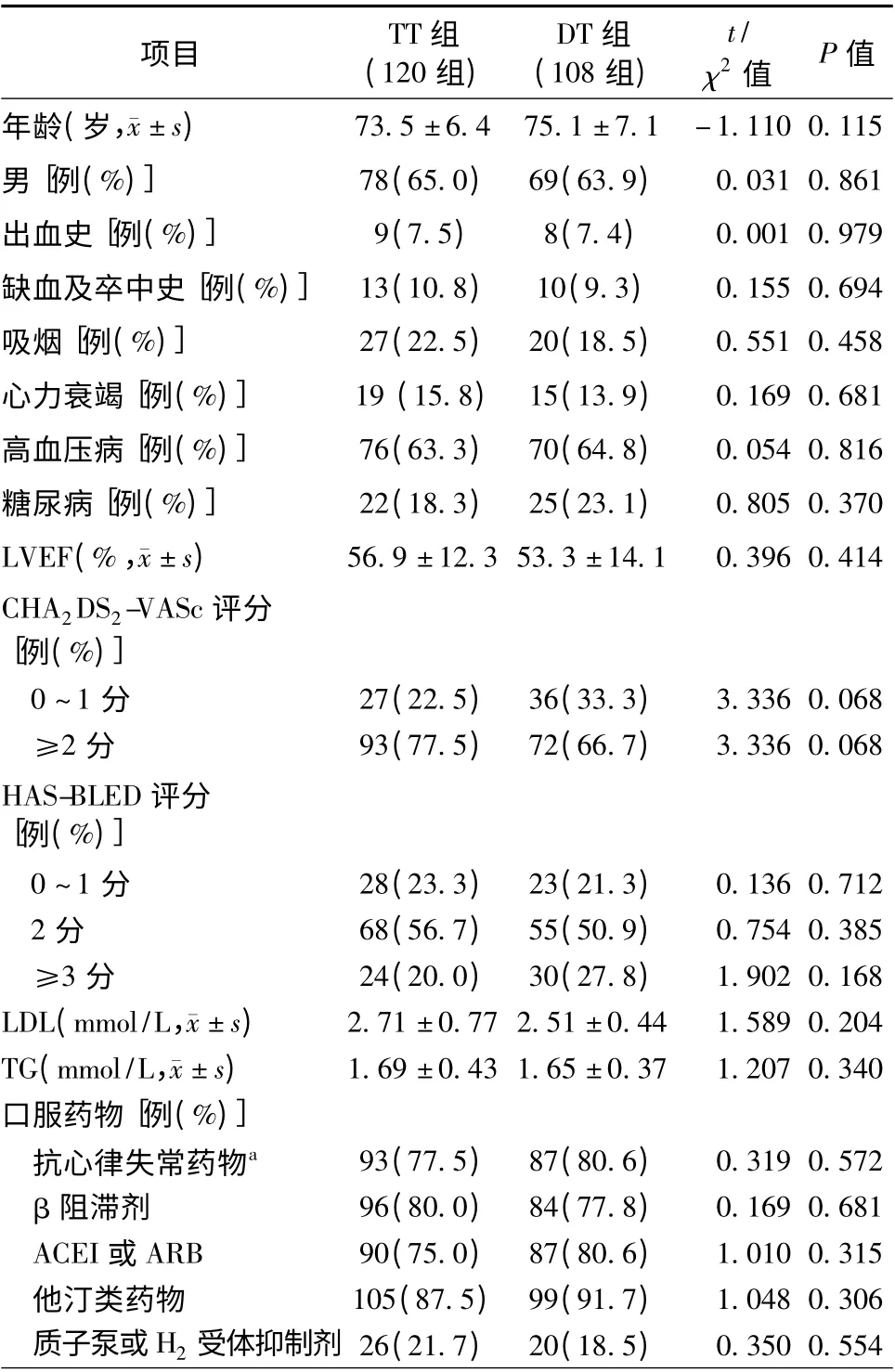
表1 两组患者一般资料比较

图1 两组HAS-BLED 评分(A)和CHA2DS2-VASc 评分(B)比较

图2 两组患者早期出血情况比较
2.3 两组患者晚期出血发生率比较

图3 两组患者晚期出血情况比较
在术后90 ~360 d 的随访中发现,与DT 组比较,TT 组仍伴随着较高的总出血事件发生率(24.2%比11.1%,P =0.010,图3A);TT 组主要出血事件发生率虽然高于DT 组,但差异无统计学意义(9.2%比5.6%,P =0.300,图3B)。TT 组颅内出血2 例,1 例经积极治疗后好转,1 例因出血性卒中死亡,其余患者均为轻到中度的消化道或者皮肤黏膜以及鼻出血;DT 组未出现严重颅内出血事件。Kaplan-Meier 生存分析可见,TT 组无出血事件生存率显著低于DT 组(75.8% 比88.9%,P =0.011)(图3C),而无主要出血事件生存率比较,差异无统计学意义(90.8% 比94.4%,P = 0.296,图3D)。Cox 回归模型排除年龄≥65 岁、性别、高血压病、出血史(随访早期)、血小板糖蛋白Ⅱb/Ⅲa 抑制剂的使用、三支血管病变、HAS-BLED 评分≥3 分等混杂因素后发现,与DT 组相比,TT 组仍显著增加晚期出血发生率(P <0.001)。分析发现,早期随访期间出血(HR 2.818,95% CI 1.40 ~5.66,P =0.004)、血小板糖蛋白Ⅱb/Ⅲa 抑制剂的使用(HR 5.87,95% CI 2.16 ~15.96,P =0.001)、高HAS-BLED 评分(HR 2.07,95% CI 1.06 ~4.06,P =0.034)均与晚期出血呈显著相关性。
2.4 两组患者主要不良心血管事件比较
随访期间,主要不良心血管事件发生率TT 组与DT 组比较,差异无统计学意义(7.5%比10.2%,P=0.474,图4A)。TT 组PCI 术后短时间内发生支架内血栓2 例,因存在多发病变,半年后再次出现胸痛而选择再次置入药物洗脱支架的患者5 例,术后第7 个月发生急性肺栓塞和非ST 抬高心肌梗死各1 例。DT 组行再次置入药物洗脱支架治疗的患者4 例,支架内血栓1 例,因肠系膜栓塞最终死亡1例,TIA 3 例,再发心肌梗死2 例。Kaplan-Meier 生存分析显示,两组无主要不良心血管事件生存率比较,差异无统计学意义(92.5%比89.8%,P =0.473,图4B)。多因素回归分析发现,缺血及卒中史(HR 3.27,95% CI 1.15 ~9.31,P=0.026)、高CHA2DS2-VASc 评分(HR 4.85,95% CI 1.08 ~21.90,P =0.04)、心力衰竭(HR 3.9,95% CI 1.41 ~10.81,P=0.009)均与主要不良心血管事件呈显著相关性。

图4 两组主要不良心血管事件情况比较
3 讨论
AF 显著增加患者卒中和血栓事件的发生率,对于非瓣膜性AF 患者,不规范的口服抗栓药物治疗可导致卒中或死亡年发生率至少增加5 ~10 倍[13]。当AF 患者合并冠心病需要行PCI 或置入支架的情况下,容易合并异物炎症反应、局部凝血与血小板激活、慢性炎症反应刺激等血栓负荷高风险。根据2010 年/2012 年ESC AF 治疗指南[4-5]推荐,这类AF 患者均应行短期的三联抗栓治疗,以期减少血栓及卒中的发生率。然而,近年来较多临床抗栓研究提示,三联抗栓可能增加AF 患者出血及出血性卒中事件的发生率[14-19]。
本研究回顾性分析AF 患者行冠状动脉支架置入术后予以不同抗栓治疗方案后的出血与主要不良心血管事件发生情况,与二联抗栓组合(华法林+氯吡格雷)相比,不论是在随访早期的90 d 内,还是90 ~360 d,三联抗栓组合总出血事件发生率均显著增加,这与部分研究结果一致[16,20]。通过Cox 多因素回归分析发现,高HAS-BLED 评分(≥3 分)、三支血管病变、早期随访期间出血、血小板糖蛋白Ⅱb/Ⅲa 抑制剂的使用等因素均会影响抗栓治疗期间患者的出血风险。然而,两组主要不良心血管事件发生率比较,差异无统计学意义,但是缺血及卒中史、高CHA2DS2-VASc 评分(≥2 分)、心力衰竭等因素与主要不良心血管事件显著相关,这与Dewilde等[21]、Seivani 等[22]研究结果相似。提示注重患者危险因素分层及出血与血栓风险评分的情况下,选择二联抗栓治疗可有效减少AF 患者的出血风险,同时不增加主要不良心血管事件的发生率。
本研究结果进一步证实了之前研究[23-24]的结论,即口服抗凝药的AF 患者在接受PCI 治疗后出血发生率增加。然而,引起这一结果的原因可能是多方面的,诸如抗栓药物的本身、置入支架的种类、患者的临床特征以及相关伴随疾病等[25]。因此,患者抗栓方案的选择应在参考指南的同时兼顾患者自身的出血及血栓风险评分。单从CHA2DS2-VASc 评分的角度来看,高达80% ~90%的AF 患者可能伴随中度到重度的血栓风险[26],这类患者具备了行三联抗栓治疗的必要性。本研究根据CHA2DS2-VASc评分结合患者自身的临床特征,如HAS-BLED 评分等,非随机给予三联或二联抗栓方案,尽管抗栓治疗本身可能会带来更多的血栓或出血风险,但从结果分析可见,个体化的抗栓方案能使更多患者获益,避免可能的出血风险。
近年来,已有多个回顾性研究分析了三联组合抗栓治疗的优缺点,研究者最为关注的依然是相关的出血风险。Lamberts 等[16]和Hansen 等[27]研究中,AF 患者支架置入术后三联抗栓治疗30 d 内出血发生率高达22.6%。Dbrowskal 等[28]的研究比较支架置入术后两组AF 患者抗栓治疗12 个月时,TT 组出血发生率为38.9%,DT 组为17.2%。本研究中发现90 d 时TT 组出血发生率为18.3%,DT 组为6.5%;90 ~360 d 时TT 组出血发生率为24.2%,DT 组为11.1%。然而,即便前瞻性、随机化的临床研究也很难准确评估患者的出血发生率,此外,不同研究间存在诸多差异因素,如患者的年龄、生活习惯、饮食、出血和凝血评分、患者依从性等。如本研究中血小板糖蛋白Ⅱb/Ⅲa 抑制剂的使用、早期出血都是导致后期随访期间出血发生的因素。因此,更多更大临床样本的研究分析非常必要,只有在综合更多临床样本分析的基础上,排除各个样本可能的混杂因素影响,才可能得出更为客观的结果,为AF 患者冠状动脉支架置入术后的抗栓方案选择提供更多证据支持。AF 患者PCI 术后最佳抗栓方案的选择仍需进一步分析和探索。
尽管本研究可为AF 患者PCI 术后抗栓方案的选择提供一定参考价值,但是与随机大样本的前瞻性临床研究相比,还存在不足之处,如患者自我报告的出血及血栓事件可能存在一定的主观性。此外,整个研究无法准确实时监测患者的凝血功能INR,以至于未能及时预防或控制可能的出血或血栓事件。整个研究的样本量偏小,也可能是两组患者主要出血事件发生率差异无统计学意义的可能原因。
[1]马依彤,谢翔.血小板功能和基因检测指导下的抗血小板治疗进展.中国介入心脏病学杂志,2014,22:44-46.
[2]Madan S,Shah S, Partovi S, et al. Use of novel oral anticoagulant agents in atrial fibrillation:current evidence and future perspective. Cardiovasc Diagn Ther,2014,4:314-323.
[3]O'Dell KM,Igawa D,Hsin J. New oral anticoagulants for atrial fibrillation:a review of clinical trials. Clin Ther,2012,34:894-901.
[4]Camm AJ,Lip GY,De Caterina R,et al. 2012 focused update of the ESC Guidelines for the management of atrial fibrillation:an update of the 2010 ESC Guidelines for the management of atrial fibrillation. Developed with the special contribution of the European Heart Rhythm Association. Eur Heart J,2012,33:2719-2747.
[5]Kirchhof P,Ammentorp B,Darius H,et al. Management of atrial fibrillation in seven European countries after the publication of the 2010 ESC Guidelines on atrial fibrillation:primary results of the PR Evention of thromboemolic events--European Registry in Atrial Fibrillation (PREFER in AF). Europace,2014,16:6-14.
[6]Tapp LD,Lip GY,Lane DA. Optimal antithrombotic therapy in patients receiving long-term oral anticoagulation requiring percutaneous coronary intervention:"triple therapy" or "triple threat". Chest,2011,139:240-242.
[7]Renoux C,Patenaude V,Suissa S. Incidence,mortality,and sex differences of non-valvular atrial fibrillation:a population-based study. J Am Heart Assoc,2014,3:29-34.
[8]佟佳宾,施海峰,邹彤,等.高龄心房颤动患者导管消融围术期不同抗凝方案的对比观察.中国介入心脏病学杂志,2014,22:220-223.
[9]Lehto M,Mustonen P,Tierala I. The use of direct oral anticoagulants (DOAC)in the treatment atrial fibrillation (AF)patients. Duodecim,.2014,130:1709-1717.
[10]Naccarelli GV,Panaccio MP,Cummins G,et al. CHADS2 and CHA2DS2-VASc risk factors to predict first cardiovascular hospitalization among atrialfibrillation/atrial flutter patients. Am J Cardiol,2012,109:1526-1533.
[11]Roldán V,Marín F,Manzano-Fernández S,et al. The HASBLED score has better prediction accuracy for major bleeding than CHADS2 or CHA2DS2-VASc scores in anticoagulated patients with atrial fibrillation. J Am Coll Cardiol,2013,62:2199-2204.
[12]Goto S,Ogawa H,Takeuchi M,et al. Double-blind,placebocontrolled Phase Ⅱstudies of the protease-activated receptor 1 antagonist E5555 (atopaxar)in Japanese patients with acute coronary syndrome or high-risk coronary artery disease. Eur Heart J,2010,31:2601-2613.
[13]Goto S,Bhatt DL,Rther J,et al. Prevalence,clinical profile,and cardiovascular outcomes of atrial fibrillation patients with atherothrombosis. Am Heart J,2008,156:855-863.
[14]Manzano-Fernández S,Pastor FJ,Marín F,et al. Increased major bleeding complications related to triple antithrombotic therapy usage in patients with atrial fibrillation undergoing percutaneous coronary artery stenting.Chest,2008,134:559-567.
[15]Paikin JS,Wright DS,Crowther MA,et al. Triple antithrombotic therapy in patients with atrial fibrillation and coronary artery stents. Circulation,2010,121:2067-2070.
[16]Lamberts M,Olesen JB,Ruwald MH,et al. Bleeding after initiation of multiple antithrombotic drugs, including triple therapy,in atrial fibrillation patients following myocardial infarction and coronary intervention:a nationwide cohort study.Circulation,2012,126:1185-1193.
[17]Srensen R,Hansen ML,Abildstrom SZ,et al. Risk of bleeding in patients with acute myocardial infarction treated with different combinations of aspirin,clopidogrel,and vitamin K antagonists in Denmark:a retrospective analysis of nationwide registry data.Lancet,2009,374:1967-1974.
[18]Zeymer U,Zahn R. Antithrombotic therapy and atrial fibrillation:Dual or triple therapy after acute coronary syndrome and stent?Herz,2014,39:814-818.
[19]Cho JR,Angiolillo DJ. Percutaneous coronary intervention and atrial fibrillation: the triple therapy dilemma. J Thromb Thrombolysis. J Thromb Thrombolysis,2014. [Epub ahead of print]
[20]Lamberts M,Gislason GH,Olesen JB,et al. Oral anticoagulation and antiplatelets in atrial fibrillation patients after myocardial infarction and coronary intervention. J Am Coll Cardiol,2013,62:981-989.
[21]Dewilde WJ,Oirbans T,Verheugt FW,et al. Use of clopidogrel with or without aspirin in patients taking oral anticoagulant therapy and undergoing percutaneous coronary intervention:an open-label,randomised,controlled trial. Lancet,2013,381:1107-1115.
[22]Seivani Y,Abdel-Wahab M,Geist V,et al. Long-term safety and efficacy of dual therapy with oral anticoagulation and clopidogrel in patients with atrial fibrillation treated with drug-eluting stents.Clin Res Cardiol,2013,102:799-806.
[23]Khurram Z,Chou E,Minutello R,et al. Combination therapy with aspirin,clopidogrel and warfarin following coronary stenting is associated with a significant risk of bleeding. J Invasive Cardiol,2006,18:162-164.
[24]Deshmukh A,Hilleman DE,Del Core M,et al. Antithrombotic regimens in patients with indication for long-term anticoagulation undergoing coronary interventions-systematic analysis,review of literature,and implications on management. Am J Ther,2013,20:654-663.
[25]Doktorova M,Motovska Z. Clinical review:bleeding -a notable complication of treatment in patients with acute coronary syndromes:incidence,predictors,classification,impact on prognosis,and management. Crit Care,2013,17:239.
[26]Dewilde W,Berg JT. Triple antithrombotic management after stent implantation:when and how?Heart,2010,96:73.
[27]Hansen ML,Srensen R,Clausen MT,et al. Risk of bleeding with single,dual,or triple therapy with warfarin,aspirin,and clopidogrel in patients with atrial fibrillation. Arch Intern Med,2010,170:1433-1441.
[28]Dbrowska M,Ochaa A,Cybulski W,et al. Balancing between bleeding and thromboembolism after percutaneous coronary intervention in patients with atrial fibrillation. Could triple anticoagulant therapy be a solution? Postepy Kardiol Interwencyjnej,2013,9:234-240.

