替格瑞洛在行经皮冠状动脉介入治疗的急性冠状动脉综合征患者中的疗效和安全性观察
李志华 张亚臣 解玉泉 张燚 徐琛华 相银 吴红 陈漫天 孟舒 沈成兴
近年来急性冠状动脉综合征(acute coronary syndrome,ACS)已成为冠心病患者的主要死亡原因。血小板受体拮抗剂作为抗血小板聚集药物,在ACS 的治疗中发挥重要作用[1]。氯吡格雷和阿司匹林的双联抗血小板疗法是ACS 患者经皮冠状动脉介入治疗(percutaneous coronary intervention,PCI)术后药物治疗的基石,可明显降低死亡率、再发心肌梗死和支架内血栓等临床终点事件的发生率[2-3]。替格瑞洛是一种新型腺苷二磷酸(ADP)受体拮抗剂,不但可快速、强效地抑制ADP 介导的血小板聚集,且有效性不受肝CYP2C19 基因多态性影响,作为非前体药物具有起效快、抗血小板效果强、个体差异小等优点[4-5]。研究显示,与氯吡格雷相比,替格瑞洛可明显降低各种心血管事件的死亡率[6-8]。然而,替格瑞洛在国内患者中的应用还处于初级阶段,国人对于替格瑞洛的反应性尚缺乏循证医学证据。因此,本研究观察ACS 患者PCI 术后应用替格瑞洛的临床疗效和安全性,为行PCI 术的ACS患者应用替格瑞洛抗血小板治疗提供依据。
1 对象与方法
1.1 研究对象
纳入2013 年2 月至2014 年6 月于上海交通大学医学院附属新华医院心血管内科接受PCI 术的ACS 患者1200 例。
1.1.1 入选标准 (1)年龄18 ~75 岁,男女不限。(2)发病24 h 内的ST 段抬高心肌梗死(STEMI)和非ST 段抬高急性冠状动脉综合征[NSTE-ACS,包括非ST 段抬高心肌梗死(NSTEMI)和不稳定型心绞痛(UA)]患者。(3)对于STEMI 患者,需要满足以下2 个诊断标准:①≥2 个相邻导联的ST 段持续抬高至少0.1 mV,或新发的左束支传导阻滞;②计划行直接PCI。(4)对于NSTE-ACS 患者,至少需要满足以下3 个标准中的2 个:①心电图显示有ST 段改变,提示缺血;②生物标志物试验结果阳性,表明有心肌坏死;③年龄≥60 岁,既往有心肌梗死或接受过冠状动脉旁路移植术(coronary artery bypass graft,CABG),冠状动脉疾病,至少2 支血管有≥50%的狭窄,既往有缺血性卒中、短暂性脑缺血发作、颈动脉至少50%的狭窄或接受过脑血管血运重建术,糖尿病,外周动脉疾病,慢性肾功能不全(定义为肌酐清除率<60 ml/min)。(5)知情同意。
1. 1. 2 排除标准 含有以下任意一项者不能纳入本研究。(1)任何使用氯吡格雷的禁忌证。(2)随机分组前24 h 内接受了纤维蛋白溶解疗法的治疗。(3)需要口服抗凝药物治疗。(4)血小板计数<100 ×109/L 或>500 ×109/L 者。(5)6 个月内发生脑卒中,3 个月内行大手术史,活动性消化道溃疡病史。(6)严重肝肾功能不全者[谷丙转氨酶(ALT)及谷草转氨酶(AST)检测大于正常值2 倍,肌酐清除率≥60 ml/min]。(7)有严重感染合并恶性肿瘤、血液系统疾病及风湿免疫系统疾病者。(8)妊娠期妇女。(9)同时接受强CYP3A 抑制剂/诱导剂治疗。(10)贫血(血红蛋白<100 g/L)。
1.2 研究方法
使用随机数方法产生随机数字并生成处理编码保存于密封信封内,根据患者入组先后,按顺序依次拆开信封,按信封内的随机号码分为氯吡格雷组(600 例)和替格瑞洛组(600 例)。两组患者入院后均接受常规阿司匹林肠溶片(拜耳医药保健公司,进口药品注册证号J200800778,100 mg/片)治疗,术前300 mg 负荷剂量,术后100 mg/次、每日1 次。除非有禁忌,否则一律常规应用硝酸酯制剂、血管紧张素转化酶抑制剂(ACEI)或血管紧张素Ⅱ受体拮抗剂(ARB)、β 阻滞剂、他汀类药物。氯吡格雷组术前给予氯吡格雷(杭州赛诺菲民生制药有限公司,进口药品注册证号 J20040006,75 mg/片)负荷剂量300 mg,术后75 mg/次、每日1 次,口服,持续12 个月;替格瑞洛组术前给予替格瑞洛(AstraZeneca,AB 国药准字J20130020,90 mg/片)负荷剂量180 mg,术后90 mg/次、每日2 次,口服,持续12 个月。患者服药前和口服负荷剂量药物后2、24、48 h 分别抽取肘静脉血3 ml 置入枸橼酸钠抗凝真空采血管,2 h 内完成血小板抑制率的检测。应用美国Haemoscope 公司生产的TEG 分析仪(型号TEG5000),以2 μmol/L ADP 为激活物分别由计算机软件测定两组患者的血小板抑制率。
1.3 随访
术后1、3、6 个月通过门诊及住院对患者进行随访,针对患者出现的问题进行记录及干预。(1)研究的主要终点为主要不良心血管事件(MACE),包括心原性死亡、支架内血栓形成、心力衰竭、再次血运重建、再发心肌梗死等事件。再发心肌梗死的诊断标准:持续胸痛30 min 以上,心肌酶>3 倍正常值上限,心电图有动态改变。急性血栓形成:在支架置入术后24 h 内血栓性支架闭塞。亚急性血栓形成:在支架置入术l d 以后,发生血栓性支架闭塞。(2)次要终点为大出血和小出血情况。大出血:致命性颅内出血,血红蛋白下降≥50 g/L 或输血≥4 U,需要升压药物或手术治疗的低血压;伴心脏压塞的心包内出血;低血容量性休克,显著的功能丧失,如眼内出血伴永久性失明,输血2 ~3 U 或血红蛋白下降30 ~50 g/L。小出血:除大出血外的鼻出血、牙龈出血及注射部位渗血、瘀斑等。(3)一般不良反应包括过敏、呼吸困难、皮疹等。
1.4 统计学分析
采用SPSS 18.0 统计学软件进行数据分析。计量资料以珋±s 表示,两组比较采用独立样本t 检验;计数资料以率表示,两组比较采用χ2检验。以P <0.05 为差异有统计学意义。
2 结果
2.1 两组患者基线资料比较
氯吡格雷组与替格瑞洛组患者的年龄、性别、吸烟、体质量指数(body mass index,BMI)、合并症和用药情况等基线资料比较,差异均无统计学意义(均P >0.05,表1)。
2.2 两组患者不同时间点的血小板抑制率比较
口服药物前,两组间血小板抑制率比较,差异无统计学意义(P >0.05)。口服负荷剂量药物后不同时间点,替格瑞洛组血小板抑制率均明显高于氯吡格雷组(P <0.05,表2)。
2.3 两组患者随访情况比较
氯吡格雷组3 个月时失访19 例,6 个月时失访21 例;替格瑞洛组3 个月时失访20 例,6 个月时失访23 例。随访期间,两组均未发生死亡、大出血事件。替格瑞洛组主要终点事件发生率低于氯吡格雷组(1 个月:0 比0.2%,P =0.816;3 个月:10.5%比13. 1%,P =0. 506;6 个月:6. 9%比9. 8%,P =0.447),出血率高于氯吡格雷组(1 个月:13.5%比12.8%,P = 0.836;3 个月:12.8% 比11.5%,P =0.825;6 个月:11.6%比11.4%,P=0.818),但差异均无统计学意义。术后1 个月替格瑞洛组呼吸困难发生率高于氯吡格雷组(4.3% 比3.3%,P =0.310),但差异无统计学意义;两组术后3、6 个月呼吸困难例数均明显减少,且差异无统计学意义(均P >0.05)。两组间术后1、3、6 个月的皮疹发生率比较,差异均无统计学意义(均P >0.05,表3)。
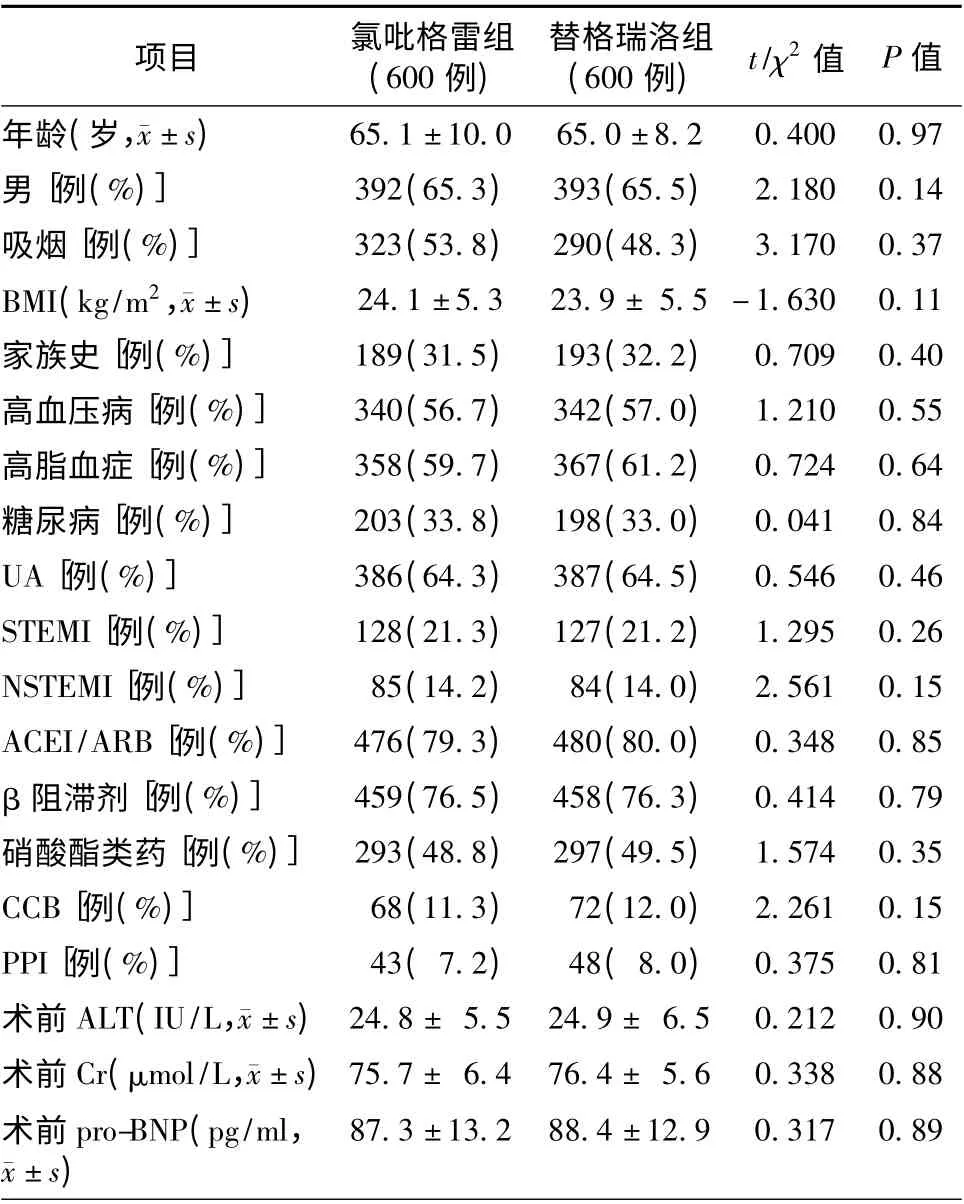
表1 氯吡格雷组和替格瑞洛组患者基线资料比较
表2 两组患者经腺苷二磷酸途径的血小板抑制率比较(%,珋±s)

表2 两组患者经腺苷二磷酸途径的血小板抑制率比较(%,珋±s)
时间点 氯吡格雷组(600 例)替格瑞洛组(600 例) t 值 P值服药前58.2 ±5.2 58.1 ± 5.3 0.043 0.90服药后2 h 62.1 ±5.5 75.2 ±20.5 3.519 <0.05 24 h 63.6 ±8.5 75.4 ±19.5 3.402 <0.05 48 h 64.3 ±7.4 78.3 ±18.6 3.733 <0.05

表3 两组患者1、3、6 个月随访情况[例(%)]
3 讨论
替格瑞洛是一种治疗ACS 的新型药物,为非前体药物,直接与P2Y12受体可逆性结合,无须经肝代谢激活,可快速生成其主要循环代谢产物ARC124910XX。药物本身及其代谢产物均有活性,可快速强效地抑制ADP 介导的血小板聚集,且有效性不受肝CYP2C19 基因多态性影响,在停药后血小板可恢复功能。这一点在临床上非常重要,可确保其安全性和有效性。而氯吡格雷是一种前体药物,须在肝内通过肝细胞色素P450酶(CYP)的作用下经两步代谢为活性代谢产物方可发挥抑制血小板效应,且有氯吡格雷抵抗发生。基因多态性是造成氯吡格雷反应变异性的主要原因之一,导致其抗血小板效应难以预测。另外,吸烟、BMI 超标、糖尿病等患者PCI 术后氯吡格雷抵抗发生率会升高[9]。替格瑞洛具有双重抑制作用,一方面通过抑制P2Y12受体,起到了很好的抗血小板作用;另一方面,通过抑制红细胞上ENT-1 对腺苷再摄取,加强局部腺苷反应,达到额外的血小板聚集/活化抑制作用,以及血管舒张、心肌保护等作用。本研究显示,口服药物2 h,替格瑞洛组患者的血小板抑制率显著高于氯吡格雷组[(75.2 ±20.5)%比(62.1 ±5.5)%,P <0.05],且血小板抑制率达到高峰,并一直持续到48 h。虽然氯吡格雷口服后抗血小板聚集作用也明显增强,并持续增强,但不同时间点血小板抑制率均低于替格瑞洛。说明替格瑞洛较氯吡格雷的抗血小板聚集作用更强。这与ONSET/OFFSET 研究[10]的结果相似。术后6 个月替格瑞洛组无大出血事件发生,小出血率虽高于氯吡格雷组,但差异无统计学意义,说明替格瑞洛在抑制血小板聚集同时并未增加出血风险,这与PLATO 研究[8]的结果相似。说明替格瑞洛更强的抗血小板作用及与P2Y12可逆结合的特点,达到了缺血与出血之间的平衡。
有文献显示,抗血小板药物在抑制血小板的同时,可以进一步抑制因血小板聚集所引起的血管内皮和心肌细胞的损伤发展过程,起到间接保护并修复血管和心肌的作用[11]。
本研究随访期间,两组均未发生死亡、大出血事件,替格瑞洛组的主要终点事件发生率低于氯吡格雷组,出血率高于氯吡格雷组,但两组间差异均无统计学意义。提示替格瑞洛在改善ACS 患者PCI 术后不良事件的发生方面,与氯吡格雷疗效相当。PLATO 研究[8]中替格瑞洛和氯吡格雷的联合有效性和安全性的复合终点事件发生率分别为16.4%和17.8%,这与本研究结果相似。
呼吸困难是替格瑞洛较常见的并发症。本研究中替格瑞洛组患者呼吸困难的发生率只在服药1 个月时高于氯吡格雷,但都为轻度,发生时间多在口服药物后1 ~2 周内,且多为合并慢性阻塞性肺疾病(COPD)的患者,持续时间比较短,患者可耐受,无停药现象。随访3、6 个月时两组患者呼吸困难发生率明显减少,且两组的差异无统计学意义。这也提示合并COPD 的患者易发生呼吸困难,因而需结合肺功能评估来调整替格瑞洛的应用。目前替格瑞洛诱发呼吸困难的原因尚不明确,多数学者认为替格瑞洛作为腺苷三磷酸类似物有支气管刺激作用,容易导致呼吸系统不良应激及支气管收缩[12-13]。此外,替格瑞洛能够抑制红细胞上ENT-1 再摄取腺苷[14],使腺苷在局部组织浓集,在部分敏感患者中引起一过性的呼吸困难,这也可能是导致呼吸困难的原因。
作为一种新型ADP 受体拮抗剂,替格瑞洛已在欧美ACS 患者中得到广泛使用。2011 年美国心脏病学会基金会/美国心脏协会/心血管造影和介入联合会(ACCF/AHA/SCAI)经皮冠状动脉介入治疗指南[15]和2012 年ACCF/AHA 不稳定型心绞痛和非ST 段抬高心肌梗死治疗指南[16]均推荐替格瑞洛作为抗血小板药物治疗的优先选择。本研究发现,替格瑞洛较氯吡格雷在ACS 患者PCI 术后应用的抗血小板聚集作用起效更快更强,且两者的安全性相当。
[1]Anderson SD,Shah NK,Yim J,et al. Efficacy and safety of ticagrelor: a reversible P2Y12 receptor antagonist. Ann Pharmacother,2010,44:524-537.
[2]李小鹰,付治卿. 老年冠心病药物治疗进展. 医学研究杂志,2011,40:3-5.
[3]马颖艳,王艳霞,徐白鸽,等.替格瑞洛用于冠状动脉介入治疗术后患者抗血小板治疗短期内的有效性和安全性研究.中国介入心脏病杂志,2014,22:380-383.
[4]Gurbel PA,Bliden KP,Butler K,et al. Randomized doubleblind assessment of the ONSET and OFFSET of the antiplatelet effects of ticagrelorversus clopidogrel in patients with stable coronary artery disease: The ONSET/OFFSET study.Circulation,2009,120:2577-2585.
[5]Montalescot G,Lassen JF,Hamm CW,et al. Ambulance or incatheterization laboratory administration of ticagrelor for primary percutaneous coronary intervention for ST-segment elevation myocardial infarction:rationale and design of the randomized,double-blind Administration of Ticagrelor in the cath Lab or in the Ambulance for New ST elevation myocardial Infarction to open the Coronary artery (ATLANTIC)study. Am Heart J,2013,165:515-522.
[6]Shand JA,Menown IB,Storey RF. Ticagrelor:from concept to clinical evaluation. Biomark Med,2011,5:53-62.
[7]Abtahian F,Yonetsu T, Vergallo R, et al. Ticagrelor immediately prior to stenting is associated with smaller residual thrombus in patients with acute coronary syndrome. Int J Cardiol,2013,168:3099-3101.
[8]Steg PG,Harrington RA, Emanuelsson H, et al. Stent thrombosis with ticagrelor versus clopidogrel in patients with acute coronary syndromes: an analysis from the prospective,randomized PLATO trial. Circulation,2013,128:1055-1065.
[9]黄晓红,陈昱,唐勇,等. 急性冠脉综合症患者经皮冠状动脉介入治疗术后氯吡格雷抵抗相关因素分析. 中华实用诊断与治疗杂志,2013,27:1153-1155.
[10]Steiner S,Moertl D,Chen L,et al. Network meta-analysis of prasugrel,ticagrelor,high- and standard-dose clopidogrel in patients scheduled for percutaneous coronary interventions.Thromb Haemost,2012,108:318-327.
[11]Varenhorst C,Alstrom U,Scirica BM,et al. Factors contributing to the lower mortality with ticagrelor compared with clopidogrel in patients undergoing coronary artery bypass surgery. J Am Coll Cardiol,2012,60:1623-1630.
[12]朱永宏,贾国良,周妙,等. 替格瑞洛治疗41 例急性冠状动脉综合征患者的临床疗效. 中国介入心脏病杂志,2013,21:374-376.
[13]Storey RF,Becker RC,Harrington RA,et al. Pulmonary function in patients with acute coronary syndrome treated with ticagrelor or clopidogrel (from the Platelet Inhibition and Patient Outcomes [PLATO]pulmonary function substudy). Am J Cardiol,2011,108:1542-1526.
[14]Ohman J,Kudira R,Albinsson S,et al. Ticagrelor induces adenosine triphosphate release from human red blood cells.Biochem Biophys Res Commun,2012,418:754-758.
[15]Levine GN,Bates ER,Blankenship JC,et al. 2011ACCF/AHA/SCAI Guideline for Percutaneous Coronary Intervention:a report of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines and the society for Cardiovascular Angiography and Interventions.J Am Coll of Cardiol,2011,58:e44-122.
[16]Anderson JL,Adams CD,Antman EM,et al. 2012 ACCF/AHA focused update incorporated into the ACCF/AHA 2007 guidelines for the management of patients with unstable angina/non-STelevation myocardial infarction:a report of the American College of Cardiology Foundation Task Forc on Practice Guidelines. J Am Coll Cardiol,2013,61:e179-347.

