气体生物脱硫及硫回收研究进展
宋子煜, 吴 丹, 董 健, 张 建, 李清方, 邢建民, 刘会洲
(1.中国科学院 过程工程研究所 生化工程国家重点实验室, 北京100190;2.中国科学院 过程工程研究所 中科院绿色过程与工程重点实验室, 北京100190;3.中国石化 石油工程设计有限公司,山东 东营 257026)
气体生物脱硫及硫回收研究进展
宋子煜1, 吴 丹1, 董 健3, 张 建3, 李清方3, 邢建民1, 刘会洲2
(1.中国科学院 过程工程研究所 生化工程国家重点实验室, 北京100190;2.中国科学院 过程工程研究所 中科院绿色过程与工程重点实验室, 北京100190;3.中国石化 石油工程设计有限公司,山东 东营 257026)
硫化氢脱除是石油天然气开采、炼化、煤化工、水处理等行业清洁安全生产所面临的重大任务之一。气体生物脱硫及硫回收是基于生物硫氧化原理建立起来的以硫磺回收为目标的湿法硫化氢脱除方法,具有生物催化剂可再生、生物硫磺不易堵塞等优点。围绕硫化氢脱硫的方法及应用研究,重点介绍了气体生物脱硫及硫回收过程机理的研究进展,分析总结其优势和特点,并根据现有研究不足展望其未来发展。
气体生物脱硫;硫氧化菌;硫化氢;硫磺回收;生物硫氧化
硫化氢(H2S)是一种恶臭、剧毒、腐蚀、易燃的气体,可导致大气污染、设备腐蚀、自燃隐患、危及人身安全等一系列问题。石油天然气开采、炼化、煤化工、水处理、冶炼、印染、造纸等行业生产均不同程度地产生H2S,尤其是天然气开采和沼气生产,H2S脱除是最必要的生产工艺。近年来,随着环保标准提高,高含硫天然气开发和煤化工快速发展,亟待开发清洁高效H2S脱除方法,以解决目前H2S脱除所面临的成本高、硫堵、二次污染等问题。气体生物脱硫及硫回收是基于生物硫氧化原理建立起来的以硫磺回收为目标的湿法H2S脱除方法,具有生物催化剂可再生、生物硫磺水分散性好等优点。
笔者首先介绍H2S危害及工业生产中常用的H2S脱除方法,分析现有工艺的局限性,进而介绍气体生物脱硫及硫回收工艺原理,比较分析其优势和特点,重点综述生物硫氧化过程的机理研究和应用研究的进展,最后,分析其面临的技术瓶颈,展望其未来重点研究的发展。
1 H2S的危害、来源和脱除方法
1.1 H2S的危害
H2S是一种恶臭、剧毒、腐蚀、易燃的气体,其嗅觉阈值低,仅为0.8 μg/m3,是造成厂区及周边环境恶臭的主要原因。H2S毒性强,其质量浓度达到200 mg/m3时,短时间可致人死亡,是石油开采、石油化工、煤化工等行业重点防范的危险气体[1]。
石化生产中普遍存在H2S对设备和管道产生强烈腐蚀的问题,尤其在湿环境中H2S腐蚀问题更为严重,极易产生应力开裂、应力腐蚀开裂、氢鼓泡及氢致裂纹,危及安全生产[2-3]。
H2S不仅是易燃气体,而且会与铁反应生成自燃点仅为40℃的硫化铁。当硫化温度高于50℃时,腐蚀产物的主要成分为FeS2,其自燃性更高。H2S腐蚀产物的自燃是引发火灾和爆炸事故的主要点火源之一[4]。
1.2 H2S的来源
全球几乎所有发现的气藏中都或多或少含有H2S。天然气中H2S体积分数超过2%被称为高含硫天然气。目前已在四川、渤海湾、鄂尔多斯、塔里木和准噶尔等含油气盆地发现了含H2S天然气,其中四川盆地川东北气区、华北赵兰庄气田和胜利油田罗家气田为高含H2S气田,仅“十五”期间探明的天然气中就有990亿m3为高含H2S[5-6]。目前,我国已探明的天然气气田中,含硫天然气气田约占31.7%[7]。国家对商品天然气的H2S含量有严格的规定,脱硫是天然气加工的关键步骤[8]。
原油含有多种无机硫和有机硫,硫体积分数为1.0%以上的高含硫原油产量占世界总量的55%以上,汽、柴油等燃料中硫含量有严格的要求。目前,加氢是原油脱硫的主要方法,氢气在催化剂的作用下将原油中各种硫还原为H2S。加氢裂化和催化裂化等原油加工过程中也会产生H2S[9-10]。
焦炉气是煤炭炼焦过程中产生的可燃气,用于生产合成氨、甲醇等有机物。焦炉气原料干煤全硫质量分数在0.5%~1.2%范围,加工过程中20%至45%的硫会转至焦炉气中,其中95%以上为H2S[11]。
沼气由厌氧产甲烷菌分解有机物产生,同时厌氧条件下硫酸盐也会被硫酸盐还原菌转化为硫化物。因此,沼气都含有体积分数在0.005%~2%的H2S,高含硫酸盐废水产生的沼气,H2S体积分数可达到4%[12]。此外,硫酸盐还原作用还存在于水解酸化和兼氧反硝化中,由此产生的含H2S的恶臭气体,可污染厂区及周边环境[13-14]。
1.3 H2S脱除方法
H2S脱除方法主要分为干法和湿法2大类。干法脱硫包括吸附剂法、氧化铁法、氧化锌法,具有脱硫精度高、对无机硫和有机硫都有较高脱除效率等特点,多用于小规模深度脱硫[15-17]。Claus法脱硫也属于干法脱硫,部分H2S先燃烧成SO2,再在催化剂的帮助下与剩余的H2S反应生成单质硫。与其他方法不同,Claus法脱硫主要应用于大规模H2S处理,但脱硫精度不高,尾气中含有较高浓度的SO2。
湿法脱硫可分为吸收和氧化2类。湿法吸收脱硫是利用胺醇、碱液、低温甲醇等对H2S溶解度较高的溶液吸收H2S。但H2S仅被吸收,仍存在后续处理的问题。因此,此类方法大多作为H2S富集分离,常作为Claus等其他脱硫方法辅助工艺。湿法氧化脱硫在碱性溶液中加氧化剂或者催化剂,达到快速脱除H2S,包括络合铁法、栲胶法等[18-20]。
此外,H2S也可直接制硫酸,代表方法是丹麦托普索公司的WSA工艺。H2S燃烧生成SO2,在钒催化剂的作用下,直接被水蒸气吸收转化为工业浓硫酸成品。该方法具有SO2排放量优于国家标准、不消耗工艺水、不产生废水、不消耗吸收剂等优点[21]。
1.4 现存H2S脱除法的不足
随着环保标准不断提高,以及对生产效率不断追求,工业上使用的主要脱硫方法暴露出很多问题。Claus工艺和WSA工艺均依赖H2S燃烧,对于H2S体积分数有较高要求(>25%),常与醇胺法或低温甲醇法相结合,先通过醇胺或低温甲醇吸收H2S,再解吸H2S,从而制取高浓度H2S气体[22-23]。醇胺和甲醇吸收H2S时也会吸收CO2,不仅消耗吸收容量,而且影响解吸气体的H2S浓度[24]。Claus工艺和WSA工艺不适于CO2/H2S摩尔比较高的气体脱硫,并且存在工艺路线长、设备投资大、操作难度大等问题。此外,醇胺吸收产生难处理的废液,低温甲醇能耗高且设备昂贵。CO2含量较高的气体脱硫一般采用碱性湿法脱硫,如络合铁法或栲胶法[25-26]。以弱碱性碳酸钠溶液为吸收剂,CO2几乎不被吸收,不会影响脱硫效率。目前,湿法脱硫存在的主要问题是配体降解、副盐累积和硫堵,导致经济性差,连续生产困难[27]。气体生物脱硫及硫回收方法属于湿法脱硫,以硫氧化菌代替络合铁等化学催化剂,不仅具有湿法脱硫的优点,而且克服了药剂消耗量大和硫磺堵塞的问题。
2 生物硫氧化脱硫过程的机理研究和研究进展
2.1 硫氧化菌和生物硫氧化
硫氧化菌是一类具有氧化硫能力的微生物的总称,包括光合细菌、化能自养菌、异养菌,如Chromntium、Chlorobium、Thiobacillus、Thiothrix、Beggiatoa、Thiomicrospira、Achromatium、Desulfovibrio、Desulfomonas、Desulfococcus、Desulfuromonas、Pseudomonas、Mycobacterium、Arthrobacter、Flavobacterium、Xanthobacter[28-30],其中最重要的是以Thiobacillus为代表的化能自养硫化氧菌。该类硫氧化菌可将硫化物氧化为单质硫,从硫氧化中获得生长和代谢的能量,生长所需碳源来自于CO2固定化,并对硫醇、硫醚等有机硫也有一定的氧化能力[31-33]。
硫生物氧化与化学氧化的反应过程显著不同。化学氧化的中间产物和终产物种类更多,主要为单质硫、硫代硫酸盐、亚硫酸、硫酸,其中主要产物为硫代硫酸盐[34-36]。硫化物化学氧化反应过程中,硫化物被自催化氧化为多聚硫化物,多聚硫化物再被氧化为多聚硫酸盐,多聚硫酸盐不稳定,水解为硫酸盐和硫代硫酸盐。在水相中,硫代硫酸盐和亚硫酸的化学氧化速率比硫化物氧化速率慢,尤其是硫代硫酸盐,氧化速率非常缓慢,可以认为是稳定的反应产物[37-40]。硫化物的生物氧化不产生硫代硫酸盐,但会产生稳定中间产物硫磺[41]。虽然在生物氧化体系中会检测出硫代硫酸盐,但其由伴随生物氧化的化学氧化而产生[42]。硫生物氧化速率比化学氧化快。贡俊等[43]比较了机械搅拌式反应器内好氧条件下脱氮硫杆菌(Thiobacillusdenitrificans)生物氧化与化学氧化。结果表明,在25~35℃范围内,生物氧化速率较高,温度继续升高,菌体会受到明显抑制;而H2S的化学氧化则随着温度的升高而增强,化学氧化速率缓慢增大;化学氧化速率在最佳菌体生长条件范围内占总氧化速率的比值较小,在8.6%~19.1%范围。
化能自养硫氧化菌用于气体生物脱硫具有2个显著的优势。(1)菌体生长繁殖及代谢的能量来源于硫化物氧化,碳源来自于CO2,不依赖外加碳源,脱硫过程仅消耗碱,不需要催化剂、辅助剂等其他药品。绝大部分消耗碱可在生产单质硫的过程中再生。与化学脱硫方法相比,气体生物脱硫的吸收剂配方简单,药剂消耗少。(2)生物硫磺在水中分散性好,不易形成堵塞,设备使用率高。
目前,气体生物硫氧化及硫回收有2种工艺,分别基于酸性和碱性硫杆菌而建立,代表工艺为Bio-SR和Thiopaq。前者中,H2S吸收的同时,利用Fe3+氧化硫化物,Fe3+被还原为Fe2+,然后氧化亚铁硫杆菌等利用氧气将Fe2+氧化为Fe3+[44-45]。后者中,直接利用碱性溶液吸收H2S,然后脱氮硫杆菌等利用氧气将硫化物直接氧化。Bio-SR工艺pH值为1~2,导致吸收液中硫化物在酸性条件腐蚀性更强,且容易释放H2S气体,限制了此工艺的工业应用。Thiopaq工艺由荷兰Paques公司开发,是最成功的工业化气体生物脱硫工艺,1993年,最先应用于沼气生物脱硫。2004年,Paques与Shell公司合作开发用于高压天然气生物脱硫的Shell-Paques工艺。
2.2 生物硫氧化机制
H2S生物氧化过程由一系列酶促反应组成,硫酸是最终产物,硫磺是最重要的中间产物。已发现的与硫氧化相关的酶系有3个,分别是黄素细胞色素C氧化还原酶(Flavocytochrome C oxidoreductase,FCC)[46-47]、硫氧化酶系(Sulfur oxidizing system,SOX)[48-49]和硫醌氧化还原酶(Sulfide:quinone oxidoreductase,SQR)[50-52],其中FCC和SQR有共同的祖先和相似催化结构域。Johannes等[53]发现,硫氧化菌的实际氧消耗量比理论计算值低大约25%,推测可能是NADH脱氢酶也参与了硫化物氧化。硫化物的电子不传递给氧,而是传递给NAD+,用于CO2同化,合成大分子物质。在限制氧气条件下,单质硫氧化成硫酸最可能是通过NADH途径。他们基于预测的硫氧化菌氧化硫的代谢途径(见图1),建立了用于描述生物硫氧化过程的复合型Michaelis-Menten细胞色素C动力学模型,并通过模拟计算预测气升反应器内产物选择性,模型预测单质硫最大产率可达到约98%[54]。

图1 H2S生物氧化形成单质硫和硫酸根的可能反应途径[54]
2.3 生物硫磺
在水相中,由单质硫或其他富含硫复合物组成的胶体溶液称为硫磺溶胶。硫磺溶胶分为S8构成的疏水性硫溶胶和带磺酸盐等末端亲水性基团的长链硫磺复合物构成的亲水性硫溶胶。这2种硫磺溶胶的胶粒表面都带有负电荷,依靠表面电荷的排斥力维持胶体稳定[55]。
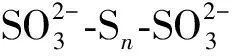
3 气体生物脱硫的脱除能力、过程调控和工艺优化
3.1 生物脱硫的脱除能力
生物硫氧化最早用于脱除恶臭气体中少量的H2S,净化效果好,多以生物滴滤床为反应器。空气与恶臭气体同时进入生物滴滤床,在硫氧化菌的作用下,H2S被完全氧化为硫酸。生物硫氧化脱臭过程中,部分H2S被氧化为单质硫。这些硫磺会在滴滤床内聚积,影响气、液接触。生物滴滤床在缺氧条件下的脱除能力(Elimination capacity,EC)较低,仅为6.9 g/(m3·h)[65];通常提供过量的空气,将H2S完全氧化为硫酸,生成的硫酸被碱中和。由于生物滴滤床的EC较低,限制了气体脱硫的处理规模,所以相关研究多集中在如何改进填料、菌种、工艺条件等,以提高EC。徐潇文等[66]通过改进生物滴滤床填料,使允许进气质量浓度提高至1870 mg/m3,ECmax达到98.4 g/(m3·h)。Fortuny等[67]利用装填特殊表面特性载体的生物滴滤床,去除燃料气中H2S,H2S质量浓度在13000~17400 mg/m3范围内,ECmax提高至235.3~263.5 g/(m3·h)范围。
除改进填料结构外,多菌种混合培养可显著提高EC。姜安玺等[68]以异养黄单胞菌H10与自养排硫硫杆菌A4组成的混合菌群进行脱硫,ECmax达到了134.8 g/(m3·h)。张兰河等[69]从污泥中筛选得到2株硫氧化菌的混合培养物,ECmax也达到了192 g/(m3·h)。
生物脱硫多使用化能自养硫氧化菌,世代周期较长,导致生物滴滤床启动挂膜时间长。为缩短挂膜时间,伍永钢等[70]使用新型高密度聚乙烯改良型拉西环专利填料,采用液相连续流强化挂膜方法,挂膜时间缩短至7 d。以生长代谢更快的异养硫氧化菌代替化能自养菌,也可以缩短挂摸时间。Chung等[71]尝试2种异养硫氧化菌PseudomonasputidaCH11与ArthrobacteroxydansCH8混合培养,徐桂芹等[72]也使用固定化假单孢菌作为硫氧化菌脱除H2S,然而ECmax仅分别为6.25 g/(m3·h)和3.77 g/(m3·h),远低于化能自养菌。
H2S是酸性气体,常以碱液吸收。氧化亚铁硫杆菌(Acidithiobacillusthiooxidans)等酸性硫氧化菌与Fe3+联合,也可用于H2S脱硫[73]。Fe3+氧化H2S,被还原为Fe2+,然后硫氧化菌将Fe2+氧化为Fe3+,完成H2S间接氧化[74]。虽然在酸性条件下,生物滴滤床的EC可达到370 g/(m3·h),但处理的H2S浓度较低,且脱除率不高;当H2S质量浓度为590 mg/m3时,H2S脱除率仅为90%[75]。
3.2 生物脱硫过程调控
硫化物的生物氧化产物种类与S2-/O2摩尔比有关。低溶氧或高硫化物浓度条件下,生物硫氧化的主要产物是单质硫[76]。当硫化物摩尔浓度为0.2 mmol/L和溶氧质量浓度为0.7 μg/L时,仅有10%的硫化物转化为硫酸盐;若溶氧质量浓度提高至6.3 μg/L,硫酸盐生成率可达60%[77]。当S2-/O2摩尔比较高时,硫化物被不完全氧化为单质硫,如式(1)所示;当S2-/O2摩尔比低时,硫化物被完全氧化为硫酸盐,如式(2)所示。当生成单质硫时,氧气不足,溶解氧与硫化物反应后,反应体系中残余溶氧质量浓度往往低于0.1 mg/L(溶氧电极的最低检出限为0.1 mg/L),直接控制溶氧变得非常困难。Janssen等[78]提出,可用氧化还原电势(Redox potential,Et)控制H2S氧化,H2S含量与Et成对数关系,如式(3)所示,通过控制Et,单质硫生成率可达到90%[79-82]。
2HS-+O2→2S0+2OH-
(1)
(2)
Et=-42×1g[HS-]-158
(3)
3.3 生物脱硫工艺优化
生物滴滤床脱除H2S动力学模型预测,ThiobacillusthioparusATCC 23645的ECmax为55 g/(m3·h),Thiobacillusdenitrificans的ECmax可达到627.5 g/(m3·h)[83-85]。生物滴滤床的实际效果远低于模型预测值,这表明滴滤床内部结构和填料还有很大改进空间,有必要设计新型高效生物脱硫反应器。例如,以气升式反应器代替生物滴滤床,最大容积负荷为133.3~155 g/(m3·h)[86-87],高于未使用特殊填料的生物滴滤床。Qiu等[88]利用比活性炭和琼脂更高效的新型磁性多孔球固定化Thiobacillusthioparus,并以磁稳定流化床为反应器,最大容积负荷达到了360 g/(m3·h)。Krishnakumar等[89]设计了一种新型逆流式流化床,用于硫氧化;Thiobacillusdenitrificans在限制氧气的条件下,最大负荷可达到458.3 g/(m3·h),90%硫化物被转化为单质硫;在氧气充足条件下,最大负荷可达到1250.0 g/(m3·h)。
由于生物脱臭以硫酸根为主要产物,每脱除1 mol H2S需要2 mol NaOH中和,碱消耗量较大,所以生物涤气工艺仅适于少量低H2S含量气体净化,不适于含较高浓度或大量H2S气体处理。
生物硫氧化过程最显著的优点在于,将H2S转化为单质硫,吸收消耗的碱可以在生物氧化过程中完全再生,生成的单质硫的水分散性好,不易形成堵塞。基于生物硫氧化的上述特点,人们开发出了高效气体脱硫及硫回收方法,最先用于沼气生物脱硫及硫回收。与生物脱臭相比,国内相关报道较少。
气体生物脱硫及硫回收最佳应用领域为天然气、焦炉气、化工尾气等较大规模脱硫,可以替代络合铁和栲胶湿法氧化脱硫工艺。与湿法化学氧化法相比,生物脱硫在硫磺和硫容等指标上具有明显优势,但对生物脱硫的硫磺转化率、碱消耗量、容积负荷等项指标提出了较高要求,需要在硫氧化高效菌、生物脱硫反应器、工艺控制策略等方面取得技术突破。国际上仅Shell和Paques公司掌握着大规模气体生物脱硫及硫回收技术。通过引进Shell-paques技术,2013年中国石油在四川遂宁建立1.2×106Nm2/d天然气生物脱硫及硫回收工厂。2009年,中国科学院过程工程研究所生化工程国家重点实验室开展气体生物脱硫及硫回收关键技术及装备研究,在我国自然环境中筛选硫氧化菌,针对生物硫氧化产单质硫过程特点,设计了新型生物硫氧化反应器[90],建立了沼气生物脱硫及硫回收工艺。在此基础上,他们又与中国石化石油工程设计有限公司合作,开展天然气生物脱硫及硫回收技术研发,力争建立具有完全自主知识产权的天然气生物脱硫及硫回收工艺。
4 结论与展望
气体生物脱硫及硫回收是一种高效的湿法氧化脱硫工艺,其核心是H2S高选择性氧化为单质硫。然而,生物硫氧化菌有硫氧化的完整酶系,不仅可氧化硫化物,而且会氧化硫磺。目前,生物脱硫为得到较高单质硫产率,采用氧气供应限制的控制策略,即保持最适S2-/O2摩尔比,阻止硫氧化菌将硫磺进一步氧化为硫酸。然而,由于溶氧浓度受到气泡聚并、气液传质速率、气泡氧气浓度变化等因素的影响,所以在大型生物脱硫反应器内控制溶氧浓度分布难度大。这就要求对气液分布等反应器内部结构做出针对性设计,准确控制反应器内各处的硫化物浓度和溶氧浓度,保持反应器内S2-/O2摩尔比在最适范围内。另外,从化学反应动力学来看,高浓度O2有利于加快硫化物氧化速率,提高反应器容积负荷。对硫氧化菌进行基因改造是解决上述问题最直接、最有效的方法。通过基因手段敲除硫磺氧化相关酶,可使硫氧化菌丧失氧化硫磺的能力,从而在任何S2-/O2摩尔比下都能得到高硫磺产率,降低气体生物脱硫及硫回收对反应器和过程控制的依赖。
气体生物脱硫及硫回收在高含CO2气体脱硫领域有显著优势,在四川盆地等高含硫高含CO2天然气气田开采方面应用前景广阔。然而,天然气生物脱硫对处理规模和硫磺产率有较高的要求。国内生物脱硫技术仍针对小规模低浓度恶臭气体脱除,对生物产硫磺不重视,远达不到天然气脱硫标准,必须在高效菌种选育和新型反应器设计等方面取得突破。
[1] 尹忠,廖刚, 梁发书,等. 硫化氢的危害与防治[J]. 油气田环境保护,2004,14(4):37-39.(YIN Zhong, LIAO Gang, LIANG Fashu, et al. Harm of hydrogen sulfide to oil-gas fields and prevention measures[J]. Environmental Protection of Oil & Gas Fields, 2004, 14(4): 37-39.)
[2] 刘伟,蒲晓林, 白小东,等. 油田硫化氢腐蚀机理及防护的研究现状及进展[J]. 石油钻探技术,2008,36(1):83-86.(LIU Wei, PU Xiaolin, BAI Xiaodong, et al. Development of hydrogen sulfide corrosion and prevention[J]. Petroleum Drilling Techniques, 2008, 36(1): 83-86.)
[3] 姚艾. 石油化工设备在湿硫化氢环境中的腐蚀与防护[J]. 石油化工设备,2008,37(5):96-97.(YAO Ai. Corrosion of petrochemical equipment in wet H2S condition and the protection[J]. Petro-Chemical Equipment, 2008, 37(5): 96-97.)
[4] 张振华,赵杉林, 李萍,等. 常温下硫化氢腐蚀产物的自燃历程[J]. 石油学报(石油加工),2012,28(1):122-126.(ZHANG Zhenhua, ZHAO Shanlin, LI Ping, et al. Spontaneous combustion process of hydrogen sulfide corrosion products formed at room temperature[J]. Acta Petrolei Sinica(Petroleum Processing Section), 2012, 28(1): 122-126.)
[5] 戴金星,胡见义, 贾承造,等. 科学安全勘探开发高硫化氢天然气田的建议[J]. 石油勘探与开发,2004,31(2):1-4.(DAI Jinxing, HU Jianyi, JIA Chengzao, et al. Suggestions for scientifically and safely exploring and developing high H2S gas fields[J]. Petroleum Exploration and Development, 2004, 31(2): 1-4.)
[6] 朱光有,戴金星, 张水昌,等. 含硫化氢天然气的形成机制及分布规律研究[J]. 天然气地球科学,2004,15(2):166-170.(ZHU Guangyou, DAI Jinxing, ZHANG Shuichang, et al. Generation mechanism and distribution characteristics of hydrogen sulfide bearing gas in China[J]. Natural Gas Geoscience, 2004, 15(2): 166-170.)
[7] 周璇,刘棋, 魏志强,等. 高含硫气田天然气处理工艺的研究[J]. 天然气与石油,2013,31(2):43-46.(ZHOU Xuan, LIU Qi, WEI Zhiqiang, et al. Research on natural gas treatment process in high sulfide gas field[J]. Natural Gas and Oil, 2013, 31(2): 43-46.)
[8] 陈颖,杨鹤, 梁宏宝,等. 天然气脱硫脱碳方法的研究进展[J]. 石油化工,2011,40(5):565-570.(CHEN Ying, YANG He, LIANG Hongbao, et al. Advances in research of decarbonization and desulfurization for natural gas[J]. Petrochemical Technology, 2011, 40(5): 565-570.)
[9] 于国庆,高金森, 徐春明. 催化裂化加工含硫原油的技术[J]. 石化技术,2004,11(1):58-60.(YU Guoqing, GAO Jinsen, XU Chunming. Process technology of the sour crude oil with catalytic cracking[J]. Petrochemical Industry Technology, 2004, 11(1): 58-60.)
[10] 刘勇军,刘晨光. 硫化氢对渣油加氢脱金属的影响[J]. 石油学报(石油加工),2010,26(3):389-393.(LIU Yongjun, LIU Chenguang. Effects of hydrogen sulfide on residue hydrodemetallization[J]. Acta Petrolei Sinica (Petroleum Processing Section), 2010, 26(3): 389-393.)
[11] 姚占强,任小坤, 史红兵,等. 焦炉气综合利用技术的最新发展及特点[J]. 煤炭加工与综合利用,2009,(2):34-37.(YAO Zhanqiang, REN Xiaokun, SHI Hongping, et al. Latest development and special features of the technology for comprehensive utilization of coke oven gas[J]. Coal Processing and Comprehensive Utilization, 2009, (2): 34-37.)
[12] RYCKEBOSCH E, DROUILLON M, VERUAEREN H. Techniques for transformation of biogas to biomethane[J]. Biomass and Bioenergy, 2011, 35(5): 1633-1645.
[13] 刘广民,任南琪, 王爱杰,等. 产酸-硫酸盐还原系统中的产酸菌的发酵类型及其与SRB的协同作用[J]. 环境科学学报,2004,24(5):782-788.(LIU Guangmin, REN Nanqi, WANG Aijie, et al. The fermentation type of acidogenic bacteria and their cooperation with SRB in an acidogenic sulfate-reducing reactor[J]. Acta Scientiae Circumstantiate, 2004, 24(5): 782-788.)
[14] 何厚波,郑金伟, 金彤,等. 生物滤池工艺处理污水厂恶臭气体[J]. 环境科学与技术,2006,29(6):86-88.(HE Houbo, ZHENG Jinwei, JIN Tong, et al. Bio-filtration technology for removing odor from a wastewater treatment plant[J]. Environmental Science & Technology, 2006, 29(6): 86-88.)
[15] 杨婷婷,熊运涛, 崔荣华,等. 天然气湿法脱硫技术研究进展[J]. 天然气与石油,2013,31(2):40-42.(YANG Tingting, XIONG Yuntao, CUI Ronghua, et al. Progress in study of natural gas wet desulfurization technology[J]. Natural Gas and Oil, 2013, 31(2): 40-42.)
[16] 王青宁,韩维亮, 蒋金龙,等. 脱除硫化氢的凹凸棒石基纳米氧化锌脱硫剂的实验研究[J]. 石油学报(石油加工),2012,28(5):757-763.(WANG Qingning, HAN Weiliang, JIANG Jinlong, et al. Experimental study on nano-zinc oxide desulfurizer with attapulgite as support for H2S removal[J]. Acta Petrolei Sinica (Petroleum Processing Section), 2012, 28(5): 757-763.)
[17] 李劲,雷萌, 唐浠. 对中低含硫天然气脱硫技术的认识[J]. 石油与天然气化工,2013,42(3):227-233.(LI Jin, LEI Meng, TANG Xi. Understanding of desulfurization technologies for medium and low H2S-bearing natural gas[J]. Chemical Engineering of Oil and Gas, 2013, 42(3): 227-233.)
[18] 李澜,赵秋萍, 陈俊伊,等. 负载氧化铁凹凸棒石脱硫剂的制备及再生工艺[J]. 石油学报(石油加工)2013,29(3):487-493.(LI Lan, ZHAO Qiuping, CHEN Junyi, et al. Preparation of iron oxide supported attapulgite desulfurizer and its regeneration process[J]. Acta Petrolei Sinica (Petroleum Processing Section), 2012, 29(3):487-493.)
[19] 张冬云,薛敏华, 王孝英,等. 栲胶-NTA络合铁体系的脱硫研究[J]. 天然气化工:C1化学与化工,2005,30(4):39-42.(ZHANG Dongyun, XUE Minhua, WANG Xiaoying, et al. Study on desulfurization in the toes-NTA chelated iron system[J]. Natural Gas Chemical Industry: C1 Chemistry and Chemical Engineering, 2005, 30(4): 39-42.)
[20] 尚海茹,刘有智, 于永. 络合铁法脱除硫化氢技术的发展[J]. 天然气化工:C1化学与化工,2010,35(1):71-75.(SHANG Hairu, LIU Youzhi, YU Yong. Development of chelated iron processes for H2S removal from gases[J]. Natural Gas Chemical Industry: C1 Chemistry and Chemical Engineering, 2010, 35(1): 71-75.)
[21] JENSEN F, KRISTIANSEN F J A,黄新. 用于低含硫气体处理的托普索WSA工艺[J]. 硫酸工业,2005,(4):1-6.(JENSEN F, KRISTIANSEN F J A, HUANG Xin. The Topsφe WSA process for lean sulfurous gases[J]. Sulfuric Acid Industry, 2005, (4): 1-6.)
[22] 刘健,张述伟,孙道青. 低温甲醇法净化天然气工艺流程的研究[J]. 天然气化工:C1化学与化工,2007,32(5):47-50.(LIU Jian, ZHANG Shuwei, SUN Daoqing. The Rectisol process for natural gas purification[J]. Natural Gas Chemical Industry: C1 Chemistry and Chemical Engineering, 2007, 32(5): 47-50.)
[23] 常宏岗,王荫砃. 胺法脱硫、硫磺回收工艺现状及发展[J]. 石油与天然气化工,2002,31(增刊):33-36.(CHANG Honggang, WANG Yindan. Present situation and development trends on amine desulfurization and sulfur recovery technologies[J]. Chemical Engineering of Oil and Gas, 2002, 31(Suppl): 33-36.)
[24] 高涵,郭亚平, 褚联峰,等. 醇胺法吸收二氧化碳在填料塔中的应用[J]. 过程工程学报,2010,10(6):1091-1097.(GAO Han, GUO Yaping, CHU Lianfeng, et al. Absorption of carbon dioxide into aqueous solutions of alkanolamines in a packed column[J]. The Chinese Journal of Process Engineering, 2010, 10(6): 1091-1097.)
[25] 于永,刘有智, 祁贵生,等. 超重力旋转填料床中络合铁法选择性脱除酸气中H2S[J]. 石油学报(石油加工), 2014,30(1):60-65.(YU Yong, LIU Youzhi, QI Guisheng, et al. Selective removal of H2S from acid gas with chelated iron method in a rotating packed bed[J]. Acta Petrolei Sinica (Petroleum Processing Section), 2014, 30(1): 60-65.)
[26] 祁贵生,刘有智, 潘红霞,等. 错流旋转填料床中湿式氧化法脱除气体中硫化氢[J]. 石油学报(石油加工),2012,28(2):195-199.(QI Guisheng, LIU Youzhi, PAN Hongxia, et al. Hydrogen sulfide removal by wet oxidation method in a cross-flow rotating packed bed[J]. Acta Petrolei Sinica (Petroleum Processing Section), 2012, 28(2): 195-199.)
[27] 罗莹,朱振峰, 刘有智. 络合铁法脱H2S技术研究进展[J]. 天然气化工:C1化学与化工,2014,39(1):88-94.(LUO Ying, ZHU Zhenfeng, LIU Youzhi. Research progress in technologies for removal of H2S with iron chelate solutions[J]. Natural Gas Chemical Industry: C1 Chemistry and Chemical Engineering, 2014, 39(1): 88-94.)
[28] ELSHAHED M S, SENKO J M, NAJAR F Z, et al. Bacterial diversity and sulfur cycling in a mesophilic sulfide-rich spring[J]. Applied and Environmental Microbiology, 2003, 69(9): 5609-5621.
[29] JORGENSEN B B, POSTGATE J R. Ecology of the bacteria of the sulphur cycle with special reference to anoxic-oxic interface environments[J]. Philosophical Transactions of the Royal Society of London B, 1982, 298(1093): 543-561.
[30] PASTERIS J D, FREEMAN J J, GOFFREDI S K, et al. Raman spectroscopic and laser scanning confocal microscopic analysis of sulfur in living sulfur-precipitating marine bacteria[J]. Chemical Geology, 2001, 180(1-4): 3-18.
[31] SIPMA J, SVITELSKAYA A, VAN DER MARK B, et al. Potentials of biological oxidation processes for the treatment of spent sulfidic caustics containing thiols[J]. Water Research, 2004, 38(20): 4331-4340.
[32] KIM J Y, KIM B W. Removal of dimethyl sulfide in ceramic biofilters immobilized withThiobacillusthioparusTK-m[J].Journal of Microbiology and Biotechnology, 2003, 13(6): 866-871.
[33] DE BOK F A M, VAN LEERDAM R C, SMIDT H, et al. Degradation of methanethiol by methylotrophic methanogenic archaea in a lab-scale upflow anaerobic sludge blanket reactor[J]. Applied and Environmental Microbiology, 2006, 72(12): 7540-7547.
[34] FISCHER H, SCHULZEKLOFF G, WOHRLE D. Oxidation of aqueous sulfide solutions by dioxygen 1 Autoxidation reaction[J]. Chemical Engineering & Technology, 1997, 20(7): 462-468.
[35] OBA Y, POULSON S R. Oxygen isotope fractionation of dissolved oxygen during a biological reduction by aqueous sulfide[J]. Chemical Geology, 2009, 268(3-4): 226-232.
[36] KLEINJAN W E, DE KEIZER A, JANSSEN A J H. Kinetics of the chemical oxidation of polysulfide anions in aqueous solution[J]. Water Research, 2005, 39(17): 4093-4100.
[37] NIELSEN A H, VOLLERTSEN J, HVITVED-JACOBSEN T. Determination of kinetics and stoichiometry of chemical sulfide oxidation in wastewater of sewer networks[J]. Environmental Science & Technology, 2003, 37(17): 3853-3858.
[38] NIELSEN A H, VOLLERTSEN J, JACOBSEN T H. Chemical sulfide oxidation of wastewater—Effects of pH and temperature[J]. Water Science and Technology, 2004, 50(4): 185-192.
[39] CHEN K Y, MORRIS J C. Kinetics of oxidation of aqueous sulfide by O2[J]. Environmental Science & Technology, 1972, 6(6): 529-537.
[40] OBRIEN D J, BIRKNER F B. Kinetics of oxygenation of reduced sulfur species in aqueous solution[J]. Environmental Science & Technology, 1977, 11(12): 1114-1120.
[41] KLEINJAN W E, DE KEIZER A, JANSSEN A J H. Equilibrium of the reaction between dissolved sodium sulfide and biologically produced sulfur[J]. Colloids and Surfaces B: Biointerfaces, 2005, 43(3-4): 228-237.
[42] JANSSEN A J H, LETTINGA G, DE KEIZER A. Removal of hydrogen sulphide from wastewater and waste gases by biological conversion to elemental sulphur. Colloidal and interfacial aspects of biologically produced[J]. Colloids and Surfaces a-Physicochemical and Engineering Aspects, 1999, 151(1-2): 389-397.
[43] 贡俊,张肇铭. 脱氮硫杆菌氧化硫化氢过程中的生物氧化和化学氧化[J]. 环境科学学报,2006,26(3):477-482.(GONG Jun, ZHANG Zhaoming. Biological and chemical oxidation during oxidation of hydrogen sulfide byThiobacillusdenitrificans[J]. Acta Scientiae Circumstantiate, 2006, 26(3): 477-482.)
[44] 叶姜瑜,沈秀红, 王琳,等. Bio-SR工艺去除硫化氢气体的研究[J]. 环境工程学报,2012,6(2):584-588.(YE Jiangyu, SHEN Xiuhong, WANG Lin, et al. Research on H2S removal by Bio-SR process[J]. Chinese Journal of Environmental Engineering, 2012, 6(2): 584-588.)
[45] TIAN S L, ZHANG L H, WANG Q H, et al. Study on the Bio-SR process for natural gas desulfurization[J]. Natural Gas Chemical Industry, 2008, 33(1): 43-46.
[46] SOROKIN D Y, DE JONG G A H, ROBERTSON L A, et al. Purification and characterization of sulfide dehydrogenase from alkaliphilic chemolithoautotrophic sulfur-oxidizing bacteria[J]. FEBS Letter, 1998, 427(1): 11-14.
[47] MUYZER G, SOROKIN D Y, MAVROMATIS K, et al. Complete genome sequence of “Thioalkalivibriosulfidophilus” HL-EbGr7[J]. Standards in Genomic Sciences,2011, 4(1): 23-35.
[48] BAMFORD V A, BRUNO S, RASMUSSEN T, et al. Structural basis for the oxidation of thiosulfate by a sulfur cycle enzyme[J]. The EMBO Journal, 2002, 21(21): 5599-5610.
[49] SAKURAI H, OGAWA T, SHIGA M, et al. Inorganic sulfur oxidizing system in green sulfur bacteria[J]. Photosynthesis Research, 2010, 104(2-3): 163-176.
[50] BRITO J A, SOUSA F L, STELTER M, et al. Structural and functional insights into sulfide: quinone oxidoreductase[J]. Biochemistry, 2009, 48(24): 5613-5622.
[51] VALDÉS J, PEDROSO I, QUATRINI R, et al.Acidithiobacillusferrooxidansmetabolism: From genome sequence to industrial applications[J]. BMC Genomics, 2008, 9: 597-620.
[52] FOTI M, MA S, SOROKIN D Y, et al. Genetic diversity and biogeography of haloalkaliphilic sulphur-oxidizing bacteria belonging to the genusThioalkalivibrio[J]. FEMS Microbiology Ecology, 2006, 56(1): 95-101.
[53] JOHANNES B M K, DE GRAAFF M, VAN DEN BOSCH P L F, et al. A physiologically based kinetic model for bacterial sulfide oxidation[J]. Water Research,2013, 47(2): 483-492.
[54] JOHANNES B M K, VAN DEN BOSCH P L F, BUISMAN C J N S, et al. Pathways of sulfide oxidation by haloalkaliphilic bacteria in limited-oxygen gas lift bioreactors[J]. Environmental Science & Technology, 2012, 46(14): 7581-7586.
[55] STEUDEL R. Aqueous sulfur sols[J]. Topics in Current Chemistry, 2003, 230: 153-166.
[56] ZHANG K Q, HUANG W X, JI M, et al. Characteristics of microbiologically sulfur producing during biological treatment for wastewater containing sulfide[J]. Journal of Agro-Environment Science, 2006, 25(2): 522-526.
[57] JANSSEN A J H, MA S C, LENS P, et al. Performance of a sulfide-oxidizing expanded bed reactor supplied with dissolved oxygen[J]. Biotechnology and Bioengineering, 1997, 53(1): 32-40.
[58] PRANGE A, CHAUVISTRE R, MODROW H, et al. Quantitative speciation of sulfur in bacterial sulfur globules: X-ray absorption spectroscopy reveals at least three different species of sulfur[J].Microbiology-SGM, 2002, 148(1): 267-276.
[59] STEUDEL R, STEUDEL Y. Polysulfide chemistry in sodiumsulfur batteries and related systems a computational study by G3X(MP2) and PCM calculations[J]. Chemistry-A European Journal, 2013, 19(9): 3162-3176.
[60] PICKERING I J, GEORGE G N, YU E Y, et al. Analysis of sulfur biochemistry of sulfur bacteria using X-ray absorption spectroscopy[J]. Biochemistry, 2001, 40(27): 8138-8145.
[61] TAKEUCHI T L, SUZUKI I. Cell hydrophobicity and sulfur adhesion ofThiobacillusthiooxidans[J]. Applied and Environmental Microbiology, 1997, 63(5): 2058-2061.
[62] ZHANG C G, XIA J L, DING J N, et al. Cellular acclimation ofAcidithiobacillusferrooxidansto sulfur biooxidation[J]. Minerals & Metallurgical Processing, 2009, 26(1): 30-34.
[63] HE H, XIA J L, HUANG G H, et al. Analysis of the elemental sulfur bio-oxidation byAcidithiobacillusferrooxidanswith sulfur K-edge XANES[J]. World Journal of Microbiology & Biotechnology, 2011, 27(8): 1927-1931.
[64] HE H, ZHANG C G, XIA J L, et al. Investigation of elemental sulfur speciation transformation mediated byAcidithiobacillusferrooxidans[J]. Current Microbiology, 2009, 58(4): 300-307.
[65] 董晓莹,赵勇, 寇巍,等. 一种缺氧型生物滴滤塔对硫化氢去除的最佳反应条件[J]. 环境工程学报,2012,6(7):2373-2377.(DONG Xiaoying, ZHAO Yong, KOU Wei, et al. Optimal operating conditions for H2S removal by an anoxic bio-trickling reactor[J]. Chinese Journal of Environmental Engineering, 2012, 6(7): 2373-2377.)
[66] 徐潇文,王爱杰, 任南琪,等. 改进型生物滴滤塔处理H2S臭气的最适工艺条件研究[J]. 环境污染治理技术与设备,2006,7(2):45-49.(XU Xiaowen, WANG Aijie, REN Nanqi, et al. The optimal operating conditions for H2S removal in an improved bio-trickling reactor[J]. Techniques and Equipment for Environmental Pollution Control, 2006, 7(2): 45-49.)
[67] FORTUNY M, BAEZA J A, GAMISANS X, et al. Biological sweetening of energy gases mimics in biotrickling filters[J]. Chemosphere, 2008, 71(1): 10-17.
[68] 姜安玺,杨义飞, 王晓辉,等. 人工筛选菌脱除H2S恶臭气体的实验研究[J]. 中国环境科学,2002,22(4):313-315.(JIANG Anxi, YANG Yifei, WANG Xiaohui, et al. The experimental study on the stenchful gas H2S removal by screening bacteria[J]. Chinese Environmental Science, 2002, 22(4): 313-315.)
[69] 张兰河,谢维民, 汪群慧,等. 高效硫氧化菌的筛选及其应用[J]. 哈尔滨工业大学学报,2007,39(4):566-570.(ZHANG Lanhe, XIE Weimin, WANG Qunhui, et al. Isolation and application of high efficient sulfur-oxidizing bacteria[J]. Journal of Harbin Institute of Technology, 2007, 39(4): 566-570.)
[70] 伍永钢,任洪强, 丁丽丽,等. 新型聚乙烯填料生物滴滤床净化硫化氢气体的启动研究[J]. 环境科学,2006,27(12):2396-2400.(WU Yonggang, REN Hongqiang, DING Lili, et al. Study on the start-up of an innovative polyethylene carrier biotrickling filter treating waste gas containing hydrogen sulfide[J]. Chinese Journal of Environmental Science, 2006, 27(12): 2396-2400.)
[71] CHUNG Y C, LIN Y Y, TSENG C P. Removal of high concentration of NH3and coexistent H2S by biological activated carbon (BAC) biotrickling filter[J].Bioresource Technology, 2005, 96(16): 1812-1820.
[72] 徐桂芹,姜安玺, 张英民,等. 假单孢菌固定化除硫化氢臭气的试验研究[J]. 给水排水,2005,31(2):41-43.(XU Guiqin, JIANG Anxi, ZHANG Yingmin, et al. Experimental study on removal of hydrogen sulfide odor by immobilizedPseudomonassp.[J]. Water and Wastewater Engineering, 2005, 31(2): 41-43.)
[73] 杨虹,宫磊, 徐晓军. 生物催化氧化法脱除H2S的试验研究[J]. 环境工程学报,2007,1(2):94-97.(YANG Hong, GONG Lei, XU Xiaojun. An experimental study on H2S removal by bio-catalytic oxidation[J]. Chinese Journal of Environmental Engineering, 2007, 1(2): 94-97.)
[74] 郑辉杰,陈洵, 邸进申. 固定床生物反应器中氧化亚铁硫杆菌氧化Fe2+的研究[J]. 石油化工,2008,37(6):628-632.(ZHENG Huijie, CHEN Xun, DI Jinshen. Oxidation of Fe2+by immobilizedThiobacillusferrooxidans in packed bed bioreactor[J]. Petrochemical Technology, 2008, 37(6): 628-632.)

[76] VISSER J M, STEFESS G C, ROBERTSON L A, et al.Thiobacillussp.W5, the dominant autotroph oxidizing sulfide to sulfur in a reactor for aerobic treatment of sulfidic wastes[J]. Antonie Van Leeuwenhoek, 1997, 72(2): 127-134.
[77] ROOSTA A, JAHANMIRI A, MOWLA D, et al. Mathematical modeling of biological sulfide removal in a fed batch bioreactor[J]. Biochemical Engineering Journal, 2011, 58-59: 50-56.
[78] JANSSEN A J H, SLEYSTER R, VAN DER KAA C, et al. Biological sulfide oxidation in a fed-batch reactor[J]. Biotechnology and Bioengineering, 1995, 47(3): 327-333.
[79] VAN DEN BOSCH P L F, VAN BEUSEKOM O C, BUISMAN C J N, et al. Sulfide oxidation at halo-alkaline conditions in a fed-batch bioreactor[J]. Biotechnology and Bioengineering, 2007, 97(5): 1053-1063.
[80] ECKERT W. Microbially-related redox changes in a subtropical lake 2 Simulation of metalimnetic conditions in a chemostat[J]. Biogeochemistry, 1993, 21(1): 21-38.
[81] BERNER R A. Electrode studies of hydrogen sulfide in marine sediments[J]. Geochimica et Cosmochimica Acta, 1963, 27(6): 563-575.
[82] JANSSEN A J H, MEIJER S, BONTSEMA J, et al. Application of the redox potential for controlling a sulfide oxidizing bioreactor[J]. Biotechnology and Bioengineering, 1998, 60(2): 147-155.
[85] MA Y L, YANG B L, ZHAO J L. Removal of H2S byThiobacillusdenitrificansimmobilized on different matrices[J]. Bioresource Technology, 2006, 97(16): 2041-2046.
[86] LOHWACHARIN J, ANNACHHATRE A P. Biological sulfide oxidation in an airlift bioreactor[J]. Bioresource Technology, 2010, 101(7): 2114-2120.
[88] QIU G L, LI Y L, ZHAO K.Thiobacillusthioparusimmobilized by magnetic porous beads: Preparation and characteristic[J]. Enzyme and Microbial Technology, 2006, 39(4): 770-777.
[89] KRISHNAKUMAR B, MAJUMDAR S, MANILAL V B, et al. Treatment of sulfide containing wastewater with sulfur recovery in a novel reverse fluidized loop reactor (RFLR)[J]. Water Research, 2005, 39(4): 639-647.
[90] SONG Z Y, LI Q, WANG D, ZHANG J, et al. A novel up-flow inner-cycle anoxic bioreactor (UIAB) system for the treatment of sulfide wastewater from purification of biogas[J]. Water Science and Technology, 2012, 65(6): 1033-1040.
Advances in Researches of Gas Bio-Desulfurization and Sulfur Recovery
SONG Ziyu1,WU Dan1,DONG Jian3,ZHANG Jian3,LI Qingfang3,XING Jianmin1,LIU Huizhou2
(1.NationalKeyLaboratoryofBiochemicalEngineering,InstituteofProcessEngineering,ChineseAcademyofSciences,Beijing100190,China; 2.KeyLaboratoryofGreenProcessandEngineering,CAS,InstituteofProcessEngineering,ChineseAcademyofSciences,Beijing100190,China; 3.PetroleumEngineeringCorporation,SINOPEC,Dongying257026,China)
Hydrogen sulfide removal is the major task of clean and safe production in the field of petroleum and nature gas exploitation, refining, coal chemical industry and water treatment. Gas bio-desulfurization and sulfur recovery technique was a method of wet desulfurization based on the sulfide bio-oxidation, which has many advantages, such as biocatalyst reactivation and sulfur unblock. The method and application of hydrogen sulfide desulfurization were studied, emphatically, the research progress in the mechanism of gas bio-desulfurization and sulfur recovery was introduced, and its advantages and characteristics were analyzed and summarized. Finally, its future development direction was suggested in the light of the shortcoming of current research.
gas biodesulfurization; sulfide oxidizing bacteria; hydrogen sulfide; sulfur recovery; sulfide bio-oxidation
2014-10-31
国家自然科学基金项目(21207060和31370078)和国家高技术研究发展计划“863”项目(2011AA060904)资助 第一作者: 宋子煜,男,工程师,博士,从事气体生物脱硫及硫回收过程工艺方面的研究
邢建民,男,研究员,博士,从事生物催化及代谢工程方面的研究;E-mail:jmxing@ipe.ac.cn;刘会洲,男,研究员,博士,从事生化分离科学与工程应用基础研究;E-mail:hzliu@ipe.ac.cn
1001-8719(2015)02-0265-10
Q819
A
10.3969/j.issn.1001-8719.2015.02.007

