系统性红斑狼疮患者外周血CXCL9表达水平及其临床意义
叶筱燕,戴永江,蒙秉新,王远志,梁雄安
(1.海南省人民医院皮肤科,海口 570102;2.海南医学院附属医院皮肤科,海口 570311)
论著·临床研究
系统性红斑狼疮患者外周血CXCL9表达水平及其临床意义
叶筱燕1,戴永江2△,蒙秉新1,王远志1,梁雄安2
(1.海南省人民医院皮肤科,海口 570102;2.海南医学院附属医院皮肤科,海口 570311)
目的 检测系统性红斑狼疮(SLE)患者外周血中CXCL9表达水平并探讨其临床意义。方法 采用ELISA法检测20例SLE患者(试验组)和20例健康对照者(对照组)外周血CXCL9表达水平。比较CXCL9在两组血清中表达的差异,分析CXCL9与SLE患者年龄、病程及SLE病情活动指数(SLEDAI)的相关性。结果 试验组和对照组外周血CXCL9水平分别为(1 549.14±362.74)pg/L和(602.54±83.70)pg/L。经统计学分析,试验组外周血CXCL9水平明显高于对照组,差异有统计学意义(P<0.01);试验组外周血CXCL9水平与SLEDAI评分呈正相关(r=0.892,P<0.01)。结论 CXCL9可能参与了SLE的发病过程。
红斑狼疮,系统性:趋化因子CXCL9;外周血
系统性红斑狼疮(systemic lupus erythematosus,SLE)是一种累及多系统、器官组织的自身免疫性疾病,其发病机制十分复杂,目前尚未完全明确。近年来有关T淋巴细胞异常的免疫反应对SLE的诱导和维持作用得到了公认,其典型表现为自身T细胞活化,导致血清中出现大量的自身抗体,免疫稳态遭到破坏,提示细胞因子对自身反应性T细胞的活化、效应性细胞因子的产生在SLE的发生、发展过程中可能起着重要的作用[1-2]。趋化因子9(C-X-C motif 9,CXCL9)属于趋化因子CXC家族的成员,其对T细胞及单核细胞具有诱导和趋化作用,CXCL9与CXCL10、CXCL11等趋化因子有共同的受体CRCX3。已有文献指出SLE患者外周血单一核细胞CXCR3 mRNA呈现高表达,可能参与了SLE的发病过程[3],因此推测CXCL9可能与SLE发病相关。本研究通过探讨SLE患者血清中CXCL9表达水平及其与SLE疾病活动指数(SLEDAI)的相关性,为进一步探讨SLE的发病机制提供依据。
1 资料与方法
1.1 一般资料 2011年10月至2012年9月海南省人民医院和海南医学院附属医院就诊的20例SLE患者为试验组,年龄16~52岁,平均(29.90±10.24)岁。病程约3个月至10年,平均(2.91±2.84)年。诊断标准依据1997年美国风湿病学会修订的SLE诊断标准。排除免疫性疾病、恶性肿瘤、并发肝肾功能不全、慢性炎症性疾病患者;排除近1个月内使用过免疫抑制剂或细胞毒性药物的患者。抽取同期在本院门诊体检的健康人员20例为对照组,均为女性,年龄25~48岁,平均(34.35±6.65) 岁。实验组与对照组的年龄具有可比性。所有患者及健康对照者均知情同意。
1.2 方法
1.2.1 标本采集 血清采集:SLE患者确诊后,未给予治疗,于次日凌晨8:00空腹抽取静脉血5 mL,即刻离心收集血清,吸取上清液,液氮-70 ℃冷冻保存,相同方法收集对照组血清。
1.2.2 主要试剂 CXCL9鼠抗人单克隆抗体ELISA检测试剂盒,购自R&D System。Elx800型酶标检测仪为美国BIO-TEK公司产品。
1.2.3 检测方法 采用ELISA法检测血清CXCL9含量,严格按照试剂盒说明书及相关实验步骤进行操作。
1.2.4 SLEDAI的测量 采用SLEDAI-2000评价SLE患者病情活动度。SLEDAI-2000是由原SLEDAI改进而来,主要变化表现在蛋白尿、皮疹、脱发、黏膜溃疡4项的定义。SLEDAI-2000不再要求上述病变必须是新发或复发,持续存在的病变同样可以计分,因此可以更好地体现SLE病情活动度[4-5]。为保证数据的客观性,本次SLEDAI评分由一名副主任医师执行。
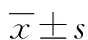
2 结果
2.1 SLEDAI评分 SLE患者SLEDAI评分4~16分,平均(7.40±2.84)分。1~4分为稳定期,≥5分为活动期。根据评分结果判定,20例SLE患者中,19例为活动期,1例为稳定期。
2.2 对照组与试验组外周血中CXCL9水平的比较 对照组的血清CXCL9值为(602.54±83.70)pg/L,试验组为(1 549.14±362.74)pg/L,结果显示试验组血清CXCL9表达水平明显高于对照组(图1)。经t′检验,两者差异有统计学意义(P<0.01)。
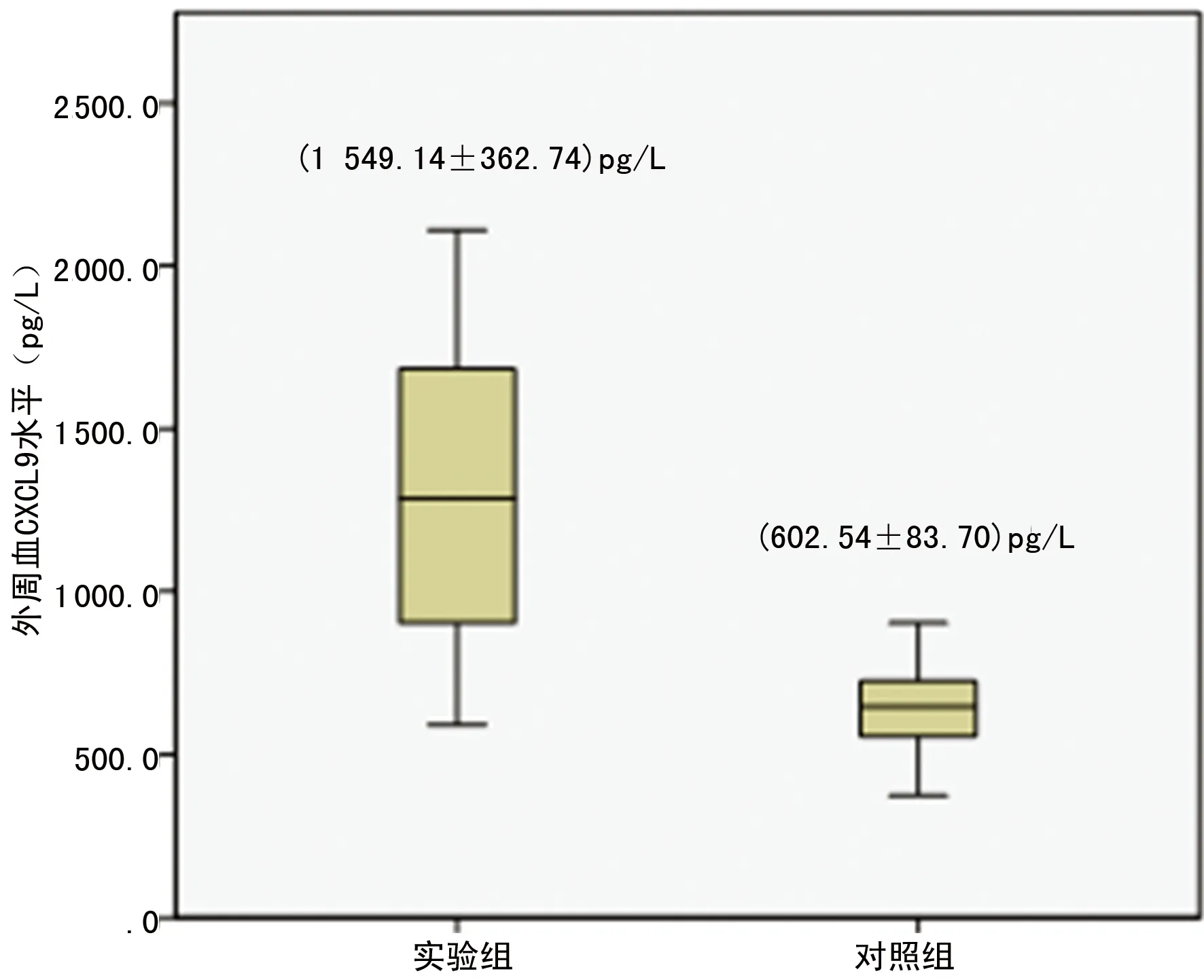
图1 两组外周血CXCL9水平的比较
2.3 SLE患者外周血CXCL9水平与SLEDAI的相关分析 采用Spearman等级相关检验SLE患者外周血CXCL9水平与SLEDAI评分的相关性,显示CXCL9在SLE患者外周血的水平与SLEDAI评分呈正相关(r=0.892,P<0.01),见图2。
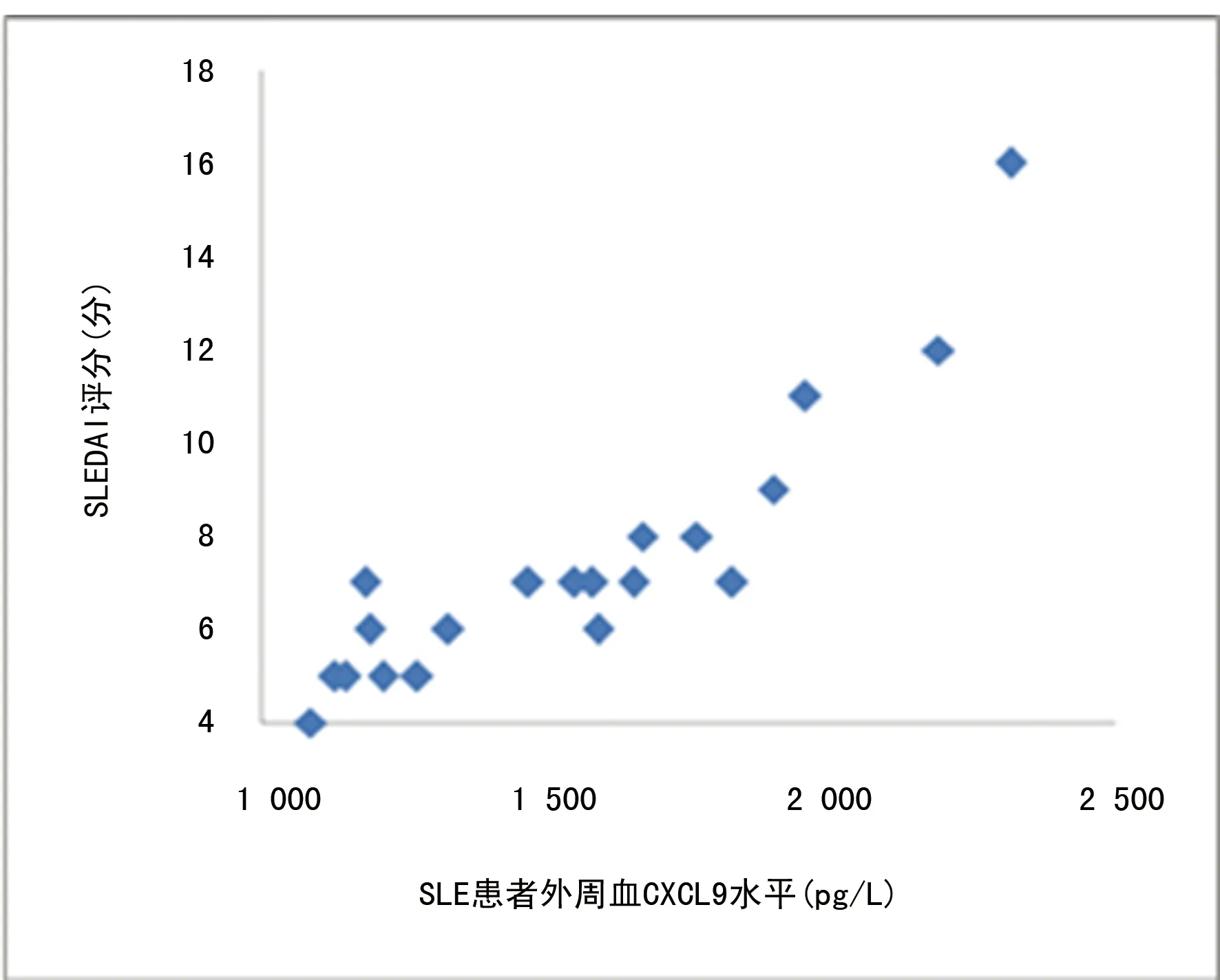
图2 SLE患者外周血CXCL9水平与SLEDAI的相关性
2.4 SLE患者外周血CXCL9水平与年龄、病程的相关性分析 见表1。

表1 SLE患者外周血CXCL9与年龄、病程的相关性分析
采用Spearman等级相关分析,结果显示,SLE患者外周血CXCL9水平与年龄、病程无相关性(P>0.05)。
3 讨论
SLE是一种以大量自身抗体产生、补体激活及免疫复合物沉积为特征的自身免疫性疾病,目前病因尚不明确。近年来有研究表明,趋化因子在SLE的发生、发展过程中起重要作用[6]。趋化因子是由组织或炎性细胞产生的具有化学趋化作用的多肽,分为C、CC、CXC、CX3C 4 个亚族[7]。CXCL9属于趋化因子CXC 亚家族,CXC趋化因子亚家族根据第一个半胱氨酸前是否具ELR(谷氨酸-亮氨酸-精氨酸)功能区,可分为ELR型和非ELR型趋化因子,大部分的非ELR趋化因子是淋巴细胞的高效趋化剂[8-9]。CXCL9属于非ELR型趋化因子,其通过与效应细胞上特异性受体CXCR3的结合,活化各类白细胞并趋化至病灶处,在机体的免疫防御中发挥作用。目前已证实,CXCL9在许多疾病中起重要作用,包括外部感染、自体免疫性疾病、移植排斥、肿瘤治疗等[10-12]。本试验中,作者观察到SLE患者外周血中CXCL9的表达明显高于健康对照组,提示在SLE发病过程中,机体在损伤因子刺激下,大量分泌趋化因子CXCL9,使效应性T淋巴细胞大量定向迁移,从而启动了与自身免疫有关的病变。同时,CXCL9在SLE患者外周血中的水平与SLEDAI评分呈显著正相关(r=0.892,P<0.01),也证实了CXCL9在SLE患者发病中具有重要作用。
本次试验由于稳定期SLE患者例数较少,因此无法对CXCL9在活动期SLE患者和稳定期SLE患者外周血中的水平作一比较,有待于在后续研究中继续探讨。尽管目前对CXCL9导致SLE的确切发病机制尚不明确,但本试验结果提示CXCL9在SLE的发病过程中起着关键性作用,有待于更深入透彻的研究。另外,探讨CXCL9在SLE中的作用机制,可能有助于SLE患者的治疗。
[1]Al-Majdoub M,Koy C,Lorenz P,et al.Mass spectrometric and peptide chip characterization of an assembled epitope:analysis of a polyclonal antibody model serum directed against the Sjgren/systemic lupus erythematosus autoantigen TRIM21[J].J Mass Spectrom,2013,48(6):651-659.
[2]Nili F,McLeod L,O′Connell C,et al.Maternal and neonatal outcomes in pregnancies complicated by systemic lupus erythematosus:a population-based study[J].J Obstet Gynaecol Can,2013,35(4):323-328.
[3]BjorkanderS,Heidari-HamedaniG,BremmeK,etal.PeripheralmonocyteexpressionofthechemokinereceptorsCCR2,CCR5andCXCR3isalteredatparturition in healthy women and in women with systemic lupus erythematosus[J].Scand J Immunol,2013,77(3):200-212.
[4]洁清,姜红.SLEDAI-2000与BILAG-2004两种评分系统评估狼疮性肾炎患儿肾脏活动度的可行性研究[J].中国当代儿科杂志,2012,14(10):775-779.
[5]程颖,魏殿军,姜琛.系统性红斑狼疮SLEDAI评分与血液学异常相关性研究[J].医学研究杂志,2011,11(2):114-117.
[6]夏羽佳,田德安,曾丹,等.CXCL9对单个核细胞的趋化作用及其机制探讨[J].中国组织化学与细胞化学杂志,2012,21(4):321-324.
[7]张丽娟.大鼠肺缺血再灌注损伤时CXCL9及FKN的表达[J].山西医科大学学报,2011,20(2):201-202.
[8]陈泉芳.趋化因子CXCL-9、CXCL-10在胸腔积液中的水平及意义[D].南宁:广西医科大学,2009.
[9]Pranzatelli MR,Tate ED,McGee NR,et al.Expression of CXCR3 and its ligands CXCL9,-10 and-11 in paediatric opsoclonus-myoclonus syndrome[J].Clin Exp Immunol,2013,172(3):427-436.
[10]朱庆超,韩晓东,金志明,等.趋化因子CXCL9在结直肠癌组织中的表达及意义[J].中国现代普通外科进展,2011,20(5):350-354.
[11]刘海莉,张野,于海涛,等.慢性丙型肝炎患者血清趋化因子CXCL9和CXCL11的检测及其临床意义[J].胃肠病学和肝病学杂志,2011,20(12):1134-1136.
[12]Zainodini N,Hassanshahi G,Arababadi MK.Differential expression of CXCL1,CXCL9,CXCL10 and CXCL12 chemokines in alopecia areata[J].Iran J Immunol,2013,10(1):40-46.
Clinical significance of CXCL9 expression in peripheral blood of patients with systemic lupus erythematosus
YeXiaoyan1,DaiYongjiang2△,MengBingxin1,Wangyuanzhi1,LiangXiong′an2
(1.DepartmentofDermatology,HainanPeople′sHospital,Haikou,Hainan570102,China;2.DepartmentofDermatology,theAffiliatedHospitalofHainanMedicalCollege,Haikou,Hainan570311,China)
Objective To investigate the expression and significance of CXCL9 in systemic lupus erythematosus (SLE).Methods The level of CXCL9 in peripheral blood from 20 patients with SLE and 20 normal controls were measured by enzyme linked immunosorbent assay.Compare the difference of the expression level of CXCL9 in peripheral blood between two groups and analyzed their correlation with ages,duration,SLE diseases activity index(SLEDAI).Results The level of CXCL9 in peripheral blood in patients with systemic lupus erythematosus was(1 549.14±362.74)pg/L,but in normal controls was(602.54±83.70)pg/L.The level of CXCL9 in peripheral blood in patients with systemic lupus erythematosus was obviously higher than that in controls by statistical analysis,there was significant difference between the two groups (P<0.01).The expression level of CXCL9 in peripheral blood of patients with systemic lupus erythematosus was positively correlated with SLEDAI (r=0.892,P<0.01).Conclusion CXCL9 may be involved in the pathogenesis of systemic lupus erythematosus.
lupus erythematosus,systemic;chemokine;CXCL9;peripheral blood
叶筱燕(1965-),副主任医师,主要从事变态反应相关疾病研究。△
,E-mail:13976909016@163.com。
10.3969/j.issn.1671-8348.2015.05.027
R593.241
A
1671-8348(2015)05-0655-02
2014-10-20
2014-12-10)

