多成分综合优化透骨消痛胶囊的提取工艺
范哲贤 胡悦 肖晓金 刘献祥 李孝栋

【摘 要】目的:对透骨消痛胶囊的提取工艺进行研究,筛选出最佳的工业化提取工艺。方法:采用
L9(34)正交表,以浸膏率、阿魏酸、水晶兰苷、芍药苷含量为指标,以乙醇浓度、固液比、提取次数、提取时间为考察因素,优选川芎的提取工艺以及巴戟天和白芍两药材合并的提取工艺,并通过二者最终优化工艺的验证结果与改良工艺试验结果的综合比较,确定适合工业化生产的最佳提取工艺。结果:改良工艺后,指标成分含量变化较小,提取次数与乙醇浓度减少,总浸膏得率降低。因此,综合优化的提取工艺是3药材合并,用10倍质量分数为30%的乙醇加热回流提取2次,每次1.5 h。结论:综合优化的提取工艺合理、可行,适用于透骨消痛胶囊的工业生产。
【关键词】 透骨消痛胶囊;正交设计;提取工艺;综合优化
doi:10.3969/j.issn.2095-4174.2015.09.009
To Comprehensively Optimize the Extraction Process for Tougu Xiaotong Capsule(透骨消痛胶囊)
FAN Zhe-xian,HU Yue,XIAO Xiao-jin,LIU Xian-xiang,LI Xiao-dong
【ABSTRACT】 Objective:To study the optimized extraction process for Tougu Xiaotong Capsule(透骨
消痛胶囊).Methods:Using L9(34) orthogonal table,regarding the extract rate and the contents of ferulic acid,
monotropein and paeoniflorin as the indexes,and considering ethanol concentration,solid-liquid ratio,extraction times and extraction time as investigating factors,the optimized extraction technology was established based on the optimized extraction process for Chuanxiong (Rhizoma Chanxiong) and complicated extraction technology for Bajitian (Radix Morindae Officinalis) and Baishao (Radix Paeoniae Alba).Results:After improvement of extraction process,the content of index components,extraction times and ethanol concentration decreased,and the total extract rate also decreased.Conclusion:The comprehensively optimized extraction process is reasonable,feasible,and thus suitable for the industrial production of Tougu Xiaotong Capsule.
【Keywords】Tougu Xiaotong Capsule(透骨消痛膠囊);orthogonal design;extraction process;comprehensive
optimization
透骨消痛方是福建中医药大学刘献祥教授的经验方,在此基础上研制的透骨消痛胶囊,由巴戟天、白芍、川芎和肿节风4味中药组成,具有补肾柔肝、活血祛风的作用[1-3]。巴戟天中的水晶兰苷与祛风湿作用密切相关,是巴戟天区别于本属其他植物的特征成分[4-6]。芍药苷为白芍主要有效成分之一,含量占3.3%~5.7%,具有镇静、解痉、抗炎,以及抑制血小板聚集等作用[7-8]。阿魏酸是川芎有效成分之一,含量为0.1%,具有改善血液循环、抗凝血、抑制血小板聚集,及抗菌消炎等药理作用[9-10]。
本文以浸膏率、阿魏酸、水晶兰苷、芍药苷含量为综合评价指标,采用正交试验综合优化透骨消痛方中巴戟天、白芍、川芎的提取工艺,为疗效确切、服用量少、质量稳定的透骨消痛胶囊的工艺改进奠定基础。
1 试验材料
1.1 仪 器 AR2140十万分之一电子天平(梅特勒—托利多仪器上海有限公司);SHB-Ⅲ循环水式多用真空泵(郑州长城科工贸有限公司);KQ-500DE超声波清洗器(昆山市超声仪器有限公司);LC-20AT型高效液相色谱仪(日本岛津公司);SPD-10Avp紫外可见检测器(日本岛津公司);DHG-9240型电热恒温鼓风干燥箱(上海精宏实验设备有限公司);FA2004N电子天平(上海精密科学仪器有限公司);RE-52旋转蒸发器(上海亚荣生化仪器厂);DZF-150数显小型恒温真空干燥箱(郑州长城科工贸有限公司)。
1.2 药物与试剂 巴戟天、川芎(甘肃陇西聚堂中药材实业有限公司,批号分别为20120710,20120315);白芍(江西樟树天齐堂中药饮片有限公司,批号1209009);阿魏酸、水晶兰苷、芍药苷对照品(中国药品生物制品检定所,批号分别为110773-201012,111870-201201,110736-200629);
冰醋酸(国药集团化学试剂有限公司,批号20140422);磷酸(天津市福晨化学试剂厂,批号20110922);甲醇(山东禹王实业有限公司化工分公司,色谱醇,批号20130308063);其他试剂均为分析纯。
2 方法和结果
2.1 色谱条件 色谱柱为Vision HT C18柱(4.6 mm×
250 mm,5 μm);填充剂为十八烷基键合硅胶;流速1.0 mL·min-1;进样量10 μL;(阿魏酸)流动相甲醇∶质量分数为0.5%的冰醋酸水= 28∶72,检测波长为322 nm,柱温为30 ℃;(水晶兰苷)流动相甲醇∶质量分数为0.1%的磷酸水= 5∶95,检测波长为237 nm,柱温为25 ℃;(芍药苷)流动相甲醇∶质量分数为0.1%的磷酸水=
25∶75,检测波长为232 nm,柱温为30 ℃。在以上色谱条件下,各指标的色谱峰与相邻成分达到基线分离,阴性对照液中色谱对测定无干扰。
见图1。
2.2 样品处理
2.2.1 对照品的制备 精密称取阿魏酸对照品1.80 mg于10 mL容量瓶中,加甲醇溶解并定容,制得每毫升含0.18 mg的川芎对照品溶液;精密称取水晶兰苷对照品1.98 mg于10 mL容量瓶中,加超纯水溶解并定容,制得每毫升含0.198 mg的对照品溶液;精密称取芍药苷对照品2.00 mg于
10 mL容量瓶中,加甲醇溶解并定容,制得每毫升含0.2 mg的對照品溶液。
2.2.2 供试品溶液的配制 分别称取川芎干浸膏适量,加甲醇适量,巴戟天、白芍干浸膏加质量分数为80%的甲醇适量,超声30 min溶解,并分别定容至10 mL,溶液用0.45 μm微孔滤膜滤过。
2.2.3 标准曲线的制备 分别精密吸取各对照品储备液0.5,1.0,1.5,2.0,2.5 mL于5 mL棕色容量瓶中,加甲醇(水晶兰苷加超纯水)稀释并定容至刻度,摇匀,0.45 μm微孔滤膜滤过,作为对照品溶液。按2.1项下各色谱条件进行测定,以吸收峰面积(A)对各对照品溶度(C)进行线性回归,求得阿魏酸标准曲线A = 6 365.7 C + 44 592 (r = 0.999 8),线性范围为11.9~238 mg·L-1。水晶兰苷标准曲线A =14 242 C+6 585.9(r = 0.999 9),线性范围为5.94~198 mg·L-1。芍药苷标准曲线A = 24 698 C+1 102.7 (r = 0.999 9),线性范围为5~200 mg·L-1。
2.3 正交设计
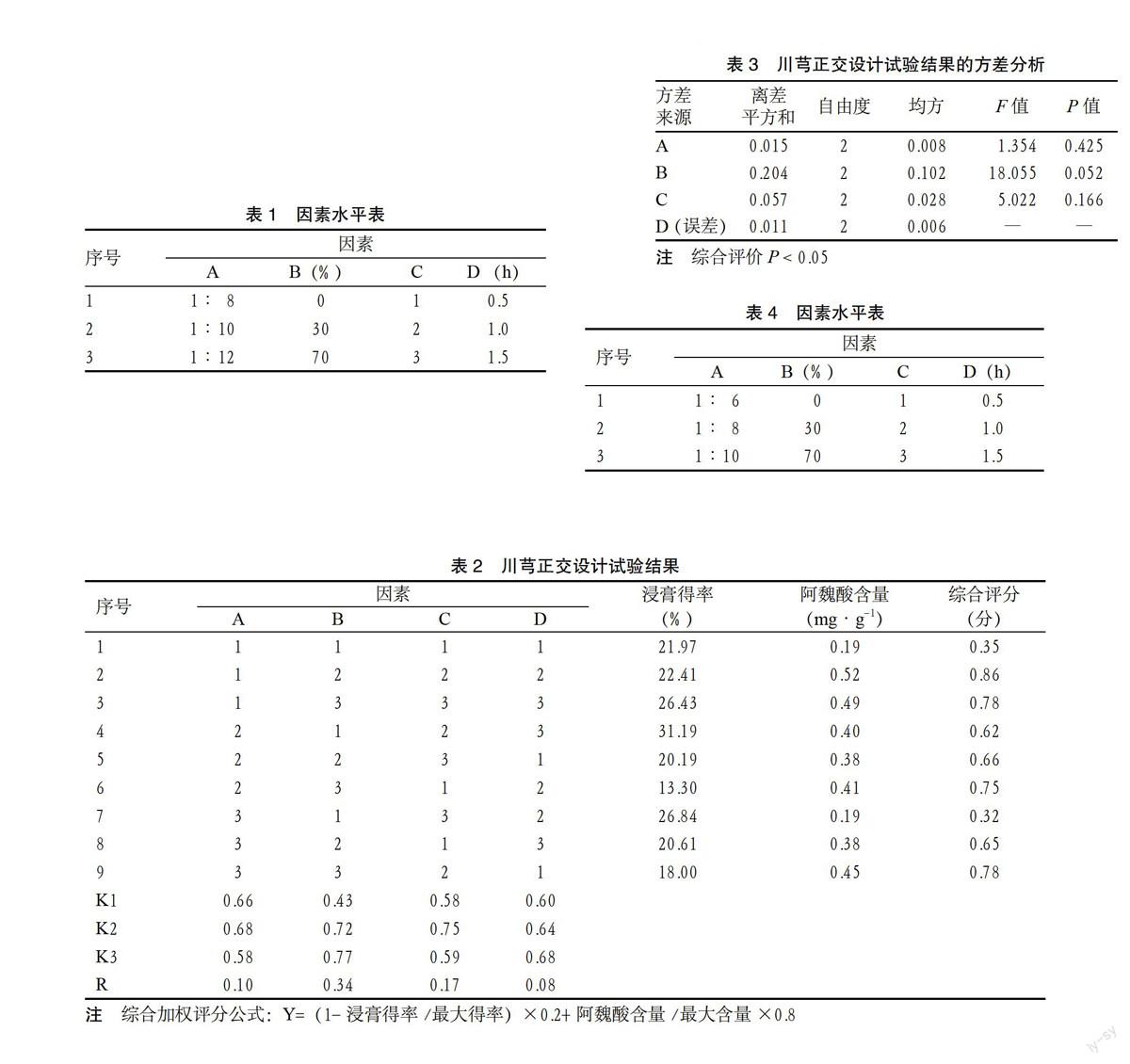
2.3.1 川芎提取工艺 采用正交试验法对川芎提取工艺进行优选,以固液比(A)、乙醇浓度(B)、提取次数(C)和提取时间(D)为考察因素,每一因素下设3个水平,以浸膏率和阿魏酸作为综合考察指标。采用正交表L9(34)进行优选,因素水平见表1。
表1 因素水平表
序号 因素
A B(%) C D (h)
1 1∶ 8 0 1 0.5
2 1∶10 30 2 1.0
3 1∶12 70 3 1.5
称取川芎共9份,每份10 g,按表2正交试验设计方法提取后,分别减压回收乙醇,置已称重的蒸发皿中,水浴浓缩至干,移入60 ℃真空干燥箱干燥3 h,取出,置常温干燥器中冷却10 min后,取出称重,计算得率。按照2.1项下的色谱条件及2.2项下的样品处理方法,分别测定9个样品的供试品溶液,结果见表2,方差分析见表3。
表3 川芎正交设计试验结果的方差分析
方差
来源 离差
平方和 自由度 均方 F值 P值
A 0.015 2 0.008 1.354 0.425
B 0.204 2 0.102 18.055 0.052
C 0.057 2 0.028 5.022 0.166
D(误差) 0.011 2 0.006 — —
注 综合评价P < 0.05
由表2可知,各因素对川芎提取因素的影响大小顺序为:B > C > A > D,由表3可知,4因素在设定的水平条件下,差异无统计学意义(P > 0.05)。结合表2极差和表3方差分析的结果,确定最佳提取工艺为A2B3C2D3,即10倍质量分数为70%的乙醇,回流2次,每次1.5 h。
2.3.2 巴戟天、白芍提取工艺 采用正交试验法对巴戟天、白芍提取工艺进行优选,以A、B、C、D为试验因素,每个因素3个水平,以浸膏率、水晶兰苷和芍药苷作为考察指标,采用正交表L9(34)进行优选,因素水平见表4。
表4 因素水平表
序号 因素
A B(%) C D(h)
1 1∶ 6 0 1 0.5
2 1∶ 8 30 2 1.0
3 1∶10 70 3 1.5
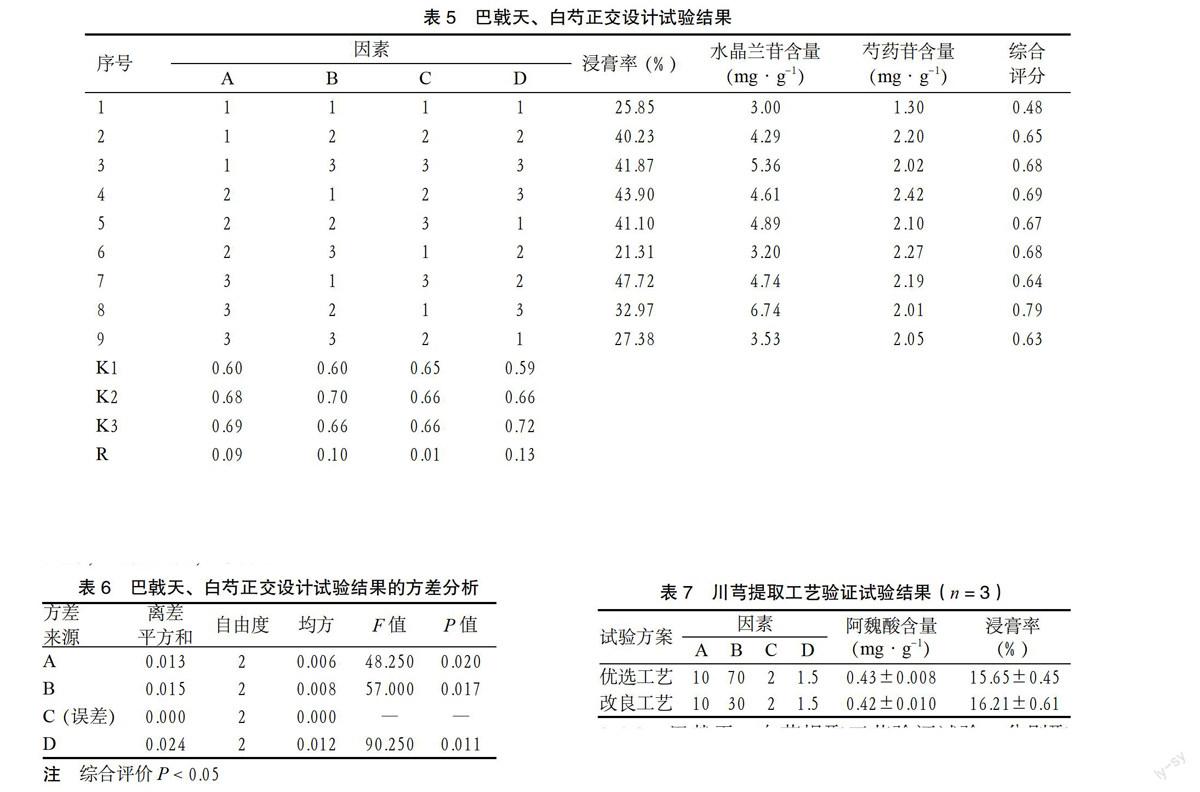
分别称取巴戟天和白芍各9份,每份10 g,按表5正交表进行试验。巴戟天和白芍按照L9(34)试验设计方法提取后,分别减压回收乙醇,置已称重的蒸发皿中,水浴浓缩至干,移入60 ℃真空干燥箱干燥3 h,取出,置常温干燥器中冷却10 min后,取出称重,计算得率。按照2.1项下的色谱条件及2.2项下的样品处理方法,分别测定9个样品的供试品溶液,结果见表5,方差分析见表6。
由表5可知,各因素对巴戟天和白芍提取因素的影响大小顺序为D > B > A > C;由表6可知A、B、D对巴戟天、白芍的提取均有显著影响(P < 0.05)。
结合表5极差和表6方差分析的结果,确定最佳提取工艺为:A3B2C3D3,即10倍质量分数为30%的乙醇,回流3次,每次1.5 h。
表6 巴戟天、白芍正交设计试验结果的方差分析
方差
来源 离差
平方和 自由度 均方 F值 P值
A 0.013 2 0.006 48.250 0.020
B 0.015 2 0.008 57.000 0.017
C(误差) 0.000 2 0.000 — —
D 0.024 2 0.012 90.250 0.011
注 综合评价P < 0.05
2.4 验证试验
2.4.1 川芎提取工艺验证试验 取川芎药材10 g,共6份。其中3份按2.3.1项下优选的工艺进行提取;另3份按改良工艺即10倍质量分数为30%的乙醇提取2次,每次1.5 h,均计算各提取方法所得干浸膏的得率及其中阿魏酸的含量。结果,
2种工艺下,各指标值较接近,从工业生产角度考虑,确定川芎提取工艺为药材加10倍质量分数为30%的乙醇,提取2次,每次1.5 h。工艺验证试验结果见表7。
表7 川芎提取工艺验证试验结果(n = 3)
试验方案 因素 阿魏酸含量
(mg·g-1) 浸膏率
(%)
A B C D
優选工艺 10 70 2 1.5 0.43±0.008 15.65±0.45
改良工艺 10 30 2 1.5 0.42±0.010 16.21±0.61
2.4.2 巴戟天、白芍提取工艺验证试验 分别取巴戟天、白芍药材各10 g,共6份。其中3份按2.3.2项下优选的工艺进行提取;另3份按改良工艺即10倍质量分数为30%的乙醇提取2次,每次1.5 h,均计算各提取方法所得干浸膏的得率及其中水晶兰苷、芍药苷的含量。结果,2种工艺下,各指标值较接近,从工业生产角度考虑,确定巴戟天白芍提取工艺为药材加10倍质量分数为30%的乙醇,提取2次,每次1.5 h。工艺验证试验结果
见表8。
由表8可知,巴戟天、白芍和川芎的较佳提取工艺一致,因此,鉴于工业生产的可行性,确定巴戟天、白芍和川芎的提取工艺为3药材合并,加10倍质量分数为30%的乙醇,提取2次,每次
1.5 h,验证试验结果见表9。
由表9可知,巴戟天、白芍和川芎3药合并提取时,相对川芎单独提取各指标含量变化较小,其中水晶兰苷和芍药苷提取率稍微升高,阿魏酸提取率略微降低;总浸膏得率明显降低,从而能够减少给药量,表明优选的提取工艺稳定可行。
3 讨 论
本研究采用高效液相色谱的方法对阿魏酸、水晶兰苷和芍药苷的含量进行测试,所获得的方法学结果良好,由于研究重点在于提取工艺的优化,所以只列出各成分对应的线性方程,便于计算各成分的含量。
川芎药材中除了阿魏酸外,还包括生物碱药效成分川芎嗪,含量为0.01%~0.02%[11],也具有活血化瘀、抗血小板凝集、扩张血管、改善微循环等作用[12]。但由于其含量相对较低,因此,本研究选择阿魏酸作为川芎的评价指标。
本研究根据巴戟天、白芍指标成分水晶兰苷和芍药苷同为苷类,其极性大小和溶解性相近,而川芎的指标成分阿魏酸为苯丙素类,现将川芎的优化提取工艺和巴戟天、白芍合并优化的提取工艺分别操作,结合二者实际的优化结果,再通过各自的优选工艺和改良工艺的比较,获得二者3种药材全部混合提取的优化工艺。与同类药材的提取工艺相比,本研究通过对2种提取工艺结果的比较,在各指标成分含量变化不大情况下,得到3种药材的改良工艺,具有良好的工业化前景,对同类药材的工业化提取具有一定的借鉴作用。
综上所述,本研究按照最终提取工艺获得的样品经药效研究,具有延缓软骨退变、减轻炎症的良好效果[13-14],说明本优化方法可行。
4 参考文献
[1] 林木南,刘献祥.透骨消痛方治疗膝骨性关节炎
30例[J].福建中医药,2005,36(4):15-16.
[2] 陈燕,肖晓金,包侠萍,等.透骨消痛方镇痛抗炎作用实验研究[J].中医学报,2013,28(11):1675-1676.
[3] 李孝栋,张丽红,肖晓金,等.透骨消痛胶囊质量标准的研究[J].福建中医药,2012,43(1):57-59.
[4] 郑素玉,陈健.巴戟天有效成分及其药理作用实验研究进展[J].世界中西医结合杂志,2012,7(9):823-825.
[5] 国家药典委员会.中华人民共和国药典(2010年
版)[M].北京:中国医药科技出版社,2010:75.
[6] 王玉磊,黄世敬,迟德军,等.巴戟天中主要环烯醚萜苷的稳定性研究[J].中国实验方剂学杂志,2011,17(21):65-68.
[7] 陈华,叶柳贤.白芍醇提取液的镇痛抗感染作用效果实验研究[J].中国当代医药,2010,17(1):18-19.
[8] 朱蕾,魏伟.白芍总苷对大鼠胶原性关节炎及其免疫功能的影响[J].中国药学杂志,2007,42(20):
1547-1549.
[9] 赵东平,杨文钰,陈兴福.阿魏酸的研究进展[J].时珍国医国药,2008,19(8):1839-1841.
[10] 金玉青,洪远林,李建蕊,等.川芎的化学成分及药理作用研究进展[J].中药与临床,2013,4(3):44-48.
[11] 朱美晓,黄志芳,肖红斌,等.HPLC法测定川产道地药材川芎中川芎嗪的含量[J].药物分析杂志,2011,31(1):103-106.
[12] 贾绿琴,孙秀英.中药川芎的研究进展[J].黑龙江科技信息,2009(11):146-147.
[13] 吴广文,沈寿康,范怀玲,等.透骨消痛胶囊含药血清对退变软骨细胞表达caveolin-1、p38MAPK的影响[J].福建中医药大学学报,2014,24(2):17-20.
[14] 肖晓金,包侠萍,陈文列,等.透骨消痛胶囊对兔膝骨关节炎模型血清与关节液炎症因子的影响[J].风湿病与关节炎,2013,2(11):35-38.
收稿日期:2015-04-27;修回日期:2015-06-01