抗结核药物的应用与研发
石文卉 初乃惠
·综述·
抗结核药物的应用与研发
石文卉 初乃惠
随着耐药结核病的出现,抗结核新药的研发进入了一个新的阶段,既有一些抗生素如氟喹诺酮类和噁唑烷酮类药物、又有老药新用如环丝氨酸和氯法齐明;还有一些处于不同临床试验阶段的一类新药,如硝基咪唑类、二芳基喹啉类、吡咯类、噁唑烷酮类、乙二胺类等药物,其中较有开发前景的抗结核候选药物有贝达喹啉、德拉马尼、PA-824(硝基咪唑类化合物)和SQ-109(乙二胺类化合物)等。这些药物的研发为提高耐药结核病的治愈率提供了重要保证。
抗结核药; 抗生素类, 抗结核; 药物设计
结核病(tuberculosis,TB)是一个古老的疾病,几千年来由于缺乏有效的抗结核治疗药物,在20世纪40年代以前是人类死亡的主要疾病。自从1943年链霉素发现以来,结核病治疗进入了化疗时代,结核病疫情得到有效控制。如今耐药问题逐渐成为结核病控制的主要问题,使全球结核病疫情变得十分严峻。目前,抗结核药物的研发多集中在开发新作用机制的抗结核药物、原有药物的修饰、已知具有抗结核作用的抗生素的探索、原有药物新用途的开发等。
中国防痨协会根据世界卫生组织2014年出版的《耐药结核病规划管理指南伙伴手册》[1]和我国的实际情况,在2015年由中国防痨协会发布了我国《耐药结核病化学治疗指南(2015)》[2],药物分类见表1。
第一组、第二组和第三组药物研究较多,因此,本综述重点介绍第四组和第五组的药物,如老药新用抗结核药物、新型抗结核药物、已知具有抗结核作用的抗生素在耐药结核病治疗中的应用和部分处于不同临床试验阶段的抗结核药物等。
老药新用抗结核药物
一、环丝氨酸(cycloserine,Cs)
Cs是D-丙氨酸的拟似物,是一种结核分枝杆菌的抑菌剂,其作用机制为抑制丙氨酸消旋酶和D-丙氨酸连接酶,从而影响肽聚糖合成及随后的结核分枝杆菌细胞壁生物合成。口服Cs后,生物利用度可达70%~90%[2],可透过血脑屏障。Cs在人体内的半衰期为10 h,主要通过肾脏排泄[2]。
自1999年以来,Cs用于MDR-TB的治疗。在2001年土耳其的MDR-TB研究中,含有Cs的方案治疗MDR-TB治愈率达77%[3],取得了较好的临床效果,近40年我国没有Cs在临床上应用,耐药的发生率较低,故推荐用于耐药结核病治疗。但由于严重的不良反应限制了临床应用,我国也报道采用Cs出现精神症状的患者[3]。因此,在应用Cs之前应做筛查,有条件的地方做血药浓度监测,以保证安全;最常见的不良反应是嗜睡、头晕、精神病、癫痫等。
二、氯法齐明(clofazimine,Cfz)
Cfz是麻风病治疗中使用的脂溶性染料。在人体的半衰期约70 d。Cfz的生物利用度有较高的体内和个体差异,脂肪餐的时候浓度较高[4]。由于本药在脂肪组织中浓度较高,几乎100%患者可出现皮肤橘色至棕色的色素沉着[5]。
在孟加拉国的队列研究中,对515例MDR-TB患者应用包含Cfz和Gfx的9个月的治疗方案获得了成功。治愈率达到84.5%[6]。目前,世界上多国在孟加拉国研究的基础上,开展治疗方案中含有Cfz的研究,如国际防痨和肺部疾病联合会(The International Union Against Tuberculosis and Lung Disease)在南非和越南等国家开展的大规模临床研究,这些研究均表明Cfz可作为联合化疗方案的重要药物。
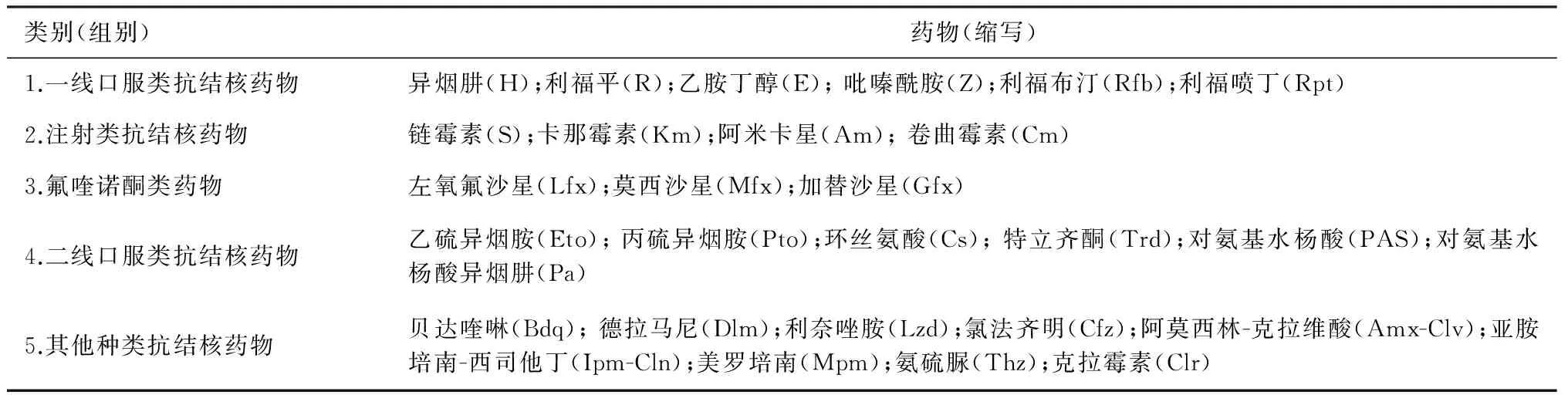
表1 抗结核药物分类
注 第1组为一线抗结核药物,本次修订增加了Rpt,Rpt主要用于潜伏感染的治疗(不作为初治结核病的治疗药物);第2组药物S,虽然放在第一组,但不作为耐药结核病的治疗药物;第3组的氧氟沙星因生物活性低,不再作为第3组药物,加替沙星可引起较严重的糖尿病或血糖代谢紊乱,在某些国家已禁止使用和销售,应用时需要注意;第4组药物WHO版本中增加了PASNa,我国增加了对氨基水杨酸异烟肼(Pa),建议用于①对异烟肼敏感的耐药结核病;②经药敏试验证实对氨基水杨酸异烟肼敏感的耐异烟肼结核病患者。特立齐酮研究资料较少,且与环丝氨酸具有相同的抗结核活性;第5组药物包括了新型抗结核药物,也包括没有大规模临床试验证实的药物
新型抗结核药物
一、贝达喹啉(bedaquiline,Bdq)
Bdq,商品名斯耐瑞(Sirturo),曾称TMC207、R207910。Bdq是一种二芳基喹啉类化合物,能够抑制结核分枝杆菌ATP合成酶,主要作用于细菌细胞壁中的ATP合成酶F0亚单元C亚基,导致菌体内ATP耗竭和pH失调而发挥杀菌作用,该药于2012年12月经美国FDA批准在美国上市,与其他药物联合治疗耐多药肺结核(MDR-TB)[7]。这是自20世纪70年代以来,全球首个全新化学结构的抗结核上市的新药,也是首个被批准用于MDR-TB治疗的新药。
Bdq口服吸收良好,单剂给药后达到峰浓度的时间为5 h,半衰期达24 h,耐受性良好,未见与药物本身有关的不良反应[8]。研究表明,本品对敏感及耐药结核分枝杆菌均表现出杀菌作用,对休眠菌也具有良好的灭菌作用,与传统的抗结核药物之间无交叉耐药性。其最小抑菌浓度(MIC)值≤INH和RFP的MIC值。Ⅰ期临床试验显示,对人体的安全性和耐受性良好。Bdq的Ⅱa期多中心、分层、随机双盲安慰剂对照研究显示,试验组和对照组的痰结核分枝杆菌培养阴转的平均时间为83 d和125 d。在治疗24周时,试验组的痰结核分枝杆菌培养阴转率为78.8%,高于安慰剂组的57.6%(P=0.008)。最常见的不良反应为恶心、关节痛、头痛、高尿酸血症和呕吐,其他常见不良反应包括:头晕、转氨酶升高、肌痛、腹泻和心电图QT间期延长[9]。
为规范Bdq的使用,WHO在2013年制定了应用指南,建议治疗耐药结核病的适应证为:(1)耐多药结核病(MDR-TB)不能组成有效的化疗方案时,如对第2组、第3组和第4组二线药物中的某种药物或Z体外耐药或出现药物不良反应、耐受性差或禁忌证。(2)广泛耐药结核病前期(Pre-XDR-TB),即对氟喹诺酮类或二线注射药物(Km、Am、Cm)耐药的MDR-TB患者。(3)广泛耐药结核病(XDR-TB)[1]。
二、硝基咪唑类
本类药物被认为对Mtb等分枝杆菌有很好的体内外活性。实验证实,5-位硝基咪唑类CGI-17341对MDR-TB具有较好的活性,虽然曾因较高的基因突变性阻碍其开发进程,但仍具有抗结核新药的开发前景。目前对CGI-17341结构进行修饰以得到不良反应少的抗结核活性衍生物,包括候选药物PA-824、Dlm及TBA-354。
1. PA-824:PA-824是对鸟型结核分枝杆菌和耐多药结核分枝杆菌有高度活性的化合物,在低氧非复制状态下,作为氧化亚氮供体而发挥杀菌作用,这一过程伴随一氧化氮的释放及细胞色素C氧化酶的抑制[10]。此外,PA-824还能降低细菌ATP水平而导致细菌无法获得足够的能量而致死。PA-824具有良好的体外抗Mtb活性,其对敏感菌和耐多药菌株同等有效,且对生长旺盛的菌群和不复制的菌群都有杀灭作用。这些特性表明其作用机制独特,且与其他抗结核药物之间不存在交叉耐药性。
本品有良好的组织穿透能力,达峰时间为4~5 h,半衰期为18 h。人体耐受性良好[11]。近期的一项研究显示,用本品替代联合疗法中的INH时细菌阴转更为迅速,但2个治疗组在治疗结束后的复发率方面没有明显差异[12]。而替代利福平或吡嗪酰胺其杀菌活性会降低[13]。PA-824虽然相对其母体CGI-17341的突变性大大减小,但还是呈现出相当高的突变性,这可能将成为其作为抗结核新药的一个主要障碍[14]。
该药的Ⅱ期临床试验纳入207例初治敏感肺结核患者,观察2个月的治疗效果,试验组采用莫西沙星、PA-824(100 mg,200 mg)、吡嗪酰胺,对照组为标准治疗方案(HRZE)。含PA-824 200 mg组的杀菌活性明显强于HRZE组。表明含PA-824 200 mg的化疗方案优于目前的标准方案。常见的不良反应有恶心呕吐。治疗期间没有发生任何药物的表型耐药[15]。表明PA-824是一种效果较好的新型抗结核药物。目前该药仍在进行耐药结核病治疗的研究。
2.德拉马尼(delamanid,Dlm):Dlm由日本Otsuka公司研制,其作用机制是通过抑制分枝菌酸的合成而抑制细胞壁的生物合成[16],是经过结构改造后的硝基咪唑类衍生物,作用机制与PA-824非常类似,两者有交叉耐药性。与PA-824不同,Dlm对堪萨斯分枝杆菌有活性,也具高度体外抗Mtb(包括MDR-TB)活性(MIC:0.006~0.024 μg/ml),而且,本品与目前一线抗结核药物无交叉耐药[12],暗示其可能具有新的作用机制,可缩短疗程[16]。
本品用药后血药浓度很低(0.297 mg/L),其半衰期7.6 h,可用于治疗Mtb与HIV双重感染的TB。临床Ⅱb阶段的208试验结果显示100 mg和200 mg两种不同剂量的Dlm组的痰培养转阴率(45.4%、41.9%)均高于安慰剂组(29.6%)(P=0.008)。不良反应有QT间期延长[17]。该临床试验表明Dlm能提高痰培养转阴率。
3. TBA-354:TBA-354是第二代硝基咪唑类化合物,其体外对复制和非复制结核分枝杆菌有抗菌活性。在急性和慢性结核感染小鼠模型显示,TBA-354在体内呈时间和剂量依赖的杀菌活性,均与Dlm相当,显著优于PA-824;本品与Dlm、PA-824的最大优点是生物利用度高,半衰期长,这表明其将来可能用于每日1次给药[18]。
已知具有抗结核作用的抗生素治疗耐药结核病
在结核病药物的研发中,有些药物主要用于抗感染领域,但在对结核分枝杆菌的筛查中,发现对结核分枝杆菌有效,特别是氟喹诺酮类药物和噁唑烷酮类药物。这些药物没有治疗结核病的适应证,但部分药物已经作为耐药结核病治疗的核心药物,氟喹诺酮类药物临床医生比较熟悉,这里重点介绍噁唑烷酮类药物。
噁唑烷酮是继氟喹诺酮类药物之后又一类全合成的新型抗生素,与其他抗生素比较,其作用机制独特,通过与细菌50S核糖体亚基中的23S rRNA结合而抑制细菌核糖体蛋白质的合成[19]。
一、利奈唑胺(linezolid,Lzd)
Lzd是第一代噁唑烷酮类药物,并且是目前唯一上市的噁唑烷酮类抗生素。近期体外实验报道,Lzd对敏感和耐药的结核分枝杆菌具有同样良好的抗菌活性[20]。Lzd生物利用度可达100%,口服给药后的达峰时间为1~2 h,血浆蛋白结合率低,主要以游离原药的形式广泛分布于人体各组织。
韩国的一项临床试验纳入了41例痰培养阳性的XDR-TB患者,大部分患者[87% (34/39)])在原方案中加入Lzd后6个月出现阴转。39例接受Lzd治疗的患者中,31例(80%)出现较严重不良反应。降低剂量为300 mg/d后,药物不良反应少于服用600 mg/d的患者,但4例患者发生了耐药[21]。提示Lzd治疗XDR-TB较为有效,但会引起明显的不良反应,降低用药剂量可以减轻不良反应,但需注意耐药的产生。
由于Lzd用于抗结核治疗的剂量和疗程尚无统一定论,因此,据相关文献报道,建议以600 mg/次,1次/d进行治疗,总疗程暂推荐为3~6个月[22]。
二、PNU-100480
PNU-100480是Lzd的结构类似物,体外对结核分枝杆菌的MIC值为0.03~0.5 μg/ml,比Lzd和依哌唑胺活性更高。Ⅰ期临床试验已经完成。给健康受试者每天2次PNU-100480,每次600 mg,共服用28 d,未见明显不良反应。研究人员还发现本品与PZA的协同作用[23]。目前该药正在进行Ⅱ期临床试验。
其他正在研发的抗结核药物
一、乙二胺类SQ109
SQ109为乙二胺类最具代表性的候选物,本品能阻断细胞壁生物合成,其准确的作用机制尚未阐明。SQ109对耐乙胺丁醇的结核分枝杆菌菌株有效,故其可能存在与乙胺丁醇不同的作用机制[24]。由于SQ109作用于不同的细胞靶点,故也可将其视为一类新的抗结核药物,而非仅是乙胺丁醇的类似物。SQ109半衰期长达61 h,药效持久。剂量增至300 mg时人体仍具良好的耐受性,用药安全[23]。SQ109在体内外与RFP、INH或PZA联用均表现出抗Mtb的协同作用,抗菌活性更好,呈现出低浓度高效性[25-26]。
二、其他药物
吡咯类(pyrrole group)BM212及LL-3858,最近研究发现基于某些唑类化合物具有明显的体内、外抗结核活性。Deidda等设计合成了一系列吡咯衍生物,其中代表化合物BM212对分枝杆菌表现出高度的选择性抗菌活性,对耐药株显示出良好的活性。另一个有代表性的吡咯类化合物是LL-3858,目前正处在Ⅰ期临床试验阶段。研究显示对敏感及耐药的结核分枝杆菌均有活性。
结 语
抗结核药物的研发虽然有了一定的进展,但面对耐药结核病的疫情,我们仍然需要更多的新药,以便缩短治疗时间并增加对耐药结核病的有效性。最新研究的新药或许可以应对该挑战,但在这些药物应用之前,还有很多问题存在。包括剂量优化及开发新方案,在新药加入到方案中需要增加疗效、降低不良事件及药物间的相互作用。
[1] World Health Organization.Companion handbook to the WHO guidelines for theprogrammatic management of drug- resistant tuberculosis.Geneva: World Health Organization,2014.
[2] 中国防痨协会.耐药结核病化学治疗指南(2015).中国防痨杂志,2015,37(5):421-469.
[3] 缪昌东,姜继军. 环丝氨酸致精神异常一例. 中国防痨杂志,2013,35(6): 480.
[4] Nix DE, Adam RD, Auclair B, et al. Pharmacokinetics and relative bioavailability of clofazimine in relation to food, orange juice and antacid. Tuberculosis, 2004, 84(6): 365-373.
[5] Moore VJ. A review of side-effects experienced by patients taking clofazimine. Lepr Rev, 1983, 54(4): 327-335.
[6] Dey T, Brigden G, Cox H, et al.Outcomes of clofazimine for the treatment of drug-resistant tuberculosis: a systematic review and meta-analysis. J Antimicrob Chemother, 2013,68(2): 284-293.
[7] Diacon AH, Pym A, Grobusch M, et al. The diarylquinoline TMC207 for multidrug-resistant tuberculosis. N Engl J Med, 2009, 360(23): 2397-2405.
[8] Andries K,Verhasselt P,Guillement J,et al.Adiarylquinoline drug active on the ATP synthase ofMycobacteriumtuberculosis.Science,2005,307(5707):223-227.
[9] WHO Guidelines Approved by the Guidelines Review Commmittee.The use of bedaquiline in the treatment of multidrug-resistant tuberculosis——Interim policy guidance. Geneva:World Health Organization,2013.
[10] Singh R, Manjunatha U, Boshoff HI, et al. PA-824 kills nonreplicatingMycobacteriumtuberculosisby intracellular NO release. Science, 2008, 322(5906): 1392-1395.
[11] Stover CK, Warrener P, VanDevanter DR, et al.A small-molecule nitroimidazopyran drug candidate for the treatment of tuberculosis. Nature, 2000, 405(6789): 962-966.
[12] 李艳萍,刘明亮.抗结核药物研究进展.国外医药抗生素分册, 2009, 30(6): 241-247.
[13] Tasneen R, Tyagi S, Williams K, et al. Enhanced bactericidal activity of rifampin and/or pyrazinamide when combined with PA-824 in a murine model of tuberculosis. Antimicrob Agents Chemother, 2008, 52(10): 3664-3668.
[14] Barry CE 3rd, Boshoff Hl, Dowd CS. Prospects for clinical introduction of nitroimidazole antibiotics for the treatment of tuberculosis. Curr Pharm Des, 2004, 10(26): 3239-3262.
[15] Dawson R, Diacon AH,Everitt D,et al. Efficiency and safety of the combination of moxifloxacin, pretomanid (PA-824), and pyrazinamide during the first 8 weeks of antituberculosis treatment: a phase 2b, open-label, partly randomised trial in patients with drug-susceptible or drug-resistant pulmonary tuberculosis. Lancet, 385(9979): 1738-1747.
[16] Matsumoto M, Hashizume H, Tomishige T, et al. OPC-67683, a nitro-dihydro-imidazooxazole derivative with promi-sing action against tuberculosis in vitro and in mice. PLoS Med, 2006, 3(11): e466.
[17] Lewis JM,Sloan DJ.The role of delamanid in the treatment of drug-resistant tuberculosis.Ther Clin Risk Manag, 2015,11(5):779-791.
[18] Upton AM,Cho S,Yang TJ, et al.In vitro and in vivo activities of the nitroimidazole TBA-354 againstMycobacteriumtuberculosis. Antimicrob Agents Chemother, 2015,59(1): 136-144.
[19] Falagas ME,Vardakas KZ. Benefit-risk assessment of linezolid for serious gram-posotove bacterial infections.Drug Saf, 2008,31(11):753-768.
[20] Yang C,Lei H,Wang D,et al.In vitro activity of linezolid againstMycobavteriumtuberculosis,including multidrug-resistant and extensively drug-resistant strains from Beijing,China. Jpn J Infect Dis,2012,65(3):240-242.
[21] Lee, M, Lee J,Carroll MW,et al. Linezolid for treatment of chronic extensively drug-resistant tuberculosis.N Engl J Med, 2012, 367(16): 1508-1518.
[22] 唐神结,肖和平.利奈唑胺抗结核作用的研究及其最新进展.中华临床医师杂志(电子版),2010,4(1):63-66.
[23] 卢曦,杨信怡,游雪甫. 抗结核药物最新研究进展. 药学研究,2013,32(1):36-41.
[24] Protopopova M, Hanrahan C, Nikonenko B, et al. Identification of a new antitubercular drug candidate, SQ109, from a combinatorial library of 1, 2-ethylenediamines. J Antimicrob Chemother, 2005, 56(5): 968-974.
[25] Chen P, Gearhart J, Protopopova M, et al. Synergistic interac-tions of SQ109, a new ethylene diamine, with front-line antitubercular drugs in vitro. J Antimicrob Chemother, 2006, 58(2): 332-337.
[26] Nikonenko BV, Protopopova M, Samala R, et al. Drug therapy of experimental tuberculosis (TB): improved outcome by combining SQ109, a new diamine antibiotic, with existing TB drugs. Antimicrob Agents Chemother, 2007, 51(4): 1563-1565.
(本文编辑:范永德)
Application of anti-tuberculosis drugs, research and development
SHI Wen-hui, CHU Nai-hui.
Department of Tuberculosis, Beijing Chest Hospital Affiliated to Capital Medical University,Beijing 101149,China
CHU Nai-hui, Email: dongchu1994@sina.com
With the emergence of drug-resistant TB, the research and the development of new drugs have entered a new phase, there are not only some antibiotics such as fluoroquinolone and oxazolidinone drugs but also older drugs which be used for drug-resistant TB such as cycloserine and clofazimine.Meanwhile, some new drugs are in the different stages of clinical trials, such as nitroimidazoles, diarylquinoline, pyrrole,oxazolidinone, ethylenediamine and so on, among these drugs, beta quinoline, PA-824, Delamani and SQ-109 have better prospects. The research and development of these anti-tb drugs will improve the cure rate of drug-resistant TB.
Antitubercular agents; Antibiotics, antitubercular; Drug design
10.3969/j.issn.1000-6621.2015.11.015
“十二五”国家科技重大专项(2012ZX09303002)
101149 首都医科大学附属北京胸科医院结核科
初乃惠,Email: dongchu1994@sina.com
2015-08-11)

