二维离子色谱法同时测定4种无机阴离子和葡萄糖酸根离子
陈爱连, 丁 卉, 方琳美, 施超欧
(华东理工大学分析测试中心, 上海 200237)
技术与应用
二维离子色谱法同时测定4种无机阴离子和葡萄糖酸根离子
陈爱连, 丁 卉, 方琳美, 施超欧*
(华东理工大学分析测试中心, 上海 200237)
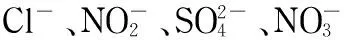
二维离子色谱;电导检测;脉冲安培检测;无机阴离子;葡萄糖酸根
复杂体系的分离分析一直是化学分析的重要研究方向。对于复杂样品的分离,一种分离模式往往不能提供足够的分离效率,组合不同的分离模式构建二维和多维系统是解决这一问题的有效途径。二维的分析模式在高效液相色谱中的发展已经比较成熟,其机理是将两支或多支不同类型的色谱柱串联或并联,样品经过第一维的色谱柱分离后,通过浓缩富集、中心切割等各种类型的阀切换方式进入第二维色谱柱中,使分离效率大幅度提高。在二维离子色谱研究中,由于其流动相的特殊性(强酸和强碱)以及抑制器的存在,相对于二维液相色谱而言进展缓慢,受制约的因素更多。在近年来的分析中,多采用Dionex公司的离子色谱仪,也有部分使用其他公司的仪器,如Metrohm的离子色谱仪[1,2]。第一维分离系统以4 mm色谱柱为主,少数使用2 mm色谱柱[3-5]。第二维近期多采用0.4 mm的毛细管离子色谱柱体系[5-7],早期多使用2 mm的色谱柱体系[8,9];也有少数使用4 mm色谱柱体系[4,5,10]。检测系统中第一维均使用电导检测器,第二维以电导检测器为主,安培检测器[2]、质谱以及电感耦合等离子体质谱(ICP-MS)[1,11]也有一定的应用。二维离子色谱法主要利用第二维的分离特点分析一些特殊的离子。
葡萄糖酸锌是常见的食品补锌添加剂,具有调节皮脂分泌的功能,在化妆品行业中作为除臭剂、肌理调节剂。医药方面,葡萄糖酸锌对儿童厌食、腹泻和轮状病毒导致的肠道感染[12]等有很好的治疗效果,对高血压性脑出血也有显著疗效[13]。在葡萄糖酸的检测方法中,液相色谱应用得较多[14,15],离子色谱相对较少[16]。葡萄糖酸是糖的衍生物,在阴离子色谱柱上保留弱,出峰快,且与氟离子、乙酸、乳酸出峰时间相差无几,易受干扰,定性和定量困难。而在糖柱上则有较强的保留,且在安培检测器中有一定的响应,因此在本文中的二维离子色谱方法中,利用脉冲安培检测器对其高灵敏度响应以及电导检测器对阴离子普适性的分析,建立了电导和安培双检测器的两维模式。一维采用常规的4 mm阴离子色谱柱分离,第二维利用糖柱延长葡萄糖酸根的保留时间将葡萄糖酸根和其他干扰基质分离,安培检测器的选择性响应消除其他离子干扰,对其进行定性和定量分析。利用阀切换将先出峰的葡萄糖酸根切换到安培检测系统,其他无机离子进入电导检测系统;实现了同步测定并具有较高的灵敏度和较快的分析速度。目前国内外对二维离子色谱的研究报道较少,但二维离子色谱是离子色谱发展的一个趋势,构建两维模式,选择合适的分析柱、阀切换方式及高灵敏度的检测器对复杂样品进行分离和分析,可以提高分离效率以及检测的准确度和精密度。
1 实验部分
1.1 仪器、试剂与标准品
美国Dionex公司双系统ICS-3000离子色谱仪(包括DP四元泵,GP50四元泵,AS自动进样器,DC控制单元,Chromeleon 6.8色谱工作站); Millipore公司Milli-Q Advantage A10超纯水机;BRANSON公司BRANSON 2510超声仪。
氯离子、亚硝酸根离子、硫酸根离子和硝酸根离子标准储备液(100 mg/L,上海计量测试技术研究院);氢氧化钠(50%(质量分数),默克公司);葡萄糖酸锌(含量99.8%,武汉鲜保生物技术有限公司)。
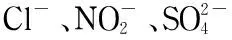
1.2 色谱条件
第一维:电导检测系统。色谱柱:Ionpac AG18(50 mm×4 mm)+Ionpac AS18(250 mm×4 mm);捕获柱:Ionpac ATC-3 (4 mm);抑制器:ASRS 300(4 mm); CO2去除装置:CRD 200(4 mm);流速:1.0 mL/min;柱温:30 ℃;进样量:25 μL;淋洗条件:0~5 min, 5 mmol/L NaOH溶液(富集待测葡萄糖酸根); 5~20 min, 20 mmol/L NaOH溶液(洗脱无机阴离子);电导检测器检测。
第二维:脉冲安培检测系统。色谱柱:CarboPac PA1 (50 mm×4 mm)+CarboPac PA20(30 mm×3 mm);淋洗液:90 mmol/L NaOH溶液;流速:0.8 mL/min;柱温:30 ℃; ICS-3000离子色谱仪自带六通阀为切换阀,Ionpac AG15保护柱(捕获柱)(50 mm×4 mm);脉冲安培检测器:金工作电极,Ag/AgCl参比电极,四电位检测。
1.3 系统组成
二维双检测器系统的结构如图1所示。在进样之前两个四元泵分别对两个系统进行平衡,调节Vavle 1自动进样器开始进样,样品随流动相经过AG18+AS18柱进行第一维分离,葡萄糖酸根在阴离子分析柱上保留能力弱,很快被洗脱出来。根据阴离子和葡萄糖酸根保留时间的差异控制Vavle 2,通过阀切换时间的计算,将葡萄糖酸根切割到AG15柱上,利用AG15柱的保留时间差进行收集。收集结束后,第二维的流动相将AG15柱上富集的葡萄糖酸根和其他干扰组分洗脱至串联的PA1和PA20保护柱上分离后经脉冲安培器检测。保留在阴离子分析柱上未被切割的无机阴离子组分用高浓度的NaOH溶液依次洗脱再经过抑制器和CRD 200到电导检测器检测。
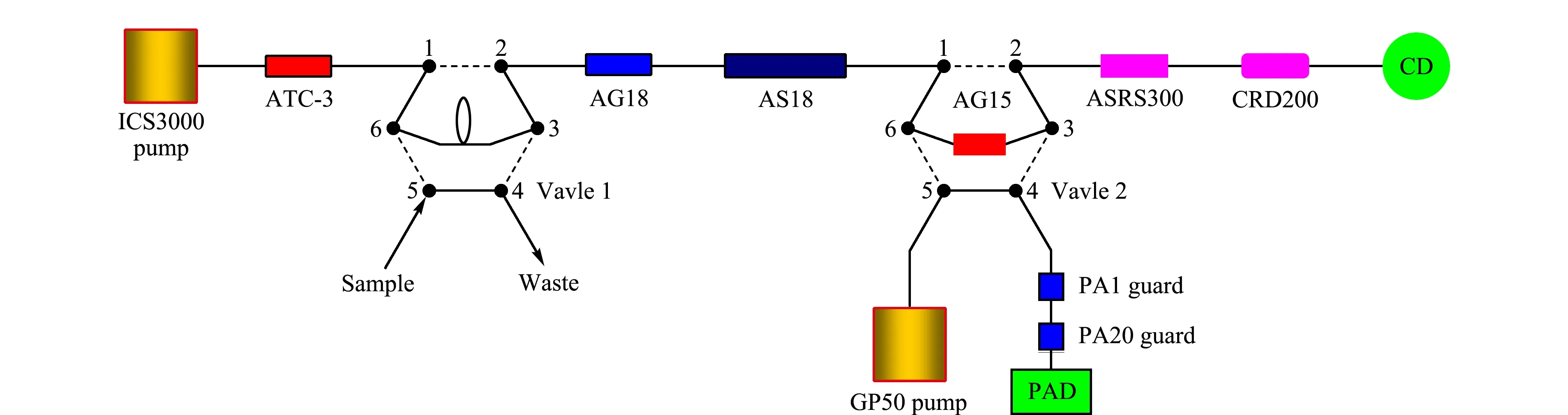
图 1 二维离子色谱系统的结构图Fig. 1 Structural diagram of two-dimensional ion chromatographic system
2 结果与讨论
2.1 色谱柱的选择
2.1.1 ATC-3柱(捕获柱)
在二维离子色谱系统中,进样阀和泵之间接有ATC-3捕获柱,其作用在于除去淋洗液中的阴离子,尤其是CO2,以避免CO2对手配NaOH淋洗液在进行梯度分离时对基线和样品测定的干扰。
2.1.2 AG18柱+AS18柱(第一维阴离子分析柱)
AS18柱是标准的常用阴离子分离柱之一,既可以用于等度分离,也可以用于梯度分离,在实验过程中为了获得较低的起始淋洗液浓度和较好的分离效果,采用高低两个浓度进行等度分离。
2.1.3 AG15柱(捕获柱)
Dionex公司标准的离子捕获柱(例如TAC-LP1)对葡萄糖酸根的保留很弱,回收率低,因此用保留能力较强的AG15保护柱替代常规的离子捕获柱。
2.1.4 CRD 200(CO2去除装置)
CRD 200接在抑制器的后面,用于除去经过抑制器抑制后流动相中的残留CO2,避免对被测离子的干扰,同时降低了背景电导,可提高被测离子灵敏度约20%~30%。CRD 200相当于第二个抑制器(柱),但其不能单独使用。
2.1.5 PA1+PA20保护柱(第二维葡萄糖酸根分析柱)
在第二维离子色谱体系中,如果直接连接糖保护柱和分析柱,由于葡萄糖酸根在糖柱上的保留能力远高于葡萄糖,要得到较快的分离,必须采用极高浓度的NaOH淋洗液洗脱,但高浓度的NaOH溶液会对两维切换不利。因而采用两根保护柱串联方式,既能使葡萄糖酸根有一定的保留,且NaOH溶液的浓度不高,同时与一维分离时间匹配。
2.2 两维系统的选择分析
2.2.1 第一维系统中淋洗液体系和第二维系统中脉冲安培体系的选择
在第一维系统中,如果KOH淋洗液采用淋洗液发生器发生,由于淋洗液发生器产生KOH是一个电化学反应过程,该反应过程会电解出氢气,虽然氢气会被脱去,但仍会有少量进入淋洗液系统,同时电解会产生一些电活性物质,这些电活性物质被AG15柱富集后,会在第二维安培系统中产生很高的干扰峰,严重影响到第二维系统的分析。ICS-3000的EG模块自带脱气装置,不能完全去除氢气,需外接一个真空脱气泵连接至淋洗液自动发生器脱气装置的出口将氢气抽除完全。而脱气泵和淋洗液自动发生器脱气装置连接的组件较多,且安装复杂。考虑到实验成本和可操作性,本实验选择手动配制的NaOH溶液为淋洗液,在泵后连上Ionpac ATC-3柱(4 mm)除去淋洗液中的干扰阴离子,以平稳基线。

图 2 AG15柱对葡萄糖酸根的保留作用Fig. 2 Retention of AG15 column for gluconate a. sample treated with AG15 column; b. sample without AG15 column processing. Peaks: 1. gluconate; 2. Cl-; 3..
Ionpac AG15柱是Ionpac AS15柱的保护柱。在较低浓度的NaOH溶液下对葡萄糖酸根有较强的保留作用,在待测离子被淋洗出富集柱之前,留出足够的时间进行阀切换。如图2所示,葡萄糖酸根经过AG18柱和AS18柱分离后直接进入电导检测器检测的时间为5.157 min,而经过AG15柱富集分离后到达电导检测器的时间为7.434 min,抑制器和CRD的系统死时间为0.306 min,因此在4.6~5.3 min(考虑了抑制器、CRD的死时间)之间切换Vavle 2使葡萄糖酸根进入AG15柱,从而将其与干扰杂质分离,更有效地收集葡萄糖酸根并进入安培检测器进行检测。
第二维中葡萄糖酸根的分析不采用常规的糖分析柱,而用2根串联的保护柱是因为在碱性条件下,糖柱对弱电离的糖类有较强的保留,对易电离的离子保留性极强,即使是在阴离子分析体系中弱保留的葡萄糖酸根也是如此。因此,为了得到一定的分离效果,同时保留时间与一维时间基本一致且淋洗液浓度合适,经过多次测试,选用2根保护柱串联的特殊方式用于葡萄糖酸根的分离。
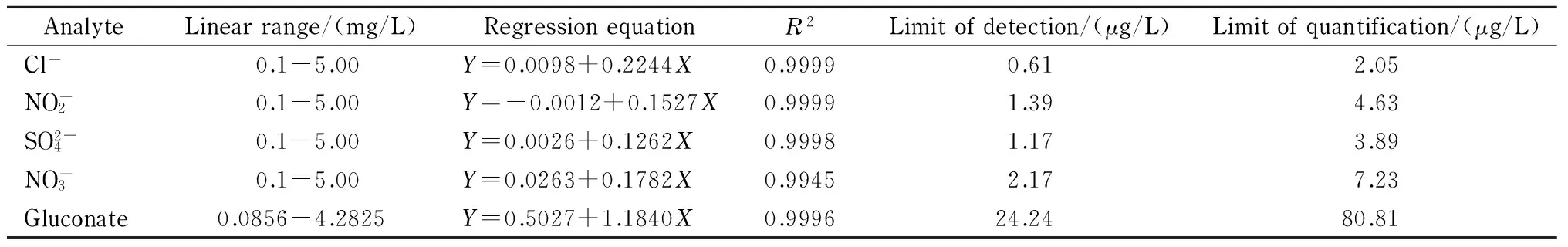
表 1 4种无机阴离子和葡萄糖酸根的线性范围、回归方程、线性相关系数(R2)、检出限和定量限Table 1 Linear ranges, regression equations, correlation coefficients (R2), limits of detection and limits of quantification of the four inorganic anions and gluconate
Y: peak area;X: mass concentration, mg/L.
2.2.2 分离分析过程和结果
进样之前,用淋洗液分别对第一维系统和第二维系统进行平衡。进样后,在0~4.6 min之间,样品在5 mmol/L NaOH溶液淋洗下在AG18+AS18柱上被分离。由于阴离子分析柱对葡萄糖酸根的保留很弱,很快被洗脱出来。4.6~5.3 min时,通过阀切换用AG15柱对葡萄糖酸根离子进行富集。无机阴离子此时仍保留在第一维的色谱柱中。5.3 min~分析结束,第一维的无机阴离子用20 mmol/L NaOH溶液洗脱,经过抑制器和CRD 200被电导检测器检测。第二维分离系统中用90 mmol/L NaOH淋洗液将富集在AG15柱上的组分带入PA1和PA20柱进行分离并进入安培检测器检测,图3和图4分别为5 mg/L的4种阴离子和4.282 5 mg/L的葡萄糖酸根的色谱分析图。
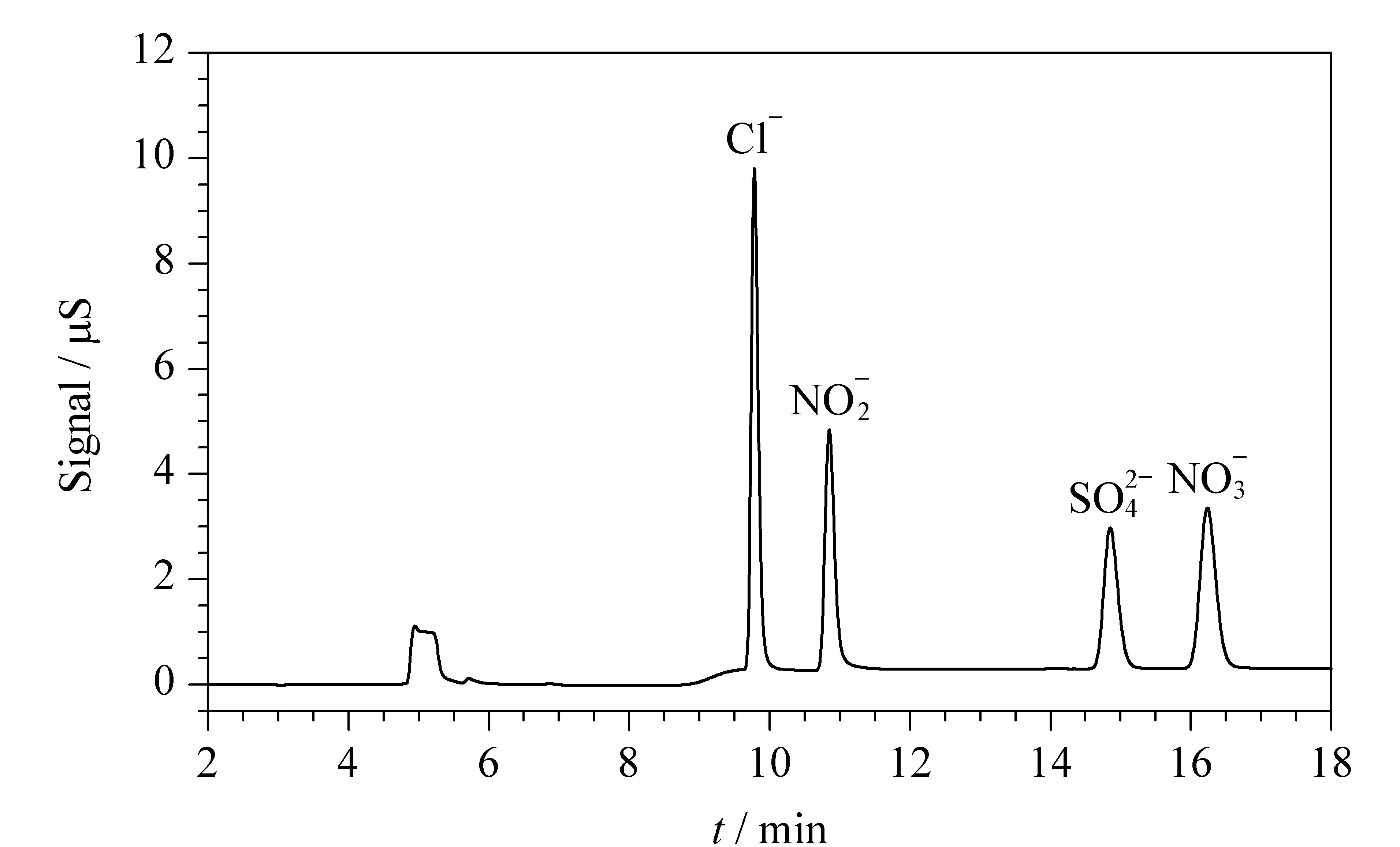
图 3 氯离子、亚硝酸根离子、硫酸根离子和硝酸根离子混合标准溶液的色谱图Fig. 3 Chromatogram of a mixed standard solution of chloride, nitrate, nitrite and sulfate ions
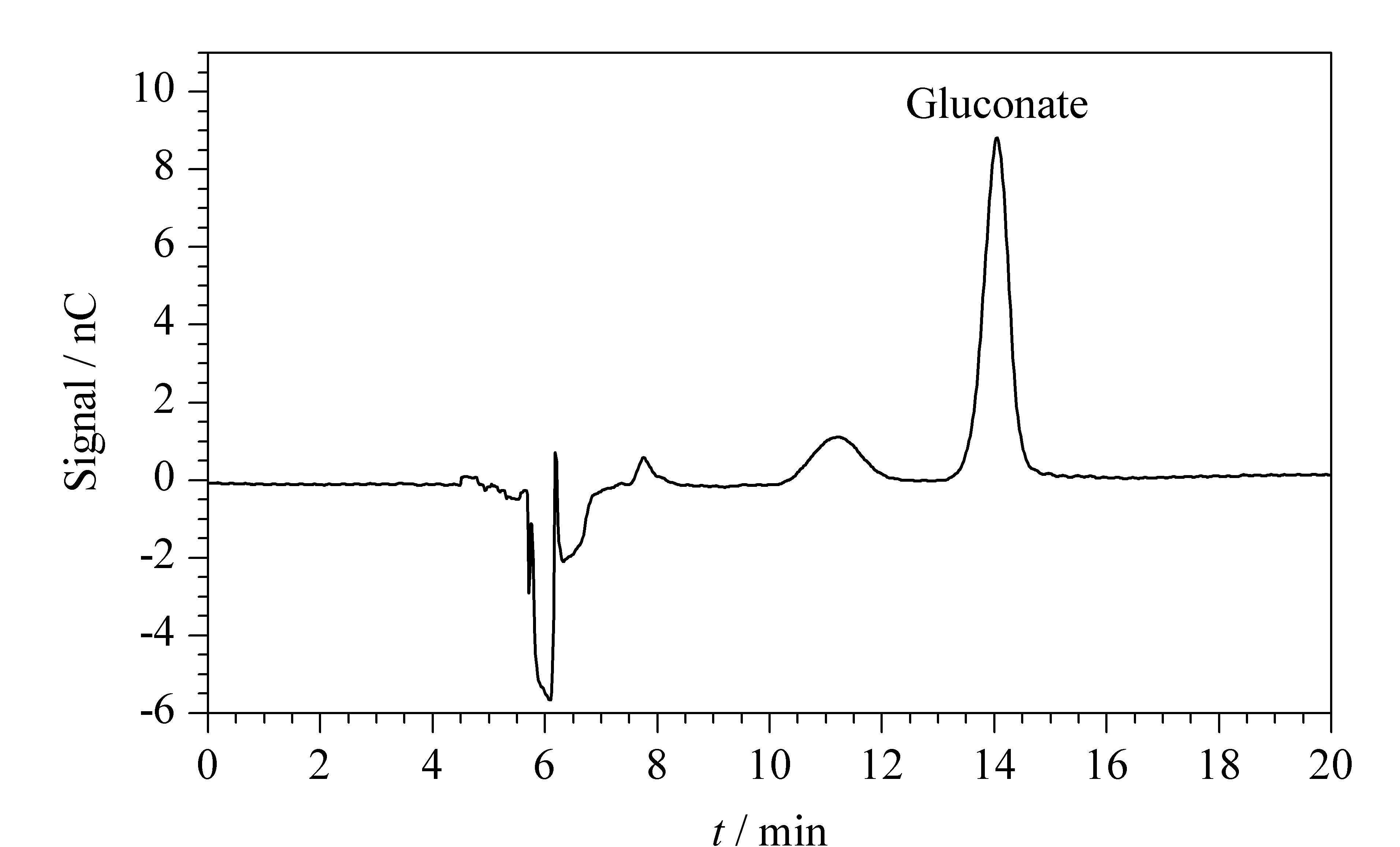
图 4 葡萄糖酸根标准溶液的色谱图Fig. 4 Chromatogram of gluconate standard solution
2.3 线性关系、进样重复性、检出限和定量限

对质量浓度为1.00 mg/L的混合阴离子标准溶液和0. 8 565 mg/L的葡萄糖酸根标准溶液连续重复进样8次,目标物峰面积的RSD在1.05%~1.94%之间(见表2),表明重复性较好。

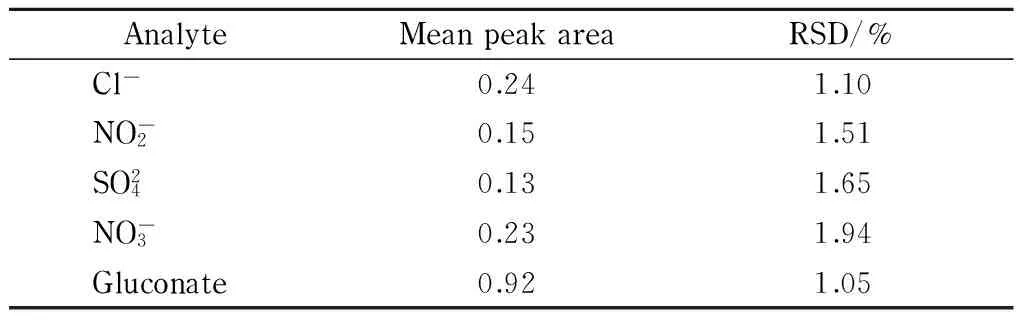
表 2 4种无机阴离子和葡萄糖酸根的进样重复性(n=8)Table 2 Injection repeatability of the four inorganic anions and gluconate (n=8)
3 结论
本文建立了一种电导检测器和安培检测器同时在线测定4种无机阴离子和有机糖酸葡萄糖酸根的二维离子色谱模式。在该分析系统中,通过精确计算阀切换时间,选择合适的捕获柱,并创新性地选择了2根离子色谱保护柱串联作为第二维系统的分析柱,优化了第二维安培检测的色谱条件,使氯离子、亚硝酸根离子、硫酸根离子、硝酸根离子和葡萄糖酸根同时在线测定达到理想效果,线性关系和重复性好,方法的灵敏度和准确度高。
离子色谱因其抑制器结构和安培检测器响应的特殊性,使得二维离子色谱的实现存在一定的困难。本文通过一系列的方法优化实验,成功地将电导检测器和安培检测器并联,从而用不同的检测模式分析了无机阴离子和有机糖酸根,为今后二维离子色谱方法的设计开发提供了一个借鉴。
[1] Kraft V, Grützke M, Weber W, et al. J Chromatogr A, 2015, 1409: 201
[2] Yang X L, Tao L, Sun Z D. Chinese Journal of Inorganic Analytical Chemistry (杨秀丽, 陶玲, 孙郑冬. 中国无机分析化学), 2012, 2(Supp 1): 49
[3] Qiu H M, Geng J J, Han C, et al. Chinese Journal of Analytical Chemistry (邱慧敏, 耿金菊, 韩超, 等. 分析化学), 2013, 41(12): 1910
[4] Johns C, Shellie R A, Pohl C A, et al. J Chromatogr A, 2009, 1216: 6931
[5] Teh H B, Li S F Y. J Chromatogr A, 2015, 1383: 112
[6] Lin L, Wang H B, Shi Y L. Chinese Journal of Chromatography (林立, 王海波, 史亚利. 色谱), 2013, 31(3): 281
[7] Verrey D, Louyer M V, Thomas O, et al. Microchem J, 2013, 110: 608
[8] Wagner H P, Pepich B V, Pohl C, et al. J Chromatogr A, 2007, 1155: 15
[9] Dionex China Limited. Environmental Chemistry (戴安(中国)有限公司. 环境化学), 2007, 26(6): 869
[10] Lin Q, Lin H M, Bao Y M. Chemical Analysis and Meterage (林奇, 林红梅, 包洋鸣. 化学分析计量), 2014, 23(Z1): 22
[11] Zheng J, Shibata Y, Furuta N. Talanta, 2003, 59(1): 27
[12] Lai M L. Chinese Journal of Medical Guide (来蔓丽. 中国医药导刊), 2015, 17(6): 583
[13] Liu L. Contemporary Medicine Forum (刘丽. 当代医药论丛), 2015, 13(15): 233
[14] Gao G, Sun X D, Zhao J H, et al. China Journal of Modern Medicine (高革, 孙祥德, 赵俊环, 等. 中国现代医学杂志), 2006, 16(3): 387
[15] Wang H. Journal of North Pharmacy (王慧. 北方药学), 2014, 11(2): 18
[16] Liu W Y, Xu Q, Sheng L S, et al. Journal of China Pharmaceutical University (刘文英, 许茜, 盛龙生, 等. 中国药科大学学报), 1990, 21(1): 31
Determination of inorganic anions and gluconate by two-dimensional ion chromatography
CHEN Ailian, DING Hui, FANG Linmei, SHI Chaoou*
(AnalysisandTestingCenter,EastChinaUniversityofScienceandTechnology,Shanghai200237,China)

two-dimensional ion chromatography; conductivity; pulsed amperometric; inorganic anion; gluconate
10.3724/SP.J.1123.2015.08036
2015-08-31
O658
A
1000-8713(2015)12-1333-05
* 通讯联系人.E-mail:shico@ecust.edu.cn.

