采用前驱体混合烧结法制备的LiCoO2的 电化学性能
涂 健,赵孝连,周铁刚,李枝贤,向黔新,董 侠
(1. 湖南立方新能源科技有限公司,株州 412007; 2. 深圳振华新材料有限公司,深圳 518102; 3. 东莞新能源有限公司,东莞 523080)
自1990年商业化以来,锂离子电池由于其高能量密度、高功率、长寿命,无记忆效应及高效率的优点,被广泛应用在便携式的消费类电子产品上[1]。而随着化石能源的危机和温室效应,锂离子作为一种绿色环 保的储能方式,成为电动车以及大中型储能系统的选择,具有广阔的市场前景[2]。
20多年以来,锂离子电池的能量密度增加了2倍,但仍远远落后于下游产业对能量密度要求。 大量的新材料及新的研究方向期望能够突破每年6%~ 8%的增长,如正极上高容量的富锂Li2MnO3-LiMO2、高电位的LiNi0.5Mn1.5O4、Li3V2(PO4)3等[3-6],负极上的Si、SiO、Sn等[7-10],但目前以LiCoO2或Li(NiCoMn)O2为主的正极材料,仍主导着商业化的锂离子电池在便携式电器上的应用。另一个困扰锂电池的问题是价格和安全性。Co作为一种昂贵的战略物资,决定了LiCoO2的高价格。尽管Li(NiCoMn)O2,尤其是高Ni含量的 LiNi0.5Mn0.3Co0.2O2具有价格较低(低30%~40%)、安全性好的优点[11],但由于其较低的压实密度和首次效率,导致其体积能量密度低于LiCoO2的8%~10%,因此影响材料的广泛应用。如何有效地利用Li(NiCoMn)O2的成本优势并进一步改善其能量密度也成为目前锂电池产业的研究方向。目前,将LiCoO2及Li(NiCoMn)O2进行物理混合来降低成本是相关研究的主流,但均会造成能量密度的损失。此外,KIM等[12]采用高Ni三元材料LiNi0.8Co0.1Mn0.1O2与LiCoO2混合,能够有效地改善锂离子电池正极材料的过充安全性能,但并未对其安全改善的原因做进一步分析。
本文作者采用的合成方法有别于简单将LiCoO2及Li(NiCoMn)O2两种材料物理混合的方法,而是通过直接将LiCoO2及LiNi0.5Mn0.3Co0.2O2前驱体按一定比例混合烧结,形成了一种具有协同效应的正极材料,在保证其高能量密度的同时,能够极大地改善该材料的电化学性能及安全性能。
1 实验
将LiOH、Co(C2O4)或Co、Ni、Mn的草酸盐按一定的化学计量比配比共沉淀后,采用溶胶-凝胶法制备Li与过渡金属氧化物的均匀混合物,在400 ℃保温4 h,然后单独烧结将两种材料的前驱体按比例球磨混合均匀后,升温到800 ℃,保温20 h制成LiCoO2、LiNi0.5Mn0.3Co0.2O2(NMC)和 60%LiCoO2-40%LiNi0.5- Mn0.3Co0.2O2复合试样(简称复合试样)[13]。将合成的试样在充满氩气的手套箱中组装成CR 2025型纽扣电池,并与单独烧结及物理混合的材料进行对比。其中正极膜的组成为85%复合试样、5%乙炔黑、10%聚偏二氟乙烯(PVDF) (质量分数)。将它们混合后以N-甲基吡咯烷酮为溶剂涂覆在铝箔上,对电极为金属锂片,电解液为l mol/L LiPF6/碳酸乙烯酯(EC)+二乙基碳酸酯(DEC)+甲基乙基碳酸酯(EMC)(体积比为1:1:1),隔膜为Celgard聚丙烯/乙烯/丙烯膜三层隔膜。扣式电池的充放电实验均在英国Solatron电化学工作站上进行。聚合物电池的容量为1600 mA·h (电芯型号为4.6 mm×44 mm×62 mm)。循环寿命测试时充、放电倍率为1.0C,充、放电电压范围为3.0~4.2 V。
试样的X射线衍射实验在D/MAX-2550PC型X射线衍射仪上进行,管电压为50 kV,管电流为300 mA,用Cu靶Kα,λ=0.154056 nm,步宽为0.02°,停留时间为0.2 s,扫描范围2θ为15°~85°。采用美国FEI公司生产的SIRION型FESEM分析试样的显微组织。采用Phoenix型X射线能量散射谱仪测量试样中Co、Ni、Mn和O的含量。试样的热分析在NETZSCH STA449F3型热分析仪上进行,将试样用DMC洗去电解液,并在20~450 ℃的温度范围内进行分析,升温速度为10 ℃/min。
2 结果与讨论
2.1 结构分析
图1所示为各试样的XRD谱。由图1可以看出,各试样呈现出完好的R3m层状结构,并无其他杂相出现。复合试样的衍射是前两者衍射峰的叠加。由于混合烧结后,可能会导致过渡金属元素如Co、Ni、Mn等相应在NMC及LiCoO2颗粒表面的扩散,这部分内 容将在后续做进一步的测试分析。

图1 不同试样的XRD谱 Fig.1 XRD patterns of different samples: (a) LiCoO2; (b) NMC; (c) Compound sample
图2 所示为LiCoO2、NMC与复合试样的SEM像。由图2可见,LiCoO2颗粒为结晶良好的层状结构,NMC则为多晶颗粒的团聚体。而从复合试样的SEM像中可以清楚地看到NMC多晶颗粒和LiCoO2类单晶颗粒部分融合,而能谱数据也表明图2中的多晶颗粒为NMC颗粒。这说明经过两种前驱体的混合高温烧结,LiCoO2和NMC的部分颗粒融合在一起,这种融合能有效地通过LiCoO2来改善NMC的导电性能,从而改善复合试样的电化学性能。
图3所示为复合试样极片的全电池经过水磨抛光后的截面SEM像。从图3中也可以看出,由大颗粒的LiCoO2搭建了一个三维的立体导电网络,实现了从极片到每个颗粒的电子传输(如图3中粗黑线所示)。

图2 不同试样的SEM像 Fig.2 SEM image of different samples: (a) LiCoO2; (b) NMC; (c) Compound

图3 水磨抛光后复合试样的截面SEM像 Fig.3 Cross-section SEM image of compound sample after polishing
尽管电池工艺过程中的搅拌及对辊工艺可能会破环融合,但材料制作过程多次混合所产生的均匀性, 可以增强整体的导电性能和结构稳定性,进而改善复合试样的电化学性能,如极化和循环稳定性。
2.2 电化学性能
图4所示为LiCoO2、NMC、物理混合的LiCoO2和LiNi0.5Mn0.3Co0.2O2试样以及复合试样在0.1C的充放电曲线。表1所列为各试样的克容量、压实密度、平均电位及体积能量密度。相比较而言,复合试样除了具有156 mA·h/g的克容量,高于物理混合试样的(146 mA·h/g),接近NMC试样的;同时,复合试样还拥有比物理混合试样更高的放电平台。复合试样的充放电曲线明显的分为两个阶段。这种特点在放电曲线上表现更加明显:在放电初期,NMC约60%曲线与LiCoO2试样放电曲线几乎完全重合;在后续的放电过 程中,约40%放电曲线接近NMC的放电曲线。这表明复合材料中的两种材料在脱插锂的过程中可能存在次序性, 这与物理混合材料的混合脱插锂过程不同。这种差异性应该来自于晶体的融合和元素的扩散,其差异性原因有待于进一步分析。

图4 不同试样在0.1C的首次充放电曲线 Fig.4 Charge-discharge curves of different samples at 0.1C: a—LiCoO2; b—NMC; c—Sample physically mixed with LiCoO2 and NMC; d—Compound

表1 不同试样的性能参数 Table1 Performance parameters of different samples
图5所示为用复合试样制成的1.6 A·h的聚合物锂离子电池在常温和45 ℃时1C/1C充放电倍率下的循环性能曲线。复合试样在聚合物全电池中的克容量为151~152 mA·h/g,显示出优良的循环性能。其在常温和45 ℃下循环500次,容量保持率仍在85%以上。这说明通过混合烧结,不但改善了材料的克容量,同时也稳定了材料的电极结构。
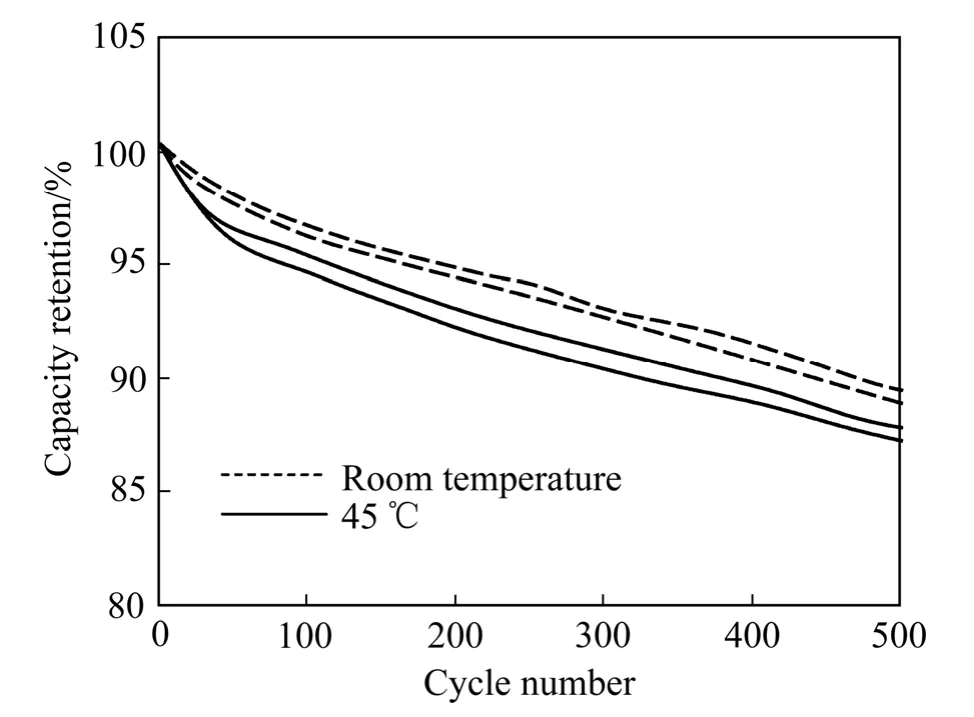
图5 1C/1C充/放电倍率下复合试样在常温和45 ℃的循环性能 Fig.5 Cycling behavior of compound at room temperature and 45 ℃ with 1C/1C charge-discharge rate
2.3 安全性能
图6 所示为不同试样满充状态的TG-DSC曲线。通常热分解反应受充电状态、合成反应、试样准备条件、平均粒径大小以及电解液的影响。图6中曲线1所示的与VELUCHAMY等[14]和KWEON等[15]所研究的结果基本一致。放热反应主要在3个阶段:在100 ℃时,放热来自于SEI膜的分解;在200 ℃时,放热来自于电解液及电解液与正极材料的反应;在300 ℃时,放热来自于正极材料的塌陷。由图6可以看出,复合材料放热峰的强度比其它两种材料的均有降低,尤其是在200 ℃左右的放热峰得到了明显的抑制;此外,由热重曲线也可以看出,复合材料的释氧量也比LiCoO2的明显减少,表明热安全性得到明显改善。

图6 不同试样满充状态的TG-DSC曲线 Fig.6 TG-DSC curves of different samples at full charged state: 1—NMC; 2—Compound; 3—LiCoO2
图7 所示为1.6 A·h 464462聚合物电池进行1C/12 V过充测试曲线。从图7(b)可见,整个过程分为4个阶段[16-17]: 第Ⅰ阶段为锂离子插层进入石墨中,这是一个吸热的过程,与电池的焦耳热相抵,温度只是略微降低;第Ⅱ阶段电压在4.3 V以上,由于过充导致锂枝晶在阳极表面形成,正极氧化物发生不可逆的脱锂,温度基本不变;第Ⅲ阶段为在正极材料与电解液反应,电解液不断氧化产气,电池产生鼓胀,伴随着SEI的分解和阳极电解液的反应;第Ⅳ阶段为随着电解液的分解,电池内阻不断增加,同时正极材料由于结构塌陷,释氧的剧烈放热,升温速度加快,直到内阻增加到使电压达到12 V的虚电位时,过充实验结束。其中,第Ⅳ阶段最为关键。对比图7(a)和(b)可知,由于复合材料在过充时结构的稳定性和热安全性增加,有效地降低了在第Ⅳ阶段时的剧烈放热,使其散热速度大于其放热速度,从而通过了过充滥用测试。而纯LiCoO2则因为产热过快无法散开,引发阳极上Li和氧气及电解液反应,导致热失控而燃烧。

图7 不同样品1.6 A·h聚合物电池的1C/12 V过充曲线 Fig.7 1C/12 V overcharge curves of 1.6 A·h polymer cell with different samples: (a) LiCoO2; (b) Compound
3 结论
1) 利用前驱体混合烧结的方法合成了LiCoO2和LiNi0.5Mn0.3Co0.2O2的复合材料,并与简单物理混合材料进行了比较。XRD分析表明合成复合材料为标准层状结构。
2) 从复合材料中两个组分结晶产生了粘连或融合。由于融合的存在,复合材料的导电性较混合材料的得到了明显的改善。电化学性能分析表明:该材料的克容量远远超过了物理混合材料的,达到156 mA·h/g (半电池),全电池的容量也达到151 mA·h/g。由于其4.0 g/cm3的压实密度,在其体积能量密度与LiCoO2的相当的水平下,其成本比LiCoO2降低15%~20%。
3) 该复合材料显示出良好的循环性能和安全性能,制成的464462聚合物锂离子电池在常温和45 ℃下循环500次,容量保持率在85%以上,而且通过了1C/12 V过充滥用测试。
[1] NAGAURA T,TOZAWA K. Lithium ion rechargeable battery[J]. Prog Batteries Sol Cells,1990,9: 209-211.
[2] NOTTER D A,GAUCH M,WIDMER R,WAGER P,STAMP A,ZAH R,ALTHAUS H. Contribution of Li-ion batteries to the environmental impact of electric vehicles[J]. Environ Sci Technol,2010,44(17): 6550-6556.
[3] THACKERAY M,KANG S,JOHNSON C S,VAUGHEY J T,BENEDEK R,HACKNEY S A. Li2MnO3-stabilized LiMO2(M=Mn,Ni,Co) electrodes for lithium-ion batteries[J]. J Mater Chem,2007,17: 3112-3125.
[4] 屈超群,魏英进,姜 涛. 聚阴离子型锂离子电池正极材料Li3V2(PO4)3的研究进展[J]. 无机材料学报,2012,27(6): 561-567.
QU Chao-qun,WEI Ying-jin,JIANG Tao. Research progress in Li3V2(PO4)3as polyanion-type cathode materials for lithium ion batteries[J]. Journal of Inorganic Materials,2012,27(6): 561-567.
[5] ZHENG J M,ZHANG Z R,WU X B,DONG Z X,ZHU Z,YANG Y. The effects of AlF3coating on the performance of Li[Li0.2Mn0.54Ni0.13Co0.13]O2positive electrode material for lithium ion battery[J]. J Electrochem Soc,2008,155(10): 775-782.
[6] MAKIMURA Y,OHZUKU T. Lithium insertion material of LiNi1/2Mn1/2O2for advanced lithium-ion batteries[J]. J Power Sources,2003,119/121: 156-160.
[7] SCROSATI B,HASSOUN J,SUN Y K. Lithium ion batteries. A look into the future[J]. Enery Environ Sci,2011,4(9): 3287-3295.
[8] GREEN M,FIELDER E,SCROSATI B,WACHTLER M,MORENO J S. Structured silicon anodes for lithium battery application[J]. Electrochem Solid-Sate Lett,2003,6(5): 75-79.
[9] MAGASINSKI A,DIXON P,HERTSBERG B,KVIT A,AYALA J,YUSHIN G. High-performance lithium ion andoes using a hierarchical bottom-up approach[J]. Nature Material,2010,9(4): 353-358.
[10] KASAVAJJULA U,WANG C,APPLEBY A J. Nano- and bulk- silicon-based insertion anodes for lithium ion secondary cells[J]. J Power Sources,2007,163(2): 1003-1039.
[11] 马全新,孟军霞,杨 磊,曹 文. 锂离子电池正极材料LiNi0.5Mn0.3Co0.2O2的制备及电化学性能[J]. 中国有色金属学报,2013,23(2): 456-462.
MA Quan-xin,MENG Jun-xia,YANG Lei,CAO Wen. Preparation of Li ion battery cathode material LiNi0.5Mn0.3Co0.2O2and its electrochemical performances[J]. The Chinese Journal of Nonferrous Metals,2013,23(2): 456-462.
[12] KIM J,NOH M,CHO J. Improvement of 12 V overcharge behavior of LiCoO2cathode material by LiNi0.8Co0.1Mn0.1O2addition in a Li-ion cell[J]. J Power Sources,2006,153(2): 345-349.
[13] 向黔新,赵孝连. 多晶钴镍锰三元正极材料及其制备方法,二次锂离子电池. 中国,200910110132.9[P]. 2009-11-09.
XIANG Qin-xin,ZHAO Xiao-lian. The synthesis of NMC triple oxide cathode material,Secondary lithium ion batteries. China 200910110132.9[P]. 2009-11-09.
[14] VELUCHAMY A,DOH C,KIM D,LEE J,SHIN H,JIN B,KIM H,MOON S. Thermal analysis of LixCoO2cathode material of lithium ion battery[J]. J Power Sources,2009,189(1): 855-858.
[15] KWEON H,PARK J,SEO J J,KIM G,JUNG B,LIM H. Effects of metal oxide coatings on the thermal stability and electrical performance of LiCoO2in a Li-ion cell[J]. J Power Sources,2004,126(1/2): 156-162.
[16] OHSAKI T,KISHI T,KUBOKI T,TAKAMI N,SHIMURA N,SATO Y,SEKINO M,SATOH A. Overcharge reaction of lithium-ion batteries[J]. J. Power Sources,2005,146(1/2): 97-100.
[17] HIROAKI K,TOYOTAKA Y,NASANORI Y. Thermal stability of Li1-yNixMn(1-x)/2O2layer-structured cathode materials used in Li-ion batteries[J]. J Power Sources,2011,196(16): 6884-6888.

