磁性纳米流体及其终端技术应用
孙爱娟,方 芬
(宁夏大学 化学化工学院,银川 750021)
磁性纳米流体及其终端技术应用
孙爱娟,方 芬
(宁夏大学 化学化工学院,银川 750021)
综述了磁性纳米粒子制备技术的发展,重点讨论了磁性纳米粒子形成磁流体过程在极性或非极性载液中稳定悬浮的机理和磁性纳米流体的终端技术及其应用进展,并指出今后磁性纳米流体技术的研究工作应包括磁性纳米流体性能的主要影响因素、磁性纳米粒子与基液间的相容性、高温和长期使用条件下磁性纳米流体的稳定性以及添加剂的形状和属性对磁性纳米流体性能的影响等方面。
磁性纳米流体;制备方法;分散机理;终端技术
磁性纳米流体是兼具液体属性和磁性的新型智能纳米流体,同时也是一种三组分的胶体稳定体系。该体系通常由超顺磁性纳米粒子、载液及表面活性剂组成。载液是磁性纳米流体的主要组成部分,体系的黏度主要取决于载液的类型。磁性纳米粒子决定磁流体的饱和磁化强度。而磁性纳米粒子能否稳定分散在载液中取决于表面活性剂的分子结构、粒子表面电荷及其与流液的匹配性。此外,制备磁性纳米流体主要步骤包括:(1)制备超顺磁性纳米粒子;(2)表面活性剂修饰纳米粒子并将其分散在非极性或极性载液中。
一些特殊的磁性纳米流体也可由合成高分子[1,2]、二氧化硅[3]、生物大分子[4]等将磁性纳米粒子改性后分散在载液中获得。水基磁性纳米流体无需表面活性剂,只需将磁性纳米粒子进行离子化处理[5],使其表面带电荷,然后分散在水基载液中。
磁性纳米流体具备固体磁铁所没有的流动性,这为磁性材料的应用开辟了新的篇章。其潜在的应用领域涵盖机械、生物医学和光学行业。目前磁性纳米流体的终端应用技术包括无泄漏密封、智能冷却、微型机器人、微机械传感器、传感器、可调光学无损缺陷过滤器、致动器、光学光栅、磁光波导、磁光波长滤波器、光开关、生物传感器、热疗治疗、肿瘤治疗、细胞分离、磁共振成像、药物靶向等技术[6]。本文将详细介绍磁性纳米粒子的制备方法,磁性纳米流体的稳定机理及其部分终端应用技术。
1 磁性纳米粒子的制备
1.1 机械化学合成法
在表面活性剂的存在下通过球磨机研磨是制备磁性纳米粒子[7]最早的方法。采用该方法获得的磁性粒子粒度分布较宽,通常需要离心分离去除大颗粒,否则可能导致磁流体凝聚和沉淀。该方法的缺点还在于研磨时间太长(1000h)。目前,机械化学合成法经改进后仍被用来制备磁性纳米粒子。Bellusci等[8]使用高能球磨机在柠檬酸存在下制备锰铁氧体纳米粒子。经1h研磨便可产生直径约8nm的单晶体磁性纳米粒子。该纳米粒子呈超顺磁性且因均匀包覆柠檬酸而具有生物相容性。
1.2 共沉淀法
共沉淀法是制备氧化铁磁性纳米粒子最常用的方法。该方法的优点是可通过控制实验条件来制备不同粒径(3~20nm)的磁性纳米粒子。大量研究证明[9,10],Fe3+和Fe2+的浓度与摩尔比,碱及其浓度是决定粒子大小的关键因素。沉淀温度,在碱性介质中加热沉淀以及在反应混合物中添加表面活性剂对粒径也会产生影响[11]。当未改性的磁性纳米粒子在碱性介质中加热,其粒径增加,增加的程度取决于粒子加热温度。在不加碱的情况下提高沉淀温度(2~90℃),粒子粒径也会增加。在Fe3+和Fe2+摩尔比约为2 ∶1的水溶液中加碱可制备Fe3O4纳米粒子[12]。Danescu等[13]将FeCl3·6H2O和FeSO4·7H2O两种盐以摩尔比Fe2+∶Fe3+= 1 ∶2混合后溶于300mL水中,加入质量分数为10%的NaOH溶液并加热到80℃。生成的Fe3O4沉淀用0.1mol/L的盐酸反复清洗后分散在油酸中形成混合液,将混合液加入到绝缘油中制成磁流体。Fe3O4纳米粒子,油酸,绝缘油的体积分数分别为5%,10%,85%。而制备γ-Fe2O3的方法相对简单,在Fe3O4纳米粒子中加入0.34mol/L硝酸铁并加热到90℃保持30min便可将Fe3O4纳米粒子[14]氧化制得纳米γ-Fe2O3。
用一种或几种二价金属离子如Co2+,Mn2+, Ni2+, Zn2+等全部或部分取代Fe2+可制备取代的铁氧体纳米粒子。Li+也可以用来制备取代铁氧体。部分采用共沉淀法制备的取代铁氧体纳米粒子如表1所示。

表1 部分取代的铁氧体纳米粒子
采用共沉淀法制备Fe3O4纳米粒子与取代铁氧体纳米粒子在原理上是相同的。但二者的磁性能差异较大[30]。因此,通过共沉淀法可以定制不同性质的磁性纳米粒子,以满足不同的应用需求。例如,需要高磁晶各向异性的粒子,钴铁氧体[11]是最佳选择;若在热磁对流和热传导[31]、热电转换[25]方面应用,可制备具有强烈热磁效应和较低居里温度的取代铁氧体。
1.3 水热法
水热还原法[32]制备水分散型Fe3O4纳米粒子大小可控,而且具有成本低、环境友好等特点。在水热合成磁性纳米粒子的过程中可以加入表面活性剂进行粒子表面改性,特别适合制备生物相容性的磁性纳米粒子[33]。Behdadfar等[34]利用一步水热合成法制备了平均粒径为10nm柠檬酸修饰的锌取代铁氧体纳米粒子(ZnxFe3-xO4)(x=0,0.25,0.3,0.37,0.4)。结果表明:一定量的柠檬酸有助于获得单晶型锌取代Fe3O4纳米粒子。柠檬酸作为调节剂和还原剂可以控制粒子大小并促进尖晶石晶体结构的形成。
1.4 微乳液法
Fe3O4或γ-Fe2O3纳米粒子也可由微乳液法制备[35]。该方法需要借助表面活性剂制备两种微乳液:一种含有金属盐溶液,另一种含有碱溶液[36];以适当的比例将这两种微乳液混合并反应得到磁性纳米粒子。微乳液法的缺点是用于合成的表面活性剂与流液可能不匹配。
1.5 有机金属化合物热分解法
有机金属化合物热分解法是制备铁、钴纳米粒子等高磁化率磁性纳米粒子的重要方法。通过改变反应混合物及合成条件,能够对纳米粒子的组成、尺寸及尺寸分布进行精确控制[37]。羰基铁/钴、乙酰丙酮铁/钴以及铁和钴的羧酸盐络合物都可作为前驱体制备铁、钴及其氧化物的单分散纳米粒子。在油酸的存在下通过分解溶解在辛醚中的五羰基铁可获得高度单分散的γ-Fe2O3纳米颗粒[38]。粒子的平均粒径为(4.9±0.7)nm。其中94%的粒子尺寸为3.5~5.75nm,所有粒子均小于8nm。80~90℃时[39],在3000mL甲苯中加入171g Co2(CO)8和88mL Al(C8H17)3并加热到110℃反应18h。将反应混合物冷却至室温,由一个小的毛细管导入空气对粒子进行钝化处理,可得到Co纳米粒子,该粒子可制备磁化强度较高的磁流体。
2 磁性纳米粒子分散在极性或非极性载液中稳定悬浮机理
磁性纳米流体是稳定的胶体分散体系。胶粒的质量远远大于分子。因此,在重力的影响下胶粒会发生沉积。但磁流体中纳米粒子粒径足够小,可以像分子一样进行布朗运动,从而抵消了由重力作用引起的沉积。然而,胶粒间由于范德华力会相互吸引且每个磁性纳米粒子都具有磁性,粒子间的静磁相互作用也会破坏胶体的稳定性。若要获得稳定的胶体分散体系就必须增加胶粒间的斥力作用。一般而言,这种斥力作用来自于粒子间的静电排斥和物理隔绝。因此磁性纳米流体的稳定分散机理可分为静电稳定、位阻稳定和静电位阻稳定三种机理。
位阻稳定即磁性纳米粒子经表面活性剂修饰后,其分子链会在粒子间形成物理屏障从而增强空间排斥[40]。如果粒子分散在非极性介质中,表面活性剂亲油端在粒子表面形成一个外部疏水层,起到粒子间物理隔绝作用。磁性纳米粒子若是分散在极性介质中,在粒子表面会生成一个双层表面活性剂吸附层从而形成外部亲水层,起到位阻稳定作用。另外,如果表面活性剂极性端是阴离子或阳离子,那么这个双层表面活性剂吸附层使纳米粒子表面带正电荷或负电荷,粒子稳定悬浮来源于静电、位阻稳定双重作用。图1为磁性纳米粒子吸附表面活性剂分子模型[41]。

图1 磁性纳米粒子吸附表面活性剂分子模型(a)单层吸附模型;(b)双层吸附模型[41]Fig.1 Sketch of magnetic nanoparticles adsorbed surfactant molecules (a)single-layered grains;(b)double-layered grains[41]
静电稳定模型如图2所示。对于水基磁性纳米流体可采用四甲基氢氧化铵来促进纳米粒子稳定悬浮。四甲基氢氧化铵的氢氧根首先吸附到磁性纳米粒子表面并与四甲基铵阳离子形成双电层,使粒子间由于静电斥力而稳定[42]。

图2 静电稳定型磁性纳米流体模型[42]Fig.2 Static stable magnetic nano-fluid model[42]
将表面离子化的磁性纳米粒子分散在水中也可制得静电稳定型磁流体。离子化的纳米粒子表面带电荷,由于静电排斥使胶体系统保持稳定。这类磁流体载液通常为水,粒子的表面电荷取决于pH值的大小(pH值介于2~12之间)。酸性磁流体(pH<7)粒子表面带正电,而碱性磁流体(pH>7)粒子表面带负电。图3为表面带正电荷和表面带负电荷的磁性纳米粒子[43]。

图3 离子化的磁流体粒子 (a)带正电荷粒子;(b)带负电荷粒子[43]Fig.3 Ionization of magnetic particles(a)positively charged particle;(b)negatively charged particle [43]
3 磁性纳米流体的终端技术
3.1 微流控技术
磁性液体的流量可通过磁场进行调节。基于此特性,磁流体已被广泛应用于高压密封和冷却液中。然而,最近磁流体又被用于微流控制装置的开发。其中有关诊断、药物输送、基因测序及芯片实验室的微流控技术引起了各国研究者的极大关注[44]。实际上,兼具可靠性、准确性和低成本的一次性微流控设备仍然面临巨大的挑战。开发新的具备高可靠性(对抗振动)和灵活性(可在原管道进行)尤其是当尺寸严重萎缩(例如,微电机械系统)情况下的微流控技术是急需解决的问题之一。Ando等[45]制作了一种新颖的磁流体泵(FP1泵)。 该泵不需要任何机械运动部件,而是由一滴铁磁流体作为活性物质来实现流体控制。FP1泵具备一定的灵活性和适用性,可在不破坏原有管道的情况下安装此泵,能在紧急却必须安装的特殊情况 (如血管外科)下使用。图4为FP1泵的原理和模型,可以看出磁流体由永久磁铁吸引可以平铺在玻璃管壁内,使管内液体顺利通过;也可因电磁体和线圈作用在玻璃管内形成帽型液体阀或活塞进而限制管内液体通过。

图4 FP1泵设计原理和模型[45]Fig.4 Schematic of the proposed design for FP1 pump architecture[45]
微流体控制是“芯片实验室”的关键技术。开发集成的多功能微化学反应堆和分析平台取决于芯片上的阀门和泵。Hartshorne等[46]将玻璃槽焊接盖板,然后超声钻洞制得微流体泵控制设备。该设备包含由外部磁铁驱动的长度约为10mm的铁磁流体塞。该铁磁流体是以疏水性氟碳化合物为流液的胶体稳定体系。若微通道中流体为空气,此微流控设备能够承受的压力可达12kPa,开启和关闭阀门的压力分别为8.5kPa和5.0kPa。该设备的原理如图5所示,微通道内黑色部分为铁磁流体,小磁盘代表永久磁铁。箭头代表流体流动方向。实验证明磁流体泵微流控设备可用空气作为流体,并可达到“芯片实验室”所需压力。同时,该设备可以用作气相微反应器或作为微通道网络内的压力源驱动液体流动。

图5 磁流体井阀和Y阀设计及关闭和打开配置[46]Fig.5 Well valve and Y-valve designs in closed and open configurations[46]

图6 热磁泵原理图[47]Fig.6 A schematic diagram of the thermomagnetic pump[47]
磁性纳米流体的饱和磁化强度随温度的升高而显著减小,因此其热磁对流现象十分明显。处于外磁场和非等温状态下的磁流体内部会产生磁力的不平衡状态,从而驱动流体做宏观对流运动。通过外磁场和温度场的协同作用,可以实现对磁流体的流动控制。Pal等[47]通过焊接方法制作了一种微型热磁泵,可通过施加适当的温度和磁场来驱动铁磁流体在一个直径为2cm的玻璃毛细管内流动而不需要借助任何外部压力。在一个密封的微型机电系统中便可操作这样的泵运行而无需任何活动部件。该泵能够处理微流体样品且样品不会受到污染。图6所示为热磁泵原理图,热磁泵含电磁线圈可使在毛细管中的铁磁流体暴露在磁场中,在管壁内还包含一个小的电阻加热器来提供温度梯度。当开启电磁线圈和电阻加热器,磁流体便从毛细管的冷端传递到暖端。研究结果表明,该泵能产生的压头高达2.75cm,而其最大输出量则高达0.02mL/s等同于 1200mL/min。该热磁泵比另外两种磁场驱动泵拥有更精确的流量控制和更高的流速,同时输出量更高而所需电压和磁场强度更低。
以流体传递为目的新型微流控系统,是医学和生物学领域中微型全分析系统(I-TAS)的核心设备。Ahn等[48]设计的微射流控制装置(如图7所示),以精确驱动和快速采样为目的,实现了样品采集在纳升范围。铁磁流体被注入圆形通道,而取样液体注入直通道。磁流体与取样液体间充满空气。因此,在取样过程中避免了样品受到污染。永磁步进电机可以控制磁流体在一定磁场梯度作用下流过圆形通道。这样取样液体在直通道内也流经相同的距离,由此完成了样品采集。控制样品采集的核心是电机的步进角,为了采样在纳升水平,该设备的步进角设计为18°。研究结果还表明,铁磁流体在圆形微通道流动的最大净压力超过2kPa。
3.2 体内治疗技术
磁流体用作体内高热治疗的研究始于1993年Chan等[49]和 Jordan等[50]的研究工作。 实验证明超顺磁性的纳米流体能吸收交变磁场的能量并将它转化为热量。由于肿瘤细胞比正常细胞对温度更敏感[51,52]。
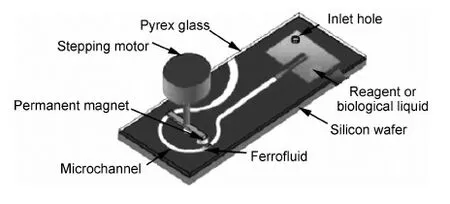
图7 铁磁流体微流体控制系统的原理[48]Fig.7 A schematic of the microfluidic control system using ferrofluid[48]
因此,可以利用磁流体外加交变磁场增加肿瘤组织的温度来破坏病理细胞,达到治愈肿瘤的目的。在所有的高热治疗方式如微波、激光和超声波治疗中,磁性纳米流体高热疗法对目标肿瘤细胞的选择性最好。这样可以减少化疗和放疗剂量从而减少治疗的毒副作用。磁性纳米流体进行体内高热治疗可分为以下三个步骤(如图8所示):(1)磁性纳米流体进入肿瘤或癌症组织;(2)施加几百千赫的交变磁场;(3)肿瘤或癌细胞凋亡。

图8 磁性纳米流体的高热治疗示意图[50] (a)施加外部磁场的高热治疗模型;(b)将磁液注入肿瘤或癌症病灶Fig.8 Schematic illustration of magnetic nano-fluid hyperthermia[50] (a)hyperthermia model by applying an external magnetic field;(b)feeding magnetic fluid to tumor or cancer
其中磁性纳米流体如何进入肿瘤组织成为治疗的关键。一般来讲,磁性纳米流体以四种方式进入肿瘤组织:(1)动脉注射:磁性纳米流体从动脉注入并通过血管到达肿瘤部位;(2)直接注入:磁流体直接注射到肿瘤部位。粒子被直接固定在肿瘤组织,并且大多数粒子位于细胞间隙而小部分在血管或细胞内[53]。因此,当开启磁场时热量大多在细胞外部产生。直接注入法还可以将磁性纳米粒子用特定的肿瘤抗体修饰,然后进行注入治疗[54-56],以便它们有选择地被肿瘤细胞所吸收,从而减少正常细胞的损失;(3)原位移植[57]:采用可注射的磁性纳米凝胶原位移植至病灶组织并由体外磁诱导产生局部高热,作为癌症微创治疗的方法之一;(4)靶向输入:将磁性纳米粒子表面修饰一种肿瘤特异性抗体[58]。当这些磁性纳米粒子进入血管,粒子会在磁场引导下寻找肿瘤组织并绑定具体的目标受体[59]。
由pH 和温度敏感聚合物(如嵌段共聚物和共聚物水凝胶)与磁性纳米粒子结合可形成具备磁芯生热和多响应性壳层的智能治疗体系[60]。通过药物与磁流体绑定进行热疗和药物治疗已经潜在地增强了高热治疗的效果[61]。而若将药物封装在具有温度敏感性的壳层内,则药物如加包衣一样在到达病灶区域时,磁芯温度增加(由交变磁场作用)导致热敏聚合物分子结构或构象发生变化(共价或非共价键遭到破坏)。壳层崩塌,使药物只在癌变区域释放[62,63](如图9所示)。具有pH敏感性的聚合物也可用于目标病灶组织的治疗[60]。
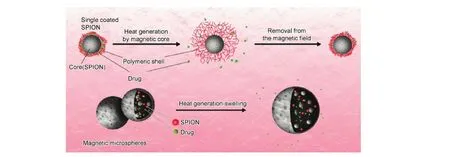
图9 高热和药物治疗相结合的多功能治疗系统[60]Fig.9 Popular multi-purpose systems in hyperthermia and drug delivery[60]
3.3 分离技术
在许多化学和生物应用领域常常需要对粒子和细胞进行分离。根据粒子属性如大小、密度、电荷和形状等提供外部或内部诱导力包括电[64]、磁[65]、声[66]、光[67]和水动力[68]就能实现粒子的连续分离。然而,对颗粒进行连续分离的多数方法需要昂贵的设备或设备构造极为复杂。相比之下,磁性纳米流体分离技术不仅成本低廉(廉价磁铁),而且没有液体加热的问题[69]。Zeng等[70]提出了利用磁场诱导分离非磁性粒子和细胞的简单方法。该方法凭借一个直微通道和一对永磁铁能够对与磁流体混合的非磁性颗粒或细胞进行连续分离。第一块磁铁放置在离微通道500mm的位置上,用来使所有粒子聚集。第二块磁铁放置在离微通道2600mm的位置上,使粒子按粒径大小进行分流。图10所示为磁场诱导粒子分离装置。磁流体的平均流速为0.6mm/s。 图10中a,c分别为进出微通道粒子的分布图像。图10b为实验(顶部行)和理论(底行,红色线为10mm颗粒和绿色线为3mm颗粒)两方面,粒子在b1,b2,b3,b4四个观察窗的运动轨迹。箭头指示方向为粒子流动方向。结果表明,实验数据与预测的分析模型相吻合。在相同的设备中还实现了活酵母细胞和10μm聚苯乙烯粒子的连续分离。

图10 连续磁分离装置分离3mm和10mm聚苯乙烯粒子示意图[70]Fig.10 Illustration of the continuous magnetic separation device for 3mm and 10mm polystyrene particles[70]
Zhu等[71]利用在静磁场中的一个微流体装置对非磁性微粒进行分离。经测试该分离装置可分离1μm和9.9μm,1.9μm和9.9μm,3.1μm和9.9μm的混合粒子。处理量为105个粒子/h,分离效率接近100%。该方法具有成本低、处理量大、高效并且无需标记的特点。相同的装置还可用来分离大肠杆菌、酿酒酵母[72],处理量为107个细胞/h,分离效率接近100%。
3.4 其他磁控设备
Baglio等[73]应用磁性纳米流体设计了一种新颖的惯性传感器,该传感器具有较宽的可调工作范围及高灵敏度。具体装置是由一个激励线圈和两个内部传感线圈缠绕一个含磁流体的玻璃管组成,如图11所示。激励线圈产生偏离中心的磁力,从而吸引磁流体偏离管的中心,其作用等效于机械弹簧。惯性质量振荡振幅由内置的差动变压器的输出电压决定,该电压是磁流体凝聚位置的函数。在该传感器的基础上还可以进行谐振加速计和陀螺仪的设计。

图11 磁性纳米流体惯性传感器示意图[73]Fig.11 Schematic view of the ferrofluidic accelerometer for tilting measurements[73]
Bibo等[74]使用磁流体设计制作了一个小型电磁发电机进行振动能量采集。利用晃动的铁磁流体柱将机械能直接转化为电能。与传统的使用固体磁铁的电磁发电机不同,基于铁磁流体的能量采集器具有一些独特的优势,磁流体易发生形状变化而产生响应很小的加速度,利用这一点可设计能伸缩的能量采集器,如图12所示。该能量采集器可在一些有针对性的场合中应用,从而代替移动的固体磁铁。Bibo等通过实验验证了该能量采集器的可行性,并对其效率进行了讨论。

图12 基于磁流体的能量采集器示意图[74]Fig.12 Schematic diagram of the ferrofluid-based energy harvester[74]
未来微型机器人需要致动器在有限体积内产生高驱动力和冲程。致动器主要的技术壁垒是在高度密封情况下实现低泄露。Devolder等[75]设计了一种基于磁流体密封技术的线性射流微型致动器。如图13所示,致动器密封的原理如下:当驱动压力达到极限值时,致动器左边的铁磁流体密封会失效,并存在一定的泄漏量Q,此时泄露的磁流体流入活塞内的回流通道。而在左边的磁铁限制并降低了作用于右边铁磁流体密封环的压力。因此,有效防止了右边密封环失效而使磁流体泄露于密封室外。该致动器的外径为2mm,长度为13mm,可同时使用压缩空气和水,能够在1.6MPa压力下工作而无泄漏,且其冲程为10mm,最大压力可达到0.65N。

图13 磁流体密封的微型致动器 75]Fig.13 Illustration of a micro actuator with ferrofluid seals[75]
4 展望
研究磁性纳米流体涉及约30个学科领域:理论物理学家描述磁流体复杂的液体行为;化学工程师合成磁性纳米粒子;实验工作者测量流体性质;机械工程师设计磁流体的应用技术设备等。磁性纳米流体技术的进步依赖于各领域的交叉和合作。对于化学工程师而言,磁性纳米流体的发展前景依然广阔,在后续的研究工作中以下方面值得关注:(1)进一步明确磁性纳米流体性能的主要影响因素。迄今为止,不同科研小组获得的相关实验数据有显著差异。因此,系统地研究并确定这些影响因素非常重要,而胶粒详细而准确的结构特征应是最关键的因素之一;(2)黏度大是磁性纳米流体的主要缺点。通过表面修饰调节两相界面性质,可增加纳米粒子和基液之间的相容性以改善磁流体的黏度特性;(3)磁性纳米粒子的悬浮稳定性在科学研究和实际应用中非常关键。尤其是长期使用或经千万次热循环后的稳定性更加值得关注;(4)在已开展的工作中还缺乏对磁性纳米流体在高温下热性能的研究。高温下会加速分散剂的降解,还可能产生更多的泡沫等问题应考虑进去;(5)添加剂的形状和属性与磁性纳米流体的性质密切相关。因此,合成新的显微结构可控的磁性纳米流体将是今后非常重要的研究方向之一。
5 结束语
磁性纳米流体是具有磁性的可流动液体,同时也是包含磁性纳米粒子和载液的非均相胶体稳定体系。该体系的稳定性由粒子间的静电斥力和物理隔绝作用决定。表面离子化和表面活性剂改性可增加纳米粒子间斥力促进胶体体系的稳定。通过改变合成方法和原料可为特定的技术应用量身定做磁性纳米粒子。磁性纳米流体现已用于微流控、传感器、致动器等纳米电动机械系统的设计和制造。而在目前开展的研究工作中仍然存在不确切、不完善、不全面的部分。若能解决上述技术问题,将使磁性纳米流体向更高性能、更多应用以及智能化方向发展。
[1] BRULLOT W, REDDY N K, WOUTERS J, et al. Versatile ferrofluids based on polyethylene glycol coated iron oxide nanoparticles[J]. Journal of Magnetism and Magnetic Materials,2012, 324(11):1919-1925. [2] SONIA G J, JOAN E. Ferrofluid based on polyethylene glycol-coated iron oxide nanoparticles: characterization and properties[J]. Colloids and Surfaces A: Physicochem Eng Aspects,2013, 420:74-81.
[3] CHEN H J, WANG Y M, QU J M, et al. Preparation and characterization of silicon oil based ferrofluid[J].Applied Surface Science,2011, 257(24):10802-10807.
[4] SAFARIKOVA M, MADEROVA Z, SAFARIK I. Ferrofluid modified Saccharomyces cerevisiae cells for biocatalysis[J].Food Research International,2009, 42(4):521-524.
[5] LI J, QIU X Y, LIN Y Q, et al. A study of modified Fe3O4nanoparticles for the synthesis of ionic ferrofluids[J].Applied Surface Science,2010, 256(23):6977-6981.
[6] PHILIP J, LASKAR J M. Optical properties and applications of ferrofluids-a review[J].Journal of Nanofluids,2012, 1(1):3-20.
[7] PAPELL S S. Low viscosity magnetic fluid obtained by the colloidal suspension of magnetic particles[P].US Patent:3215572,1965-02-11.
[8] BELLUSCI M, ALIOTTA C, FIORANI D, et al. Manganese iron oxide superparamagnetic powder by mechanochemical processing.Nanoparticles functionalization and dispersion in a nanofluid[J].J Nanopart Res,2012, 14:904-915.
[9] CABUIL V, NEVEU S, ROSENSWEIG R E. Magnetic fluids bibliography[J].J Magn Magn Mat,1993, 122:437-482.
[10] MASSART R. Preparation of aqueous magnetic liquids in alkaline and acidic media[J].IEEE Trans Mag Mag,1981, 17(2):1247-1248. [11] DAVIES K J, WELLS S, CHARLES S W.The effect of temperature and oleate adsorption on the growth of maghemite particles[J]. J Magn Magn Mat,1993, 122(1-3):24-28.
[12] KHALAFALLA S, REIMERS G. Magnetofluids and their manufacture[P].US Patent: 3764540, 1973-10-09.
[13] PISLARU-DANESCU L, MOREGA A, TELIPAN G, et al. Nanoparticles of ferrofluid Fe3O4synthetised by coprecipitation method used in microactuation process[J].Optoelectronics and Advanced Materials-Rapid Communications,2010,4(8):1182-1186. [14] BEE A, MASSART R, NEVEU S. Synthesis of very fine maghemite particles[J].J Magn Magn Mat,1995,149(1-2):6-9.
[15] VAIDYANATHAN G, SENDHILNATHAN S. Characterization of Co1-xZnxFe2O4nanoparticles synthesized by co-precipitation method[J]. Physica B:Condensed Matter,2008, 403(13-16):2157-2167.
[16] VAIDYANATHAN G, SENDHILNATHAN S. Synthesis and magnetic properties of Co-Zn magnetic fluid[J].Journal of Magnetism and Magnetic Materials,2008, 320(6):803-805.
[17] LO′PEZ J, GONZA′LEZ-BAHAMO′N L F, PRADO J, et al. Study of magnetic and structural properties of ferrofluids based on cobalt-zinc ferrite nanoparticles[J].Journal of Magnetism and Magnetic Materials,2012,324(4):394-402.
[18] UPADHYAY R V, MEHTA R V. Magnetic properties of ultra-fine particles of Mn0.5Fe0.5Fe2O4spinel system[J].Journal of Physics,1993, 41(5):429-442.
[19] ABRAHAM V S, NAIR S S, RAJESH S, et al. Magnetic field induced assembling of nanoparticles in ferrofluidic liquid thin films based on NixFe1-xFe2O4[J].Bull Mater Sci,2004, 27(2):155-161.
[20] NAIR S S, XAVIAR F, JOY P A, et al. Enhanced shape anisotropy and magneto-optical birefringence by high energy ball milling in NixFe1-xFe2O4ferrofluids[J].Journal of Magnetism and Magnetic Materials,2008, 320(6):815-820.
[21] TACKETT R, SUDAKAR C, NAIK G, et al. Magnetic and optical response of tuning the magnetocrystalline anisotropy in Fe3O4nanoparticle ferrofluids by Co doping[J].Journal of Magnetism and Magnetic Materials,2008,320(21):2755-2759.
[22] BHUVANESWARI M, SENDHILNATHAN S. Preparation and Characterization of Cobalt Doped Mn-Zn Ferrites[M]. New Delhi: Springer India,2012.603-609.
[23] ARORA M, KUMAR A, PANT R P. Gd3+substituted of Mn0.5Zn0.5GdxFe2-xO4(x=0.1, 0.2, 0.3, 0.4) ferrites for ferrofluids application[J].Physics Procedia,2010, 9:24-27.
[24] FARAZ A, MAQSOOD A. Synthesis, structural, electrical magnetic curie, temperature and Y-K angle studies of Mn-Cu-Ni mixed spinel nanoferrites[J]. J Supercond Nov Magn,2012, 25(2):509-517.
[25] SANSOM C L, JONES P, DOREY R A, et al. Synthesis and characterization of Mn0.5Zn0.5Fe2O4and Fe3O4nanoparticle ferrofluids for thermo-electric conversion[J].Journal of Magnetism and Magnetic Materials,2013,335:159-162.
[26] GIRI J, PRADHAN P, SOMANI V, et al. Synthesis and characterizations of water-based ferrofluids of substituted ferrites[Fe1-xBxFe2O4,B=Mn, Co (x=0-1)] for biomedical applications[J].Journal of Magnetism and Magnetic Materials,2008, 320(5):724-730.
[27] TOURINHO F, FRANCK R, MASSARTL R, et al. Synthesis and magnetic properties of manganese and cobalt ferrite ferrofluids[J].Progr Colloid Polym Sci,1989, 79:128-134.
[28] WANG L J, GUO C W, YAMANE R, et al. Tribological properties of Mn-Zn-Fe magnetic fluids under magnetic field[J].Tribology International,2009, 42(6):792-797.
[29] KUMAR A, ANNVEER, ARORA M, et al. Induced size effect on Ni doped nickel zinc ferrite nanoparticles[J].Physics Procedia,2010, 9:20-23.
[30] DORMANN J L, NOGUES M. Magnetic structure of substituted ferrites[J].J Phys:Condens Mat,1990, 2(5):1223-1237.
[31] NAKATSUKA K, HAMA Y, TAKAHASHI J. Heat transfer in temperature-sensitive magnetic fluids[J].J Magn Magn Mat,1990, 85(1-3): 207-209.
[32] BEHDADFAR B, KERMANPUR A, SADEGHI-ALIABADI H, et al. Synthesis of high intrinsic loss power aqueous ferrofluids of iron oxide nanoparticles by citric acid-assisted hydrothermal-reduction route[J].Journal of Solid State Chemistry,2012, 187:20-26.
[33] MCCARTHY J R, WEISSLEDER R. Multifunctional magnetic nanoparticles for targeted imaging and therapy[J].Advanced Drug Delivery Reviews,2008, 60(11):1241-1251.
[34] BEHDADFAR B, KERMANPUR A, SADEGHI-ALIABADI H, et al. Synthesis of aqueous ferrofluids of ZnxFe3-xO4nanoparticles by citric acid assisted hydrothermal-reduction route for magnetic hyperthermia applications[J].Journal of Magnetism and Magnetic Materials,2012, 324(14):2211-2217.
[35] PILENI M P. Structure and Reactivity of Reverse Micelles[M].New York: Elsevier Amst,1989.230-261.
[36] GOBE M, KON-NO K, KITAHARA A. Preparation of magnetite superfine sol in W/O microemulsion and its properties[J].J Coll Int Sci,1984, 93:293-295.
[37] JEONG U, TENG X, WANG Y, et al. Superparamagnetic colloids: controlled synthesis and niche applications[J].Adv Mater,2007, 19(1):33-60.
[38] TABOADA E, RODRIGUEZ E, ROIG A, et al. Relaxometric and magnetic characterization of ultrasmall iron oxide nanoparticles with high magnetization. Evaluation as potential T1magnetic resonance imaging contrast agents for molecular imaging[J].Langmuir,2007, 23(8):4583-4588.
[39] BÖNNEMANN H, BRIJOUX W, BRINKMANN R, et al. A size-selective synthesis of air stable colloidal magnetic cobalt nanoparticles[J]. Inorg Chim Acta,2003,350: 617-624.
[40] CHARLES S W, POPPLEWELL J. Ferromagnetic Material[M]. Amsterdam: North-Holland Publishing Company, 1980. [41] SCHERER C, NETO A M F. Ferrofluids: properties and applications[J].Brazilian Journal of Physics,2005, 35: 718-727.
[42] BERGER P, ADELMAN N B, BECKMAN K J, et al. Preparation and properties of an aqueous ferrofluid[J].Journal of Chemical Education,1999, 76(7):943-948.
[43] MMKHERJEE A, CHILDRESS W, YECKO P. Taylor-Couette flow of ferrofluid: spin field and spin boundary condition effects[J].Physics Procedia,2010, 9:156-161.
[44] JIN-WOO C, KWANG W O, JENNIFER H, et al. An integrated microfluidic biochemical detection system for protein analysis with magnetic bead-based sampling capabilities[J]. Lab Chip,2002, 2(1):27-30.
[45] ANDO B, ASCIA A, BAGILO S, et al. The “One drop” ferrofluidic pump with analog control[J].Sensors and Actuators A,2009, 156(1):251-256.
[46] HARTSHORNE H, BACKHOUSE C J, LEE W E. Ferrofluid-based microchip pump and valve[J].Sensors and Actuators B,2004, 99:592-600.
[47] PAL S, DATTA A, SEN S, et al. Characterization of a ferrofluid-based thermomagnetic pump for microfluidic applications[J].Journal of Magnetism and Magnetic Materials,2011, 323(21):2701-2709.
[48] AHN J J, OH J G, CHOI B. A novel type of a microfluidic system using ferrofluids for an application of l-TAS[J].Microsystem Technologies,2004, 10(8-9):622-627.
[49] CHAN D C F, KIRPOTIN D B, BUNN P A Jr. Synthesis and evaluation of colloidal magnetic iron oxides for the site-specific radiofrequency-induced hyperthermia of cancer[J].J Magn Magn Mater,1993, 122(1-3):374-378.
[50] JORDAN A, WUST P, FAHLING H, et al. Inductive heating of ferrimagnetic particles and magnetic fluids: physical evaluation of their potential for hyperthermia[J]. Int J Hyperthermia,1993, 9(1):51-68.
[51] JORDAN A, SCHOLZ R, WUST P, et al. Endocytosis of dextran and silan-coated magnetite nanoparticles and the effect of intracellular hyperthermia on human mammary carcinoma cells in vitro[J].J Magn Magn Mater,1999, 194:185-196.
[52] MOROZ P, JONES S K, GRAY B N. Magnetically mediated hyperthermia: current status and future directions[J].Int J Hyperthermia,2002, 18(4):267-284.
[53] JORDAN A, SCHOLZ R, MAIER-HAUFF K, et al. Presentation of a new magnetic field therapy system for the treatment of human solid tumors with magnetic fluid hyperthermia[J].J Magn Magn Mater,2001, 225(1-2):118-126.
[54] FUNOVICS M A, KAPELLER B, HOELLER C, et al.MR imaging of the her2/neu and 9.2.27 tumor antigens using immunospecific contrast agents[J]. Magn Reson Imaging,2004, 22(6):843-850. [55] PENG X H, QIAN X, MAO H, et al.Targeted magnetic iron oxide nanoparticles for tumor imaging and therapy[J].Int J Nanomedicine,2008, 3(3):311-321. [56] SERDA R E, ADOLPHI N L, BISOFFI M, et al.Targeting and cellular trafficking of magnetic nanoparticles for prostate cancer imaging[J].Molecular Imaging,2007, 6(4):277-288.
[57] LERENARD P E, JORDAN O, FAES A, et al. The in vivo performance of magnetic particle-loaded injectable, in situ gelling, carriers for the delivery of local hyperthermia[J].Biomaterials,2010, 31(4):691-705.
[58] ITO A, SHINKAI M, HONDA H, et al. Medical application of functionalized magnetic nanoparticles[J].J Biosci Bioeng,2005, 100(1):1-11.
[59] HAFELI U O. Magnetic Nano- and Microparticles for Targeted Drug Delivery[M].London: Kentus Books, 2006.77-126.
[60] DIMITROV I, TRZEBICKA B, MULLER A H E, et al. Thermosensitive water-soluble copolymers with doubly responsive reversibly interacting entities[J].Prog Polym Sci,2007, 32(11):1275-1343.
[61] BRAZEL C S. Magnetothermally-responsive nano-materials: combining magnetic nanostructures and thermally-sensitive polymers for triggered drug release[J]. Pharm Res,2008, 26(3):644-656.
[62] BRAZEL C S, PEPPAS N A. Pulsatile local delivery of thrombolytic and antithrombotic agents using poly (N-isopropylacrylamide-co-methacrylic acid) hydrogels[J].J Control Release,1996, 39(1):57-64.
[63] CHILKOTI A, DREHER M R, MEYER D E, et al. Targeted drug delivery by thermally responsive polymers[J].Adv Drug Deliv Rev,2002, 54(5):613-630.
[64] REGTMEIER J, EICHHORN R, VIEFHUES M, et al. Electrodeless dielectrophoresis for bioanalysis: theory, devices and applications[J]. Electrophoresis,2011, 32(17):2253-2273.
[65] PAMME N.Magnetism and microfluidics[J]. Lab on a Chip,2006, 6(1):24-38.
[66] STEVENLIN S C, MAO X L, HUANG T J. Surface acoustic wave (SAW) acoustophoresis: now and beyond[J].Lab on a Chip,2012, 12(16):2766-2770.
[67] KAYANI A A, KHOSHMANESH K, WARD S A, et al. Optofluidics incorporating actively controlled micro- and nano-particles[J].Biomicrofluidics,2012, 6(3): 31501-31533.
[68] TSUTSUI H, HO C M. Cell separation by non-inertial force fields in microfluidic systems[J].Mechanics Research Communications,2009, 36(1):92-103.
[69] NGUYEN N T. Micro-magnetofluidics: interactions between magnetism and fluid flow on the microscale[J].Microfluidics and Nanofluidics,2012, 12(1-4):1-16.
[70] ZENG J, DENG Y X, VEDANTAM P, et al. Magnetic separation of particles and cells in ferrofluid flow through a straight microchannel using two offset magnets[J].Journal of Magnetism and Magnetic Materials,2013, 346:118-123.
[71] ZHU T T, MARREO F, MAO L D. Continuous separation of non-magnetic particles inside ferrofluids[J].Microfluid Nanofluid,2010, 9(4-5):1003-1009.
[72] ZHU T T, CHENG R, LEE S A, et al.Continuous-flow ferrohydrodynamic sorting of particles and cells in microfluidic devices[J].Microfluid Nanofluid,2012, 13(4):645-654.
[73] BAGLIO S, BARRERA P, SAVALLI N. Novel ferrofluidic inertial sensors[A]. IMTC 2006[C]. Sorrento: IMTC 2006-Instrumentation and Measurement,2006.2368-2372.
[74] BIBO A, MASANA R, KING A, et al. Electromagnetic ferrofluid-based energy harvester[J].Physics Letters A,2012, 376(32):2163-2166.
[75] De VOLDER M, REYNAERTS D. Development of a hybrid ferrofluid seal technology for miniature pneumatic and hydraulic actuators[J].Sensors and Actuators A: Physical,2009, 152(2):234-240.
Magnetic Nano-fluid and Its Terminal Technology Application
SUN Ai-juan,FANG Fen
(School of Chemistry and Chemical Engineering, Ningxia University,Yinchuan 750021,China)
The development of magnetic nanoparticles preparation technology was summarized. The mechanism of stable suspension in the polar or nonpolar carrier liquid during the formation of magnetic nano-fluid and the application progress of its terminal technology were discussed. It is pointed out that further research work on magnetic nano-fluid should include: the major factors influencing the performance of nano-fluid, the compatibility between nanoparticles and the base fluids, the effect of the shape and property of the additive, stability of nano-fluid on the performance of magnetic nano-fluid at high temperature and under long term use conditions.
magnetic nano-fluid;preparation method;dispersion mechanism;terminal technology
10.11868/j.issn.1001-4381.2015.09.016
TQ584+.9
A
1001-4381(2015)09-0103-10
宁夏大学科学研究基金项目(ZR1202)
2013-10-07;
2015-06-25
孙爱娟(1980-),女,硕士,主要从事高分子及其复合材料方面的工作,联系地址:宁夏回族自治区银川市贺兰山西路489号宁夏大学化学化工学院(750021),E-mail:sunaj@nxu.edu.cn

