乙酰化处理对含银甲壳胺纤维性能的影响
秦益民,莫 岚,朱长俊,胡贤志,申胜标,陈 凯
(1.嘉兴学院材料与纺织工程学院,浙江嘉兴 314001;2.青岛明月海藻集团有限公司,山东青岛 266400)
甲壳胺是甲壳素脱乙酰基后得到的一种天然高分子材料[1]。由于其分子结构中含有氨基,甲壳胺可以用稀酸水溶液溶解后制备纺丝溶液,通过喷丝孔挤入碱性水溶液后形成丝条,经过牵伸、水洗、干燥等工艺得到纤维[2-3]。甲壳胺纤维具有良好的生物相容性和生物活性,在功能纺织品及医用卫生材料等领域具有很好的应用价值。
作为一种阳离子多糖,甲壳胺具有独特的抑菌性能,可以通过纤维本身负载的正电荷吸附带负电荷的细菌,从而抑制细菌的增长繁殖。目前,由甲壳胺纤维制备的医用敷料被广泛应用于烧伤创面的护理,可以起到保护创面、避免感染、促进伤口愈合的作用。在甲壳胺纺丝溶液中加入含银纳米颗粒可以制备具有更强抗菌作用的含银甲壳胺纤维[4-6],通过持续释放银离子起到杀菌作用[7-8]。
甲壳胺分子结构中的氨基对银离子有螯合作用,限制了银离子从纤维中的释放。在与乙酸酐反应后,甲壳胺纤维中的氨基被转换成乙酰胺基[9-11],其中氨基和乙酰胺基的比例取决于甲壳胺与乙酸酐的质量比[12]。由于纤维结构的规整性受乙酰化处理的影响,部分乙酰化的甲壳胺纤维具有比纯甲壳胺和充分乙酰化后的甲壳胺纤维更高的吸水性,特别适用于功能性医用敷料的生产。与此同时,乙酰化处理也降低了纤维对银离子的结合力,有利于银离子从纤维上的释放。
本文在乙酰化处理含银甲壳胺纤维的基础上,研究了改性纤维的吸水性及其释放银离子的性能,对开发抗菌医用卫生材料有重要的应用价值。
1 实验部分
1.1 含银甲壳胺纤维的制备
将50 g的甲壳胺粉末溶解在950 g的2%醋酸溶液中,加入1.5 g颗粒直径小于1 μm的含银磷酸锆钠化合物粉末,充分搅拌后形成纺丝溶液。纺丝液通过计量泵从孔数为30、孔径为150 μg的喷丝板上挤入质量分数为5%NaOH的水浴中形成丝条,水洗干燥得到含银离子的甲壳胺纤维。
1.2 甲壳胺纤维的乙酰化处理
称取5 g含银甲壳胺纤维,放入250 mL三角烧瓶中,加入100 mL甲醇后分别在6个三角烧瓶中加入0、1.5、2.5、5.0、6.5、10.0 mL 的乙酸酐溶液,振荡搅拌,于40℃恒温水浴放置5 h后用滤纸过滤,再用水/乙醇(50/50)混合液在过滤器中洗2次,然后用纯乙醇洗2次,在105℃干燥4 h,得到处理后的样品。
1.3 乙酰度的测定
由于在乙酰化过程中甲壳胺的分子结构增加了乙酰基团,整个分子结构中C、N、O、H元素的组成根据乙酰度的变化而有规律的变化,采用元素分析法可以测定纤维中C和N元素的含量[12]。根据纤维中C和N元素含量的比例计算出各种改性甲壳胺纤维的乙酰化取代度分别为19.52%、36.85%、45.7% 、64.38% 、99.42% 。
1.4 在生理盐水中释放银离子的性能
1.4.1 生理盐水的配置
在100 mL烧杯中加入9 g氯化钠,加入去离子水溶解,移入1 L容量瓶,用去离子水定容至1 L,得到质量分数为0.9%的生理盐水。
1.4.2 蛋白质溶液的配置
在100 mL烧杯中加入29 g大豆蛋白质,加入去离子水溶解,移入1 L容量瓶中,用去离子水定容至1 L,得到质量分数为2.9%的蛋白质水溶液。
1.4.3 模拟伤口渗出溶液的配置
在100 mL烧杯中加入8.3 g氯化钠、0.277 g氯化钙及29 g大豆蛋白质,加去离子水溶解后转入1 L容量瓶,加去离子水稀释至1 L后得到模拟伤口渗出液。
1.4.4 银离子的释放性能
称取10 g含银甲壳胺纤维,加入1 L生理盐水中,在磁力搅拌器上搅拌,分别在 0.5、1、3、8、24 h吸取10 mL溶液,加去离子水稀释至100 mL,过滤后在原子发射光谱仪上测定溶液中银离子浓度。
量取100 mL 2.9%蛋白质水溶液,置于37℃水浴中恒温,加入2.5 g含银甲壳胺纤维并开始计时,3 h后吸取10 mL溶液,加去离子水稀释至100 mL,过滤后在原子发射光谱仪上测定溶液中银离子浓度。
用模拟伤口渗出液替代蛋白质水溶液,采用上述步骤测试不同取代度的乙酰化含银甲壳胺纤维释放银离子的性能。
1.5 甲壳胺纤维在不同溶液中的吸水性
在6个250 mL烧杯中加入100 mL质量分数为0.9%的生理盐水,分别加入1 g含银甲壳胺纤维及不同取代度的乙酰化甲壳胺纤维,室温下放置1 h把溶胀后的纤维取出,包裹在长丝织物中,离心脱水3 min后称量(W1),然后在105℃下干燥至质量不变(W2),计算纤维的溶胀率为W1/W2。
2 结果与分析
由于甲壳胺纤维中的氨基与乙酸酐反应后转换成乙酰胺基,随着乙酸酐含量的增加及纤维乙酰度的提高,乙酰化反应过程中纤维的结构由纯甲壳胺转换成纯甲壳素。文献[13-15]表明,乙酰化的纤维由于乙酰基团的加入具有无规的超分子结构,其结晶度低于纯甲壳胺及纯甲壳素,使纤维具有更好的吸水性能。图1示出乙酰化纤维在1655 cm-1附近出现伸缩振动谱带,说明纤维中的氨基被转化成乙酰氨基。表1示出乙酰化甲壳胺纤维在去离子水和生理盐水中的溶胀率。从表1可以看出,未经处理的1号样品在去离子水中的溶胀率为2.877 g/g,随着乙酰度的增加,纤维的吸水性有很大的提高,3号样品的溶胀率达到49.030 g/g。进一步提高纤维的乙酰度使纤维的结晶度提高,其在水中的溶胀率有所下降。

图1 乙酰化甲壳胺纤维的红外光谱图Fig.1 Infrared spectrum of acetylated chitosan fibers

表1 乙酰化甲壳胺纤维在水溶液中的溶胀率Tab.1 Swelling ratios of acetylated chitosan fibers in aqueous solutions
图2示出乙酰化甲壳胺纤维(3号试样)在去离子水中润湿前后的结构变化。在甲壳胺纤维乙酰化处理过程中,纤维中部分—NH2被转换成乙酰胺基。由于纤维的有序结构受到破坏,水分子更容易被吸收,使纤维遇水后高度膨胀,形成一种类似水凝胶的结构。纯甲壳胺纤维在遇水湿润后,由于少量的水分进入纤维结构使纤维直径有所膨胀。部分乙酰化的甲壳胺纤维与水接触后,大量的水分进入纤维,使其形成高度膨胀的凝胶状结构。
图3示出含银甲壳胺纤维与生理盐水接触后溶液中银离子浓度随时间的变化。0.5、1、3、8、24 h 后溶液中银离子的浓度分别为 0.13、0.51、0.59、0.55、0.57 mg/L,说明含银甲壳胺纤维释放银离子是一个较快的过程,在与水溶液接触1 h后溶液中的银离子含量基本达到稳定状态。图4示出不同乙酰化取代度的含银甲壳胺纤维与模拟伤口渗出液接触后溶液中银离子的浓度。乙酰化取代度分别为19.52%、36.85%、45.70%、64.38%、99.42%的改性含银甲壳胺纤维释放的银离子浓度分别为0.83、0.87、0.91、0.99、1.27 mg/L,说明乙酰化改性在使甲壳胺纤维中的氨基转换成乙酰胺基的过程中,可以有效改善其释放银离子的性能。

图2 乙酰化甲壳胺纤维润湿前后的结构Fig.2 Structural changes of acetylated chitosan fibers before(a)and after(b)wetting

图3 接触液中银离子溶度随时间的变化Fig.3 Change of silver ion concentration in contact solution along with time
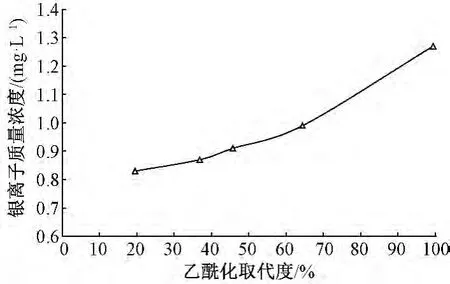
图4 不同乙酰化取代度的含银甲壳胺纤维与模拟伤口渗出液接触后溶液中银离子的浓度Fig.4 Silver ion concentrations in contact solutions of silver containing chitosan fibers with different degrees of acetylation
3 结语
本文研究结果表明:在用乙酸酐处理含银甲壳胺纤维后,随着纤维中氨基的乙酰化,纤维的有序结构受到破坏,部分乙酰化的甲壳胺纤维具有很高的吸水性能,而纯甲壳胺纤维及完全乙酰化的甲壳胺纤维在水中的溶胀率低于部分乙酰化的甲壳胺纤维。由于氨基被转换成乙酰胺基,纤维对银离子的结合力降低,使含银甲壳胺纤维释放银离子的量随着乙酰化程度的提高而有所增加。
[1] 蒋挺大.甲壳素[M].北京:化学工业出版社,2003:1-10.JIANG Tingda. Chitin [M]. Beijing:Chemical Industry Press,2003:1 -10.
[2] EAST G C,QIN Y.Wet spinning of chitosan and the acetylation of chitosan fibers[J].Journal of Applied Polymer Science,1993,50(10):1773 -1779.
[3] HIRANO S.Wet-spinning and applications of functional fibers based on chitin and chitosan[J].Macromolecular Symposia,2001,168(1):21-30.
[4] 朱长俊,秦益民.甲壳胺纤维和含银甲壳胺纤维的抗菌性能比较[J].合成纤维,2005,34(3):15 -17.ZHU Changjun, QIN Yimin. A comparison of the antimicrobial properties of chitosan and silver containing chitosan fibers[J].Synthetic Fiber in China,2005,34(3):15-17.
[5] 秦益民,陈燕珍,张策.抗菌甲壳胺纤维的制备和性能[J].纺织学报,2006,27(3):60-62.QIN Yimin, CHEN Yanzhen, ZHANG Ce. The preparation and characterization of antimicrobial chitosan fibers[J].Journal of Textile Research,2006,27(3):60-62.
[6] QIN Y,ZHU C,CHEN J,et al.Preparation and characterization of silver containing chitosan fibers[J].Journal of Applied Polymer Science,2007,104(6):3622-3627.
[7] OVINGTON L G.The truth about silver[J].Ostomy Wound Manage,2004,50(9):1-10.
[8] 秦益民.含银医用敷料的抗菌性能及生物活性[J].纺织学报,2006,27(11):113 -116.QIN Yimin. The antimicrobial properties and bioactivities of silver containing wound dressings[J].Journal of Textile Research,2006,27(11):113-116.
[9] QIN Y.Functional modifications of chitosan fibers[J].Chemical Fibers International,2006(3):159 -161.
[10] CHO Y W,JANG J,PARK C R,et al.Preparation and solubility in acid and water of partially deacetylated chitins[J].Biomacromolecules,2000,1(4):609 -614.
[11] CHO Y W,CHO Y N,CHUNG S H,et al.Watersoluble chitin as a wound healing accelerator[J].Biomaterials,1999,20(22):2139 -2145.
[12] 朱长俊,冯德明,陆优优,等.乙酰化处理对甲壳胺医用敷料性能的影响[J].纺织学报,2008,29(4):18-21.ZHU Changjun,FENG Deming,LU Youyou,et al.Effect of acetylation on the properties of chitosan wound dressings[J].Journal of Textile Research,2008,29(4):18-21.
[13] CHEN R H,HUA H D.Effect of N-acetylation on the acidic solution stability and thermal and mechanical properties of membranes prepared from different chain flexibility chitosans[J].Journal of Applied Polymer Science,1996,61(5):749-754.
[14] REN D,YI H,WANG W,et al.The enzymatic degradation and swelling properties of chitosan matrices with different degrees of N-acetylation[J].Carbohydr Res,2005,340(15):2403 -2410.
[15] JE J Y,CHO Y S,KIMM S K.Cytotoxic activities of water-soluble chitosan derivatives with different degree of deacetylation[J]. Bioorg Med Chem Lett, 2006,16(8):2122-2126.

