成人病毒性胃肠炎常见病原学及其临床特征的研究进展
综述
成人病毒性胃肠炎常见病原学及其临床特征的研究进展
徐仲卿1, 钱方兴2, 朱绍琴3, 张万菊3, 胡芸文3, 孟祥军1
(1. 上海交通大学附属第六人民医院, 上海, 200233; 2. 上海市同仁医院, 上海, 200336;
3. 上海公共卫生临床中心, 201508)
关键词:急性胃肠炎; 病毒性胃肠炎
急性胃肠炎(AGE)是一种非常常见的肠道传染病,临床主要症状是腹泻,是全球范围内致病和死亡的重要原因之一,也是全球范围内仅次于感冒的第二大疾病原因[1]。2009年,世界卫生组织(WHO)估测有20亿人患有与AGE相关的严重疾病,而每年因为该疾病而死亡的人数可达180万[2]。AGE的微生物病原学包括细菌、病毒、原虫等多种病原体,症状从轻微至严重不等,重症甚至可威胁生命,其中,病毒是AGE的重要病原体。病毒性胃肠炎可影响各个年龄的人群,由多种不同的病毒引起,临床特点是起病急,典型症状为剧烈的腹泻(以水样泻为主,也有部分患者表现为稀便),可伴有恶心、呕吐、腹痛等不适,部分患者还可出现发热及其他全身症状[3]。自1972年诺瓦克病毒首次被发现后,已经有多种病毒明确可导致病毒性胃肠炎,包括轮状病毒(RV,隶属于呼肠病毒科)、诺如病毒(NV,隶属于杯状病毒科)、肠腺病毒(AdV,隶属于腺病毒科)、札幌病毒(SaV,隶属于杯状病毒科)、星状病毒(AstV,隶属于星状病毒科)以及冠状病毒科的成员[4],各病毒特征及性状见表1。
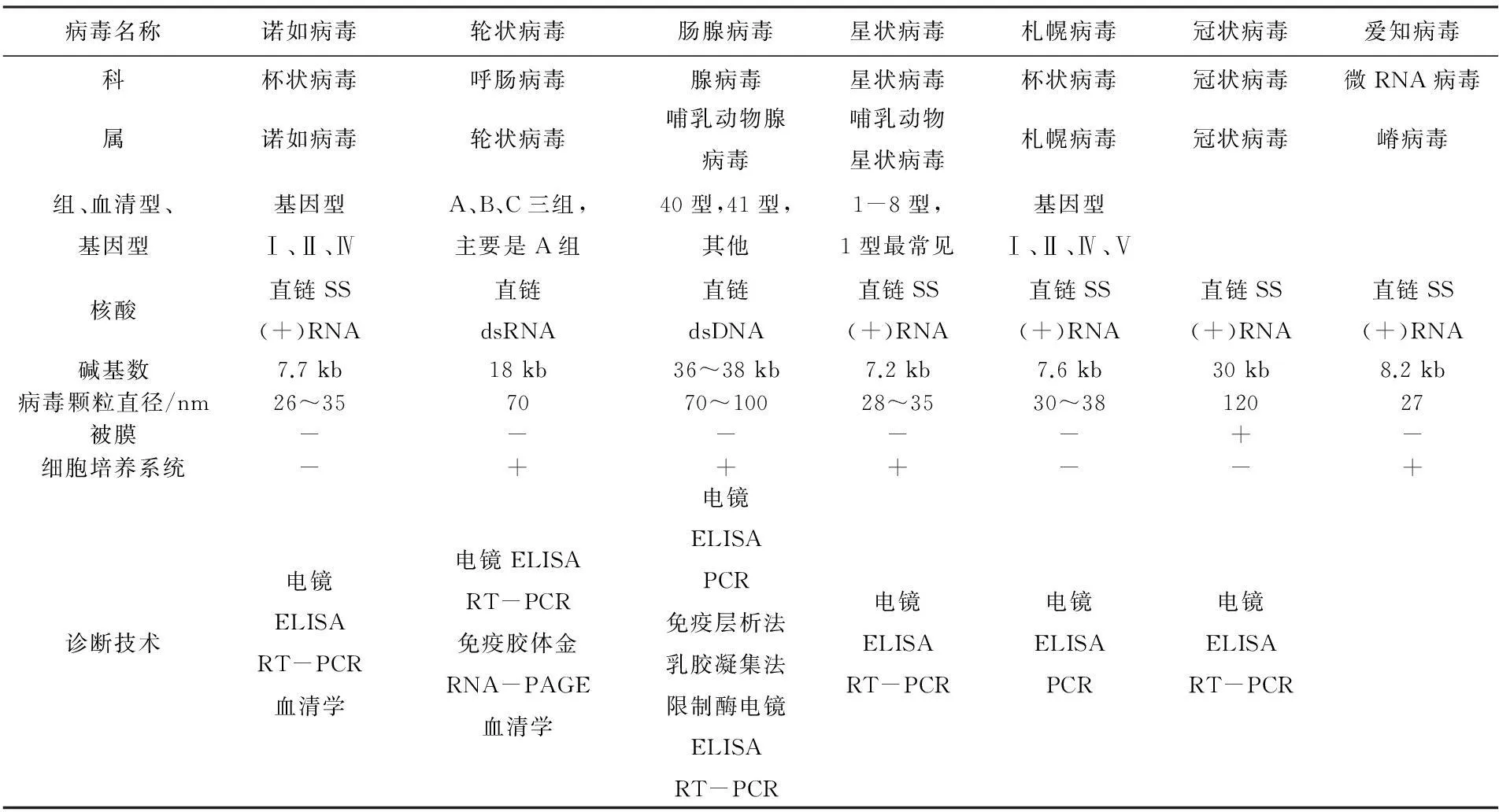
表1 人类病毒性胃肠炎的常见致病病毒特征
临床上,经常会将病毒性胃肠炎与肠道病毒感染混淆,需要说明的是病毒性胃肠炎与肠道病毒感染是两种不同的疾病。虽然这两种疾病均涉及肠道,也均是由病毒引起的,性状却完全不同。其中引起肠道病毒感染的病毒属于肠病毒属微小RNA病毒科,感染可侵袭全身多个器官,严重者可致死亡,而病毒性胃肠炎由多种不同种类的病毒引起,病变主要累及肠道,临床表现为腹泻、呕吐、发热,病程多呈自限性[5]。成人病毒性胃肠炎多见于老年人及免疫功能低下人群,病原体也与儿童有所不同,以诺如病毒及B组轮状病毒为多见,腺病毒、星状病毒等也可引起胃肠炎。
病毒性胃肠炎典型的临床症状为腹泻,尤其是水样泻,部分患者可表现为稀便、黏液便等其他性状,可伴有发热、腹痛、恶心、呕吐等不适。严重者可出现脱水、电解质及酸碱失衡,甚至威胁生命。可发生在各个年龄层,老人及免疫力低下者更为常见。可发生在各个季节,秋冬季更为多见。多为自限性疾病,病程一般小于2周。有传染性,可经粪-口传播或飞沫传播,可能造成暴发流行[6]。不同类型的病毒性胃肠炎的临床特点可能不完全相同。
1诺如病毒胃肠炎
1.1 生物学特征
诺如病毒(NV)的得名颇有波折。1968年美国诺瓦克暴发了一次典型的冬季呕吐及腹泻,某所小学半数以上的学生都病了,其密切接触者也多在48 h内发病[7]。学者Kapikian用免疫电镜(IEM)对当地患者的粪便进行提纯及抗原抗体反应后,于1972年发现了一种新的直径约27 nm、没有包膜的病毒,根据发现地,这种病毒被命名为诺瓦克病毒[8]。随着对于诺瓦克病毒的进一步认识,第八届国际病毒分类命名委员会(ICTV)于2002年8月重新命名其为诺如病毒[9]。
NV隶属于杯状病毒科诺如病毒属,是导致免疫力低下者、老年人、婴幼儿病毒性胃肠炎的主要病原体之一。它与在日本发现的札幌病毒(SaV)同属于杯状病毒科,合称为人类杯状病毒(HuCV)[9]。NV为单股正链RNA病毒,没有包膜,表面粗糙,呈球形,直径约26~35 nm,其基因组全长约7.7 kb,包括三个开放阅读框(ORFs),分别是ORF1、ORF2和ORF3。ORF1编码包括RNA依赖的RNA聚合酶(RdRp)的非结构蛋白[10-12]。ORF2编码主要衣壳蛋白VP1(分子量约为56 kda),VP1在结构上可划为两个区域,分别是S区和P区,两区相邻,P区以拱样结构突出于构成底座的S区外。其中P区又分为P1、P2两个亚区,而P2亚区位于VP1的最外层,高度变异,是免疫识别和受体结合的关键部位[12]。ORF3编码次要衣壳蛋白VP2(分子量约为22.5 kda),VP2是一种强碱性的微小结构蛋白,与NV颗粒的重组有关,体外研究显示其可上调VP1蛋白的产量[9,13]。ORF1/ORF2的重组以及P2亚区的变异极大地丰富了NV的遗传多样性。根据VP1序列的同源性,NV分为5个基因组(Genogruop),分别是GI、GII、GIII、GIV和GV,其中只有GI、GII、GIV三个基因组可感染人类,GIII、GV两个基因组主要感染猪和奶牛等动物。根据ORF2全基因序列的差异又可将基因组进一步分为基因型(Genotype),其中GI组分为14个基因型,GII组分为17个基因型。世界范围内最常见的基因型是GII.4型,其次是GII.3型[14-17]。
1.2 流行病学与临床特点
NV感染的潜伏期为24~48 h,起病急,以腹泻、呕吐为主要症状,可伴有发热、头痛、乏力及其他全身症状。NV病毒耐热、耐低温、同时也能耐受酸碱和去污剂,因此NV病毒感染具有抵抗力强、发病率高和低剂量致病的特点[18],感染的传染源主要是患者、隐性感染者以及带病毒者。NV主要通过粪-口传播,可通过污染的食物、物品、水源、空气传播,也可通过直接接触患者而发生人与人之间传播。此外,NV还存在有一些传播途径,目前尚未能解释[19]。NV常年均有流行而暴发流行则多发生在寒冷季节[20],全球范围内均有报道,主要侵袭成年人、儿童以及家庭密切接触者,是成人感染病毒性胃肠炎的最主要病毒。相对RV感染来说,NV感染的腹泻症状较为轻微,但是每年仍有大约20万左右5岁以下儿童因为感染NV而导致死亡[21]。
诺如病毒感染部位主要在小肠近端黏膜,由于病毒感染的侵袭,使上皮细胞酶活性发生改变,造成糖类及脂类吸收障碍,引起肠腔内渗透压升高,体液进入肠道,从而出现腹泻或呕吐[22]。
1.3 诊断方法
成人出现腹泻或呕吐,需考虑NV胃肠炎的可能,可通过血清学或病原学确诊:①普通电镜或IEM直接在粪便标本中发现病毒颗粒;②酶联免疫吸附测定法(ELISA);③逆转录聚合酶链锁反应(RT-PCR);④检测血清中的IgM抗体。
2轮状病毒胃肠炎
2.1 生物学特征
轮状病毒(RV)是发展中国家和欠发达国家中婴幼儿死亡的主要原因之一,由澳大利亚的Bishop通过电镜于1973年在儿童急性腹泻患者的十二指肠组织中首次发现[23],属呼肠病毒科下的轮状病毒属,包含有双链RNA的11个片段[24],基因组总长约18 kb,根据抗原性和遗传特性分为八个组(A-H),其中A、B、C三组目前已被证实可感染人类[25]。在所有感染人类的RV中,A组RV被认为是引起婴幼儿严重AGE的最主要病原体,也是婴幼儿死亡的重要原因之一,是目前世界范围内针对AGE进行预防和控制的重点,成人感染虽然相对少见,也可通过密切接触感染病毒的婴幼儿而获得。B组主要感染成人,于1983年由中国的洪涛[26]首次发现后,也在其他国家被发现,可呈大规模流行和暴发。C组感染遍布全世界,多在青少年中散发出现,各地均有报道,不构成威胁。
成熟的RV病毒颗粒直径约70 nm,无包膜。RV有三层蛋白衣壳,外壳VP4和VP7是病毒的中和抗原,可诱导机体产生中和抗体[27]。轮状病毒血清型(Serotype)是以VP4 和VP7 抗原性的不同来区分的,其中VP7决定G血清型,VP4决定P血清型[28]。RV至少有15个G血清型,在感染人类的血清型中,以G1、G2、G3、G4及G9型最常见。但是,近年来各国报道RV感染的非流行株明显上升,比如泰国报道了G12型,巴西报道了G5、G8、G10型RV感染。RV有26个P血清型,其中11个P型感染人[29]。P血清型中,以P[8]、P[4]、P[6]型最常见。世界范围内常见的GP组合有G1P[4]、G2P[4]、G3P[8]、G4P[8]、G9P[8][30-33]。RV的型别较为复杂,有亚型(Subtype)、血清型(Serotype)、基因型(Genotype)之分,因此,罹患RV胃肠炎后,仍存在感染其他型别RV的可能。
2.2 流行病学与临床特点
RV感染的潜伏期在1~3 d,主要临床表现为腹泻,腹泻可呈水样便、蛋花样便等不同性状,可伴有呕吐、发热、轻度脱水和酸中毒等症状。病程一般为5~7 d,多数患者表现为自限性疾病,部分患者病情严重,可出现重度脱水甚至死亡。RV感染的传播途径主要是经粪-口传播,在RV患者急性期的粪便中含有大量病毒颗粒,具有高传染性,近年还证实RV也可通过呼吸道途径传播。患者、隐性感染者和带病毒者是RV感染的主要传染源[22]。RV感染的主要人群是6~24个月的婴幼儿,成人虽然较少,也有各地流行及暴发的报道,尤其是在免疫功能低下和老年人群中较为多见。部分成人感染RV临床症状并不典型,可表现为无症状感染,是RV的潜在传染源。在不同的时间及不同的区域,RV感染的季节性并不相同,在季节分明的地区,RV感染一般发生在寒冷干燥的秋冬季节,因此有“秋冬季腹泻”之称,而在持续高温、季节不分明的热带地区,有报道称其呈全年散发[34]。
轮状病毒引起的腹泻可能与多种因素有关,包括肠细胞受损、绒毛局部缺血、编码病毒毒素(NSP4)和激活肠道神经系统。
2.3 诊断方法
在秋冬季节发生以水样泻为主的腹泻,特别是在有较多病例一起发生的时候,就需考虑RV胃肠炎的可能。RV胃肠炎的粪常规或血常规常无特异性,需要通过血清学或病原学确诊,诊断方法包括: ① 普通电镜或IEM可直接在粪便标本中发现病毒颗粒; ② 免疫胶体金法,可以快速诊断; ③ ELISA法; ④ 从粪便中提取病毒RNA进行聚丙烯酰胺凝胶电泳(PAGE)法检测; ⑤ RT-PCR、多重逆转录聚合酶链式反应(Multiplex RT-PCR)以及其他多种PCR技术; ⑥ 血清学检测,一般在感染5 d后,血清中即可检测出特异性的IgM抗体。
3腺病毒胃肠炎
3.1 生物学特征
Rowe[35]等在1950年代早期,在对儿童发生自发性退行性病变的腺体组织细胞培养物进行检测时,意外发现了一种新的病毒,之后这种病毒被ICTV命名为腺病毒(AdV)。1975年,英国学者Flewett等从AGE患儿粪便标本中,运用电镜技术发现了与AGE发病直接相关的腺病毒,从此正式明确了AdV为人类病毒性胃肠炎的病原之一。
AdV为线性双链DNA,为直径70~100 nm的颗粒,基因组总长约36~38 kb,目前已知至少有52个血清型,分属A~G七个亚组。 AdV不仅可引起婴幼儿急性胃肠炎,也可引起其他部位的感染,较常见的感染部位有呼吸道、尿道、眼部等。其中AdV40和41型隶属于F亚组,是引起婴幼儿AGE的主要病原体,与AdV相关的腹泻,2/3以上是由40型和41型引起的,国内外均可见其流行或暴发的报道,因此被称为肠道腺病毒(EAdV)。其他型别也可导致腹泻,但是较为少见。
AdV耐酸,在36 ℃以下病毒至少能存活7 d,较为稳定,对于物理和化学试剂的作用也有很强的抵抗性。同时,AdV对胆汁和胃肠分泌物均有较好的抵抗性,因此,AdV在胃肠内易于复制,可以产生较高的病毒载量。但是AdV的特点就是不耐热,在50 ℃~56 ℃下很快就会灭活。
3.2 流行病学与临床特点
AdV胃肠炎的临床表现为腹泻,以水样泻为主,症状较为严重,每日数次至数十次不等,患者可有不同程度的脱水征,并常伴有呼吸道不适,比如咳嗽、鼻塞、咽痛等,一般来说,患者的呕吐及发热症状较为轻微。AdV常通过人与人的密切接触传播,也可经粪-口或呼吸道传播。国内外研究显示AdV感染没有明显的季节性,全年均可发病,夏秋季略多,可呈暴发流行。
3.3 诊断方法
水样泻伴有呼吸道症状,需考虑AdV引起的胃肠炎,可通过以下方法诊断: ① 普通电镜或IEM; ② 乳胶凝集法; ③ 免疫层析法; ④ ELISA法; ⑤ 限制酶; ⑥ PCR。
4星状病毒胃肠炎
4.1 生物学特征
1975年,英国学者Appleton和Higgins对当地一起儿童AGE暴发疫情的粪便标本进行常规检测时,在电镜下找到了一种新型的病原体,这种病毒颗粒的表面有5、6个角,形状类似星形,根据这个显著的特点,Madeley和Cosgrove将其命名为星状病毒(AstV)[36]。目前已知AstV是引起免疫力低下者、婴幼儿和老年人胃肠炎的重要病原体之一,既往研究[37-41]提示AstV是婴幼儿中导致病毒性胃肠炎发生的主要病原体之一,排名仅次于RV, 位于第二或第三位。
AstV隶属于星状病毒科哺乳动物属,为单股正链RNA,没有包膜,直径约28~35 nm, 其基因组全长约7.2 kb,包括三个重叠的开放阅读框(分别是ORF1a,ORF1b和ORF2)和两端的两个非编码区(5’非编码区和3’非编码区)。根据ORF2合成的衣壳蛋白的结构差异,AstV可划分为AstV-1~8八个血清型(Serotype),与基因型(Genotype)一致[42-44]。其中最主要的流行型别是AstV-1型,全球范围内均有爆发流行的报道,部分区域曾有AstV-2、3、4型流行发生的报道,AstV-5~AstV-8型的报道则非常少有[45]。
AstV耐酸,在室温下非常稳定,在粪便中更是能存活数天甚至数周,也能耐受含氯消毒剂和紫外线,不过AstV有一个特点,就是不能耐热,60 ℃ 10 min即可将其灭活[46]。
4.2 流行病学与临床特点
AstV感染的症状主要表现为腹泻,可伴有呕吐、发热、腹痛等其他症状,潜伏期在1~3 d。AstV的感染具有典型的季节性的特征,在不同区域,季节特征有所不同,在气候分明的温带地区,寒冷干燥的秋冬季是AstV的流行季节,在气候不分明的热带地区,炎热而又潮湿的雨季是AstV的流行季节,而在中国,与温带地区类似,寒冷而又干燥的秋冬季是AstV感染的主要季节。
4.3 诊断方法
AstV的诊断方法包括: ① 电镜; ② ELISA法; ③ RT-PCR; ④ 荧光免疫法(immunofluorescece)。
5札幌病毒胃肠炎
札幌病毒(SaV)也属于杯状病毒科,最早于二十世纪七十年代在日本札幌市发现,根据发现地而命名[47]。SaV感染在五岁以下的儿童中多见,成人虽然较为少见,也有可能感染[48]。SaV是单股正链RNA,直径约30~38 nm,基因组全长约7.6kb,根据RNA聚合酶区(RdRP)和衣壳蛋白区的基因多因性,分为五个基因组(GI-GV),已知GI、GII、GIV、GV感染人, GIII感染猪[49]。研究[50]发现SaV引起的腹泻较轮状病毒和诺如病毒为轻, 主要是散发分布,较少出现暴发流行[51]。但近几年,SaV引起的感染在世界范围内均有分布且增加的趋势。SaV的诊断方法包括电镜、ELISA和RT-PCR。
6冠状病毒胃肠炎和爱知病毒胃肠炎
冠状病毒(Coronavirus)是单股正链RNA病毒,直径约120 nm, 有包膜,基因组全长约30 kb,主要引起呼吸道感染,也可引起急性胃肠炎,表现为水样泻、发热、呕吐等不适,成人和儿童均可感染,通过电镜、ELISA、PCR可发现。爱知病毒(Aichi Virus)是一种微RNA病毒,直径约27 nm, 无包膜,基因组全长约8.2 kb, 于1989年在日本爱知县一起AGE暴发疫情的病人粪便中发现,根据发现地而命名,可通过电镜、ELISA、RT-PCR等方法被诊断。
7病毒性胃肠炎的治疗
对于病毒性胃肠炎尚未有特异性的治疗药物,一般不需要抗病毒治疗,同时也不宜应用抗生素,以免出现菌群失调、细菌耐药等不良反应。伴有严重腹泻的病人,尤其是老年人,应充分评估其脱水的可能及程度,给予适当的液体支持、维持水电解质及酸碱平衡。脱水的评估主要通过以下体征来判断:皮肤是否干燥和皮肤弹性试验,是否无泪、眼球凹陷,脉搏次数,是否有体位性低血压或低血压,体质量下降程度,以及意识状况。据此将脱水分型如下: ① 无脱水。意识正常,无眼球凹陷,皮肤弹性好,无口干; ② 轻度脱水。脉搏加快,烦躁,眼球凹陷,皮肤弹性差,口干; ③ 严重脱水。血压下降或休克,嗜睡或倦怠,眼球凹陷,皮肤皱褶试验2 s不恢复,少尿或无尿[52]。
轻度脱水患者建议口服补液治疗,以下患者需要考虑输液治疗: ① 呕吐频繁,无法饮水或者进食的患者; ② 伴有高热等严重全身症状,特别是有意识障碍的患者; ③ 伴有重度脱水、循环衰竭以及重度酸碱失衡和电解质紊乱的患者; ④ 其他各种不适合口服补液治疗的情况。静脉补液量、液体成分和补液时间应根据患者病情决定。脱水引起休克者的补液应遵循“先快后慢、先盐后糖、先晶体后胶体、见尿补钾”的原则[52]。
急性胃肠炎是一种常见疾病,给人们的健康造成了沉重的负担[53],其中病毒是AGE重要的病原体。虽然有关病毒性胃肠炎的流行病学研究已经广泛开展,但多数研究的对象都是婴幼儿患者,成人中的研究相对较少,因此,对成人病毒性胃肠炎的患者进行全面而彻底的病原学的分析,研究和探讨各种致病病毒在成人中的流行病学,尤其是病毒进化和基因分子特征,对于相关疾病的研究,可以提供理论和数据支持,对于疫苗的开发和疾病的预防,也可提供必要的背景资料,对于减轻社会的经济和医疗负担,促进人们的健康,具有一定的意义。
参考文献
[1]Liu J, Kibiki G, Maro V, et al. Multiplex reverse transcription PCR Luminex assay for detection and quantitation of viral agents of gastroenteritis[J].J Clin Virol, 2011, 50: 308.
[2]World Health Organization.Diarrhoea disease.Fact sheet No.330.WHO: 2009.Available at: http: //www.who.int/mediacentre/factsheets/fs330/en/index.html (accessed December 28, 2012).
[3]吕秋艳, 李龙建, 王志越. 2011-2013年北京市门头沟区病毒性腹泻监测结果分析[J]. 国际病毒学杂志, 2014, (2): 76.
[4]洪涛, 王大燕. 胃肠炎病毒的研究进展[J].传染病信息, 2006, (2): 10.
[5]缪晓辉, 龚智翔.病毒性胃肠炎的诊治[J].内科理论与实践, 2009, 4(2): 132.
[6]徐潜.病毒性胃肠炎的诊治[J].中国临床医生, 2009, 37(10): 25.
[7]Adler J, Zickl R.Winter vomiting disease[J].J Infect Dis, 1969, 119: 668.
[8]Kapikian AZ, Wyatt RG, Dolin R, et al. Visualization by immune electron microscopy of a 27-nm particle associated with acute infectious nonbacterial gastroenteritis[J]. J Virol, 1972, 10: 1075.
[9]肖镜, 贺争鸣. 诺瓦克病毒及实验动物感染[J].实验动物科学, 2009, 26(3): 46.
[10]Jiang X, Wang M, Wang K, et al. Sequence and genomic organization of Norwalk virus[J].Virology, 1993, 195(1): 51.
[11]Lambden P R, Caul E O, Ashley C R, et al. Sequence and genome organization of a human small round-structured (Norwalk like)virus[J].Science, 1993, 259(5094): 516.
[12]沈震, 王刚, 宰淑蓓, 等.诺如病毒新型GII.4流行株Sydney_2012在上海地区的检出和鉴定[J].病毒学报, 2013, 29(6): 608.
[13]Phan T G, Takanashi S, Kaneshi K, et al. Dection and genetic circulating among infants and children with acute gastroenteritis in Japan during 2004-2005[J].Clin Lab, 2006, 52(9/10): 519.
[14]Ramani S, Kang G.Viruses causing childhood diarrhea in the developing world[J].Curr Opin Infect Dis, 2009, 2295: 477.
[15]Abugalis M, Curvas L, Kirby A, et al. Clinical features and molecular epidemiology of rotavirus and norovirus infections in Lybian children[J].J Medd Virol, 2011, 83(10): 1849.
[16]Ferreira M S, Victoria M, Carvalho-Costa F A, et al. Surveillance of norovirus infections in the state of Rio De Janeiro, Brazil 2005-2008[J].J Med Virol, 2010, 82(8): 1442.
[17]Xu J, Yang Y, Sun J, et al. Molecular epidemiology of norovirus infection among children with acute gastroenteritis in Shanghai, China, 2001-2005[J].J Med Virol, 2009, 81(10)1826.
[18]Dolin R.Norovirus-challenges to control[J].N Eng J Med, 2007, 357(11): 1072.
[19]Sdiri-Loulizi KKAH.Molecular epidemiology of norovirus gastroenteritis investigated using samples collected from children in Tunisia during a four-year period: detection of the norovirus variant GGII.4 Hunter as early as January 2003[J].Clin Microbiol, 2009, 47: 421.
[20]Patel MM, Hall A J, Vinje J, et al. Noroviruses: a comprehensive review[J].J Clin Virol, 2009, 44(1): 1.
[21]Patel M M, Widdowson M A, Glass R I, et al. Systematic literature review of role of noroviruses in sporadic gastroenteritis[J].Emerg Infect Dis, 2008, 14(8): 1224.
[22]邓莉.儿童病毒性胃肠炎[J].实用儿科临床杂志, 2011, 26(10): 727.
[23]Bishop RF, Davidson GP, Holmes IH, et al. Virus particles in epithelial cells of duodenal mucosa from children with acute non-bacterial gasteronteritis[J].Lancet, 1973, 2: 1281.
[24]Matthijnssens J, Otto PH, Ciarlet M, et al. VP6-sequence-based cutoff values as a criterion for rotavirus species demarcation[J].Arch Virol, 2012, 157: 1177.
[25]Nakata S, Estes M K, Graham D Y, et al. Detection of antibody to group B adult diarrhea rotaviruses in humans[J].J Clin Microbiol, 1987, 25(5): 812.
[26]Hung T, Chen GM, Wang CG, et al. Waterborne out-break of rotavirus diarrhoea in adults in China caused by a novel rotavirus[J].Lancet, 1984, 1(8387): 1139.
[27]余海燕.轮状病毒分子生物学研究进展[J].畜牧与饲料科学, 2014(10): 103.
[28]潘以韵, 黄瑛. 轮状病毒腹泻的研究进展[J].国际儿科学杂志, 2009(3): 296.
[29]Ramachandran M, Gentsch J R, Parashar U D, et al. Detection and characterization of novel rotavirus stains in the Uniter States[J].J Clin Microbiol, 1998, 36(11): 3223.
[30]Cortese M M, Parashar U D.Prevention of rotavirus gastroenteritis among infants and children: recommendations of the Advisory Committee on Immunization Practices[J].MMWR Recomm Rep, 2009, 58(RR-2): 1.
[31]Kawai K, O’brien M A, Goviea M G, et al. Burden of rotavirus gastroenteritis and distribution of rotavirus stains in Asia: a systematic review[J].Vaccine, 2012, 30(7): 1244.
[32]Malek M A, Teleb N, Abu-Elyazeed R, et al. The epidemiology of rotavirus diarrhea in countries in the Eastern Mediterranean Region[J].J Infect Dis, 2010, 202(Suppl): s12.
[33]Fang Z Y, Yang H, Qi J, et al. Diversity of rotavirus stains among children with acute diarrhea in China: 1998-2000 surveillance study[J].J Clin Microbiol, 2002, 40(5): 1875.
[34]Faifr M, Neubauerova V, Fajfrova J.Viral gastroenteritis[J].Klin Mikrobiol Infect Lek, 2012, 18(1): 11.
[35]Rowe W P, Huebner R J, Gilmore L K, et al. Isolation of a cytopathogenic agent from human adenoids undergoing spontaneous degeneration in tissue culture[J].Proc Soc Exp Biol Med, 1953, 84(3): 570.
[36]Madeley C R, Cosgrove B P.Letter: 28nm particles in faeces in infantile gastroenteritis[J].Lancet, 1975, 2(7932): 451.
[37]Utagawa E T, Nishizawa S, Sekine S, et al. Astrovirus as a cause of gastroenteritis in Japan[J].J Clin Microbiol, 1994, 32(8): 1841.
[38]Akihara S, Phan T G, Nguyen T A, et al. Existence of multiple outbreaks of viral gastroenteritis among infants in a day care center in Japan[J].Arch Virol, 2005, 150(10): 2061.
[39]Lyman W H, Walsh J F, Kotch J B, et al. Prospective study of etiologic agents of acute gastroenteritis outbreaks in child care centers[J].J Pediatr, 2009, 154(2): 253.
[40]Svraka S, Duizer E, Vennema H, et al. Etiological role of viruses in outbreaks of acute gastroenteritis in The Netherlands from 1994 through 2005[J].J Clin Microbiol, 2007, 45(5): 1389.
[41]Marshall J A, Bruggink L D, Sturge K, et al. Molecular features of astrovirus associated with a gastroenteritis outbreak in an aged-care center[J].Eur J Clin Microbiol Infect Dis, 2007, 26(1): 67.
[42]Noel J S, Lee T W, Kurtz J B, et al. Typing of human astroviruses from clinical isolates by enzyme immunoassay and nucleotide sequencing[J].J Clin Microbiol, 1995, 33(4): 797.
[43]Walter J E, Mitchell D K, Guerrero M L, et al. Molecular epidemiology of human astrovirus diarrhea among children from a periurban community of Mexico City[J].J Infect Dis, 2001, 183(5): 681.
[44]Monceyron C, Grinde B, Jonassen T O.Molecular characterization of the 3ndof the astrovirus genome[J].Arch Virol, 1997, 142(4): 699.
[45]Jeong A Y, Jeong HS, Jo M Y, et al. Molecular epidemiology and genetic diversity of human astrovirus in South Korea from 2002 to 2007[J].Clin Microbiol Infect, 2011, 17(3): 404.
[46]Lin H C, Kao C L, Chang L Y, et al. Astrovirus gastroenteritis in children in Taipei[J]. J Formos Med Assoc, 2008, 107(4): 295.
[47]顿灿, 范静文. 札幌病毒研究进展[J]. 中国动物保健, 2010, 2010: 11.
[48]Hainian Y, Toshiaki A, Tung G P. Outbreak of acute gastroenteritis associated with group a rotavirus and genogroup I sapovirus among adults in a mental health care facility in Japan[J]. Med Virol, 2005, 75(11): 475.
[49]邓恬宁, 卢钟山, 潘良文, 等.人类札幌病毒检测研究进展[J]. 检验检疫科学, 2008, 18(5): 68.
[50]Hansman G S, Doan L T, Kguyen T A, et al. Detection of norovirus and sapovirus infection among children with gastroenteritis in Ho Chi Minh City, Vietnam[J]. Arch Virol, 2004, 149(9): 1673.
[51]Lee L E, Cebelinski E A, Fuller C, et al. Sapovirus outbreaks in long-term care facilities, Oregon and Minnesota, USA, 2002-2009[J]. Emerg Infect Dis, 2012, 18(5): 873.
[52]缪晓辉, 冉陆, 张文宏, 等.成人急性感染性腹泻诊疗专家共识[J].中华传染病杂志, 2013, 31(12): 705.
[53]Yan Chen, Wei-Xing Yan, Yi-Jing Zhou, et al. Burden of self-reported acute gastrointestinalillness in China: a population-based survey[J].BMC Public Health, 2013, 13: 456.
基金项目:卫生部重大传染病防治科技重大专项基金: 2012ZX10004-211
通信作者:孟祥军xiangjunmenggoodman@hotmail.com
收稿日期:2015-05-10
中图分类号:R 573.3
文献标志码:A
文章编号:1672-2353(2015)24-245-06
DOI:10.7619/jcmp.201524103

