氟比洛芬酯脂微球注射液的制备及质量研究
陆 军,黄晶晶,徐 伟
(1.南京优科生物医药有限公司,南京 210009, 2.江苏省中国科学院植物研究所,南京 200014; 3.南京工业大学药学院,南京 211816; 4.福建中医药大学药学院,福州 350003)
药物制剂
氟比洛芬酯脂微球注射液的制备及质量研究
陆 军1,3,黄晶晶2,徐 伟4
(1.南京优科生物医药有限公司,南京 210009, 2.江苏省中国科学院植物研究所,南京 200014; 3.南京工业大学药学院,南京 211816; 4.福建中医药大学药学院,福州 350003)
目的:制备氟比洛芬酯脂微球注射液。方法:通过正交实验优化筛选得到氟比洛芬酯脂微球的最佳处方和工艺,并研究所得制剂的粒径、pH 值、有关物质及含量等性质。结果:确定氟比洛芬酯脂微球注射液的处方组成及工艺为: 10%的注射用大豆油、1.2%精制蛋黄卵磷脂、0.5%油酸、2.3%甘油、0.032%磷酸氢二钠、0.03%枸橼酸和95%的注射用水。均质8次,121 ℃灭菌15 min,灭菌后仍能保持良好的稳定性, 制得脂微球注射液氟比洛芬酯的含量为99.45%,最大单一杂质0.085%,其他杂质总和0.23%。结论:该处方工艺可行,制得的脂微球质量可控。
氟比洛芬酯,脂微球,处方优化,工艺优化,质量可控
氟比洛芬酯脂微球注射液是通过药物传递以脂质微球为药物载体,将氟比洛芬酯包裹在里面的新型制剂, 是目前唯一可用于静脉注射的非类固醇制剂。氟比洛芬作为氟比洛芬酯前体,难溶于水,氟比洛芬酯化后即是氟比洛芬酯,有非常强的亲脂性,在注射用大豆油中可以完全溶解,用特殊工艺, 制成脂质微球。氟比洛芬酯脂微球注射液的特点主要有以下几方面:①具有很强的靶向作用,可以使包裹的药物在病发部位发挥疗效;②可以控制释放药物,使药物疗效时间延长,减少药物的使用剂量;③易于跨越细胞膜,加快药物的吸收,缩短药物起效时间;④可以用于静脉注射,避免了口服给药对消化道黏膜的损伤[1]。
目前市售品多为氟比洛芬的口服制剂,许多患者无法口服吞咽药物,而且易引起胃肠道功能紊乱等不良反应。在治疗术后疼痛或因癌症引起的疼痛时,与口服制剂相比,氟比洛芬酯脂微球注射液可避免服用不方便和口服引起的不良反应,并且起效更快。氟比洛芬酯脂微球注射液(商品名:凯纷)在中国2004年上市,生产企业是北京泰德制药有限公司,但在国内零售价高,普通患者不能承受。本实验以稳定参数制备其处方和工艺,解决了产业化等关键问题,并通过体内外指标判定制得的氟比洛芬酯脂微球注射液较稳定,能适应工业化生产[2]。
1 仪器与试药
DF-101S 集热式恒温加热磁力搅拌器(上海东玺制冷仪器设备有限公司);T18 basic高速剪切机(德国IKA有限公司);KH-250B型数控超声波清洗器(昆山市禾创超声仪器有限公司);AH-1500高压均质机(加拿大ATS公司);S20精密pH计(德国梅勒特有限公司);SYQ-DSX-280B型立式压力蒸汽灭菌器(上海申安医疗器械厂) ;CX31显微镜(日本奥林巴斯有限公司);UV-2550 紫外分光光度计(岛津公司); Mastersizer 2000粒度检测仪(英国MALVERN有限公司);安捷伦1260高效液相色谱仪(安捷伦科技有限公司,DAD 检测器,广州艾欣科学仪器有限公司色谱柱)。氟比洛芬酯对照品(南京优科制药有限公司,批号100696-200401);氟比洛芬酯原料药(南京优科制药有限公司);注射用大豆油(广州汉方现代中药研究开发有限公司); 精制蛋黄卵磷脂(Q P Corporation);油酸(国药集团化学试剂有限公司);注射用甘油(江西益普生药业有限公司);磷酸氢二钠(湖南九典制药有限公司);枸橼酸(湖南华日制药有限公司);凯纷(北京泰德制药有限公司,批号5031P);自制氟比洛芬酯脂微球注射液(批号20120301、 20120302、20120303);乙腈、无水乙醇、冰醋酸为分析纯。
2 方法和结果
2.1 乳剂的质量评价指标
2.1.1 外观 在自然光下采用目测、鼻闻法检查。即为白色乳液,略带黏性,有特异性气味。
2.1.3 粒径 用Mastersizer 2000粒度检测仪测定乳剂的粒径,评价乳剂粒径的分布情况,以评价稳定性。
2.2 处方工艺
2.2.1 处方优化 根据初步预实验和日本文献资料[2]能判定氟比洛芬酯脂微球的处方是:精制蛋黄卵磷脂0.8%~1.2%、大豆油 10%、油酸0.3%~0.7%、注射用甘油2.0%~3.0%、磷酸氢二钠0.032%、枸橼酸0.03%,加注射用水定量。在预实验的基础上,对影响制剂稳定性的3个主要因素: 精制蛋黄卵磷脂用量(A)、油酸用量(B)、注射用甘油用量(C)进行正交优化实验,实验设计与结果见表1和表2, 并以外观和相对密度为评价指标,对处方进行筛选。

表1 处方优化因素水平表
选用L9(32)正交表可得9组处方,按照外观和相对密度为评价指标,可见各因素对制剂质量影响的大小依次为: A>B>C,最佳组合为 A3B2C2,即精制蛋黄卵磷脂用量为1.2%,油酸为0.5%,甘油为2.3%。
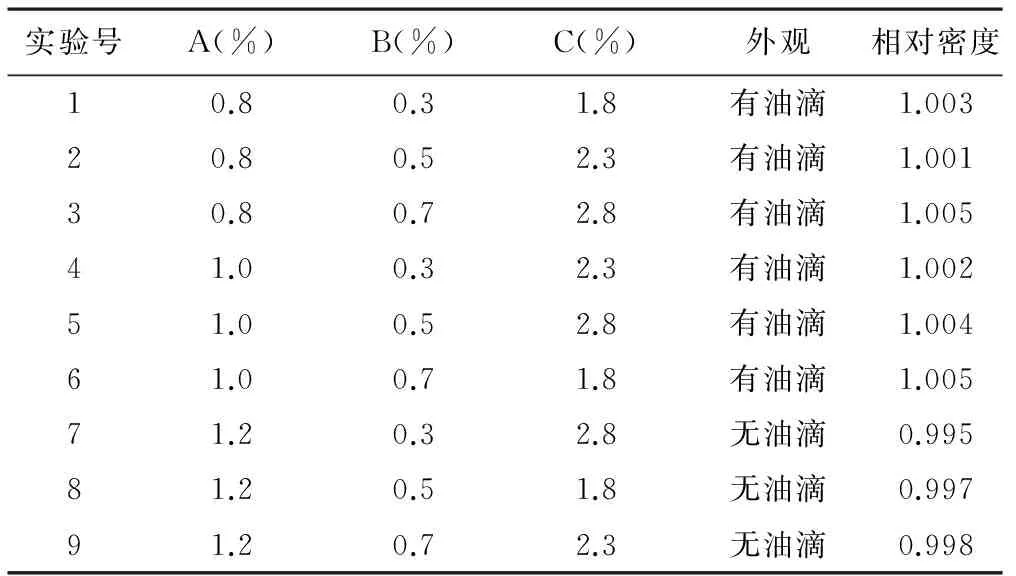
表2 氟比洛芬酯脂微球注射
2.2.2 工艺优化 选择已优化好的处方进行工艺筛选,经初步实验确定初乳的制备温度(D)、初乳剪切分散的时间(E)、均质次数(F)为工艺考查因素,以外观和显微镜观察粒径分散和大小进行评价指标,以确定工艺中的生产参数,为工业化生产做基础研究[2]。正交实验设计及其结果见表3和表4。
正交表得9组工艺,按照乳剂评价方法,用极差分析法分析正交实验结果, 可见各工艺因素对制剂稳定性影响的大小依次为:F>E>D,最佳组合为 D2E2F2, 即油水两相混合温度为65 ℃,剪切时间为10 min,均质次数为8次。

表3 工艺优化因素水平表

表4 氟比洛芬酯脂微球注射液正交实验工艺筛选结果
2.2.3 氟比洛芬酯脂微球注射液的处方工艺确认 称取处方量的氟比洛芬酯、蛋黄卵磷脂、油酸和注射用大豆油放在油相罐中,65 ℃加热至完全溶解;称取处方量甘油、磷酸二氢钠和注射用水放在水相罐中,65 ℃加热至完全溶解;在水相罐中开启高剪切,缓慢加入全部油相,再继续剪切10 min,制得初乳。开启高压均质机,将初乳经30 000 KPa高压均质一次后转移到均质罐中,然后60 000 KPa均质一次,80 000 KPa均质6次后使用饱和枸橼酸溶液调节pH 5.5~6.5,过滤,灌装,121 ℃灭菌15 min,即得成品。
最后,合同文本的篇章也具有显著特征。首先从结构上看,合同文本条目清楚,语篇规整;从文本内容上看,合同基本由约首、正文和约尾构成,每部分包含的款项和结构比较固定。其正文部分完整且详尽,条理清晰,逻辑严密。
2.3 氟比洛芬酯脂微球注射液理化性质的考查
2.3.1 粒径分布 自制氟比洛芬酯脂微球注射液和凯纷分别用水适当稀释后测定其粒径,所得结果见图1,其平均粒径分别为 163 nm和165 nm。
2.3.2 相对密度 测定3批自制氟比洛芬酯脂微球注射液和凯纷相对密度,分别为0.997 1、0.997 3、0.996 8和0.997 6。
2.3.3 pH值测定 测定3批自制氟比洛芬酯脂微球注射液和凯纷的pH值,分别为5.89、5.92、5.87和6.06。

图1 自制氟比洛芬酯脂微球注射液(A) 凯纷(B)粒径分布图
2.4 氟比洛芬酯脂微球注射液含量测定[3]
2.4.1 色谱条件 色谱柱: Kromasil 100-5 C18柱; 流动相: 乙腈-水-冰醋酸(54∶46∶0.15);检测波长:254 nm;流速: 2.0 ml/min;柱温: 40 ℃; 进样量: 10 μl。
2.4.2 标准曲线的制备 取氟比洛芬酯约10 mg,精密称定,置20 ml量瓶中,加无水乙醇溶解并稀释至刻度,摇匀。分别精密量取适量,加无水乙醇稀释制成每1 ml中含氟比洛芬酯约1.0、5.0、10.0、50.0、100.0和500.0 μg的溶液作为对照品系列溶液,摇匀,分别精密量取系列溶液各10 μl,注入液相色谱仪,记录色谱图,以进样量(X)为横坐标,峰面积之和(Y)为纵坐标,绘制标准曲线,并计算回归方程,Y=1.513 4X+8.765 2(r=1.000 0),试验结果表明,进样量在10.32~5 160.00 ng范围内线性良好。
2.4.3 专属性试验 取氟比洛芬酯对照品适量,精密称定,加无水乙醇溶解并定量稀释制成每1 ml中约含10 μg的溶液作为氟比洛芬酯对照品溶液;分别精密量取空白辅料、自制氟比洛芬酯脂微球注射液和凯纷溶液各5 ml,置100 ml量瓶中,加无水乙醇溶解并稀释至刻度,摇匀,分别精密量取1 ml,置50 ml量瓶中,用无水乙醇稀释至刻度,摇匀得空白溶液和供试品溶液。取对照品溶液、空白溶液、10 μg/ml的氟比洛芬酯注射液溶液和10 μg/ml凯纷溶液,分别进样10 μl,记录色谱图,见图2。
2.4.4 氟比洛芬酯脂微球注射液含量测定 取本品适量,精密称定,加无水乙醇溶解并定量稀释制成每1 ml中约含10 μg的溶液,摇匀,精密量取10 μl,注入液相色谱仪,记录色谱图;另取氟比洛芬酯对照品,同法测定。按外标法以两个对映异构体峰面积之和计算,即得。测得3批样品含量百分比分别为99.45%、99.84%和100.6%。
2.5 氟比洛芬酯脂微球注射液有关物质
2.5.1 色谱条件 色谱柱:Innovation CD串联Kromasil 100-5;流动相: 乙腈-水-冰醋酸(54∶46∶0.15);检测波长: 254 nm 流速: 1.5 ml/min;柱温: 40 ℃; 进样量: 10 μl。
2.5.2 专属性试验 设计了空白干扰试验、强制降解试验(酸、碱、氧化、高温、光照),主要考查在各种剧烈条件下,供试品新增加的降解杂质情况、降解产物与主峰的分离度情况,以此来评价色谱条件的专属性。试验结果表明,本品在酸、碱、氧化、高温和光照条件下均有不同程度的破坏,其中酸破坏、碱破坏和氧化破坏最严重,在主峰前后产生数个降解产物峰,各降解产物峰与主峰分离较好,说明本色谱条件专属性好,可用于本品的有关物质测定。见图3。

1.S-氟比洛芬酯 2.R-氟比洛芬酯
2.5.3 定量限及检测限 取氟比洛芬酯适量,加无水乙醇溶解并逐级稀释,分别量取10 μl,注入液相色谱仪,记录色谱图,按信噪比为10∶1计算检测定量限,结果为1.5 ng;按信噪比为3∶1计算最低检测限,结果为0.45 ng。
2.5.4 氟比洛芬酯脂微球注射液有关物质测定 量取本品1 ml,用无水乙醇溶解并定量稀释配制成每1 ml中约含氟比洛芬酯0.4 mg的溶液,作为供试品溶液;量取1 ml,置100 ml量瓶中,用无水乙醇定量稀释至刻度,摇匀,作为对照溶液;取对照溶液10 μl,注入液相色谱仪,调节检测灵敏度,使氟比洛芬酯峰的峰高约为满量程的10%~20%。再精密量取溶剂、对照溶液与供试品溶液各10 μl,分别注入液相色谱仪,记录色谱图至氟比洛芬酯峰保留时间的2倍。供试品溶液色谱图中如有杂质峰,除溶剂峰外,其他最大杂质的峰面积不得大于对照溶液两个对映异构体峰面积之和的0.2%;其他各杂质峰面积的和不得大于对照溶液两个对映异构体峰面积之和的0.5%。测得三批样品有关物质见表5。


1.S-氟比洛芬酯 2.R-氟比洛芬酯

批号最大单一杂质(%)其他杂质总和(%)201203010.0850.23201203020.0810.19201203030.0820.21
3 讨论
3.1 精制蛋黄卵磷脂呈颗粒黏稠状,加入注射用大豆油中,在适当的温度下搅拌很长时间不能完全溶解,加入适量的油酸可以让精制蛋黄卵磷脂完全溶解在注射用大豆油中,增强乳化效。由于卵磷脂易氧化,在加热过程中不稳定,温度不能过高,控制在65 ℃~70 ℃之间。
3.2 制备3批氟比洛芬酯脂微球注射液,其工艺稳定,质量可控,适合工业化大生产。
1 于国华,刘淑真,任海朋.氟比洛芬酯脂微球制剂在止痛领域的研究概况[J].中华肿瘤防治杂志,2007,14(20):1595-1598
2 吴燕,李冬梅, 徐超斗,等.氟比洛芬酯脂微球注射液的制备及其质量评价[J].中国药学杂志,2013,48(21):1847-1851
3 苏俊,李杨,张鹏,等.高效液相色谱法测定氟比洛芬酯[J].广东化工,2010,37(12):128-129
2015-03-27
南京工业大学校基金(No.42657631)
TQ463 R927.11
A
1006-5687(2015)03-0018-04

