MnO2/CNTs电催化剂及其对C—H键的选择性催化活化
朱英红,李艳芳,朱 颖,陈姿颖,张健青,马淳安
(浙江工业大学 绿色化学合成技术国家重点实验室培育基地,浙江 杭州 310014)
MnO2/CNTs电催化剂及其对C—H键的选择性催化活化
朱英红,李艳芳,朱颖,陈姿颖,张健青,马淳安
(浙江工业大学 绿色化学合成技术国家重点实验室培育基地,浙江 杭州 310014)
摘要:通过化学沉淀法制备了MnO2/CNTs复合电催化剂,采用X-射线衍射(XRD)对其晶型进行了表征.采用循环伏安法(CV)、恒电位电解研究了MnO2/CNTs电催化活化对甲氧基甲苯(p-MT)中C—H键的电化学氧化行为,实验结果表明:MnO2和CNTs之间具有良好的催化协同作用.恒电位电解主要氧化产物为对甲氧基苯甲醛(p-MBA).通过扫描电子显微镜(SEM)、透射电子显微镜(TEM)和高分辨透射电子显微镜(HRTEM)对MnO2/CNTs复合材料的形貌和微观结构进行了表征,结果表明:MnO2具有细须状结构。
关键词:电催化氧化;MnO2/CNT复合材料;对甲氧基甲苯;对甲氧基苯甲醛
MnO2modified CNTs electro-catalyst and its selective
electro-oxidation of C—H bond
ZHU Yinghong, LI Yanfang, ZHU Ying, CHEN Ziying, ZHANG Jianqing, MA Chunan
(State Key Laboratory of Green Chemistry Synthesis Technology, Zhejiang University of Technology, Hangzhou 310014, China)
Abstract:MnO2/CNTs electro-catalyst was prepared through a chemical deposit process, and its phase structure was characterized by X-ray diffraction (XRD). The electro-catalytic activity of MnO2/CNTs toward C—H bond in p-MT was studied by cyclic voltammetry (CV) and the constant potential electrolysis. It can be seen that MnO2and CNTs showed a synergistic catalytic activity. The major product in the electro-oxidation process was p-methoxybenzaldehyde(p-MBA). The morphology and structure of MnO2/CNTs composite were further characterized by scanning electron microscopy (SEM), transmission electron microscopy (TEM) and high-resolution transmission electron microscopy (HRTEM), and MnO2showed nanoscale architectures with fine whiskers。
Keywords:electro-catalytic oxidation; MnO2/CNTs composite; p-methoxy toluene; p-methoxybenzaldehyde
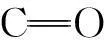
碳纳米管(CNTs)作为“C”的一种存在形式,因有较好的导电性能[10],较大的比表面积及在酸性电解液中良好的稳定性等被认为是一种比较有前景的电极材料[11-13].更有意义的是CNTs还可以通过吸附金属氧化物对表面进行修饰来提高其性能以适用于不同的电解体系[14].金属氧化物中二氧化锰不但具有价格低廉,储量丰富等特点,而且存在可变的氧化价态,是一种重要的氧化还原反应的催化剂和活性电极材料,Mn(Ⅲ)/Mn(Ⅱ)媒质也是间接电氧化合成p-MBA有效氧化还原电对[15].笔者通过化学沉积法制备MnO2/CNTs电催化剂,有效结合CNTs和金属氧化物的活性,并研究了其对p-MT中C—H键的电催化活化性能。
1实验部分
1.1实验试剂与仪器
碳纳米管(深圳市纳米港有限公司),直径为40~60 nm,长度5~15 μm,纯度≥98%,所有试剂均为分析纯.CHI660B电化学工作站(上海辰华),瑞典Biotage全自动微波合成仪,气相色谱仪(GC,Agilent 7890A,美国),DSQ单四极杆气质联用仪(GC-MS,Agilent 7890A,美国).样品的物相表征在X,Pert PRO型X射线衍射(XRD)仪上进行,X射线源为Cu Kα,电压40 kV,电流40 mA.样品的形貌和结构分析在Hitachi S-4700Ⅱ型扫描电子显微镜(SEM,操作电压15 kV)以及JEM-2010Ex型高分辨透射电子显微镜(HRTEM,操作电压为200 kV)上进行。
1.2MnO2/CNTs复合催化剂的制备
1.2.1CNTs的预处理
将多壁碳管置于浓硝酸(质量分数为65%)中,升温至150 ℃,搅拌回流4 h,冷却,水洗过滤至滤液成中性,100 ℃下干燥12 h。
1.2.2MnO2/CNTs的合成
将100 mg硝化后CNTs置于100 mL蒸馏水中,超声分散2 h,随后将不同量的KMnO4(18.2,54.5,90.8,145.3 mg)和6 mL的H2SO4(0.5 M)加入上述混合液中磁力搅拌1 h,50 ℃下微波加热10 min,水洗过滤至滤液成中性,将产物于100 ℃下通风干燥得MnO2/CNTs复合催化剂.将MnO2和CNTs的比例为0.1,0.3,0.5,0.8的复合材料依次标记为MnO2/CNT-0.1,MnO2/CNT-0.3,MnO2/CNT-0.5,MnO2/CNT-0.8。
1.3电化学性能测试
电化学测试在CHI660B型电化学工作站进行.循环伏安测试(CV)在三电极电解池中进行,其中阳极室和阴极室之间用多孔烧结玻璃隔膜分隔.工作电极的制备如下:取10 mg的电催化剂、1 mL的异丙醇和80 μL质量分数为5%的Nafion溶液超声分散成均匀的浆液,取3 μL浆液均匀滴加到直径为3 mm的玻碳电极表面,自然晾干制得工作电极.对电极为大面积铂片(2 cm×2 cm),饱和甘汞电极(SCE)为参比电极,电解液为p-MT(0.02 mol/L)+30 mL H2SO4(0.5 mol/L)+30 mL丙酮,扫描速率为50 mV/s,扫描范围为0~2.2 V。
恒电位电解实验在H型电解池中进行,电解池的阴、阳极室用离子膜分隔;阳极为复合电催化剂修饰碳纸电极(1 cm×2 cm),制备如下:取150 μL上述浆液滴加在碳纸上,自然晾干备用.阴极为大面积铂片,参比电极为饱和甘汞电极.电解电压为1.55 V,阳极液为p-MT(0.02 mol/L)+15 mL H2SO4(0.5 mol/L)+15 mL丙酮,阴极液为15 mL H2SO4(0.5 mol/L)+15 mL丙酮,阳极液用磁力搅拌器搅拌。
2结果与讨论
2.1MnO2/CNTs复合催化剂的XRD表征
图1为电催化剂MnO2/CNTs和硝化后CNTs的XRD表征结果.硝化后CNTs在2θ为26.4°处出现尖锐的(002)晶面特征衍射峰,42.2°、54.5°则为CNTs的(100)、(004)晶面[16-18].图1中2θ为12.23°,36.66°和65.66°处出现的特征衍射峰分别归属于MnO2的(002),(006)和(119)的晶面,2θ值与JCPDS 00-018-0802标准数据的2θ值相比基本一致;其特征衍射峰较弱,表明具有一定的无定形结构,这种结构不但可以使电解液自由地进出MnO2矩阵,而且在一定程度上可以增加了电解液与电极中电催化剂的接触面[19].谱图中没有出现锰的其他化合物衍射峰,因此该复合电催化材料主要由MnO2和CNTs组成。
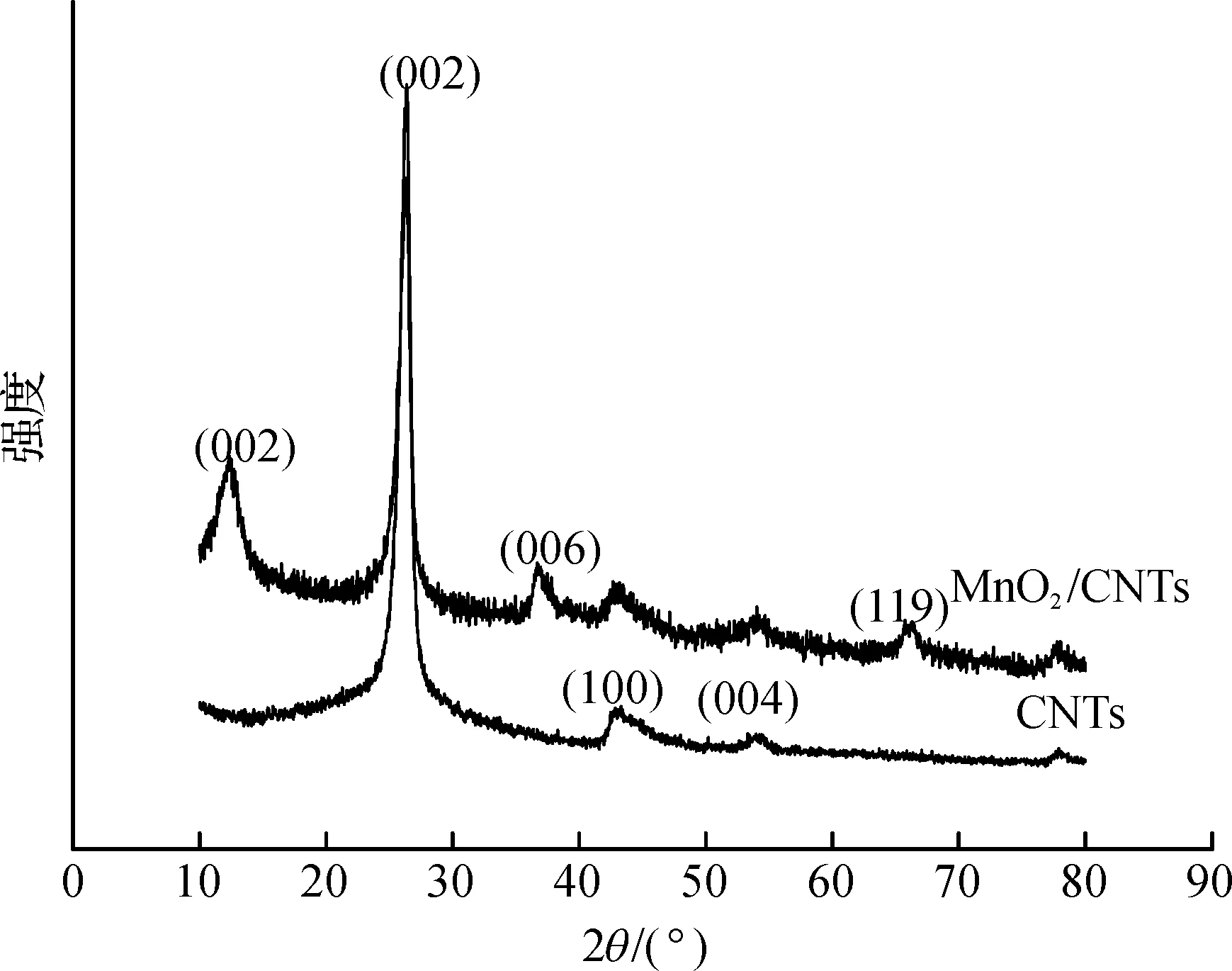
图1 CNTs和MnO2/CNTs的XRD图Fig.1 XRD pattern of CNTs and MnO2/CNTs
2.2MnO2/CNTs复合电极上p-MT的直接电催化氧化
图2为p-MT在硝化后CNTs和MnO2/CNTs电极材料上的循环伏安曲线.由图2可知:在1.55 V左右均出现了明显的p-MT氧化峰,说明在这两种电极材料上p-MT发生了电氧化反应,反扫过程中并没有观察到还原峰,说明p-MT在硫酸丙酮体系中发生的电化学氧化反应是不可逆的.MnO2/CNTs的氧化峰电流较CNTs明显增加,这表明:MnO2和CNTs之间存在协同作用,因此复合材料具有更好的电催化氧化性能。
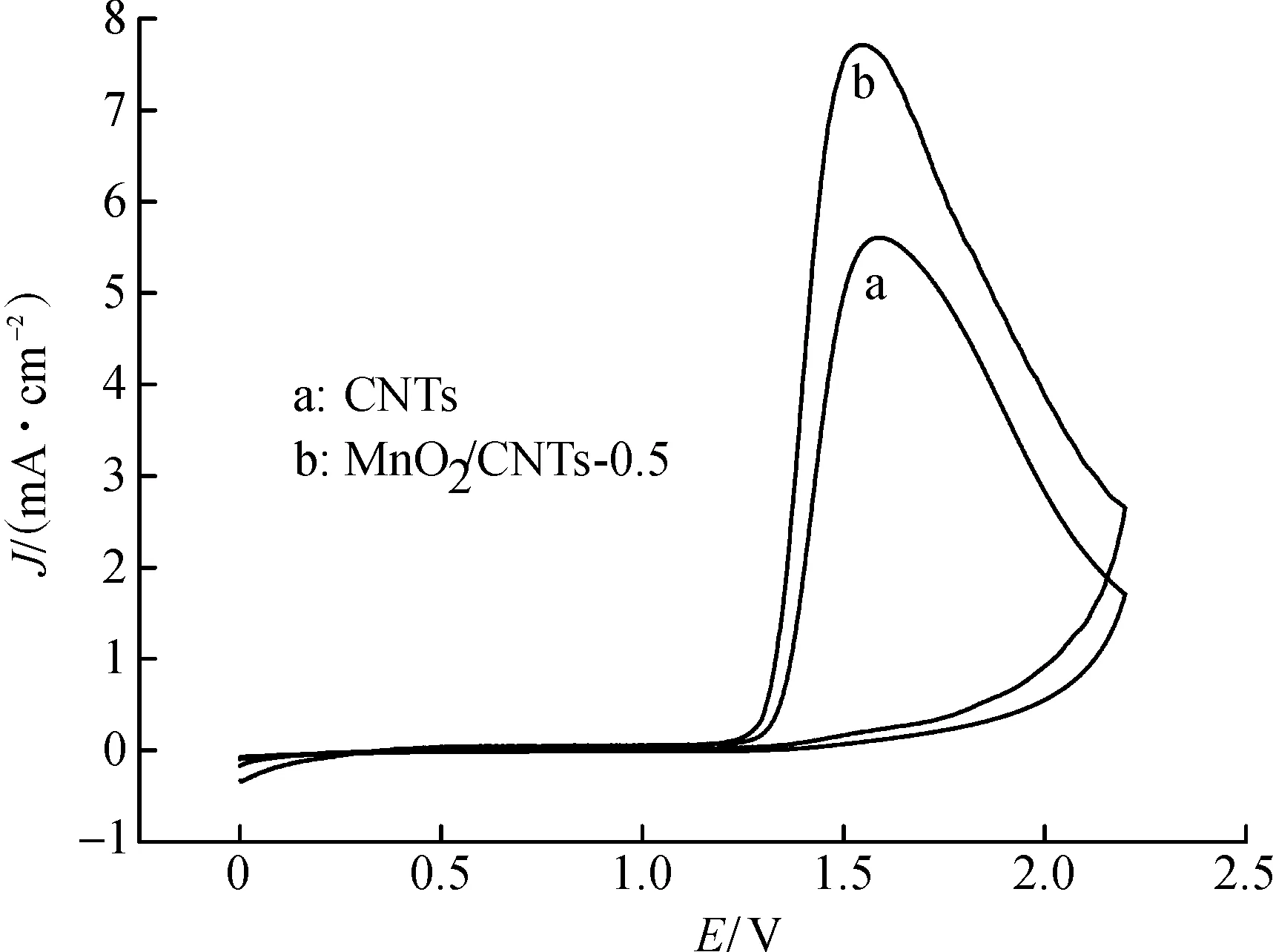
图2 p-MT在不同电极上的循环伏安曲线Fig.2 Cyclic voltammograms of p-MT on different electrodes
图3为在不同质量比的MnO2/CNTs复合电极电催化氧化p-MT的循环伏安曲线.由图3可知:在以不同MnO2含量的复合催化剂作为电极电化学氧化p-MT时,起峰电位均在1.2 V左右,且在1.55 V左右峰电流达到最大.当MnO2和CNTs的比例低于0.5时,随着MnO2负载量的增大,氧化峰电位基本保持不变,峰电流增大;随着MnO2负载量继续增大,峰电流变化不大.为了进一步证明不同MnO2负载量对电氧化的影响,以不同MnO2含量的MnO2/CNTs修饰的碳纸作电极,进行恒电位电解实验,在313 K下电解7 h,结果列于表1中:当MnO2的含量低于0.5,随着MnO2含量的增加,电氧化产物中p-MBA的产率明显提高,而后随着MnO2含量的继续增加,p-MBA的产率变化不大,这与循环伏安中的结果一致.这说明MnO2和CNTs之间存在一个最佳含量比例,此时两者之间的协同催化作用最强,电催化氧化p-MT的活性位点达到最多。
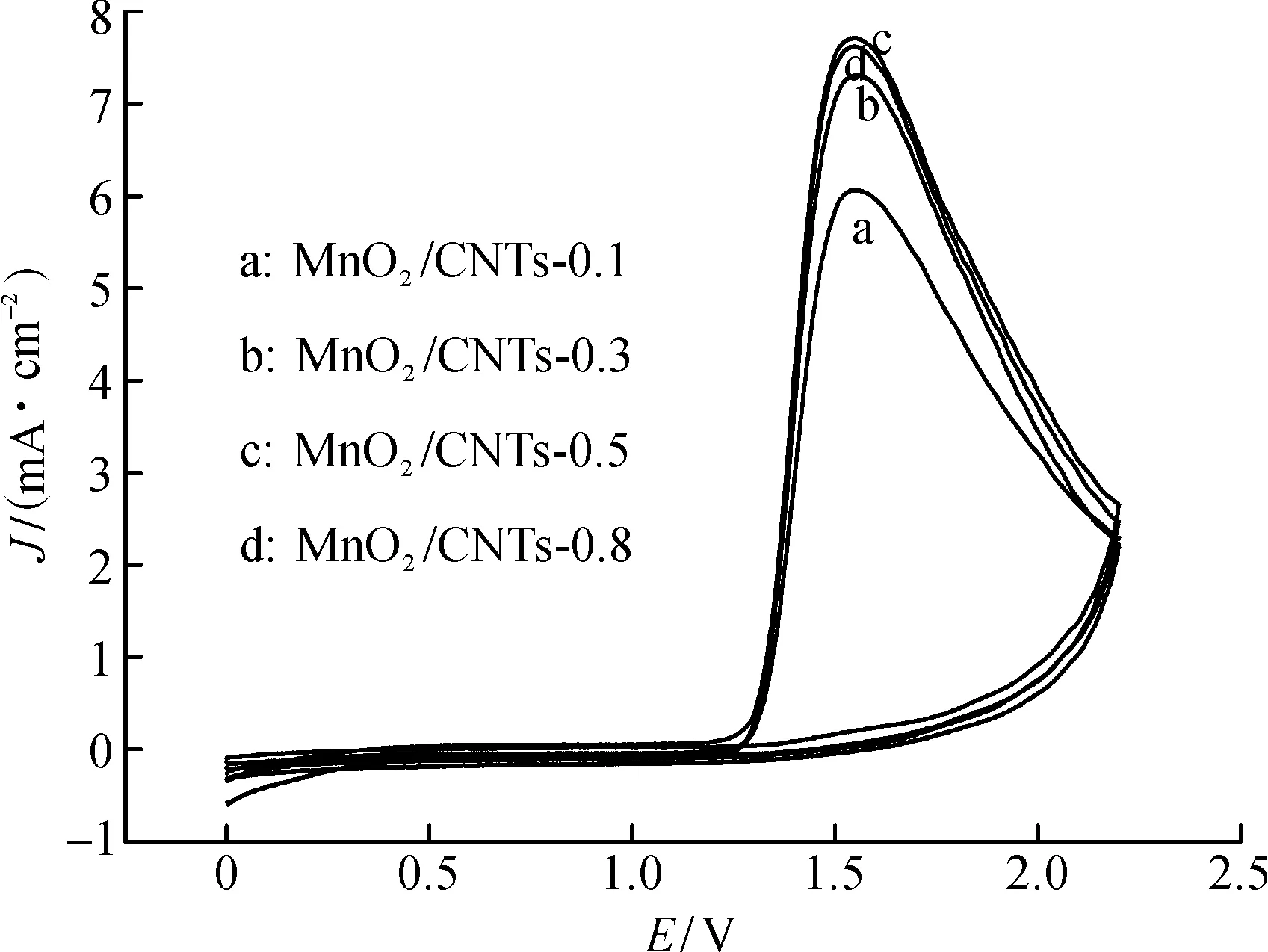
图3 不同质量比的复合电极电氧化p-MT的循环伏安曲线Fig.3 Cyclic voltammograms of p-MT on different percentage of composite electrodes
表1不同质量比的复合电极电氧化合成p-MBA的产率(T=313 K,t=7 h)
Table 1Yield ofp-MBA on on different percentage of composite electrodes
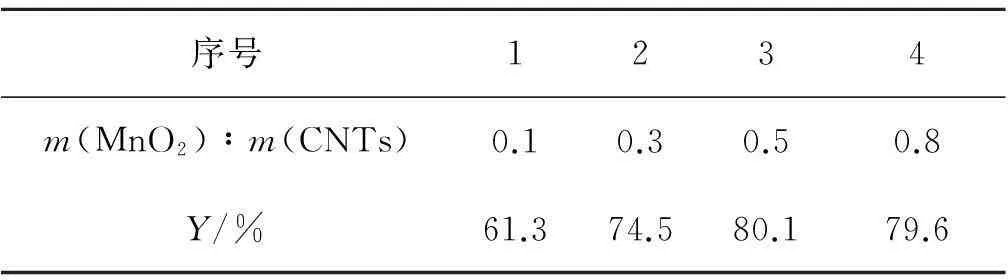
序号1234m(MnO2)∶m(CNTs)0.10.30.50.8Y/%61.374.580.179.6
图4为在MnO2/CNTs-0.5复合电极上不同温度下p-MT电化学氧化的循环伏安曲线.由图4可知:当电解液的温度由293 K升高到323 K时,峰电位保持不变,而峰电流会随着温度的升高而增加.这是因为反应温度的升高,加快了反应底物p-MT向电极表面上的扩散,因此反应速度增加,峰电流增加[20].表2为不同温度下在MnO2/CNTs-0.5复合电催化剂修饰的碳纸电极上恒电位电解5 h结果,由此可知:适当增加温度有利于电氧化合成p-MBA,但温度升高到313 K以上后,产率增加不是很明显,同时由于323 K已接近丙酮的沸点,容易引起实验误差,所以本实验中取313 K为研究温度。
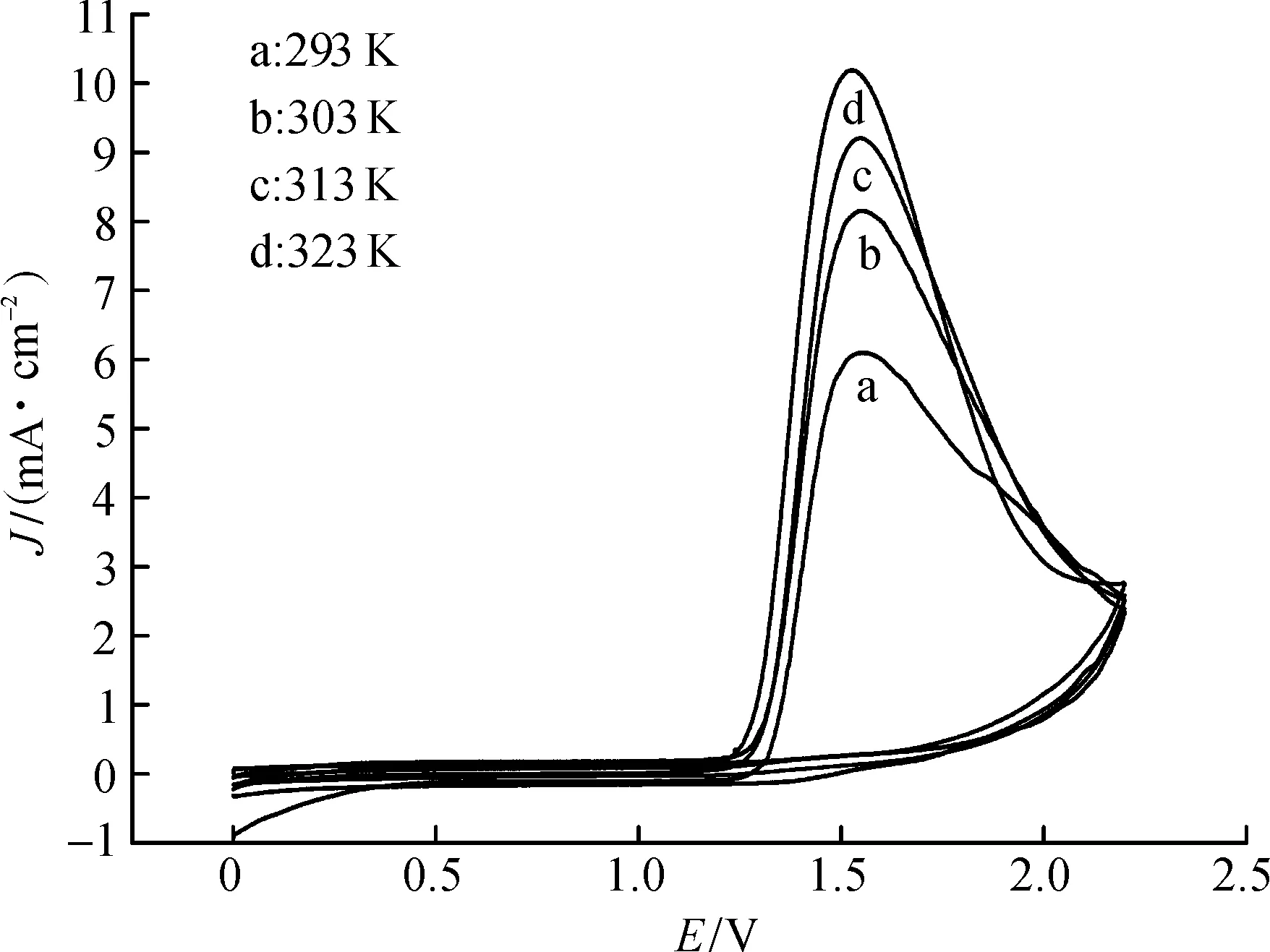
图4 MnO2/CNTs-0.5复合电极上不同温度下电氧化p-MT的循环伏安曲线Fig.4 Cyclic voltammograms of p-MT under different temperatures on MnO2/CNTs-0.5 composite electrode
表2在MnO2/CNTs-0.5复合电极上不同温度下p-MBA的产率(t=5 h)
Table 2Yield ofp-MBA under different temperatures on MnO2/CNTs-0.5 composite electrode
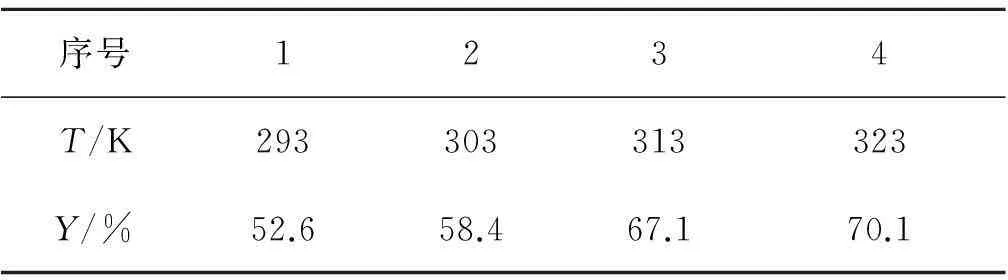
序号1234T/K293303313323Y/%52.658.467.170.1
图5为313 K时在MnO2/CNTs-0.5复合电极上p-MT电氧化电解过程中不同物种随电解时间的变化情况:随着电解时间的增加,p-MT的含量减少,p-MBA的含量逐渐增加,而对甲氧基苯甲醇的含量基本不变.这说明在MnO2/CNTs复合电极上p-MT可能首先被氧化成对甲氧基苯甲醇,醇很容易进一步被氧化成p-MBA,产物中没有检测到醛的进一步氧化产物对甲氧基苯甲酸,说明在该体系中对p-MBA具有较好的选择性。
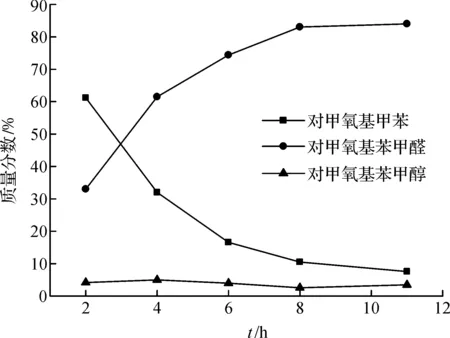
图5 电解过程中不同物种随电解时间的变化情况Fig.5 Percentage of reactant and products on different electrolysis time
2.3MnO2/CNTs复合电催化剂的形貌结构表征
电催化剂表面形貌结构直接影响其电催化活性,因此我们进一步采用SEM、TEM和HRTEM对具有最佳性能的MnO2/CNTs-0.5复合材料进行表征(图6).由图6(a)可见纳米碳管的表面均匀地分布着许多颗粒;图6(b)上可以更清楚看到这些颗粒由生成的MnO2和纳米碳管缠绕在一起构成,而且MnO2具有像细须一样的形貌,长度在30~40 nm之间;而在HRTEM图6(c)中可以清晰地观察到MnO2和CNTs的晶格条纹,晶格间距d=0.71 nm归属于MnO2的(002)晶面,d=0.32 nm归属于CNT的(002)面.这进一步说明经过硝化处理的CNTs表面产生的亲水性官能团(如―COOH,―OH)等有利于负载活性物质金属氧化物,同时KMnO4在酸性溶液中发生如下分解反应:
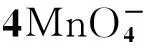
生成的MnO2会吸附在或者沉积在CNTs的表面,同时生成的O2气体有利于使MnO2形成更细微的表面结构[21]。

图6 MnO2/CNTs-0.5的表征图Fig.6 Images of MnO2/CNTs-0.5
3结论
MnO2/CNTs复合材料对p-MT中C—H键选择性氧化为―CHO具有较好的电催化性能;适当提高MnO2的负载量以及电解液的温度都会提高电催化活性,而且在313 K,MnO2/CNTs-0.5复合电极上电解7 h,p-MBA的产率可达80%.制得的MnO2/CNTs复合材料,能有效利用MnO2和CNTs之间的协同催化作用,将其作为电极材料应用于直接有机电化学合成领域并能解决催化剂的回收利用问题。
参考文献:
[1]MARTIN A, LUCKE B. Ammoxidation and oxidation of substituted methyl aromatics on vanadium-containing catalysts[J]. Catalysis Today,2000,57:61-70。
[2]PONZI M, DUSCHATZKY C, CARRASCULL A, et al. Obtaining benzaldehyde via promoted V2O5catalysts[J]. Applied Catalysis A: General,1998,169:373-379。
[3]李美超,许志花,马淳安,等.有机合成中的绿色化学[J].浙江工业大学学报,2002,30(5):500-505。
[4]张虹,储诚普,徐颖华,等.弱碱体系中的电化学合成3,6-二氯吡啶甲酸[J].浙江工业大学学报,2012,40(4):379-383。
[5]褚道葆,何建国,侯源源,等.乙二醛在Ti/纳米TiO2-Pt修饰电极上的电催化氧化[J].物理化学学报,2009,25(7):1434-1438。
[6]OKAJIMA M, SOGA K, NOKAMI T, et al. Oxidative generation of diarylcarbenium ion pools[J]. Organic Letters,2006,8(22):5005-5007。
[7]CHU Daobao, XU Mai, LU Jia, et al. Electrocatalytic reduction of diethyl oximinomalonate at a Ti/nanoporous TiO2electrode[J]. Electrochemistry Communications,2008,10:350-353。
[8]FALGAYRAC G, SAVALL A. Anodic oxidation of p-methoxytoluene in acetic acid on graphite[J]. Journal of Applied Electrochemistry,1998,28:1137-1140。
[9]吴玲玲,朱英红,李姗姗,等.茴香醛的直接电氧化合成研究[J].电化学,2011,17(2):227-230。
[10]张诚,祝军,马淳安.聚合物/碳纳米管导电复合材料研究进展[J].浙江工业大学学报,2010,38(1):1-6。
[11]HUANG Yiyin, CAI Jindi, GUO Yonglang. Roles of Pb and MnOxin PtPb/MnOx-CNTs catalyst for methanol electro-oxidationInt[J]. International Journal of Hydrogen Energy,2012,37:1263-1271。
[12]BASRI S, KAMARUDIN S K, DAUD W R W, et al. Nanocatalyst for direct methanol fuel cell (DMFC)[J]. International Journal of Hydrogen Energy,2010,35:7957-7970。
[13]滕文娟,毛信表,马淳安.碳纳米管载碳化钨的制备及其对甲醇氧化的电催化性能[J].浙江工业大学学报,2011,39(4):364-368。
[14]ZHANG Xinwei, ZHU Hong, GUO Zhijun, et al. Design and preparation of CNT@SnO2core-shell composites with thin shell and its application for ethanol oxidation[J]. International Journal of Hydrogen Energy,2010,35:8841-8847。
[15]钱海燕,曾跃,李源栋.茴香脑间接电氧化合成茴香醛[J].应用化工,2009,38(4):477-482。
[16]XU Dongwei, LI Baohua, WEI Chunguang, et al. Preparation and characterization of MnO2/acid-treated CNT nanocomposites for energy storage with zinc ions[J]. Electrochimica Acta,2014,133: 254-261。
[17]SODTIPINTA J, PON-ON W, VEERASAI W, et al. Chelating agent- and surfactant-assisted synthesis of manganese oxide/carbon nanotube composite for electrochemical capacitors[J]. Materials Research Bulletin,2013,48: 1204-1212。
[18]SUN Zhenyu, LIU Zhimin, HAN Buxing, et al. Fabrication of ruthenium-carbon nanotube nanocomposites in supercritical water[J]. Advanced Materials,2005,17(7) :928-932。
[19]ZHANG Yong, YAO Qianqian, GAO Haili, et al. Facile synthesis and electrochemical performance of manganese dioxide doped by activated carbon, carbon nanofiber and carbon nanotube[J]. Powder Technology,2014,262: 150-155。
[20]朱英红,曾红燕,李姗姗,等. 离子液体BMIMBF4中对甲氧基甲苯的电化学氧化[J]. 物理化学学报,2012,28(2): 421-426。
[21]HUANG Xiangpin, PAN Chunxu, HUANG Xingtang. Preparation and characterization of γ-MnO2/CNTs nanocomposite[J]. Materials Letters,2007,61: 934-936。
(责任编辑:陈石平)
中图分类号:O646
文献标志码:A
文章编号:1006-4303(2015)02-0128-05
作者简介:朱英红(1975—),女,浙江义乌人,副教授,研究方向为绿色有机电合成、有机催化,E-mail:yhzhuchem@zjut.edu.cn。
基金项目:国家973重点基础研究发展计划资金资助项目(2012CB722604)
收稿日期:2014-11-11

