多排螺旋CT血管重建对腹部精原细胞瘤的诊断价值
多排螺旋CT血管重建对腹部精原细胞瘤的诊断价值
顾国华1,吴晓1,黄小燕1,耿小川2
1浙江省湖州市中心医院放射科,浙江湖州 313000
2上海交通大学医学院附属仁济医院放射科,上海 200127
关键词:精原细胞瘤;腹部;多排螺旋CT;血管重建
腹部精原细胞瘤临床少见,由于患者难以启齿,一般临床均无提供隐睾病史,为影像诊断带来一定的困难。多排螺旋CT(multi-detector row spiral CT,MSCT)血管重建对明确腹部肿瘤来源,诊断本病具有很大优势。本研究回顾性分析了6例经临床病理证实为腹部精原细胞瘤的MSCT影像表现,评估了MSCT对腹部精原细胞瘤的诊断价值。
资料和方法
资料来源收集2010年1月至2014年4月在湖州市中心医院和上海交通大学医学院附属仁济医院经手术或穿刺病理证实的精原细胞瘤患者6例,均为男性,平均年龄(43±5)岁(35~65岁);临床表现为腹痛、腹胀及腹部肿块,病程1个月~1年,CT扫描前临床均无提供隐睾病史。6例均行CT平扫加增强扫描。
检查方法采用东芝Aquilion 16螺旋CT及西门子16螺旋CT,行常规平扫+增强扫描,动脉期扫描时间 25~30 s,静脉期扫描时间60~70 s,延迟期扫描120~150 s。对比剂采用欧乃派克(300 mgI/ml)或碘海醇(300 mgI/ml)100 ml,注射速率3~4 ml/s。扫描参数:管电压120 kV,管电流200 mA,准直器1.0 mm×16 mm,螺距1,FOV400 mm,0.5 s/rot,重建层厚1 mm,重建间隔0.5 mm,重建函数10。CT轴位扫描获得图像数据传至工作站行后处理,以多平面重建(multiplanar reformation,MPR)、最大密度投影(maximum intensity projection,MIP)及容积演示(volume rendering,VR)进行多方位观察。
结果
6例均为腹膜后椭圆形软组织肿块,肿块大小不等,最大9.1 cm×12.3 cm,最小6.5 cm×8 cm。5例位于右侧,1例位于左侧。1例较大肿块边界不清,位于右侧前腹壁,与腹壁及周围肠道黏连(图1);5例肿块边界清、包膜完整,周围肠道均有轻度受压移位,均未见肠梗阻。1例右侧肿块压迫同侧输尿管,引起右侧肾盂少量积水。平扫时6例肿块密度均不均匀,肿块近体中线见囊变或坏死,其中1例肿块内见钙化及同侧髂外动脉旁淋巴结肿大转移(图2),但肿块及淋巴结经放化疗后随访明显缩小。肿块平扫CT值32~48Hu,增强后均有不均匀强化,静脉期CT值达50~68Hu,囊变、坏死灶未见强化。6例肿块血供均由同侧位于肠系膜下动脉上缘2~3 cm处的睾丸动脉供血(图3),供血动脉呈扭曲状、无分支且细长从肿块后下缘进入肿块,肿块内见分支状条状强化血管影(图4)。2例右侧肿块后缘见引流静脉(图5),静脉回流至下腔静脉;左侧肿块未见明显引流静脉。6例肿块同侧睾丸及精索均未见,但睾丸引带均见,至于同侧腹股沟外口。
病理表现6例瘤细胞大小不等,圆形或多边形,胞浆透亮,核大,核仁明显,间质内见淋巴细胞浸润,肿瘤内可见坏死。
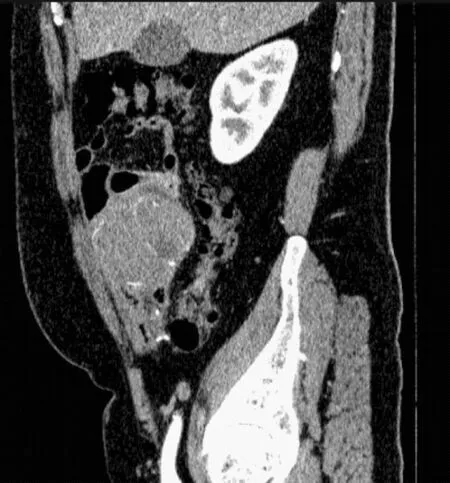
图 1患者,男,48岁,多平面重建显示精原细胞瘤边界不清,与前腹壁及周围肠道黏连,内见坏死及条状强化血管

图 2患者,男,65岁,精原细胞瘤位于右侧髂窝,内见钙化,髂外动脉旁见肿大淋巴结坏死

图 3患者,男,53岁,容积演示显示精原细胞瘤供血动脉(箭头)由同侧位于肠系膜下动脉上缘2~3 cm处的睾丸动脉发出,呈扭曲状、无分支进入肿块
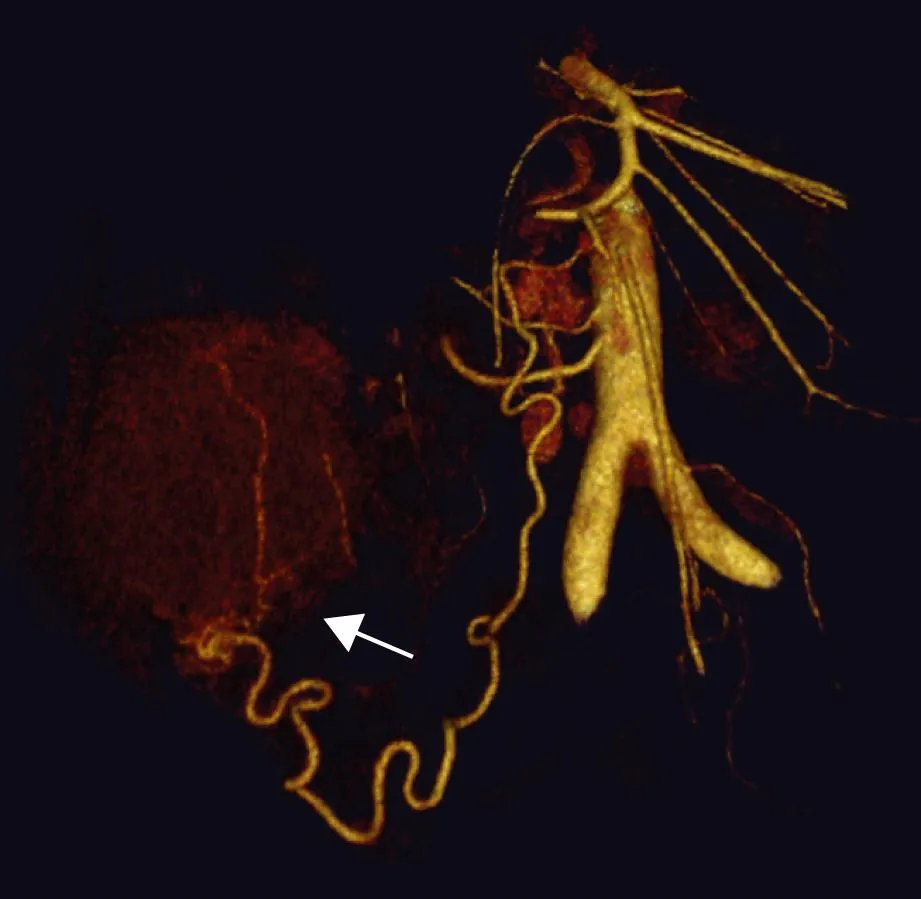
图 4患者,男,53岁,容积演示显示供血动脉进入精原细胞瘤(箭头)后呈分支状供应肿块,内见多发粗大血管影

图 5患者,男,35岁,精原细胞瘤后缘见引流静脉,肿块包膜完整边界清,内见坏死灶
讨论
睾丸在下降过程中受到激素、内分泌作用及物理机械作用等因素影响,停留于下降过程的任何一处,从而形成隐睾,隐睾发生肿瘤的概率是正常睾丸的20~40倍[1]。隐睾分为腹内型和腹股沟型,腹内型隐睾肿瘤发生率达22.7%[2],腹股沟型肿瘤位置浅容易发现,肿瘤发生率相对较低。Ueno等[3]认为,纯精原细胞瘤占未降睾丸肿瘤的90%。未降睾丸发生恶变的原因可能与睾丸的先天性缺陷、血供障碍、位置及周围的温度有关[4]。睾丸精原细胞瘤好发于30~50岁[5],右侧多见,有隐睾史及腹痛、腹胀和腹部肿块等症状,本组6例均有隐睾史,5例发生于右侧及此年龄段,与文献基本一致,有腹痛者5例,腹胀3例,1例自己摸到腹部肿块就诊。
腹膜后精原细胞瘤平扫时肿瘤均较大,呈椭圆形,边界清,包膜完整,密度不均匀,内见囊变及坏死,是因肿瘤位置深,常位于腹膜后及盆腔,病程又较长,所以肿瘤发现时均较大。本组5例边界清,包膜完整,因睾丸白膜韧厚所致,只有1例肿块边界不清,周围腹膜及肠道有黏连,是因肿瘤突破包膜对周围组织侵犯所致。6例肿块近体中线均见囊变及坏死,是因肿瘤生长缓慢,缺血所致。肿瘤较大时可压迫周围组织,本组6例周围肠道均有受压,但均未见肠梗阻,1例右侧输尿管受压引起同侧肾盂少量积水。钙化罕见,本组有1例内见点状钙化。淋巴道转移较常见,但本组仅有1例肿块突入右侧髂窝伴右侧髂外动脉旁淋巴结转移。增强后肿瘤有不均匀强化,实性部分轻-中度强化,囊性坏死灶未见强化,本组6例肿块均呈持续强化,实性部分CT值强化程度在18~28Hu之间,内见条状血管影,肿瘤血供丰富但强化呈轻-中度强化,董丽卿等[6]认为其与睾丸在青春期后迅速形成的血睾屏障有关,此屏障阻碍了造影剂通过,而腹部隐睾来源的睾丸肿瘤保留睾丸一些组织,以致肿瘤血供丰富但强化一般。以往研究对腹膜后精原细胞瘤血供分析较少,本组6例经血管重建肿瘤供血动脉均位于肠系膜下动脉上缘约2~3 cm,直接从腹主动脉前外侧发出,经腰大肌前缘呈扭曲、无分支向前向外进入肿瘤,进入肿瘤后呈分支状,肿瘤供血动脉走行完全符合睾丸动脉走行,故笔者认为此动脉走行为诊断本病提供了充分依据。由于正常睾丸动脉细小,本组健侧均未见睾丸动脉。Lim等[7]提出了肿瘤引流静脉,但国内均未见此报道。本组6例中2例右侧肿块显示引流静脉,引流静脉从肿块后缘发出,向后沿腰大肌前缘汇入下腔静脉,此静脉回流与睾丸静脉回流一致,更加支持睾丸肿瘤的诊断。所以笔者认为16排以上CT经过VR、MIP及MPR后处理,通过对肿瘤供血血管重建,对明确肿瘤来源、定位、定性均具有重要价值。腹膜后精原细胞瘤是由于睾丸未降所致,因此本组6例同侧睾丸均缺如,但肿瘤均有引带,至于腹股沟外口,同侧精索均未见。精原细胞瘤对放、化疗比较敏感,本组1例肿块伴同侧髂动脉旁淋巴结转移、坏死,经放化疗后,肿块及淋巴结明显缩小,腹膜后精原细胞瘤均由睾丸动脉供血,较大肿瘤可介入栓塞,为临床手术提供机会。
腹膜后精原细胞瘤主要与间质瘤、腹膜后纤维化、神经源性肿瘤、淋巴瘤及转移瘤鉴别,虽然这些肿瘤与腹部精原细胞瘤有许多影像学上相同点[8],但根据隐睾病史,肿瘤的强化程度及肿瘤的睾丸动脉供血,与以上肿瘤鉴别相对不难。
综上,MSCT加血管成像是发现和诊断腹膜后精原细胞瘤的重要手段,腹部肿块,有隐睾病史,肿块包膜完整、内见坏死,增强后不均匀强化,血管成像是睾丸动脉供血时,可对肿瘤作出睾丸精原细胞瘤的定性诊断。
参考文献
[1]武志刚,蔡健,林礼彰,等. 双侧隐睾并发单侧恶变精原细胞瘤1例报告[J]. 中华男科学杂志,2010,16(7):662- 663.
[2]梁玉安,赵云江. 腹内型隐睾并精原细胞瘤的CT征象分析[J]. 医学影像学杂志,2011,21(11):1779- 1780.
[3]Uenot T,Tanaka YO,Nagata M,et al.Spectrum of germ cell tumors:from head to toe[J].Radiographies,2004,24(3):387- 404.
[4]陈杰,李瑞英. 睾丸精原细胞瘤78例临床分析[J].中国肿瘤临床,2003,30(3):203- 205.
[5]田保玲,高霭峰,徐灿,等. 精母细胞型精原细胞瘤的临床病理分析[J].中华病理学杂志,2012,41(11):752- 755.
[6]董丽卿,陈伟建,韩萍,等.多层螺旋CT血管成像对腹部隐睾肿瘤的诊断价值[J].中华放射学杂志,2006,40(8):860- 862.
[7]Lim YJ,Jeong MJ,Bae BN,et al.Semioma in undescended testis[J].Abdom Imaging,2007,31(4):511- 513.
[8]Woodward PJ. Case70:sem seminom a in an undescended testis[J]. Radiology,2004,231(3):388- 392.
·短篇论著·
收稿日期:(2014- 06- 26)
DOI:10.3881/j.issn.1000- 503X.2015.01.017
中图分类号:R697+.22;[R445.3]
文献标志码:A
文章编号:1000- 503X(2015)01- 0090- 03
通信作者:吴晓电话:0572- 2023301,电子邮件:wuxiao@163.com

