共沉淀法和燃烧法制备纳米Fe3O4及其磁性能研究
高慧昀,王晓丽
(毕节学院 物理科学与技术学院,贵州 毕节 551700)
近年来,磁性铁氧化物(尤其是Fe3O4)越来越受关注,由于具有特殊的磁导向性、超顺磁性,以及表面可连接生化活性功能基团等特性,使其在颜料、磁共振成像、磁给药、铁液、录音材料、催化剂及数据存储等方面具有广泛应用[1-3]。磁铁矿纳米粒子的超顺磁特性源于颗粒磁化循环时的微弱能量[4]。目前,Fe3O4已经可以通过多种方法制备,如电弧放电法,机器研磨法,激光烧蚀法,以及高温有机分解法等[5],最常用的是共沉淀法、热水法及溶胶-凝胶法[6-8]。燃烧法也是合成纳米颗粒的一种有效方法[9-13],已被用于合成不同的氧化物,其中包括铁氧体和钙铁矿等,但用于制备Fe3O4纳米颗粒的研究很少。试验采用共沉淀法和燃烧法制备纳米Fe3O4颗粒,并对其微观结构、光学特性和磁性进行研究。
1 试验部分
1.1 试验材料
试验所用试剂:六水氯化铁(FeCl3·6H2O),四水氯化亚铁(FeCl2·4H2O),氨溶液(26%,Aldrich公司),硝酸铁,甘氨酸,淀粉,硝酸铵,均为分析纯。
1.2 试验方法
1.2.1 共沉淀法
按2∶1的质量比配制氯化铁和氯化亚铁混合溶液。将溶液在50℃下加热10min,然后在50℃的磁性搅拌器中加氨水连续搅拌至产生黑色沉淀物(氧化铁)。用强磁性磁铁将这些沉淀物颗粒分离出来,用蒸馏水多次洗涤,最后放置于100℃的热空气炉中加热10h。
制备过程的总反应为
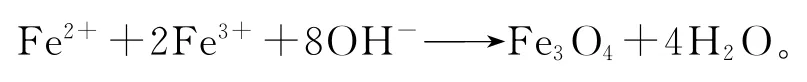
1.2.2 燃烧法
用硝酸铁作氧化剂,甘氨酸、硝酸铵和淀粉作燃料。按化学计量称取原料,用研钵研磨混匀。把石英坩埚加热到约500℃,将研磨后的混合物放入坩埚中加热2h,最后,收集黑色粉末。
1.3 试样的特性观察
用X射线衍射仪分析Fe3O4纳米颗粒的物相组成(Cu-Kα射线,扫描范围20°~70°,扫描速度21次/min),用X′pert high score plus软件计算颗粒的结构和晶胞参数,用JEOL JSM 6480 LV扫描电子显微镜观测试样表面形貌,用投射电子显微镜(TEM)观察颗粒的形态和大小,用UV CARY 100紫外-可见光谱扫描仪研究试样的光学特性。室温下,用Quantum Design公司的磁强计研究试样的磁特性。
2 试验结果与讨论
图1(a)为共沉淀法制备的Fe3O4纳米颗粒的X-射线衍射图。可以看出,XRD衍射峰清晰可见,层次分明,没有次杂峰,说明试样具有良好的结晶性和均一性,纯度较高。
图1(b)为燃烧法制备的Fe3O4纳米颗粒的XRD图。与共沉淀法制备的试样相比,其X射线衍射峰相对较宽,更具有纳米晶体特性。与标准卡(JCPDS,No.88-0315)匹配结果表明,Fe3O4纳米颗粒具有单相性。利用文献[6]方法计算Fe3O4纳米颗粒的晶体尺寸,结果表明,燃烧法制备的Fe3O4纳米颗粒的平均尺寸小于共沉淀法制备的Fe3O4颗粒平均尺寸。用X′pert high score plus软件计算的Fe3O4纳米颗粒晶胞参数见表1。

图1 Fe3O4纳米颗粒的X-射线衍射图
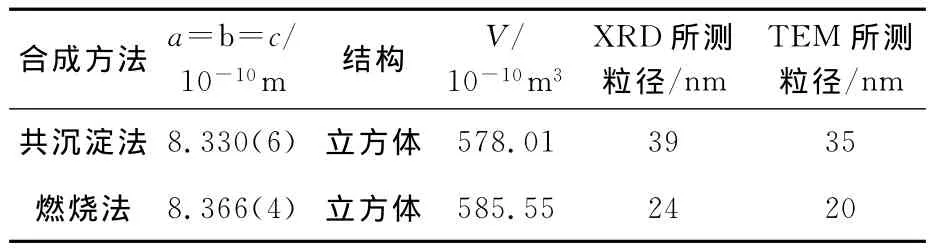
表1 Fe3O4纳米颗粒的晶胞参数
从表1看出:燃烧过程中,颗粒尺寸减小,晶格参数增大;共沉淀法和燃烧法制备的Fe3O4纳米颗粒的粒径分别为35nm和20nm。
制备的Fe3O4纳米颗粒的紫外-可见吸收光谱如图2所示。可以看出,两种方法所得试样都具有单向吸收特性,表明形成的是单相化合物。燃烧法制备的试样的吸收峰波长降低,说明带隙取决于粒径的大小。
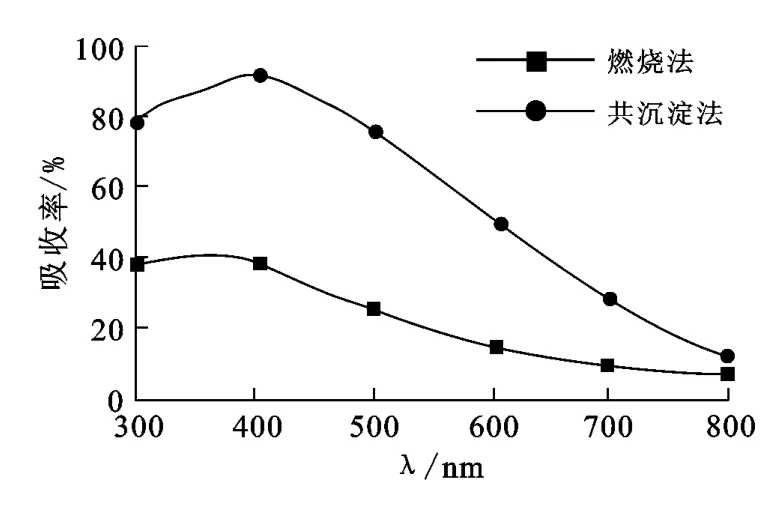
图2 Fe3O4纳米颗粒的光学特性
图3为Fe3O4颗粒的带隙。燃烧法制备的Fe3O4颗粒的带隙比共沉淀法合制备的Fe3O4颗粒带隙宽,二者的带隙分别为2.08和1.88nm。
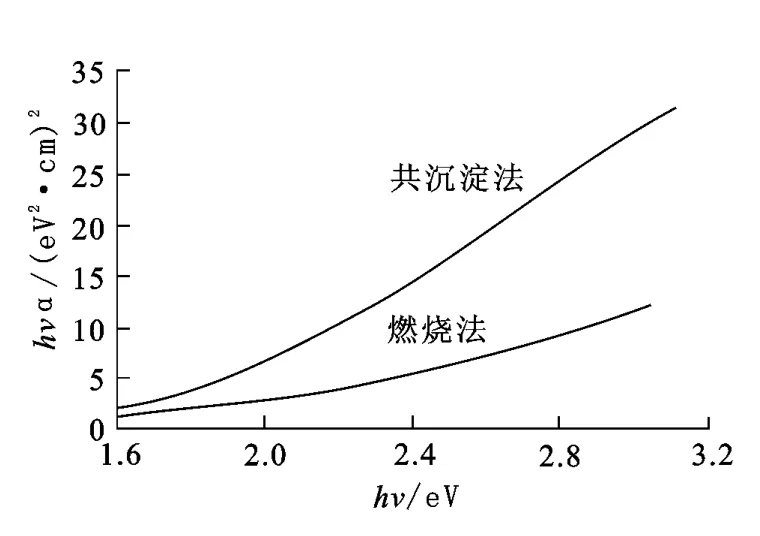
图3 共沉淀法和燃烧法制备的Fe3O4纳米颗粒带隙曲线
图4所示为Fe3O4纳米颗粒的磁化强度与磁场强度关系曲线。试样的磁性并不强烈,但具有超顺磁性,且饱和磁化强度(Ms)较高。共沉淀法合成的Fe3O4颗粒的饱和磁化强度为63.5emu/g。
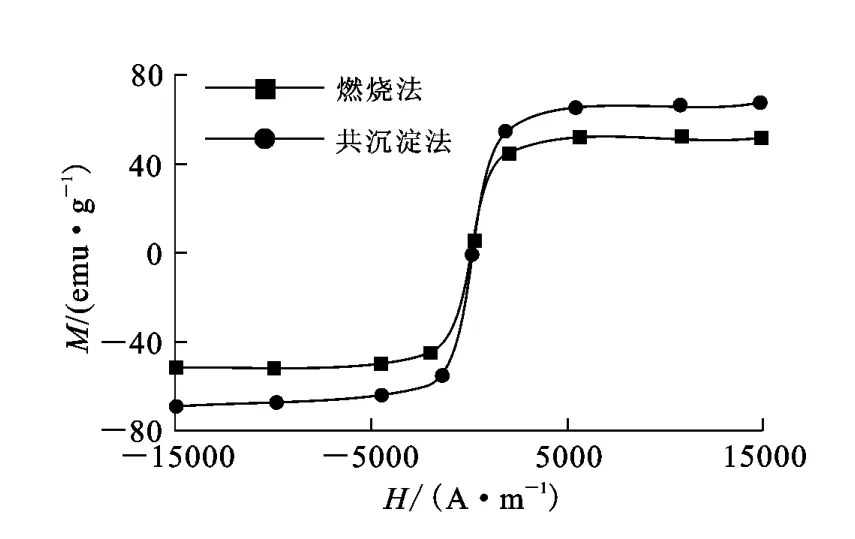
图4 Fe3O4纳米颗粒的磁化强度与磁场强度关系曲线
3 结论
用共沉淀法和燃烧法可制备Fe3O4纳米颗粒。燃烧法制备的Fe3O4纳米颗粒存在蓝光偏移。共沉淀法和燃烧法制备的Fe3O4纳米颗粒的带隙分别约为1.88nm和2.08nm,均具有超顺磁特性,并且没有磁带回线;具有极高的比表面积和优异的热稳定性;共沉淀法制备的Fe3O4纳米颗粒的饱和磁化强度高达63.5emu/g。
[1]Mihoc G,Lanos R,Pacurariu C,et al.Combustion Synthesis of Some Iron Oxides Used As Adsorbents for Phenol and P-chlorophenol Removal From Sastewater[J].Journal of Thermal Analysis and Calorimetry,2013,112(1):391-397.
[2]Teja A S,Koh P Y.Synthesis,Properties and Applications of Magnetic Iron Oxide Nanoparticles[J].Progress in Crystal Growth and Characterization of Materials,2009,55 (1/2):22-45.
[3]Wang X.Preparation of Magnetic Hydroxyapatite and their use as Recyclable Adsorbent for Phenol in Wastewater[J].Clean Soil Air Water,2011,39(1):13-27.
[4]Sun J,Zhou S,Hou P,et al.Synthesis and Characterization of Biocompatible Fe3O4Nanoparticles[J].Journal of Biomedical Materials Research Part A,2007,80(12):333-341.
[5]Ahangaran F,Hassanzadeh A,Nouri S.Surface Modication of Fe3O4-SiO2Microsphere by Silane Coupling Agent Int[J].Nano Letters,2013,3(24):23-30.
[6]Ghandoor H EI,Zidan H M,Khalil M H,et al.Synthesis and Some Physical Properties of Magnetite(Fe3O4)Nanoparticles[J].Interna-tional Journal of Electrochemical Science,2012,7(18):5734-5745.
[7]Asim N.Synthesis of Fe3O4Nanocrystals using Hydrothermal Approach[J].Journal of Magnetism and Magnetic Materials,2012,324(25):4147-4150.
[8]Raja K,Verma S,Karmakar S,et al.Synthesis and Characterization of Magnetite Nanocrystals[J].Crystal Research and Technology,2011,46(19):497-500.
[9]Patil K C,Aruna S T,Mimami T.Combustion Synthesis:an Update[J].Current Opinion in Solid State and Materials Science,2002,6(22):507-512.
[10]Mathews T.Solution Combustion Synthesis of Magnesium Compensated Sodium-β-aluminas[J].Materials Science and Engineering:B,2000,78(31):39-43.
[11]Mukasyan A S,Costello C,Sherlock K P,et al.Perovskite Membranes by Aqueous Combustion Synthesis:Synthesis and Properties[J].Separation and Purication Technology,2001,25(29):117-126.
[12]Rao G R,Sahu H R,Mishra B G.Surface and Catalytic Properties of Cu-Ce-O composite Oxides Prepared by the Combustion Method[J].Colloids and Surfaces:A,2003,220(1/3):261-269.
[13]Fu Y P,Lin C H,Preparation of CexZr1-xO2Powders by Microwave-induced Combustion Process[J].Journal of Alloys and Compounds.2003,354(42):232-235.

