锌掺杂TiO2的制备及其可见光催化性能
齐秀丽,李海燕,李秋叶
(1.河南大学 基础实验教学中心,河南 开封475004; 2.河南大学 化学化工学院,河南 开封475004;3.河南大学 特种功能材料教育部重点实验室,河南 开封475004)
随着经济的高速发展和人口的快速膨胀,环境问题正在影响着人类的生活质量、身体健康和生产活动等各个方面.空气污浊以及饮用水质量下降都威胁着人类的健康.上世纪70年代,光催化技术的发展给人们带来了新的福音,半导体光催化技术可以有效利用太阳能解决环境中的污染问题,是提高环境质量的有效途径之一.
TiO2具有化学性质稳定、廉价易得、无毒、不产生二次污染等优点,有很好的应用前景.但是TiO2在实际应用中还存在一些问题,比如:1)带隙较宽(约3.2eV),对应的吸收波长为387nm,光吸收仅局限于紫外区,对太阳光不能充分利用.而紫外光只占太阳光的一小部分(约4%~5%)[1-2];2)光量子效率比较低,光生载流子容易重新复合,这严重影响了TiO2的光催化效率.为了充分的利用太阳光,对TiO2进行修饰改性受到了众多研究者们的关注.目前,对TiO2进行改性的方法主要包括金属离子掺杂[3-5]、非金属元素掺杂[6-7]、共掺杂[8-9]、半导体复合[10-11]等,其中金属离子掺杂改性一直受到人们的关注[12],这是因为,金属离子的掺杂可以在TiO2的晶格中引入缺陷位置或改变结晶度,从而影响电子和空穴的复合;另一方面,某些金属离子的掺入也可以改变TiO2的能带结构,使TiO2的光响应范围扩展到可见光区,从而提高对太阳光的利用率,进而提高光催化效率.目前有关锌掺杂TiO2的报道已有许多[13-15],锌掺杂TiO2光催化活性的提高是由于锌的掺入提高了光生载流子的分离速率.锌掺杂TiO2的制备方法主要是溶胶凝胶法,到目前为止,有关水热法制备锌掺杂TiO2及其可见光催化的研究尚未见报道.
本文作者以钛酸纳米管(NTA)和ZnCl2为原料,在无有机溶剂存在的条件下,采用水热法制备了锌掺杂的TiO2光催化剂,并以亚甲基蓝和丙烯为模型反应物,探讨了掺杂量和水热温度对其可见光催化性能的影响.
1 实验部分
1.1 实验方法
前驱体钛酸纳米管的制备以NaOH和P25为原料,参考文献[16]进行.锌掺杂TiO2的制备是以ZnCl2为锌源,取1g NTA和适量的盐酸酸化的ZnCl2溶液(0.1mol/L)在室温搅拌下分散于去离子水中,控制Zn/Ti的物质的量之比分别为0%、0.5%、1%、3%、5%,混合液总体积为50mL;搅拌均匀后,将所得混合液转移至高压反应釜中,于130℃恒温反应3h;冷却至室温,抽滤得固体产品,用三次水进行洗涤至用饱和硝酸银溶液检测不到 Cl-为止.所得样品依次标记为0%ZnT-130、0.5%ZnT-130、1%ZnT-130、3%ZnT-130和5%ZnT-130.控制Zn/Ti物质的量之比为0.5%,分别于100℃、160℃和190℃恒温反应3h,对固体产品进行上述处理,所得样品分别标记为0.5%ZnT-100、0.5%ZnT-160和0.5%ZnT-190.
1.2 催化剂的表征
使用荷兰Philips X’Pert Pro X射线衍射仪(XRD)对样品晶型结构进行测试,测试条件为Cu Kα辐射,工作电压为40kV,电流为40mA,扫描范围为10°~90°,扫描速度为0.04°/s;使用日本株式会社JEM-100CX型电子显微镜(TEM)对样品进行形貌观察,加速电压为100kV.
1.3 催化剂的可见光活性评价
以亚甲基蓝(MB)和丙烯为评价体系,对样品的可见光催化性能进行评价.量取100mL浓度为10mg/L的亚甲基蓝溶液加入光催化反应器,再加入100mg的催化剂粉末,在暗态磁力搅拌下使亚甲基蓝吸附达到平衡;开启光源,每隔30min取出4mL溶液进行离心分离,采用722型可见光分光光度计(上海光谱仪器有限公司)测定上清液在664nm(亚甲基蓝的最大吸收波长)处的吸光度.可见光光源为PLS-SXE300/300UV(北京畅拓),光源和反应器之间使用λ≥420nm的截止滤光片滤掉紫外光.通过计算反应前后MB的浓度变化评价催化剂的可见光催化活性.
以丙烯为模型污染物评价方法如下:称取25mg催化剂样品与少量三次水混合均匀,涂在毛玻璃片上(涂片面积约为10cm2),红外干燥箱中烘干后放入石英反应器中.光源同上,光束经过λ≥420nm截止滤光片得到可见光,光源与反应器之间的距离约7cm,中间加循环水滤掉红外光.光催化性能评价所用原料气为丙烯与空气的混合物,丙烯的初始体积分数为0.06%,原料气流速为82mL/h,依次经过CO2吸收管和水汽吸收管,进入石英反应器.丙烯的浓度变化采用日本岛津GC-9A型气相色谱仪进行原位分析,用氢火焰检测器进行检测.当原料气中丙烯浓度达到稳定后开启光源,丙烯消除率达到稳态时,关闭光源,通过计算反应前后丙烯浓度的变化评价催化剂样品的可见光催化活性.
2 结果与讨论
2.1 XRD和TEM分析
图1为130℃水热温度下所制备的不同锌掺杂量的样品的XRD图谱,插图为NTA的XRD图谱.可以看出,属于正交晶系的钛酸纳米管在2θ=8.6°处有一衍射峰,这是NTA管状结构的特征峰.随着锌的掺入,130℃水热条件下,管状结构的特征峰消失,所得锌掺杂TiO2样品均表现出锐钛矿相结构特征峰,并且随着锌掺杂量的增加,衍射峰的强度增加,在0%~5%的Zn掺杂量范围内,没有金红石相的出现.
图2a是钛酸纳米管的电子显微镜图,插图为NTA的高分辨电子显微镜图.NTA具有层状结构,是一种一维纳米管状材料.从插图可以清晰的看到,其为两端开口,外径约6.8nm,壁厚约1.3nm,管长为130~150 nm,与前期的研究报道一致[16].图2b为样品0.5%ZnT-130的电子显微镜图,可以看出,在0.5%的锌掺杂量条件下,130℃水热反应3h后,钛酸纳米管的管状形貌被破坏转变为纳米颗粒,同时,催化剂的晶型也由钛酸纳米管的正交晶系转变为TiO2的锐钛矿相(图1).图2b中的插图为电子衍射,一个明显的连续的衍射环可以被看到,这表明了锌掺杂TiO2是多晶相结构.

图1 锌掺杂TiO2系列样品的XRD图谱(插图为NTA的XRD图谱)Fig.1 XRD patterns of Zn-doped TiO2samples(Insert:XRD patterns of NTA)

图2 样品的 TEM 图(a)NTA ,(b)0.5%ZnT-130(插图分别为(a)NTA的 HRTEM 图,(b)0.5%ZnT-130的 SAED图)Fig.2 TEM images of the samples(a)NTA,(b)0.5%ZnT-130(Insert:(a)HRTEM of NTA,(b)SAED of 0.5%ZnT-130)
2.2 光催化效果分析
2.2.1 锌掺杂量对催化剂可见光催化性能的影响
锌掺杂TiO2样品的可见光催化活性通过对亚甲基蓝的消除进行评价.图3表明了130℃水热温度下,不同锌掺杂量的TiO2样品对亚甲基蓝消除率的影响.可以看出,P25在可见光照下对亚甲基蓝脱色的速率常数几乎为0,这是因为P25对可见光无响应.同P25相比较,锌掺杂的TiO2对亚甲基蓝的光催化脱色均表现出较高的活性,且均高于纯的TiO2(即0%ZnT-130).当锌的掺杂量为0.5%时,所得样品0.5%ZnT-130的可见光催化活性最高,速率常数为0.58min-1,是P25的290倍,这表明锌的掺入极大地提高了样品的可见光催化活性.当锌掺杂量超过0.5%时,MB降解率随锌掺杂量的增加反而降低.由于锌掺杂量小以及Zn2+的离子半径(0.074nm)和Ti4+的离子半径(0.068nm)接近,掺杂后Zn2+将取代 Ti4+进入 TiO2晶格,故掺杂的锌应以Zn2+形式存在,而Zn2+杂质能级的存在可以形成光生电子空穴对的浅势捕获中心,从而降低了光生电子空穴对的复合速率[17].此外,前驱体钛酸纳米管在水热过程中能产生氧空位[18],而且锌的掺入能增加TiO2表面缺陷的量,而氧空位或缺陷能成为光生电子的捕获中心,从而有效地抑制了光生电子和空穴的复合[19],所以锌掺杂的TiO2催化剂对MB的降解率高于纯的TiO2.然而随着锌掺入量的进一步增加,部分Zn2+可能不再以掺杂形式进入晶格内部,而是以ZnO的形式覆盖在TiO2表面,阻碍了电子和空穴向催化剂表面的传递,同时表面锌氧化物成为电荷载流子的复合中心,导致催化剂活性降低.
为了进一步验证锌掺杂TiO2样品的可见光催化活性,实验中又以丙烯为模型污染物考察了样品0.5%ZnT-130在可见光照下的光催化活性,并以P25作为对比.如图4所示,可见光下,P25对于丙烯的消除没有表现出光催化活性.同P25相比,0.5%ZnT-130对于丙烯的消除表现出了较高的光催化活性.这表明所制备的锌掺杂TiO2光催化剂不仅对亚甲基蓝的降解有着较好的光催化活性,同样对于丙烯的可见光催化降解也表现出了较佳的光催化性能.

图3 Zn掺杂量对亚甲基蓝(MB)消除率的影响Fig.3 The effect of Zn doping content on the removal of methylene blue(MB)
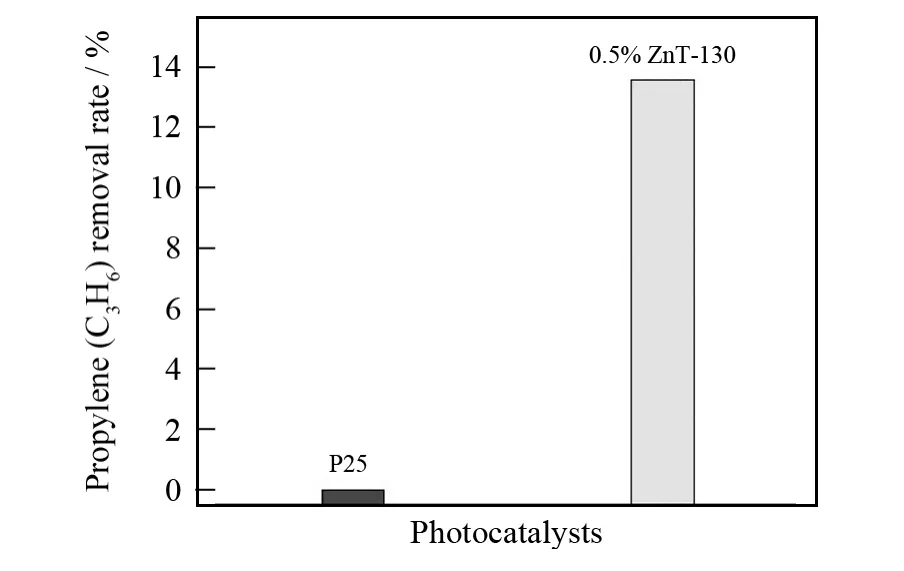
图4 丙烯在P25和0.5%ZnT-130上的可见光催化降解Fig.4 Degradation of propylene(C3H6)over P25and 0.5%ZnT-130under visible light irradiation
2.2.2 水热温度对催化剂光催化性能的影响
图5表明了0.5%Zn掺杂量时,水热温度对Zn-TiO2光催化剂可见光催化性能的影响.由图可以看出,可见光下,当锌的掺杂量为0.5%时,MB的消除率随着水热温度的升高而增加,当水热温度为130℃时,光催化活性最佳,随着水热温度的进一步升高,活性下降,这可能是由于温度升高时,TiO2颗粒容易发生聚集,颗粒变大,可能导致比表面积减小,从而导致可见光光催化活性降低[18].

图5 水热温度对MB消除率的影响Fig.5 The effect of hydrothermal temperature on the removal of MB
3 结论
以钛酸纳米管为前驱体,ZnCl2为掺杂剂,首次采用水热法制备了含锌的TiO2光催化剂,研究了锌掺杂量和水热温度对催化剂可见光催化性能的影响,结果表明,当锌掺杂量为0.5%,水热温度为130℃时,锌掺杂TiO2光催化剂的可见光催化性能最佳.
[1]CHEN Xiaobo,MAO S S.Titanium dioxide nanomaterials:synthesis,properties,modifications,and applications[J].Chem Rev,2007,107(7):2891-2959.
[2]FRANK S N,BARD A J.Heterogeneous photocatalytic oxidation of cyanide and sulfite in aqueous solutions at semiconductor powders[J].J Am Chem Soc,1977,99(15):1484-1488.
[3]BHATTACHARYYA K,VARMA S,TRIPATHI A K,et al.Effect of vanadia doping and its oxidation state on the photocatalytic activity of TiO2for gas-phase oxidation of ethene[J].J Phys Chem C,2008,112(48):19102-19112.
[4]CAI Li,LIAO Xuepin,SHI Bi.Using collagen fiber as a template to synthesize TiO2and Fex/TiO2nanofibers and their catalytic behaviors on the visible light-assisted degradation of orange II[J].Ind Eng Chem Res,2010,49(7):3194-3199.
[5]HE Chao,YU Yun,HU Xingfang,et al.Influence of silver doping on the photocatalytic activity of titania films[J].Appl Surf Sci,2002,200(1/4):239-247.
[6]ASAHI R,MORIKAWA T,OHWAKI T,et al.Visible-light photocatalysis in nitrogen-doped titanium oxides[J].Science,2001,293(13):269-271.
[7]ZHENG Jianwei,BHATTCAHRAYYA A,WU Ping,et al.The origin of visible light absorption in chalcogen element(S,Se,and Te)-doped anatase TiO2photocatalysts[J].J Phys Chem C,2010,114(15):7063-7069.
[8]吴 奇,苏钰丰,孙 岚,等.Fe、N共掺杂TiO2纳米管阵列的制备及可见光光催化活性[J].物理化学学报,2012,(3):635-640.
[9]FENG Ningdong,WANG Qiang,ZHENG Anmin,et al.Understanding the high photocatalytic activity of(B,Ag)-codoped TiO2under solar-light irradiation with XPS,solid-state NMR,and DFT calculations[J].J Am Chem Soc,2013,135(4):1607-1616.
[10]解庆范,陈延民,张素丽,等.复合光催化剂Er2O3/TiO2的制备及其性能的研究[J].中国稀土学报,2006,24(3):371-375.
[11]丁 鹏,贾欣茹,唐艳茹,等.复合氧化物TiO2/Bi2O3对甲苯的光催化作用[J].功能材料,2007,38(9):1468-1470.
[12]WU Qingping,ZHENG Qiang,KROL R.Creating oxygen vacancies as a novel strategy to form tetrahedrally coordinated Ti4+in Fe/TiO2nanoparticles[J].J Phys Chem C,2012,116(12):7219-7226.
[13]JING Liqiang,XIN Baifu,YUAN Fulong,et al.Effects of surface oxygen vacancies on photophysical and photochemical processes of Zn-doped TiO2nanoparticles and their relationships[J].J Phys Chem B,2006,110(36):17860-17865.
[14]梁鸿昌,欧宇达,丘文杰,等.Zn-TiO2纳米管的光催化活性[J].生态环境学报,2011,20(2):323-326.
[15]KANDAVELU V,KASTIEN H,THAMPI K R.Photocatalytic degradation of isothiazolin-3-ones in water and emulsion paints containing nanocrystalline TiO2and ZnO catalysts[J].Appl Catal B,2004,48(2):101-111.
[16]YANG Jianjun,JIN Zhenshen,WANG Xiaodong,et al.Study on composition,structure and formation process of nanotube Na2Ti2O4(OH)2[J].Dalton Trans,2003,20:3898-3901.
[17]LIU Guoguang,ZHANG Xuezhi,XU Yajie,et al.The preparation of Zn2+-doped TiO2nanoparticles by sol-gel and solid phase reaction methods respectively and their photocatalytic activities[J].Chemosphere,2005,59(9):1367-1371.
[18]CUI Guanjun,XU Zhanxia,WANG Yan,et al.A new method to prepare the novel anatase TiO2[J].Surf Rev Lett,2008,15(4):509-513.
[19]井立强,辛柏福,王德军,等.ZnO和TiO2纳米粒子的光致发光性能及其与光催化活性的关系[J].高等学校化学学报,2005,26(1):111-115.
- 化学研究的其它文章
- 纳米SiO2/聚甲基丙烯酸甲酯复合材料的制备和力学性能
- Synthesis and crystal structure of an organic-inorganic composite phosphotungstate[HTA]3[α-PW12O40]·6H2O
- A 2-D tetra-FeIII substituted sandwich-type antimonotungstate NdNa3[Fe4(H2O)10][β-B-SbW9O33]2·36H2O
- TiO2/12-磷钨杂多酸/金复合纳米材料的制备及电化学性能
- 水溶液中对Cr3+高选择性荧光化学传感器的研究
- Synthesis and characterization of a layered organic-inorganic hybrid(C4H9NH3)2NiCl4

