用六水氯化镁制备高纯镁砂工艺
谢垚,陈镇,吴玉龙,杨明德,魏丽乔,丁冉冉
(1太原理工大学材料科学与工程学院,山西 太原 030024;2太原理工大学新材料界面科学与工程教育部重点实验室,山西 太原 030024;3清华大学核能与新能源技术研究院,北京 100084)
高纯镁砂是一种制备耐火材料的优质原料,镁砂的主要成分为碱性MgO,熔点高于2800 ℃,同时伴有CaO、SiO2、Fe2O3等杂质[1]。目前,我国主要是通过煅烧菱镁矿获得高纯镁砂,该工艺不仅存在能耗大、成本高、环境污染严重等缺点,而且不能得到高纯度的镁砂。国外则主要是从海水、盐湖卤水中提炼获得高纯镁砂。
新疆罗布泊盐湖是我国迄今为止发现超大的含钾硫酸镁亚型卤水矿床,属于典型的液体镁矿床,盐湖卤水中Mg2+主要是以水氯镁石(MgCl2·6H2O)形式存在。预计到2015年,每年将有1.5×106t卤水排放,这对于盐湖资源来说是一种极大的浪费。从盐湖卤水中提纯水氯镁石作为镁源,以碳酸钠作为沉淀剂得到前体,之后通过煅烧前体得到高纯活性氧化镁,氧化镁再进一步真空高温烧结成镁砂,这样不仅能有效地利用盐湖卤水资源,降低环境污染程度,而且使得烧结镁砂生产成本大幅度下降,探究出了制备镁砂的新思路。
1 实验部分
1.1 主要试剂和仪器
试剂:天津光复科技发展有限公司提供分析纯六水氯化镁(MgCl2·6H2O)和碳酸钠(Na2CO3);实验室配置的 EDTA(0.02mol/L),铬黑T指示剂,氨-氯化铵缓冲溶液,柠檬酸溶液(0.07 mol/L),煤油,去离子水。
仪器:特制结晶反应器;SX-8-10型箱式电阻炉控制箱;BT50-1J恒流泵;PMQW全方位行星式球磨机;200F型场发射扫描电子显微镜;D/Max-3C型 X射线衍射仪;SDTQ600同步热分析仪;ZR-50-20真空碳管炉;马尔文Mastersizer2000激光粒度仪。
1.2 实验过程
图1所示的反应器可以保证原料恒流滴加,恒温反应之后得到理想前体。整体的工艺流程如图2所示。
1.3 样品制备
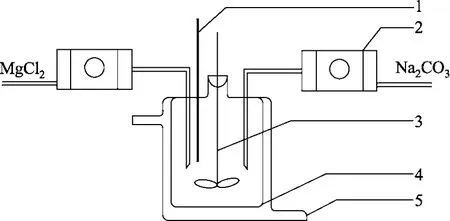
图1 特制结晶反应器示意图

图2 高纯镁砂制备的工艺流程图
(1)MgCO3·2H2O 的制备 准确称取一定的MgCl2·6H2O 和 Na2CO3,分别配置成 1 mol/L 的MgCl2·6H2O和Na2CO3标准溶液。通过蠕动恒流泵将MgCl2·6H2O和Na2CO3溶液以6.25 mL/min的恒定流速滴加至结晶器中,结晶器的温度由恒温水箱循环水控制为 35 ℃。反应全过程用温度计监测温度,温度误差控制在±0.5 ℃以内,搅拌器的搅拌速率设定为恒定的300 r/min。加料结束后,继续搅拌1 h,随后,恒温条件下陈化1 h后,抽滤得到MgCO3·2H2O。将 MgCO3·2H2O 转移至干净的 2 L烧杯中,用去离子水清洗3次。将MgCO3·2H2O转移至真空干燥箱中保持恒温60 ℃干燥2 h。测定滤液中的镁离子浓度为1.0816 g/L,计算得到镁离子利用率为99%以上。
(2)轻烧MgO的制备 为了得到颗粒大小分布均匀,活性高的MgO,在800℃煅烧2h得到粉末状的MgO,纯度为98.81%。
(3)高温烧结制备高纯镁砂 将得到的活性轻烧MgO,添加微量活性炭之后研磨,消除在轻烧过程中残留的“母盐假晶”[2],以降低MgO颗粒尺寸,减少团聚现象。首先将轻烧MgO在压强为80 MPa的模具中制成直径为Φ(20±0.02) mm的圆柱体,然后在真空度为1.33×10−1Pa,温度为1600 ℃的条件下高温真空烧结得到高纯镁砂。
2 实验结果及机理探讨
2.1 轻烧MgO的表征
为了研究轻烧对MgO的影响,通过XRD、热分析以及SEM等方法对MgCO3·2H2O和轻烧MgO进行了表征(图3~图5)。XRD结果表明前体的主要组成为MgCO3·2H2O,而800 ℃轻烧后得到产物为高纯度MgO(图3)。SEM照片中MgCO3·2H2O和MgO的微观形貌进一步证实了该结论(图5)。

图3 MgCO3·2H2O和轻烧MgO的XRD谱图

图4 MgCO3·2H2O的热解失重过程
MgCO3·2H2O轻烧是得到 MgO的重要步骤,为了得到MgCO3·2H2O具体的热分解过程,可以通过同步热分析仪分析,结果如图4所示。由图4可知,当温度在360 ℃之前,失重率达到30%,主要表现为MgCO3·2H2O失去2个水分子。温度在360~500 ℃之间,失重率达到了 32.6%,说明在此温度区间内,MgCO3晶格破裂分解出CO2[3]。当温度升高到 750 ℃以后,失重率达到 64.38%,理论失重率为66.66%,MgCO3分解完全,得到MgO颗粒。若选择的轻烧温度太低,得到 MgO的纯度达不到要求,但是轻烧温度过高,会产生颗粒团聚[4]现象,团聚颗粒之间的内部气孔会变大,这种团聚现象降低了表面自由能,这样使得烧结驱动力降低。颗粒之间的大气孔在整个烧结过程中很难排除,最终直接影响烧结的体积密度和气孔率[5]。按照热分解曲线,从750 ℃开始选择轻烧温度,就可以得到高纯度的MgO粉末。
为了选择合适的轻烧温度,按照国家黑色冶金行业标准YB/T4019—2006的规定,测定了不同轻烧温度下得到的 MgO样品的活性,结果如表1所示。由数据可知,在800 ℃轻烧2 h得到MgO具有很高的活性,最适合制备高纯度镁砂。这可能是由于在此温度下得到的 MgO的晶格中存在相对较多的点阵缺陷和位错,缺陷较多则很容易表面吸附一定数量带有不同极性的基因,这种基因是一种不饱和价键,可以提高活性[6]。
对干燥的MgCO3·2H2O和轻烧得到的MgO进行 SEM 表征,观察其微观形貌。由图5(a)可以清楚地观察到,干燥之后的MgCO3·2H2O是由很多薄片状结构团簇在一起组成花瓣状。从图5(b)观察到,经800 ℃轻烧2 h得到的MgO粉末颗粒较小,分布均匀,颗粒间有接触但相互独立存在,在颗粒之间夹杂着很多气孔。

表1 柠檬酸法测定氧化镁的活性

图5 MgCO3·2H2O和轻烧氧化镁的SEM图
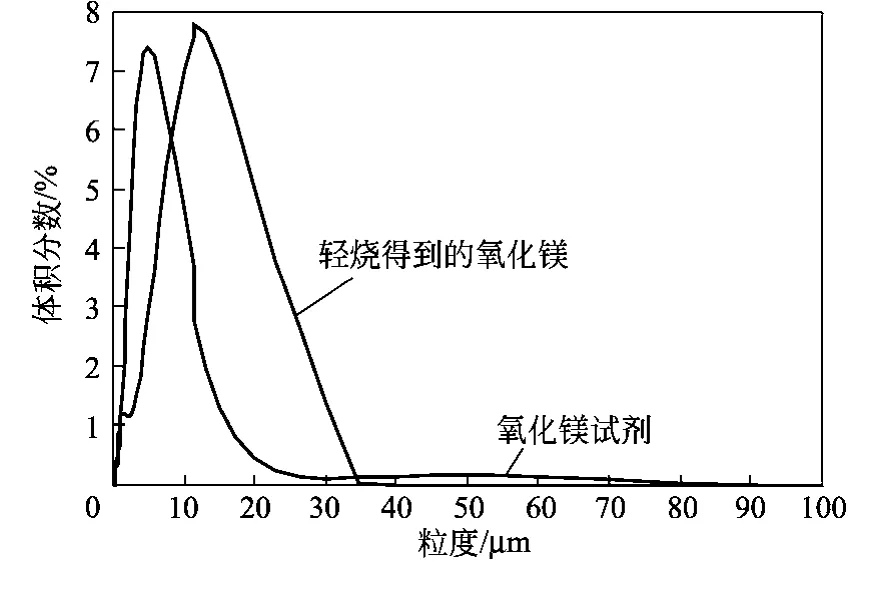
图6 轻烧2 h之后得到的氧化镁的粒度分布
对轻烧2 h之后的MgO粉末和纯度为99.9%的MgO试剂分别做粒度分布并且作图得到积分曲线,如图6所示。由图6中的曲线对比可以清楚地观察到,轻烧之后的MgO粉末和MgO试剂都具有较窄的粒度分布,说明两种MgO颗粒分布均匀;MgO试剂颗粒的平均粒径要小于轻烧得到的 MgO的平均粒径。轻烧之后的 MgO颗粒体积平均粒径为16.496 μm,比表面积1.04 m2/g,90%的颗粒的粒径小于 32.460 μm。
2.2 活性炭种类的选择
选取椰壳、果壳、焦油3种活性炭作为第二相添加剂,以探究它们对烧结的影响。焦油活性炭来源于矿物质,而椰壳、果壳活性炭则属于木质活性炭。其部分物理性质如表2所示。将3种活性炭在马弗炉中加热至550 ℃后,对样品进行对比得出焦油活性炭残留灰份比例明显高于木质活性炭的残留灰分,因此在相同添加质量的条件下,焦油活性炭能在真空高温条件下和MgO反应的C就明显少于木质活性炭,导致所得镁砂的体积密度最低,与实验结果一致。将3种活性炭按照质量分数0.03%的添加量加入到轻烧MgO中进行研磨、压制成型后,1600 ℃高温下真空烧结5 h得到的镁砂体积密度分别为3.48 g/cm3、3.21 g/cm3和3.15 g/cm3。与果壳活性炭相比,椰壳活性炭的粒径较小。根据文献[7]可知在体积分数相同的条件下,小粒子的空间弥散程度大,与晶界面接触的概率大,能频繁地对运动晶界施加阻力,使一段晶界可能被多个粒子“钉扎”受阻而导致移动速率的降低,可以使空隙有充足的时间排除,最终得到较高体积密度的镁砂。所以实验过程中选择微量椰壳活性炭作为第二相添加粒子。

表2 3种活性炭的粒径统计
2.3 烧结过程中的机理探究
为了探究烧结过程的机理,研究了不同烧结温度及活性炭含量所得样品的体积密度随时间的变化趋势。
根据Arrhenius公式:D=Klgt+C,其中D为体积密度,采用“阿基米德法”测量[8],K为速率系数,t是在一定温度下的烧结时间[9]。将lgt值对测量到的D作图,通过计算得到不同活性炭添加量的MgO在烧结过程中的速率系数K值,如图7所示。

图7 MgO在烧结过程中不同温度下的速率系数
由图7可知,相同烧结温度下,不同活性炭添加量的MgO样品胚体在烧结过程中的K值不同。活性炭含量为0.03%和0.05%的MgO的体积收缩速率系数较高,而没有添加剂的 MgO空白样的体积收缩速率系数最低,说明活性炭的存在有助于样品的烧结。这是因为在烧结的前期,可能存在下面的反应[10]:

晶界或界面处将产生少量镁蒸汽与镁离子空位,有利于扩散传质的进行。烧结初期的材料经过共同研磨和压制成型,活性炭粒子是掺杂于 MgO颗粒之间,温度的升高可以使Mg—O键开始断裂,形成新的C—O键,还原初期反应速率较快[11]。烧结炉内的真空度控制在1.33×10−1Pa,可以非常有效地使碳还原氧化镁反应的温度低于 1200 ℃[12-13]。随MgO和C反应过程的进行,MgO颗粒与活性炭颗粒体积逐渐缩小,颗粒间的距离逐渐增大,再加上 MgO颗粒本身发生分解反应就非常困难,离解生成的O更不容易扩散到C颗粒表面并与之发生反应,因此,还原反应中后期的反应速率逐渐降低,未参加反应的活性炭留在胚体中,不利于烧结的因素增,这可加以解释添加活性炭超过0.1%的样品体积密度较小的原因(小于3.30 g/cm3)。
由实验数据得出当活性炭添加量为 0.03%和0.05%的MgO的致密化过程能在较低温度下发生,体积收缩,气孔率下降,1200 ℃烧结180 min,体积密度就分别可以达到3.33 g/cm3和3.31 g/cm3,总气孔率可降低至6.98%和7.54%。Sugarman等[14]认为在晶界迁移的过程中位错的滑移可以吸收周围大量的空隙,就能有效降低气孔率;同时添加活性炭之后,分散均匀的活性炭可以抑制晶粒的长大,促进扩散,在较低的温度下就能大量排除气孔,体积密度迅速的提升。之后随着晶粒尺寸的增大,晶界扩散对样品致密化的效果减弱。1400 ℃的温度下保温180 min后,活性炭含量0.03%和0.05%的样品,其体积密度分别达到3.44 g/cm3和3.46 g/cm3,总气孔率可以降低至 3.91%和 3.35%,相对于没有活性炭添加量的空白样品体积密度有很明显的提高。处于烧结末期的样品在 1600 ℃的时候体积收缩速率系数已经很小,表明体积密度只能是随着时间缓慢地增加,烧结过程完成。
同时采用SEM观察MgO样品在不同烧结阶段的微观形貌(图8)。由图8(a)可以清楚地观察到,在样品颗粒的原始接触面,通过颗粒表面附近的原子扩散,由原来机械啮合转变为原子间的冶金结合,形成晶界,MgO的坯体强度增加,体积收缩。由图8(b)可以看到在晶界上分布着反应后缩小的圆球形椰壳活性炭颗粒,由于添加的小颗粒散落在粒径较大的 MgO颗粒之间,在晶界迁移的过程中,晶界可能被多个粒子“钉扎”而受阻。根据黄培云[15]理论,第二相粒子位于晶界上时,由于部分晶界被占据使界面能降低,在烧结过程中,晶界移动脱离粒子的时候,境界面积增加将引起界面能升高,只有当晶粒组织演变引起的系统自由能下降超过这部分增加的境界能的时候,晶界才可以继续移动,因此降低了晶界移动的速率。由图8(c)可以观察到经1600 ℃烧结5 h的镁砂,致密化程度高,气孔率低,因发生晶界与孔隙间的分离现象,故表面存在粗大集中的孔隙,并充分球化。
将真空烧结完成的样品进行破碎、稍微研磨之后在空气中加热至 550 ℃,发现前后质量没有变化,证明烧结完成的样品中没有游离态的Mg存在。测定 1600 ℃烧结完成后所得最终样品的气孔率和体积密度,同时滴定镁离子测定样品的纯度,结果如表3所示。

图8 不同温度阶段镁砂的微观形貌
3 结 论
(1)同时将MgCl2·6H2O和Na2CO3恒流匀速加入到搅拌结晶器中,制备出前体MgCO3·2H2O,原料利用率高达99%以上。选择合适的轻烧条件为:800 ℃,2 h,可以得到高活性、高纯度、粒度均匀分布的MgO粉末。
(2)经过对比实验,添加第二相的椰壳活性炭可有效地提高烧结过程中致密化速率,同时降低气孔率。添加量控制在0.03%~0.05%时,效果最优。
(3)在真空度为 1.33×10−1Pa下进行高温烧结,在温度为1200 ℃和1400 ℃,活性炭添加量为0.03%和0.05%时,体积收缩速率较快,而继续升温至 1600 ℃之后,体积收缩的速率则降低,说明烧结进入后期过程,最终保温5 h得到高体积密度、高纯度的优质镁砂。
[1]Arunachalam Lakshmanan.Sintering of Ceramics——New Emerging Techniques[M].InTech,2012:309-322.
[2]徐兴无,饶东生.菱镁矿母盐假相对 MgO烧结致密化的影响[J].硅酸盐学报,1988,16(2):244-251.
[3]Giester G ,Lengauer C L.The crystal structure nesquehonite of MgCO3·3H2O,from Lavrion,Greece[J].Mineralogy and Petrology,2000,70(3-4):153-163.
[4]李维翰,尚红霞.轻烧氧化镁粉活性测定的方法[J].武汉钢铁学学报,1992,15(1):31-37.
[5]施剑林.固相烧结——Ⅰ气孔显微结构模型及其热力学稳定性,致密方程[J].硅酸盐学报,1997,25(5):499-513.
[6]Bocanegra-Bernal M H.Microstructural evolution during sintering in MgO powders precipitated from sea water under induced agglomeration conditions[J].Powder Technology,2008,3(186):267-272.
[7]宋晓燕,刘国权,谷南驹.第二相粒子尺寸对基体晶粒长大影响仿真研究[J].金属学报,1999,35(6):565-568.
[8]钱之荣,范广举.耐火材料实用手册[M].北京:冶金工业出版社,1992.
[9]Vipink Ants Ingh.Densification of alumina and silica in the presence of a liquid phase[J].Communications of the American Ceramic Society,1981,64(10):133-136.
[10]饶东生,林彬荫,朱伯栓.降低高纯氧化镁烧结温度的研究[J].硅酸盐学报,1989,17(1):75-80.
[11]Li Rongti,Pan Wei.Kinetics and mechanism of carbothermic reduction of magnesia[J].Metallurgical and Materials Transactions B,2003,34B:433-437.
[12]刘红湘,戴永年,李一夫.真空碳热还原氧化镁制取金属镁的研究[J].真空,2009,46(5):82-86.
[13]李志华,戴永年,薛怀生.真空碳热还原氧化镁的热力学分析实验验证[J].有色金属,2005,5(1):56-59.
[14]Sugarman,Blachere.Creep of MgO containing a dispersion of carbon[J].Journal of the American Ceramic Society,1979,62(7):386-389.
[15]黄培云.粉末冶金原理[M].北京:冶金工业出版社,2004.

