SIO2催化合成甲苯二氨基甲酸丁酯反应研究
王桂荣,李 欣,赵新强,王延吉
(河北工业大学 化工学院,天津 300130)
甲苯二氨基甲酸酯是绿色合成甲苯二异氰酸酯(TDI)的重要前体,而 TDI是生产聚氨酯的重要原料.近年来,随着我国经济的增长,对TDI的需求呈现快速增长趋势.据国际异氰酸酯协会预计,未来十年,全球TDI年需求增长率为4%,中国市场仍将高达10%,到2015年,中国将成为全球最大的TDI生产及消费市场[1].目前,工业上采用光气法生产TDI,它以剧毒的光气为原料、反应条件苛刻、副产物HCL腐蚀设备[2].随着对化工过程安全生产绿色环保等要求日益严格,开发环境友好的非光气合成TDI路线成为国内外学者关注的焦点.在众多非光气法合成TDI路线中,以尿素、二氨基甲苯(TDA)及醇为原料先合成甲苯二氨基甲酸酯中间体,然后其再分解为TDI的尿素法,是采用价格便宜的尿素为原料、反应条件温和、副产物氨可循环至尿素合成单元、原则上实现“零排放”,非常具有工业化潜力[3-8].以长碳链脂肪醇与尿素及TDA反应合成的甲苯二氨基甲酸酯,其再分解成为TDI时,具有分解温度低、反应副产物醇的冷凝温度高容易回收的优点,会使得整个尿素法合成TDI工艺更容易实现[9].
课题组前期对 TDA、尿素和正丁醇为原料合成甲苯二氨基甲酸丁酯(BTDC)反应的研究表明,SiO2、CuSO4、ZnCl2和HY对合成BTDC反应具有较好的催化活性[9].本文在前期工作的基础上,通过综合分析催化剂的催化活性及其重复使用性优选催化剂,对催化剂进行结构表征,并对反应条件进行优化及分析.
TDA、尿素和正丁醇合成BTDC的反应方程式如式 (1)所示.该反应是一个多步骤反应过程[9]:TDA先与尿素反应生成甲苯单氨基脲,然后甲苯单氨基脲与正丁醇反应生成甲苯单氨基甲酸丁酯,甲苯单氨基甲酸丁酯再与尿素反应生成甲苯-氨基甲酰氨基-氨基甲酸丁酯,最后其与正丁醇反应生成目的产物BTDC.
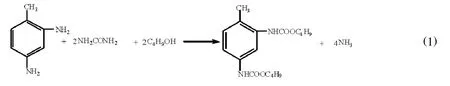
1 实验部分
1.1 主要试剂
尿素:分析纯,天津市化工试剂一厂;2,4-二氨基甲苯:分析纯,国药集团化工试剂有限公司;正丁醇:分析纯,天津市江天化工技术有限公司;二氧化硅:天津化工设计研究院;其余试剂均为分析纯.
1.2 实验过程
将一定量的TDA、尿素、正丁醇和催化剂加入到250 mL不锈钢高压反应釜中,用控温仪加热,同时打开搅拌器,待温度升至预定温度后开始计时,达到反应所要求的时间后降温、出料、分离、计量、分析.
1.3 分析方法
产物的定量分析采用Water515型高效液相色谱仪,2487型双波长紫外检测器( =254nm),Turner C18色谱柱( 4.6 nm×150 nm),流动相为 甲醇 ∶ 水 =70∶30,流速0.6 mL/min.
采用美国Micromeritics公司的ASAP2020型比表面积和孔隙度分析仪对催化剂的比表面积、孔容和孔径分布进行测定.将催化剂装入石英样品管中,在液氮冷阱中进行低温N2吸附和脱附.
2 结果与讨论
2.1 催化剂活性及重复使用性
前期工作[9]在反应温度160℃、反应时间6h、 TDA∶ 尿素∶ 正丁醇 =1∶3∶80(物质的量比)、催化剂用量为 TDA质量30%的条件下,考察了金属盐、氧化物和分子筛等几类有代表性的催化剂对合成BTDC反应的催化性能,结果表明,上述反应条件下SiO2、CuSO4、ZnCl2和HY也有较好的催化活性.由于同一催化剂在不同反应条件下催化活性也会有所不同,因此,进行改变反应温度实验,进一步考察上述几种催化剂的活性,同时实验考察、分析催化剂的重复使用性,综合考虑催化剂性能.
在反应温度200℃、反应时间6 h、 TDA∶ 尿素∶ 正丁醇 =1∶5∶65、催化剂用量为TDA质量30%的条件下,分别考察催化剂CuSO4、HY、ZnCl2以及SiO2的催化活性,不同催化剂对BTDC收率的影响如图1所示.由图1可以看出:
1)实验所考察的4种催化剂中,ZnCl2催化剂活性最低,BTDC的收率仅为37.8%.可能由于在该反应中,无论TDA、尿素及正丁醇反应生成BTDC的实际反应路径如何,要生成目的产物 BTDC,都需要正丁醇与羰基碳反应,即正丁醇中的甲氧基C4H9O作为亲核基团进攻羰基中的碳原子.而ZnCl2酸性较强,会抑制正丁醇的电离,降低了C4H9O的浓度[10],从而不利于反应的进行,造成BTDC收率较低.
2)CuSO4催化剂的催化活性比ZnCl2的高.BTDC合成反应后,回收 CuSO4催化剂.催化剂经乙醇洗涤,于80℃烘箱中干燥后,进行XRD表征,结果如图2所示.由图2可见,回收催化剂主要成分为NH42SO4.这可能是由于CuSO4在反应条件下与反应的副产物NH3结合成了NH42SO4.副产物NH3的消耗有利于反应向右进行.虽然提高了反应收率,但催化剂CuSO4本身会失去活性.

图1 不同催化剂的催化性能Fig.1 Catalytic performanceof different catalysts
通过实验考察CuSO4催化剂的重复使用性能.将反应后回收的催化剂再次用于该反应,发现BTDC的收率为43.6%,与新鲜CuSO4催化剂相比,其催化活性明显降低.这是由于回收催化剂的主要成分为NH42SO4,并非催化活性高的新鲜催化剂CuSO4.由此可见,虽然CuSO4催化剂活性高,但其催化反应过程中因与副产物反应而失活,重复使用性差.
3)以SiO2为催化剂时,BTDC的收率最高,达到81.7%.在上述反应条件下,考察SiO2的重复使用性,结果如表1所示.由表1可以看出,SiO2重复使用3次,BTDC的收率和选择性基本保持不变,说明该催化剂具有较好的稳定性.因此,下面重点考察SiO2催化剂在合成BTDC反应中的催化性能,并对其催化合成BTDC的反应条件进行优化.

表1 SiO2催化剂的重复使用性能Tab.1 Reuse of SiO2 catalyst
2.2 反应温度对BTDC收率的影响
在反应时间6h、TDA∶ 尿素∶ 正丁醇 =1∶5∶65、SiO2用量为TDA质量30%的条件下,考察反应温度对该反应的影响,结果如图3所示.
由图3可见,随着反应温度的升高,TDA转化率、BTDC收率和选择性先增大后减小,在200℃时达到最大,BTDC收率为81.7%.
由图3也可看到,在较低的温度下,TDA就有较高的转化率,但目的产物BTDC的收率不高,说明温度较低时TDA即可转化为中间产物,但由于温度较低,中间产物还难于转化为BTDC;而温度高于200℃时,TDA转化率、BTDC收率和选择性均有下降的趋势.因此,较适宜的反应温度为200℃.
通过对该条件下反应产物的液相色谱分析发现,反应温度较高时,生成副产物的种类增多,表明太高温度可能导致聚合[11]以及TDA的N-丁基化(见反应式 (2))等副反应的发生,造成产物BTDC的收率降低.另外,温度高于200℃时,尿素的分解速度加快[12],其分解生成的NH3导致反应体系NH3分压增大,而体系中的氨抑制反应向正反应方向进行[11].还有一高温不利于目的产物的原因是:温度较高时,产物容易发生分解,造成其收率下降.因此,温度太高并不利于提高目的产物的收率,该反应存在着较适宜的反应温度.

图2 回收催化剂的XRD图Fig.2 XRD pattern of recovered catalyst

图3 反应温度对合成BTDC反应的影响Fig.3 Effect of reaction temperatureon thesynthesis of BTDC

2.3 焙烧温度对催化活性及孔结构的影响
在反应温度200℃、反应时间6 h、 TDA∶ 尿素∶ 正丁醇 =1∶5∶65、SiO2用量为TDA质量30%的条件下,考察催化剂焙烧温度对该反应的影响,结果如图4所示.由图4可见,随着焙烧温度的提高,产物的收率先增大后减小;焙烧温度为400℃时,收率达到最大.再提高焙烧温度,产物的收率有所降低.因此,较为适宜的焙烧温度为400℃.
为探讨焙烧温度对SiO2催化活性的影响,对300℃、400℃和500℃3个不同焙烧温度的SiO2进行BET表征,结果如表2所示.由表2可见,不同焙烧温度时SiO2的比表面积和孔径不同.随焙烧温度升高,比表面积逐渐减小,孔径逐渐增大.焙烧温度为500℃时,孔径达到最大,但500℃焙烧SiO2的比表面积比400℃焙烧的小,使得500℃焙烧SiO2的活性位比400℃焙烧的活性位少,对催化反应不利.由图4可以看出,焙烧温度为500℃或高于500℃时,BTDC收率有下降趋势,可能与温度过高SiO2表面烧结[13]活性位减少有关.综合分析,焙烧温度为400℃时,SiO2的比表面积和孔径适宜,催化效果较好,有利于目的产物BTDC的生成.
而且,由图4也可以看到,SiO2的焙烧温度对TDA的转化率影响不大,只是对BTDC收率影响大.这说明TDA转化为中间产物较容易,而再进一步反应生成BTDC较困难.前者受催化剂活性影响较小,后者受催化剂活性影响较大.

表2 焙烧温度对SiO2结构参数的影响Tab.2 Effect of calcination temperature on structure parameters of SiO2
2.4 催化剂用量对BTDC收率的影响
在反应温度200℃、反应时间6 h、 TDA∶ 尿素∶ 正丁醇 =1∶5∶65、SiO2焙烧温度为400℃条件下,考察 SiO2用量为分别为 TDA质量的20%、30%、40%和50%时,对该反应收率的影响.结果表明,TDA的转化率随催化剂用量变化不大,而产物收率和选择性随着催化剂用量的增加先增大,当催化剂的质量分数达到30%时,产物收率达到最大值;继续增大催化剂用量,收率下降.这是由于TDA转化为中间产物较容易,催化剂活性位多少对此影响不大,而由中间产物向目的产物转化时,受催化剂活性位影响较明显:催化剂用量过少时,不能提供足够的活性中心,产物收率低;而催化剂用量过大时,其在反应体系中的分散受到影响,部分催化剂团聚,使反应体系中有效活性中心数下降,导致产物收率下降.
2.5 反应时间对BTDC收率的影响
在反应温度 200℃、 TDA∶ 尿素 ∶ 正丁醇 =1∶5∶65、SiO2焙烧温度为400℃、SiO2用量为TDA质量30%的条件下,考察反应时间对BTDC收率的影响,结果如图5示.
由图5可以看出,反应时间较短时,TDA就具有较高的转化率,说明TDA极易转化为中间产物;随着反应时间延长,中间产物逐渐向目地产物转化,BTDC收率逐渐增大.当反应时间超过6 h后,产物收率不再有明显变化.因此,适宜的反应时间为6 h.
结合反应温度对TDA,尿素和正丁醇合成BTDC反应的影响(图3)可以看出,在较低的反应温度和较短的反应时间,就可获得较高的TDA转化率,也说明TDA很容易转化为中间产物,但由中间产物转化为目的产物BTDC相对要困难,要获得较高的BTDC收率,则需要较适宜的反应温度和较长的反应时间.这与文献 [9]的研究结果是一致的.
2.6 物料配比对BTDC收率的影响
在反应温度200℃、反应时间6 h、 TDA∶ 正丁醇=1∶65、SiO2焙烧温度为400℃、SiO2用量为TDA质量30%的条件下,考察尿素与TDA物质的量比对反应收率的影响,结果如图6所示.由图6可见,尿素用量变化时,TDA转化率变化不大.但随着尿素用量增大,产物收率和选择性呈现先增大后减小的趋势,当尿素与TDA的物质的量比为5时,产物收率达到最大.这可能是由于尿素遇热不稳定性,随着尿素用量增多,分解的尿素量增多,导致副反应增多,造成产物收率和选择性下降.因此,尿素与TDA适宜的物质的量比为5.

图4 SiO2焙烧温度对合成BTDC反应的影响Fig.4 Effectof calcination temperatureof SiO2 on the synthesisof BTDC

图5 反应时间对合成BTDC反应的影响Fig.5 Effect of reaction time on the synthesis of BTDC
在反应温度200℃、反应时间6 h、 TDA∶ 尿素=1∶5、SiO2焙烧温度为400℃、SiO2用量为TDA质量30%的条件下,考察正丁醇与TDA物质的量比变化对反应的影响,结果如图7所示.
由图7可以看出,随着正丁醇与TDA物质的量配比的增大,TDA的转化率逐渐增大,产物选择性和收率均先增大后减小.这是由于正丁醇在该反应体系中既是反应物又是溶剂,适量的正丁醇有利于原料TDA及尿素的溶解,使反应向生成产物的方向移动,提高了TDA转化率和产物收率;但过量的正丁醇会降低原料的浓度,减缓反应速度.可能正丁醇过量对TDA转化为中间产物的影响不大,但对中间产物转化为目的产物BTDC的影响大,因此造成正丁醇过量反而是BTDC收率下降.
由图7可见,正丁醇与TDA适宜的物质的量比为65,此时,TDA的转化率达96.5%,BTDC收率为81.7%.
3 结论
1)对SiO2、CuSO4、ZnCl2和HY催化TDA、尿素与正丁醇合成BTDC的反应性能进行了评价,从上述催化剂的催化活性及重复使用性综合考虑,SiO2是较适宜的催化剂.SiO2重复使用3次,BTDC收率和选择性保持不变,说明SiO2催化剂具有较好的稳定性.
2) 对SiO2催化合成BTDC反应进行条件优化.较好条件为:SiO2的焙烧温度为400℃、催化剂用量为TDA质量的30%、反应温度200℃、反应时间6 h、 TDA∶ 尿素∶ 正丁醇=1∶5∶65,此时TDA转化率为96.5%,BTDC收率为81.7%.
3) 对不同焙烧温度的SiO2催化剂进行了BET表征.结果表明,适宜的比表面积和孔径有利于目的产物BTDC的生成.
4)对于SiO2催化TDA、尿素以及正丁醇合成BTDC反应,TDA转化为中间产物较容易,而中间产物进一步反应生成目的产物较困难.

图6 尿素与TDA摩尔比对合成BTDC反应的影响Fig.6 Effectof molar ratioof ureato TDA onthesynthesis of BTDC
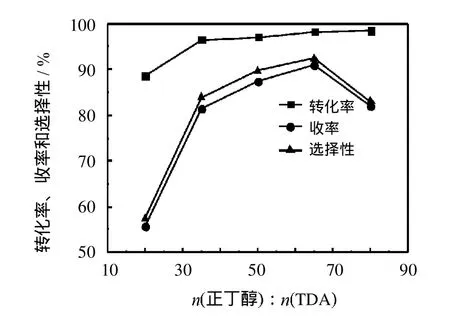
图7 正丁醇与TDA摩尔比对合成BTDC反应的影响Fig.7 Effectof molar ratio of butyl alcohol to TDA onthe synthesisof BTDC
[1]钱伯章,朱建芳.甲苯二异氰酸酯的国内外市场分析 [J].化学推进剂与高分子材料,2012,10(6):86-90.
[2]王延吉,赵新强.绿色催化过程与工艺 [M].北京:化学工业出版社,2002:102-103.
[3]Otterbach A.Multistep continuouspreparation of organic polyisocyanates:US,5386053[P].1995-01-31.
[4]Merger F,Towae F.Processfor thepreparing aromatic di-and/or polyisocyanates:EP,0028338[P].1981-05-13.
[5]Wilmes O.Processfor theproduction of diurethanesand their usefor theproduction of diisocyanates:US,5744633[P].1998-04-28.
[6]方宏刚.尿素法合成甲苯-2,4-二氨基甲酸酯反应研究 [D].天津:河北工业大学,2007.
[7]耿艳楼,方鸿刚,安华良,等.尿素法合成甲苯-2,4-二氨基甲酸正丙酯反应 [J].石油学报:石油加工,2013,29(3):494-500.
[8]李欣.尿素法合成甲苯二氨基甲酸丁酯反应研究 [D].天津:河北工业大学,2012.
[9]王桂荣,李欣,赵新强,等.尿素法合成甲苯-2,4-二氨基甲酸丁酯 [J].石油化工,2012,41(9):1017-1022.
[10]王娜.基于1-甲基-2,4-苯二脲路径的尿素法合成甲苯二氨基甲酸甲酯反应研究 [D].天津:河北工业大学,2011.
[11]秦飞,李其峰,王军威,等.苯胺、尿素、甲醇一步法合成苯氨基甲酸甲酯 [J].精细化工,2008,25(8):85-828.
[12]王臣,王越,姚洁,等.尿素催化醇解合成长碳链脂肪族碳酸二酯 [J].应用化工,2003,20(9):879-882.
[13]康武魁,康涛,马飞,等.负载PbO催化剂对苯胺与碳酸二甲酯合成苯氨基甲酸甲酯的催化性能 [J].催化学报,2007,28(1):5-9.

