HPLC 同时分析芎菊上清丸中7个化学成分的含量研究
孙承浩,王吉华
(1.辽阳市中心医院,辽宁辽阳111000;2.辽阳市食品药品检验所,辽宁辽阳111000)
HPLC 同时分析芎菊上清丸中7个化学成分的含量研究
孙承浩1,王吉华2
(1.辽阳市中心医院,辽宁辽阳111000;2.辽阳市食品药品检验所,辽宁辽阳111000)
目的建立HPLC同时测定芎菊上清丸中7个活性成分(栀子苷、连翘酯苷A、绿原酸、3,5-O-二咖啡酰基奎宁酸、盐酸药根碱、黄芩苷、盐酸小檗碱)含量的方法。方法采用PorosheLL 120 SB-C18(100mm×3.0mm,2.7μm)色谱柱,柱温30℃,以乙腈为流动相A,0.1%磷酸水溶液为流动相B,梯度洗脱,流速1.0mL/min,检测波长为230 nm 0~4.5min(测定栀子苷),348 nm 4.5~9.0 min(测定连翘酯苷A、绿原酸、3,5-O-二咖啡酰基奎宁酸),278 nm 9.0~15.0min(测定盐酸药根碱、黄芩苷、盐酸小檗碱)。结果栀子苷、连翘酯苷A、绿原酸、3,5-O-二咖啡酰基奎宁酸、盐酸药根碱、黄芩苷、盐酸小檗碱的线性范围分别为4.024~80.48μg/mL(r= 0.9991),2.042~40.84μg/mL(r=0.9993),3.956~79.12μg/mL(r=0.9996),6.090~121.80μg/mL(r=0.9990),4.026~80.52μg/ mL(r=0.9995),3.924~78.48μg/mL(r=0.9998),6.030~120.6μg/mL(r=0.9998)。平均加样回收率(n=6)分别为96.5%,97.5%,95.9%,98.6%,99.8%,98.4%和97.3%;RSD分别为1.5%,1.3%,1.2%,1.4%,1.2%,1.1%和0.9%。结论该方法操作简单,重复性好,为评价和监控芎菊上清丸的质量提供了可靠的方法。
芎菊上清丸;HPLC;含量测定
芎菊上清丸收载于《中国药典》(2010版)一部,由川芎、菊花、黄芩、连翘、黄连等15味中药材组成,具有清热解表、散风止痛之功效,用于外感风邪引起的恶风身热、偏正头痛、鼻流清涕、牙疼喉痛[1],含量测定项为薄层色谱扫描法测定黄连中盐酸小檗碱的含量。药典规定的含量测定方法基本上是在开放体系中进行,因此影响定量结果的因素较复杂,准确性差。另据现有文献报道[2-5],可见对芎菊上清丸中黄芩苷、绿原酸进行含量测定的研究,未见同时测定处方中多组分含量的研究报道。为了更好的评价和监督芎菊上清丸的质量,本文采用RP-HPLC梯度洗脱法在同一色谱条件下变换检测波长同时分析处方中5味药材的7个特征性成分的含量。
1 材料与方法
1.1 仪器与试剂 Agilent 1260高效液相色谱仪系统,由G1311A四元泵、G1314B可变波长检测器(VWD)、G1322A在线脱气机组成。
对照品栀子苷(批号为110749-201316)、连翘酯苷A(批号为111810-201103)、绿原酸(批号为110753-201314)、3,5-O-二咖啡酰基奎宁酸(批号为111782-201204)、黄芩苷(批号为110715-201117)、盐酸药根碱(批号为110733-201108)、盐酸小檗碱(批号为110713-201212)均购自中国食品药品检定研究院。供试品芎菊上清丸为北京同仁堂制药有限公司提供,批号为2083068,2083079,3082187。
甲醇、乙腈均为色谱纯,水为重蒸水,其他所用试剂均为分析纯。
1.2 方法
1.2.1 溶液的制备:混合对照品储备溶液:取栀子苷、连翘酯苷A、绿原酸、3,5-O-二咖啡酰基奎宁酸、盐酸药根碱、黄芩苷、盐酸小檗碱等对照品适量,加甲醇制成每1mL分别含上述相应物质0.2012 mg、0.1021 mg、0.1978 mg、0.3045 mg、0.2013 mg、0.1962mg、0.3015mg的混合对照品储备溶液。
混合对照品溶液:精密移取混合对照品储备溶液5.0mL于50mL容量瓶中,用60%甲醇溶液稀释至刻度,摇匀,制得混合对照品溶液。
供试品溶液:取芎菊上清丸10丸,称定重量,剪碎,混匀,研细,取3.0g,精密称定,精密加入60%甲醇水溶液50mL,称定重量,超声处理(250 w,50 kHz)30min,放冷,称重,用60%甲醇水溶液补足减失的重量,离心,取上清液,即得。
阴性样品溶液:按芎菊上清丸的处方比例和工艺方法分别制备不含栀子、连翘、菊花、黄芩和黄连的5种阴性样品,并按“1.2.1”项下供试品溶液方法制备阴性溶液。
1.2.2 色谱条件及系统适用性试验:色谱柱:安捷伦Poroshell 120 SB-C18(100mm×3.0 mm,2.7μm);流动相:乙腈(A)-0.1%磷酸水溶液(B),梯度洗脱(0~5 min,8%A;5~10 min,8%A→20%A;10~15min,20%A→40%A);流速:1.0mL/ min;检测波长:230 nm 0~4.5 min(测定栀子苷),348 nm 4.5~9.0min(测定连翘酯苷A、绿原酸、3,5-O-二咖啡酰基奎宁酸),278 nm 9.0~15.0min(测定盐酸药根碱、黄芩苷、盐酸小檗碱);进样量:5μL。理论板数按盐酸小檗碱计算应不低于5000,各峰的分离度均大于1.5。
1.2.3 重复性试验:取同一批号芎菊上清丸样品(批号2083068),称定重量,研细,取约3.0g,共6份,精密称定,分别按“1.2.1”项下方法制备供试品溶液,按上述色谱条件分别进样5μL。
1.2.4 回收率试验:取已知含量的芎菊上清丸样品(栀子苷、连翘酯苷A、绿原酸、3,5-O-二咖啡酰基奎宁酸、盐酸药根碱、黄芩苷、盐酸小檗碱的含量分别为1.485,0.784,1.012,1.544,1.069,3.969,1.221mg/g)粉末6份,每份1.5 g,精密称定,置具塞锥形瓶中,分别加入新配置的混合对照品溶液(各对照品浓度为:栀子苷0.2024 mg/mL、连翘酯苷A 0.1154 mg/mL、绿原酸0.1520mg/mL、3,5-O-二咖啡酰基奎宁酸0.2187mg/mL、盐酸药根碱0.1616mg/mL、黄芩苷0.6033 mg/mL、盐酸小檗碱0.1979 mg/mL)10mL,再精密加入60%甲醇水溶液40mL,按“1.2.1”项下方法制备供试品溶液,按上述色谱条件分别进样5μL,计算回收率。
2 结果
2.1 含量测定方法学验证结果
2.1.1 干扰性试验:在上述色谱条件下,供试品中其他成分对栀子苷、连翘酯苷A、绿原酸、3,5-O-二咖啡酰基奎宁酸、盐酸药根碱、黄芩苷、盐酸小檗碱的测定无干扰(见图1)。
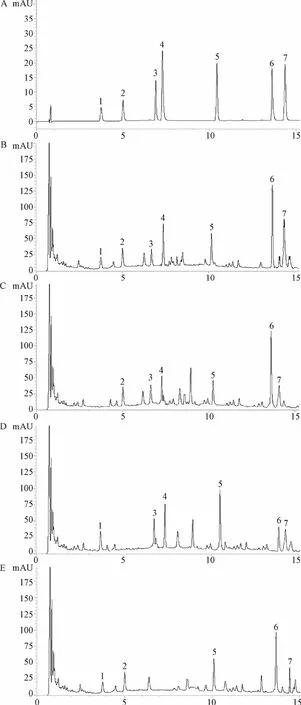
图1 HPLC色谱图A.混合对照品溶液;B.供试品溶液;C.栀子阴性溶液;D.连翘阴性溶液;E.菊花阴性溶液;F.黄芩阴性溶液;G.黄连阴性溶液吸收峰:1.栀子苷;2.连翘酯苷A;3.绿原酸;4.3,5-O-二咖啡酰基奎宁酸;5.盐酸药根碱;6.黄芩苷;7.盐酸小檗碱Fig.1 HPLC chromatogramsA.mixed reference substances solution;B.sample solution;C-Fructus Gardeniae nagtive solvent;D.Forsythiae Fructus nagtive solvent;E.Flos Chrysanthemi nagtive solvent;F.Radix Scutellariae nagtive solvent;G.Rhizoma Coptidis nagtive solvent;1.Jasminoidin;2.Forsythoside A;3.Caffeotannic acid;4.3,5-Di-O-caffeoylquinic acid;5.Jatrorrhizine hydrochloride;6.Baicalin;7.Berberine hydrochloride
2.1.2 线性关系考察:分别精密移取混合对照品储备溶液1.0,2.0,5.0,10.0,15.0,20.0mL于50mL容量瓶中,用60%甲醇溶液稀释至刻度,摇匀,制得混合对照品系列浓度溶液,依次精密吸取上述混合对照品系列浓度溶液按“1.2.2”项下色谱条件进样测定。以样品浓度为横坐标,色谱峰面积为纵坐标,绘制标准曲线,栀子苷、连翘酯苷A、绿原酸、3,5-O-二咖啡酰基奎宁酸、盐酸药根碱、黄芩苷、盐酸小檗碱的线性关系详见表1。

表1 7个成分的线性关系Tab.1 Reasults of linear equations of 7 components
2.1.3 精密度试验:精密吸取同一混合对照品溶液5μL,连续进样6次,结果栀子苷、连翘酯苷A、绿原酸、3,5-O-二咖啡酰基奎宁酸、盐酸药根碱、黄芩苷、盐酸小檗碱峰面积的RSD分别为0.6%,0.5%,1.0%,0.4%,0.7%,0.4%,0.6%。表明仪器精密度良好。
2.1.4 稳定性试验:精密吸取同一供试品溶液,在0,2,4,8,12,24 h分别进样5μL,结果栀子苷、连翘酯苷A、绿原酸、3,5-O-二咖啡酰基奎宁酸、盐酸药根碱、黄芩苷、盐酸小檗碱峰面积的RSD分别为0.8%,1.2%,1.8%,1.6%,0.6%,0.7%,0.5%。表明供试品溶液中的7个待测成分在室温放置24 h内基本稳定。
2.1.5 重复性试验:样品中的栀子苷、连翘酯苷A、绿原酸、3,5-O-二咖啡酰基奎宁酸、盐酸药根碱、黄芩苷、盐酸小檗碱含量平均值分别为1.485,0.784,1.012,1.544,1.069,3.969,1.221 mg/g;RSD分别为1.5%,0.9%,0.9%,1.2%,1.1%,1.3%,1.0%,表明其重复性良好。
2.1.6 回收率试验结果栀子苷、连翘酯苷A、绿原酸、3,5-O-二咖啡酰基奎宁酸、盐酸药根碱、黄芩苷、盐酸小檗碱的平均回收率(n=6)分别为96.5%,97.5%,95.9%,98.6%,99.8%,98.4%和97.3%;RSD分别为1.5%,1.3%,1.2%,1.4%,1.2%,1.1%和0.9%。
2.2 样品测定 取3种批号的芎菊上清丸,分别按“1.2.1”项下方法制备供试品溶液,按上述色谱条件分别进样5 μL,每批次样品取样2份,并进行2次平行测定,以外标法计算含量,平均值结果见表2。
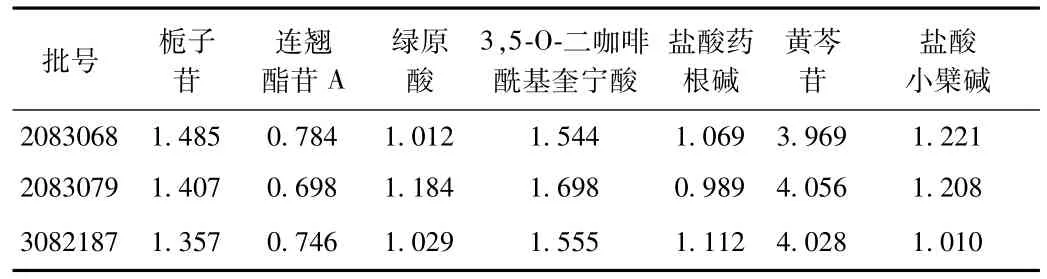
表2 芎菊上清丸中7个活性成分的含量测定结果(mg/g)Tab.1 The contents of seven active ingredients in Xiongju Shangqing pills(mg/g)
3 讨论
3.1 提取条件的选择 本实验分别采用超声提取、加热回流方法对芎菊上清丸中7个成分的提取效率进行考察,结果表明采用超声提取法提取时效率更高,且相对简便易行;提取溶剂考察水、60%甲醇溶液、甲醇、乙酸乙酯等,结果表明,60%甲醇溶液与甲醇对7个成分综合提取效率最高,二者相当,考虑到溶剂成本,采用60%甲醇溶液作提取溶剂;同时对60%甲醇溶液的用量(25、50、100mL)以及超声时间(15、30、45min)进行考察,最终确定提取条件为采用60%甲醇水溶液50 mL超声处理30min。
3.2 检测波长的选择 取混合对照品溶液,采用DAD检测器,按上述色谱条件在200~400 nm范围内光谱扫描,兼顾7个成分的紫外最大吸收波长,最终确定检测波长为230 nm 0~4.5min(测定栀子苷),348 nm 4.5~9.0min(测定连翘酯苷A、绿原酸、3,5-O-二咖啡酰基奎宁酸),278 nm 9.0~15.0min(测定盐酸药根碱、黄芩苷、盐酸小檗碱)。
3.3 流动相的确定 由于待测组分多,本实验采用HPLC梯度洗脱结合可变波长进行含量测定,分别考察3种溶剂系统:甲醇-水、乙腈-水,乙腈-0.1%磷酸水溶液,结果以乙腈-0.1%磷酸水溶液作为流动相的峰型较好,分离效果较理想。参照相关文献的液相洗脱条件[4-7],最终确定梯度洗脱条件。在15min内完成对芎菊上清丸中7个活性成分的同时分析测定,大大缩短了分析时间。
3.4 测定成分的选择 芎菊上清丸现行标准为《中国药典》2010年版一部,含量测定方法为薄层色谱扫描法检测黄连中盐酸小檗碱含量。芎菊上清丸由菊花、黄芩、连翘、黄连等15味中药材制成,现行标准不能检测出多种药材的有效成分,且该方法基本上是在开放体系中进行,因此影响定量结果的因素较复杂,准确性和重复性差,影响药品质量的评价,不能有效的对药品质量进行监测。本文同时测定处方中5味主要中药材的7个有效活性成分,并进行定量分析,可以整体反映芎菊上清丸产品质量,并节约提取溶剂及缩短分析时间。
本文采用RP-HPLC梯度洗脱法在同一色谱条件下变换检测波长同时对处方中5味药材的7个特征性成分(栀子苷、连翘酯苷A[6-7]、绿原酸、3,5-O-二咖啡酰基奎宁酸[8-9]、盐酸药根碱[10-11]、黄芩苷[12]、盐酸小檗碱[13-14])进行含量测定,具有准确、简单、快捷的特点,简化了多次制备供试品溶液及流动相的繁琐步骤,节约分析时间。采用该方法可有效的控制芎菊上清丸的质量,为芎菊上清丸质量监管提供科学依据。
[1] 国家药典委员会,中国药典2010年版一部:675.
[2]冯波,施春玲,郝乘仪,等.RP-HPLC法测定芎菊上清丸中黄芩苷[J].中草药,2009,40(5):743.
[3]王强,郝乘仪,冯波.RP-HPLC法测定芎菊上清丸中绿原酸的含量[J].吉林医药学院学报,2009,30(4):187.
[4]王永伟,赵万顺,宋新波,等.芎菊上清丸质量控制的研究[J].辽宁中医药大学学报,2009,11(5):178.
[5] 郜凤香,梁艳.高效液相色谱法测定芎菊上清丸中栀子苷含量[J].中国药业,2012,21(23):14.
[6] 齐翠翠,李竞,高英,等.太行山区不同产地连翘中连翘苷、连翘醋苷A的含量测定[J].北方药学,2014,11(1):1.
[7] 佟若菲,张囡,林宏.HPLC法测定病毒合剂中黄芩苷、绿原酸和连翘酯苷A[J].现代药物与临床,2014,29(3):259.
[8] 王英锋,谢亮亮,刘锁兰,等.HPLC法测定杏香兔耳风中绿原酸和3,5-O-二咖啡酰基奎宁酸的含量[J].药物分析杂志,2009,29 (3):430.
[9] 茅纯,郑娟,邹耀华,等.高效液相色谱法同时测定桑菊感冒片中绿原酸、木犀草苷和3,5-O-二咖啡酰基奎宁酸含量[J].中华中医药学刊,2014,32(1):193.
[10]陈芳,邓雁如,许妍妍,等.双波长HPLC同时测定黄连及金芪降糖片中6种生物碱的含量[J].中国实验方剂学杂志,2013,19 (17):60.
[11]施法,白旭东,董斌,等.HPLC法同时分析测定明目上清片中10个化学成分[J].药物分析杂志,2014,34(1):91.
[12]牟英迪,林吉茂.HPLC程序波长法测定牛黄上清丸中黄芩苷、连翘苷和盐酸小檗碱[J].中成药,2013,35(9):1933.
[13]匡艳辉,朱晶晶,王智民,等.一测多评法测定黄连中小檗碱、巴马汀、黄连碱、表小檗碱、药根碱含量[J].中国药学杂志,2009,44 (5):390.
[14]郝乘仪,郭淑英,冯波,等.RP-HPLC法同时测定芎菊上清丸中绿原酸、盐酸小檗碱和黄芩苷的含量[J].药物分析杂志,2014,34 (1):193.
(编校:吴茜)
Simultaneous determ ination of seven active ingredients in Xiongju Shangqing pills by HPLC
SUN Cheng-hao1,WANG Ji-hua2
(1.Liaoyang Central Hospital,Liaoyang 111000,China;2.Liaoyang Institute for Food and Drug Control,Liaoyang 111000,China)
ObjectiveTo establish amethod for simultaneous determination of seven active ingredients(Jasminoidin,Forsythoside A,Caffeotannic acid,3,5-Di-O-caffeoylquinic acid,Jatrorrhizine Hydrochloride,Baicalin,Berberine Hydrochloride).MethodsThe determination was carried outwith Agilent Poroshell120 SB-C18(100mm×3.0mm,2.7μm);The mobile phase consisted of acetonitrile(A)-0.1%phosphoric acid solution(B)with gradient elution at a flow rate of 1.0mL/min;The detection wavelengthswere 230 nm in 0~4.5min(determination of Jasminoidin),348 nm in 4.5~9.0min(determination of Forsythoside A,Caffeotannic acid,3,5-Di-O-caffeoylquinic acid),and 278 nm in 9.0~15.0 min(determination of Jatrorrhizine Hydrochloride;Baicalin;Berberine Hydrochloride).ResultsThe calibration curveswere linear in the ranges of4.024~80.48μg/mL for Jasminoidin(r=0.9991),2.042~40.84μg/mL for Forsythoside A(r=0.9993),3.956~79.12μg/mL for Caffeotannic acid(r=0.9996),6.090~121.80μg/mL for 3,5-Di-O-caffeoylquinic acid(r=0.9990),4.026~80.52μg/mL for Jatrorrhizine Hydrochloride(r=0.9995),3.924~78.48μg/ mL for Baicalin(r=0.9998),6.030~120.6μg/mL for Berberine Hydrochloride(r=0.9998).The average recoveries(n=6)were 96.5%,97.5%,95.9%,98.6%,99.8%,98.4%and 97.3%;RSDs were 1.5%,1.3%,1.2%,1.4%,1.2%,1.1%and 0.9%respectively.ConclusionThe method is simple and repeatable,which can be applied to the quality control of Xiongju Shangqing pills.
Xiongjushangqing pills;HPLC;content determination
R917
A
1005-1678(2014)07-0177-04
辽宁省教育厅高等学校科研计划(20100352)
孙承浩,男,本科,副主任药师,研究方向:临床药学,E-mail:sunchenghao_s@163.com。

