渤海油气田硫铁化合物自燃危险性研究①
黄 刚 涂 强 郝晓鹏 韩 涛 许 猛
(中海油安全技术服务有限公司)
硫铁化合物可与O2发生氧化反应,同时释放出大量热量,当热量积聚到一定程度便发生自燃,若周围存在爆炸性混合气体,将导致严重的火灾或爆炸事故。2013年4月,渤海某油田平台发生原油储罐爆炸事故,造成2人死亡,1人轻伤。事故调查结果显示,由于在原油转罐过程中,大量空气进入储罐,造成储罐内部硫铁化合物因氧化放热反应而发生自燃,是导致发生罐体爆炸的一个重要原因。专业技术检测公司对储罐顶部、中部、底部腐蚀物进行了检测(见表1)。由于与空气接触情况不同,硫铁化合物被氧化程度不同,罐体底部与中部硫铁化合物被氧化程度低,硫含量明显偏高;顶部由于长期与空气接触,氧化程度较高,硫含量偏低。

表1 储罐腐蚀物中硫、铁含量
在海洋石油开采生产过程中,在储罐内部、过滤器、分离器等一些关键设备或部位极易发生硫铁化合物的累积,在检维修过程中与空气接触易发生自燃。对海洋石油生产设备中硫铁化合物的生成、积聚和自燃机理及自燃危险性进行研究,将为海洋石油的安全生产提供重要保障。
1 硫铁化合物生成机理
硫铁化合物的生成途径主要有电化学腐蚀、化学腐蚀、大气腐蚀和微生物腐蚀[1-3,5]。
1.1 电化学腐蚀
电化学腐蚀为硫铁化合物的主要生成途径。在有水存在的条件下,H2S在水中可电离生成具有酸性的H+,与铁发生腐蚀。根据生成中间络合物的不同主要分为两类:
(1) 生成中间络合物Fe(HS-)的电极反应:
阳极反应:Fe + H2S + H2O→Fe(HS-) +
H3O+
Fe(HS-)→Fe(HS)++ 2e-
Fe(HS)++ H3O+→Fe2++
H2S + H2O
阴极反应:H2S + 2e-→ S2-+ H2
总反应:H2S + Fe→ FeS + H2
(2) 生成中间络合物(Fe·H2S)2+的电极反应:
阳极反应:Fe + H2S →Fe(H2S)
Fe(H2S)→(Fe·H2S)2++ 2e-
(Fe·H2S)2+→Fe2++ H2S
阴极反应:H2S + 2e-→S2-+ H2
总反应:H2S + Fe→ FeS + H2
1.2 化学腐蚀
在干燥的环境中,油品中的活性硫如H2S、单质硫和硫醇等直接与设备金属表面的Fe发生反应,生成具有高氧化活性的硫铁化合物。主要化学反应方程式如下:
Fe+S→FeS
Fe+H2S→FeS+ H2
Fe+RCH2CH2SH→CH2+ FeS+ H2
Fe2O3+3H2S→2FeS+3H2O +S
Fe3O4+4H2S→3FeS+4H2O+S
2Fe(OH)3+3H2S→2FeS+6H2O+S
若是在高温情况下,原油中的H2S就会发生分解生成单质硫,单质硫比H2S更具有强腐蚀性,促使进一步腐蚀,生成易自燃多硫化物。主要化学反应方程式如下:
FeS+S→FeS2
2FeS+S→Fe2S3
1.3 大气腐蚀
在大气中,设备金属表面的Fe可被氧气氧化为Fe2O3,继而与H2S反应生成FeS。由于本反应主要通过铁锈与H2S反应,且反应较易进行,故除锈与防腐工作不善的设备往往通过本途径产生硫化亚铁。
Fe+O2+H2O→Fe2O3·H2O
Fe2O3·H2O+H2S→FeS+H2O
1.4 微生物腐蚀
微生物腐蚀主要为硫酸盐还原菌(SRB)腐蚀。在无氧条件下,SRB可将SO42-还原为S2-,S2-与设备金属表面的Fe2+发生反应生成硫铁化合物。
SO42-+8H→S2-+4H2O
Fe2++S2-→FeS2
2 硫铁化合物自燃机理
在有O2存在的条件下,硫铁化合物受热或光照时可发生下列反应[4,6]:
FeS+3/2O2=FeO +SO2;ΔH=49 kJ/mol
FeS2+O2=FeS +SO2;ΔH=222 kJ/mol
Fe2S3+3/2O2=Fe2O3+3S;ΔH=586 kJ/mol
从上述3式的反应焓变可知,硫铁化合物与O2反应均为强放热反应。如果氧化反应放出的热量不能及时地散失,会使温度升高,达到氧化自热。当自热温度达到硫铁化合物的自燃点时,硫铁化合物起火燃烧。如果着火点周围存在可燃介质,就会引发火灾和爆炸。
3 硫铁化合物自燃危险性分析
现有渤海某平台设备腐蚀产物3份,分别为:未发生自燃的清管废物(A样品)、已发生自燃的清管废物(B样品)、注水管汇内部腐蚀物(C样品)。对这3份样品进行能谱分析、X射线衍射分析及自热特性分析。
3.1 能谱分析
采用S-4800场发射扫描电子显微镜/X射线能谱仪对样品的成分进行分析,3个样品的能谱分析结果如图1~图3所示。
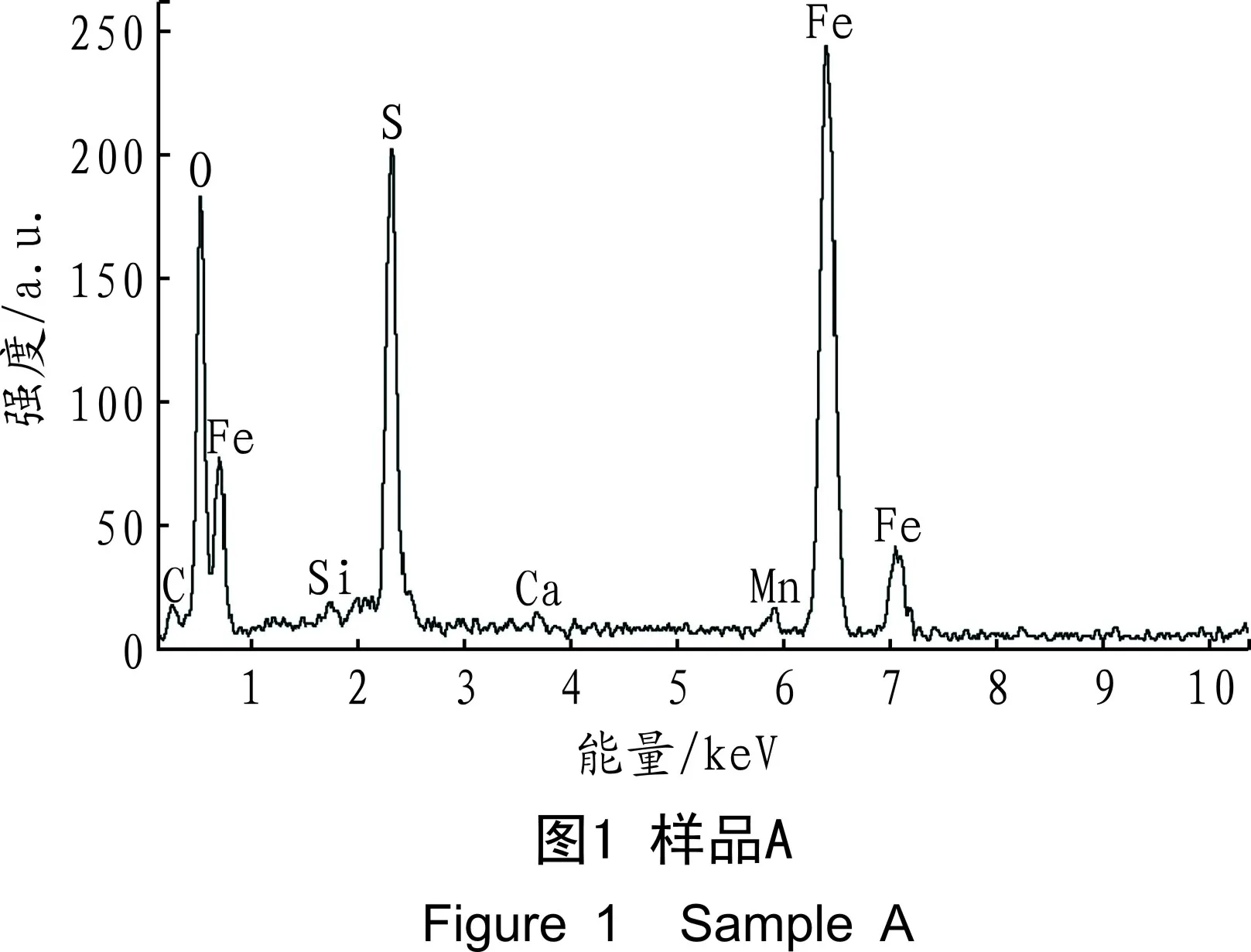


通过分析可知,3个样品中主要含C、O、Si、 S、Ca、Mn、Fe等元素,其中O、S、Fe的含量相对较高。
3.2 X射线衍射分析
采用D/MAX2500PC型X射线衍射仪对样品的相组成进行分析,X射线源为Cu(λ=0.154 056 nm),管电压45 kV,管电流40 mA,扫描速度10°/min,扫描2θ角度为10°~90°。由此可以确定样品中所含物质的类型,其X射线衍射图谱如图4~图6所示。
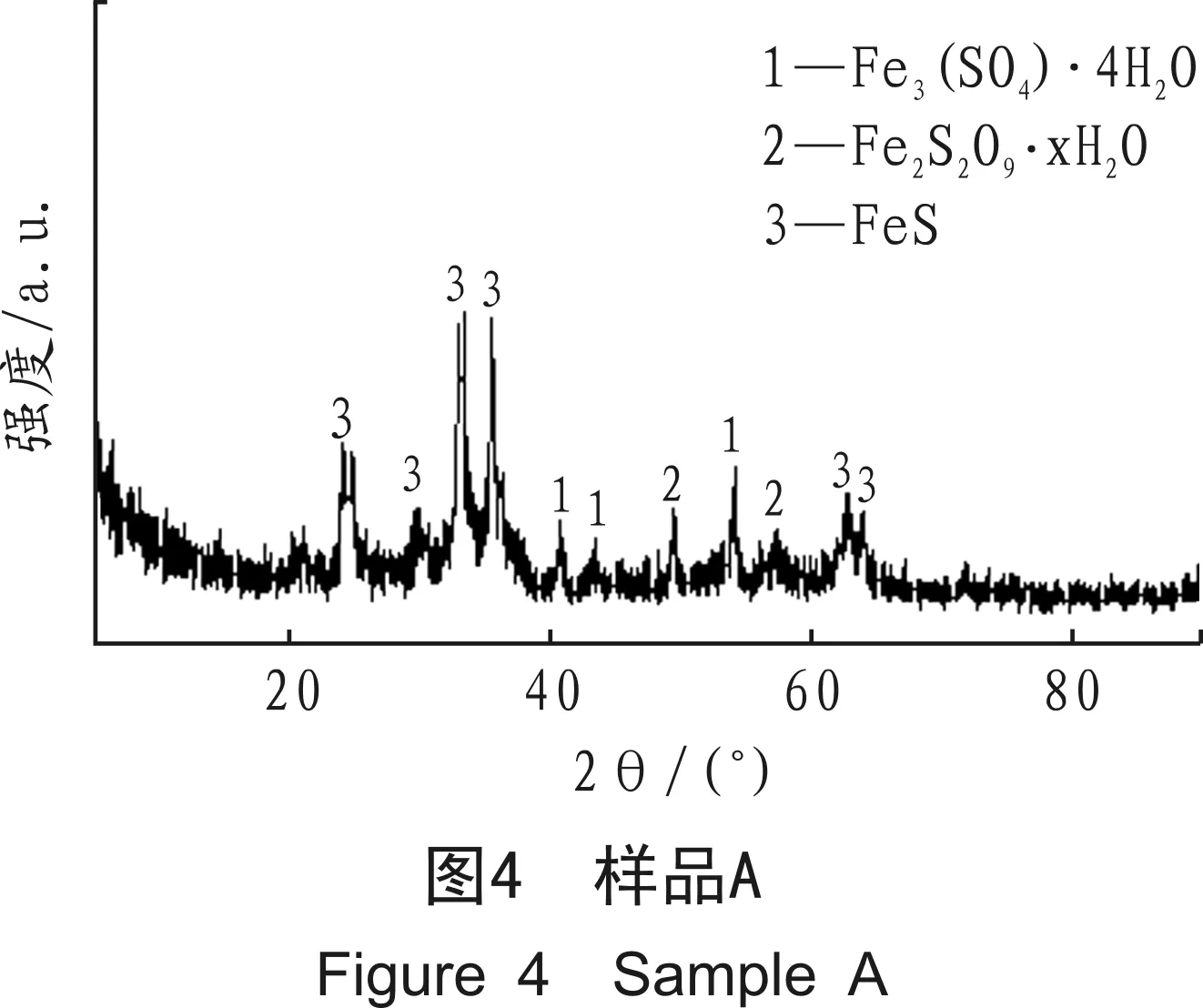
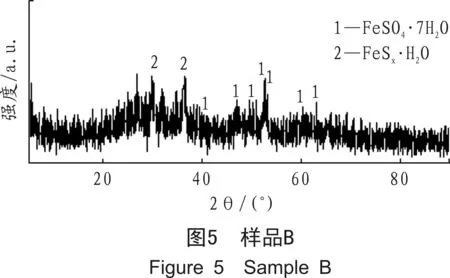

由XRD分析表明,样品A由Fe3( SO4)·4H2O、Fe2S2O9·xH2O及FeS 组成,样品B由FeSO4·7H2O和FeSX·H2O组成,样品C由Fe2( SO4)4( H2O )2、FeSx·H2O及 Fe ( OH )( SO4) ( H2O )5组成。可见,在油气生产设备内部生成的腐蚀物大部分为硫、铁、氧的化合物。
3.3 自热特性分析
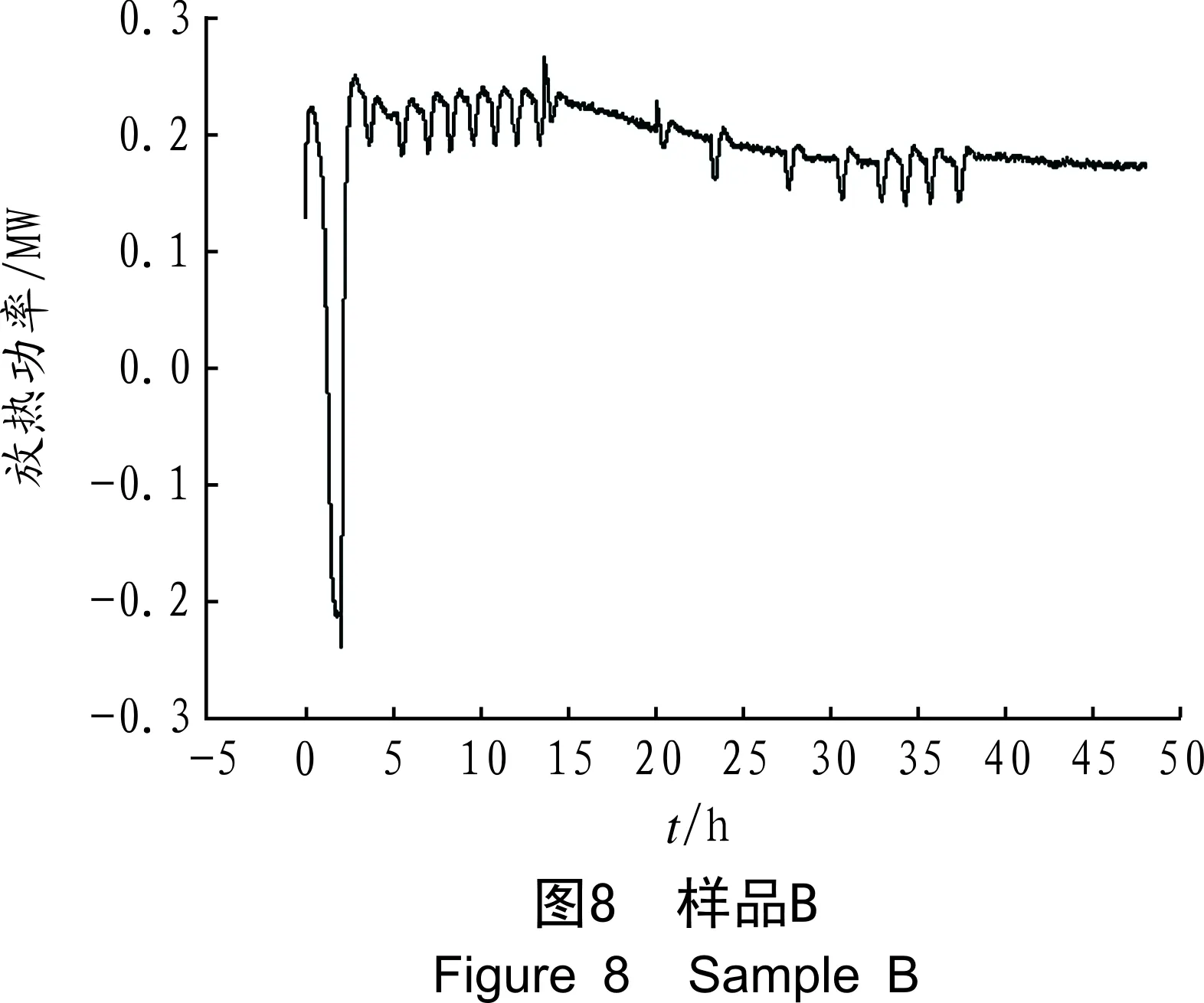
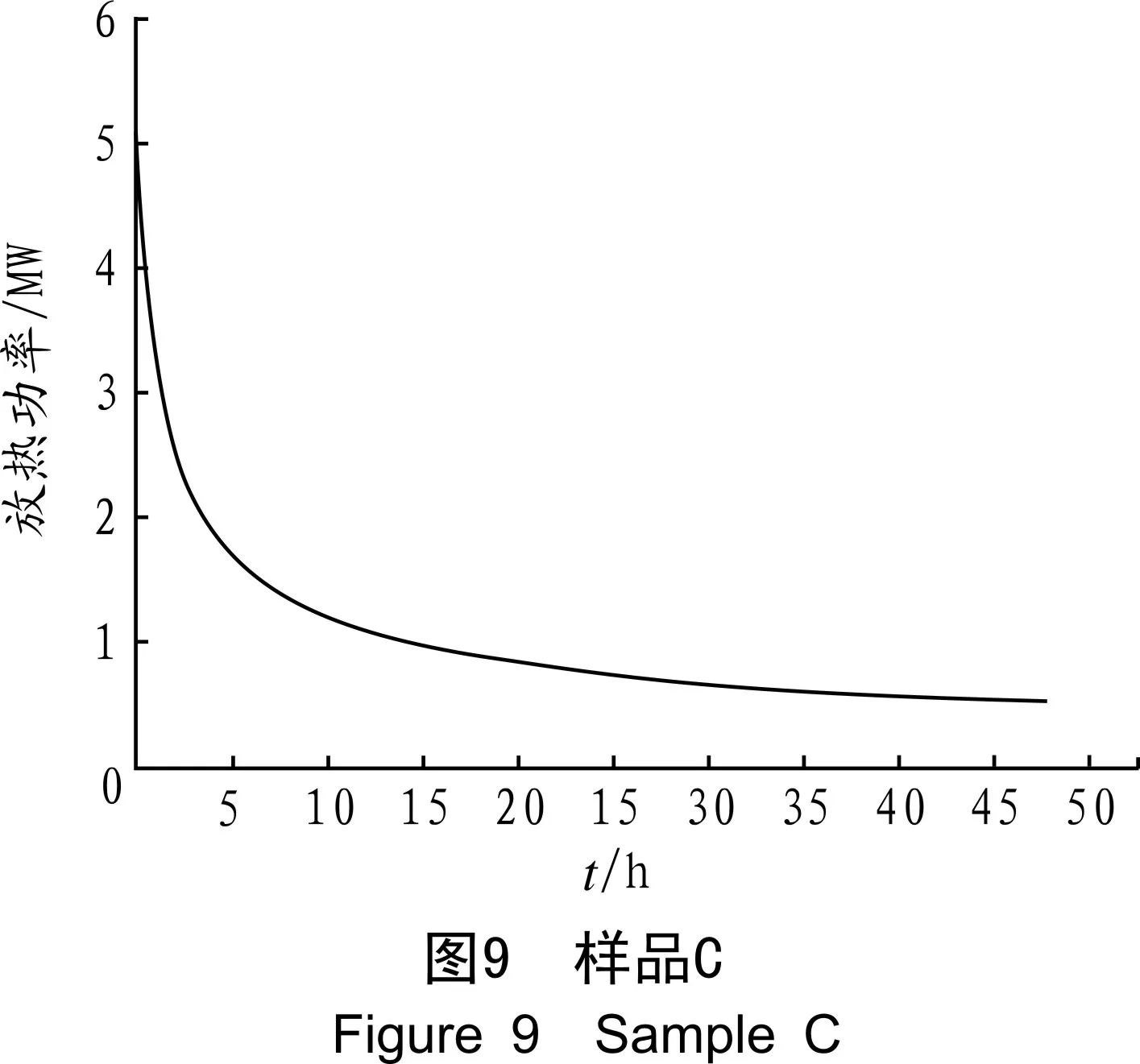
利用C80微量热仪,对样品的自放热过程进行分析。第1阶段,从26 ℃升温到30 ℃,升温速率0.5 ℃/min;第2阶段,30 ℃恒温1 h;第3阶段,在30 ℃测量48 h;第4阶段,30 ℃开始降温,降温速率0.5 ℃/min。环境温度20 ℃,分辨率:0.12 μW。图7~图9为样品的自放热曲线。通过对放热曲线进行面积分,可以得出样品的放热量。
从图7~图9可以得出,样品A从0 h 开始放热,0.3 h出现放热峰值,25 h达到稳定,放热量为209.254 J/g;样品B从0 h开始放热,0.26 h达到第一个放热峰值,第一个峰的热量为0.32 J/g,2.9 h达到第二个放热峰值,放热量为32.17 J/g,单位质量样品总放热量为32.49 J/g;样品C从0 h 开始放热,并出现放热峰值,放热量为156.14 J/g。可见,未自燃样品的放热量要远大于已经自燃的样品的放热量。

4 结 语
通过实验可以看出,硫铁化合物在生产设备内部确实存在,在油气生产过程中或检维修过程中如果与空气接触,会发生氧化反应,放出大量热量,如果环境中存在易燃易爆危险物,会导致火灾或爆炸等事故。因此,在石油生产过程中必须对这一安全隐患加以重视,从工艺、设备、管理等不同方面采取措施,防范事故的发生,建立一套切实可行的硫铁化合物防治程序,以保障石油化工生产的安全运行。
参考文献
[1] 张淑娟,孟庭宇,马翔. 硫铁化合物自燃机理及防治技术进展[J].安全、健康和环境,2013,13(1):33-36.
[2] 张振华. 硫铁化合物的生成及自燃性影响因素研究[D]. 沈阳:东北大学,2009.
[3] 宋继勇,彭志林,曾兰芳.硫化亚铁自燃在检修中的危害及预防[J].价值工程,2011,30(25):310.
[4] 马金秋,赵东风,谭科峰,等.典型炼油装置硫化亚铁自燃分析及对策[J]. 山东化工,2010,39(6):42-45,48.
[5] 李萍.含硫油品对储罐的腐蚀与自燃性的研究[D].沈阳:东北大学,2005.
[6] 赵雪娥,蒋军成,魏新利.硫化铁氧化及聚热过程影响因素[J].石油化工高等学校学报,2009,6(2):9-11.
—— 储罐

