全视网膜光凝治疗增殖型糖尿病视网膜病变临床分析
潘敏敏,张孝茹,孟 娜
全视网膜光凝治疗增殖型糖尿病视网膜病变临床分析
ClinicalAnalysisofLaserPanretinalPhotocoagulationforVitrectomyPatientsofProliferativeDiabeticRetinopathy
潘敏敏,张孝茹,孟 娜
目的探讨玻璃体切除术中术后进行全视网膜光凝对患者术后视力改善及并发症的影响。方法选择我院2009年11月~2012年12月收治的糖尿病视网膜病变患者113例(130只眼),随机分为两组,其中66只眼在手术中行全视网膜光凝,64例在术后1周分次行视网膜光凝。比较两种术后的视力恢复及并发症发生情况。结果术中光凝组视力提高55只眼,术后光凝组视力提高43只眼,两组有统计学差异(P<0.05)。术中光凝组术后发生玻璃体再出血8例,术后光凝组发生玻璃体再出血25例,两组有统计学差异(P<0.05)。两组黄斑水肿之间无显著差异。结论玻璃体切除手术中行全视网膜光凝能提高患者视力的预后,并且能降低术后玻璃体再次出血的发生率。
全视网膜光凝;增殖型糖尿病视网膜病变;玻璃体切除
增殖性糖尿病视网膜病变是目前常见的致盲性眼病,它由于新生血管的长入常引起玻璃体积血、机化甚至导致牵拉性视网膜脱离。治疗上常采用玻璃体切除手术和全视网膜光凝。全视网膜光凝主要是破坏高耗氧的色素上皮使其瘢痕化,从而改善视网膜的缺氧状态。全视网膜光凝可在玻璃体切除术后分次进行,但有文献报道[1]术中行全视网膜光凝也取得较好效果。2009年11月~2012年12月作者采用术中行全视网膜光凝和非术中光凝的方法进行手术,比较两种方法术后的视力效果及并发症发病率情况,现将结果报道如下。
1 资料与方法
1.1一般资料选择我院2009年11月~2012年12月收治的糖尿病视网膜病变113例(130只眼),患者患2型糖尿病病程10~21 a,平均15.3 a,术前检查视力≤0.1。糖尿病诊断分期标准按照中华医学会1985年标准进行[2]。所有患者均为糖尿病视网膜病变Ⅳ期以上,其中Ⅳ期74只眼,Ⅴ期38只眼,Ⅵ期18只眼。排除已行视网膜激光光凝患者,排除青光眼等其他眼病患者,排除非糖尿病引起的玻璃体积血及视网膜脱离患者,所有患者无虹膜新生血管。使用电脑软件随机将患者分为两组,一组在手术中行全视网膜激光光凝,一组术后1周分次行光凝。其中术中光凝组58例(66只眼),其中男39例,女19例,年龄38~72岁,平均(47.61±10.61)岁;术后光凝组55例(64只眼),其中男35例,女20例,年龄37~76岁,平均(48.45±10.95)岁。两组资料比较无统计学意义(P>0.05),具有可比性。所有患者均同意进行本次试验研究,并签署自愿协议书。
1.2治疗方法两组患者均由同一手术医生进行玻璃体切除手术,采用闭合式经睫状体平坦部行玻璃体手术,切除混浊、积血的玻璃体,去除纤维血管膜。伴有孔源性视网膜脱离患者使用重水展平视网膜后再行眼内激光封闭裂孔,有视网膜脱离选择硅油填充。术中光凝组(66只眼)在玻璃体切除完毕后一次完成全视网膜激光光凝,仪器采用科以人NOVUS SPECTRA激光机,激光光斑大小选择200 μm,能量选择200~500 mV,曝光时间选择0.1~0.2 s。光凝范围:视盘鼻侧、上方及下方1 PD外至赤道部,颞侧选黄斑中心凹外1 PD处到赤道部。光斑之间间距约1个光斑直径大小,总光斑数量在1 000个左右。术后光凝组按常规玻璃体切除手术方式进行,对于有视网膜裂孔患者行裂孔激光封闭,术中不行全视网膜光凝。术后光凝组在术后1周开始行全视网膜光凝,光凝从后极部开始逐渐向周边扩展,分3~4次完成视网膜光凝,每次间隔5~7 d。随访观察6~12个月,平均8个月。
1.3观测指标及并发症视力测量采用国家标准对数视力表,术前术后视力均测矫正视力,让患者从上往下读视力表,直到错误一半以上停止测量并记录视力。术后视力较术前提高大于或等于两行视为视力提高,若视力变化小于2行视为视力不变,若视力较术前下降大于或等于两行视为视力下降;术前矫正视力低于0.1者以视力变化0.04为判定标准。所有手术患者都记录术后的玻璃体出血、黄斑水肿等并发症。
1.4统计学处理所有患者数据使用Excel及SPSS 16.0进行统计处理。两组测量结果比较采用秩和检验,以P<0.05为差异有统计学意义。
2 结果
术中光凝组比术后光凝组的视力提高更明显,差异有统计学意义(Z=-2.386,P=0.016),见表1。术中光凝组与术后光凝组的并发症比较:术中光凝组术后发生玻璃体再次出血比术后光凝组低,差异有统计学意义(χ2=22.547,P=0.000)。而黄斑水肿发生率两组之间比较无显著差异。见表2。
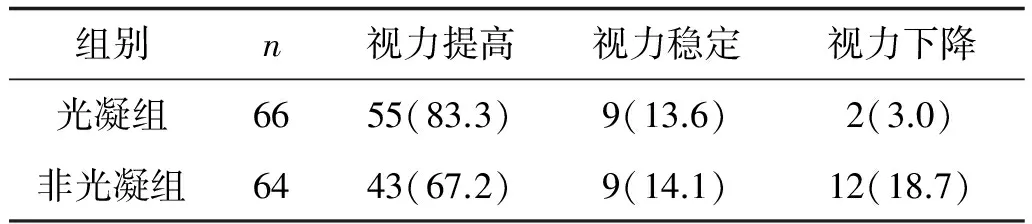
表1 术中光凝组与非光凝组术后视力比较 例(%)

表2 术中光凝组与非光凝组术后并发症的比较 例(%)
3 讨论
糖尿病引起的视网膜病变常并发玻璃体积血、牵拉性视网膜脱离、黄斑水肿等并发症而致视力下降[3]。目前玻璃体切除手术和全视网膜光凝是治疗糖尿病视网膜病变的重要手段[4]。玻璃体切除手术可以清除增生的新生血管和浑浊的玻璃体组织,同时可以减少新生血管的长入,但是新生血管可能已经参与了视网膜的能量供给,如果单纯地切除新生血管可能会导致视网膜的缺血缺氧加重,所以全视网膜激光光凝是玻璃体切除术后的关键治疗。
激光视网膜光凝是增殖型糖尿病视网膜病变的常规治疗[5]。其原理主要是破坏高耗氧的视网膜色素上皮层,使其氧耗降低,从而降低新生血管生长因子。另外破坏色素上皮层使视网膜外屏障功能降低,从而改善脉络膜对视网膜层的供养。周边视网膜破坏后能使有限的血流重新分布到黄斑中心凹上,改善黄斑的功能[6]。目前很多全视网膜光凝都是安排在眼外进行,一般术后分3~4次完成。这种光凝方式使用的光凝点量较大,约2 000个点,部分患者使用的量可以更高。本研究采用对照试验比较了眼内光凝与眼外光凝,结果显示眼内光凝组术后的视力恢复比眼外光凝组更加明显。该结果与张少冲的研究比较一致,张少冲[1]的研究结果也证实玻璃体手术中进行全视网膜光凝能收到很好的结果。这主要是因为眼内光凝直接在视网膜表面进行,它可以排除混浊的眼内屈光介质对激光能量的消耗,所以眼内激光可以使用比较小的能量,避免了对其他眼内组织的损伤。本研究中仅使用1 000个左右的激光点,比手术后的2 000个光凝点有显著的降低。另外眼内光凝可以调节光纤头与视网膜的距离,从而调整激光斑的大小,而眼外光凝不能调节激光与视网膜之间的距离,所以使用的灵活性比眼内光凝差。还有部分糖尿病视网膜病变患者合并有白内障,这些患者会影响观察眼底,同时造成眼底光凝困难。所以眼内光凝比眼外光凝有不少的优势。
玻璃体切除术后玻璃体再次出血是常见的并发症之一[7],这主要与手术过程中纤维血管膜清理不完全,止血不彻底,手术区新生血管长入有关[8]。如果术后少量的出血可自行吸收,而且对术后的光凝影响不大,如果再出血量太大长期不吸收需要再次手术,不能盲目光凝,以免误伤黄斑区。本研究结果显示眼内光凝术后出现再出血的患者比眼外光凝者少,可见及时的眼内全视网膜光凝还能有效地减少玻璃体再出血的发生。黄斑水肿也是玻璃体切除术后常见的并发症[9],陈晓等[10]认为术中进行光凝会因为一次使用的能量太多而导致术后炎症反应、视网膜水肿等并发症加重。但从本项研究结果中可以看出两组患者术后的黄斑水肿无明显的差别,说明术中光凝不会增加患者术后并发症,反而还会减少玻璃体再次出血的可能。
综上所述,玻璃体切除手术联合眼内全视网膜激光光凝比眼外术后光凝更能提高患者的视力,而且不会增加光凝的并发症。
[1]张少冲,高汝龙,丁小燕,等.玻璃体切除术中全视网膜光凝治疗晚期增生性糖尿病视网膜病变[J].中华眼科杂志,2004,39(12):740-742.
[2]中华医学会眼科学会眼底病学组.糖尿病视网膜病变分期标准[J].中华眼科杂志,1985,21(1):113.
[3]孟丽珠,陈松,赵秉水,等.玻璃体视网膜手术治疗增生性糖尿病视网膜病变合并牵拉性视网膜脱离视力预后影响因素[J].中华眼底病杂志,2010,26(2):124-127.
[4]张英楠,陈晓隆.玻璃体切割术治疗增生性糖尿病视网膜病变[J].眼科新进展,2012,32(1):56-58.
[5]刘晓玲,孙心铨.重视糖尿病视网膜病变以及眼底病激光光凝的规范化治疗[J].中华眼底病杂志,2010,26 (2):101-104.
[6]张风.糖尿病视网膜病变激光治疗的时机与方法[J].眼科研究,2007,25(6):401-403.
[7]王桂云,左玲,刘茂雄.增殖型糖尿病视网膜病变玻璃体切割手术并发症及发生因素分析[J].中国实用眼科杂志,2005,23(7):682-684.
[8]戴荣平,董方田,霍冬梅,等.糖尿病视网膜病变玻璃体切割手术后玻璃体积血的临床分析[J].中华眼底病杂志,2007,23(4):241-243.
[9]沈胤忱,许迅.糖尿病黄斑水肿的治疗现状[J].中华眼底病杂志,2013,29(1):108-111.
[10]陈晓,晏颖,宋艳萍,等.玻璃体切除术联合多波长激光光凝治疗增殖型糖尿病视网膜病变[J].中国激光医学杂志,2010,19(4): 227-230.
2014-06-10
河南科技大学第二附属医院眼科,河南洛阳 471000
潘敏敏(1966-),女,河南洛阳人,副主任医师,从事眼科眼底病、眼外伤工作。
R779.63,R587.1
B
1672-688X(2014)03-0203-03

