左卡尼汀抑制过氧化氢介导的NFATc3核转位*
戴红良, 黄 雷, 贾桂枝, 梁春光, 李 昕, 戚春玲
(辽宁医学院 1护理学院, 3生物化学与分子生物学教研室,辽宁 锦州 121001; 2锦州市食品药品检验所,辽宁 锦州 121000)
左卡尼汀是位于线粒体膜的机体内源性化合物,主要来源于肝肾合成以及体外的饮食摄入[1-2]。其基本作用是促进长链脂肪酸转运至线粒体进行β氧化,为机体供能[3]。除此之外,左卡尼汀还具有显著的抗氧化活性[4-5]。我们之前的研究发现,左卡尼汀可显著抑制过氧化氢(H2O2)诱导的心肌细胞凋亡,其抗凋亡机制与抑制Ca2+/钙调神经磷酸酶(calcineurin, CaN)信号级联有关[5-6]。胞浆活化T细胞核因子3(nuclear factor of activated T-cells, cytoplasmic 3, NFATc3)是CaN下游的重要转录因子。本研究拟通过分析左卡尼汀对H2O2刺激下心肌细胞内NFATc3表达及分布的变化,进一步探讨其抗氧化损伤的机制。
材 料 和 方 法
1 材料
1.1药物与试剂 左卡尼汀、胰蛋白酶、DMEM低糖培养基T和Hoechst 33258染料均购于Sigma;胎牛血清购自杭州四季青生物工程材料研究所;细胞核蛋白与细胞浆蛋白抽提试剂盒及BCA蛋白浓度测定试剂盒购自碧云天生物技术研究所;NFATc3及β-actin I抗购于Santa Cruz;Lamin B I抗购于Pierce;辣根过氧化物酶(horseradish peroxide, HRP)标记的II抗购于Santa Cruz;FITC标记的II抗购自北京中杉金桥公司。
1.2动物 出生1~3dSprague-Dawley(SD)大鼠乳鼠,雌雄不拘,由辽宁医学院实验动物中心提供。动物合格证号为SCXK(辽) 2003-0007。
2 方法
2.1心肌细胞培养 取出生1~3 d SD大鼠乳鼠,开胸取出心脏,用D-Hanks液冲洗3次后剪成约1 mm×1 mm×1 mm大小的碎块,在37 ℃条件下,以0.8 g/L胰蛋白酶消化分离细胞。将消化完毕的细胞以差速贴壁法进行纯化后,置于含15%胎牛血清的DMEM培养液中,置于37 ℃、5% CO2培养箱中培养。待细胞融合后,换以含0.4%胎牛血清的DMEM,继续培养24 h后,将细胞分组用于实验。
2.2细胞核蛋白及浆蛋白提取 取处理完成的细胞,弃去培养基,PBS冲洗后用细胞刮子刮下细胞后,然后按照核蛋白提取试剂盒步骤提取核蛋白与浆蛋白。
2.3Westernblotting提取细胞蛋白后,BCA法测定蛋白浓度。取30μg总蛋白,以样品缓冲液配平上样体积,沸水煮5min后进行聚丙烯酰胺凝胶电泳,待电泳完成后电转移至聚偏氟乙烯PVDF膜。用5%脱脂牛奶封闭1h,接着加NFATc3、β-actin及laminBI抗4 ℃孵育过夜。以含吐温20的三羟甲基氨基甲烷缓冲液(Tris-bufferedsalinewithTween20,TBS-T)充分洗膜后,以HRP标记的II抗室温孵育2h。TBS-T洗膜后,化学发光法显色。 利用NIHImageJ1.42软件对扫描的条带进行灰度分析。
2.4细胞免疫荧光分析 取处理完成的细胞,以4%多聚甲醛固定30 min。加入0.2% Triton X-100作用30 min。以2%标准血清室温封闭1 h。加入NFATc3 I抗于4 ℃孵育过夜。FITC标记的II抗室温孵育1 h。用Hoechst 33258复染细胞核,置于荧光显微镜下观察并拍照。
3 统计学处理
采用SPSS 16.0统计软件分析。数据以均数±标准差(mean±SD)表示。组间比较采用单因素方差分析。以P<0.05为差异有统计学意义。
结 果
1 左卡尼汀对H2O2刺激下心肌细胞内NFATc3表达的影响
结果显示,H2O2、左卡尼汀及CaN特异性抑制剂环孢素A(cyclosporin A, CsA)均不影响NFATc3的表达,见图1。
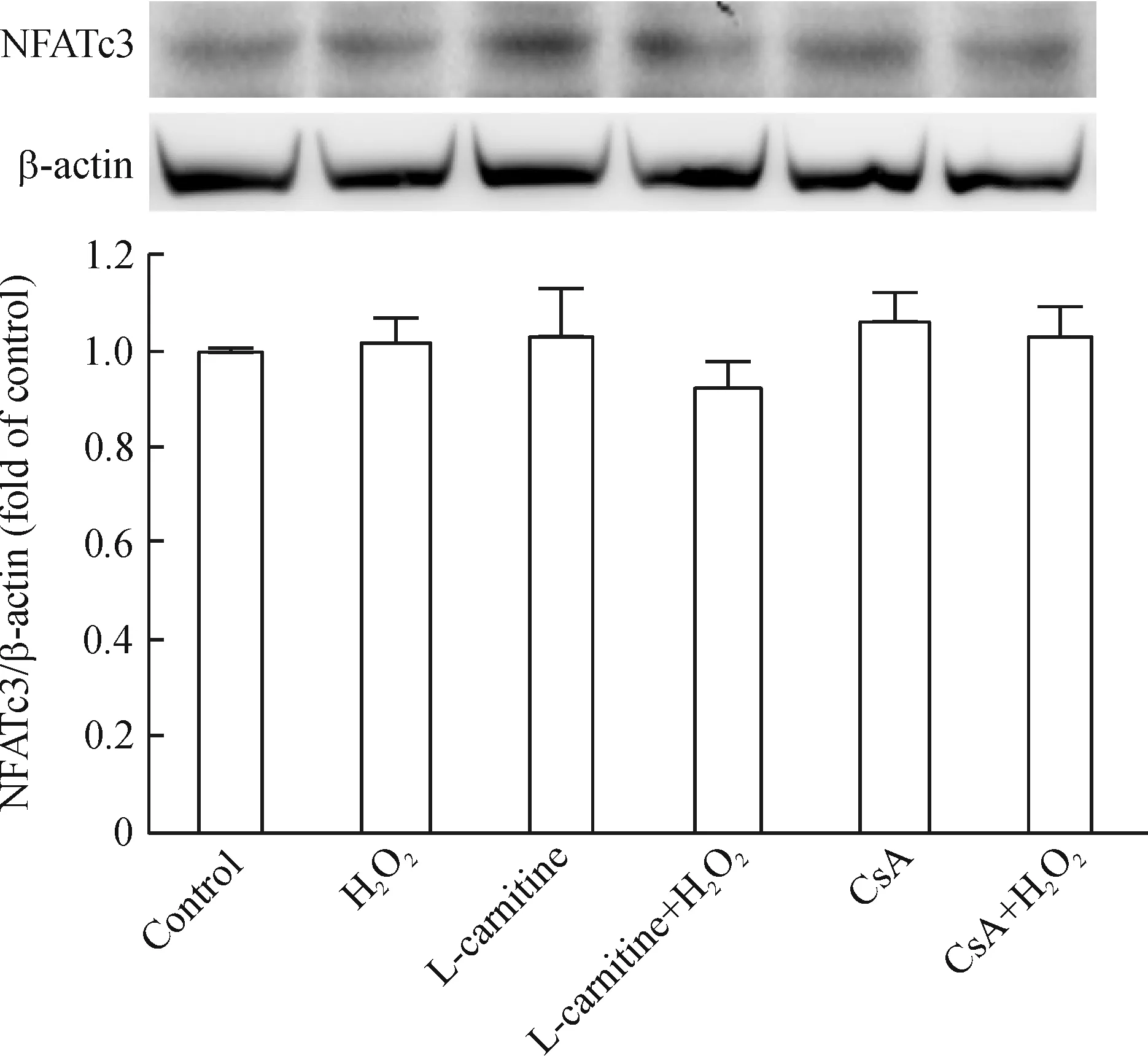
Figure 1. Effect of L-carnitine and CsA on NFATc3 expression in rat cardiac myocytes under H2O2 stimulation. Mean±SD.n=3.
2 左卡尼汀对H2O2刺激下胞浆及胞核中NFATc3表达的影响
与正常组比较,H2O2处理12 h后心肌细胞胞浆内NFATc3的表达显著降低,而其在核内的表达则显著增加,左卡尼汀及CsA本身并不影响NFATc3在胞浆及胞核的表达,但这2种药物预处理均能显著抑制H2O2诱导的上述改变,见图2。
3 左卡尼汀对H2O2诱导的NFATc3核转位的影响
免疫荧光的结果显示, H2O2处理12 h显著诱导NFATc3由胞浆到胞核的转位;左卡尼汀及CsA本身不影响NFATc3的转位,但这2种药物均能阻止H2O2的促转位作用,见图3。
讨 论
氧化应激是指细胞内氧化及抗氧化系统失衡,从而导致氧化作用过度激活的一种病理状态。心肌受到损伤后,活性氧与自由基生成大大增加。已经证实,氧化应激在心肌缺血再灌注损伤、糖尿病性心肌病及心肌纤维化等病理过程中发挥着重要作用[7-9]。而应用抗氧化剂往往能够取得良好效果[10]。
在正常的生理状态下,Ca2+是细胞内重要的第二信使。而在病理状态下,细胞内的Ca2+异常升高(Ca2+超载)则会对细胞带来严重损伤。已有研究证实,活性氧/氮应激可以通过改变细胞内正常的Ca2+稳态过程,最终诱导细胞死亡[11]。在之前的研究中我们也发现,H2O2可诱发心肌细胞内的钙超载,引起心肌凋亡。并发现左卡尼汀可通过抑制Ca2+下游CaN的过表达抑制心肌细胞凋亡[5]。

Figure 2. Effect of L-carnitine and CsA on NFATc3 expression in cytoplasmic and nuclear fractions. Mean±SD. n=3.*P<0.05 vs control group; #P<0.05 vs H2O2 group.
CaN是细胞内钙离子执行功能的重要靶蛋白之一。CaN在H2O2诱导的心肌损伤中起着重要作用[5,12]。当CaN激活后,其可直接与转录因子NFATc3结合,使其发生去磷酸化,从而使其由胞质向胞核转位。介导凋亡相关基因的表达[13]。许多物质可通过影响NFATc3的表达和(或)转位发挥其生物学作用[14-15]。在本研究中,我们发现左卡尼汀虽然不能影响NFATc3的表达,却可显著抑制其自胞浆自胞核的转位。另外,本研究还发现CaN特异性抑
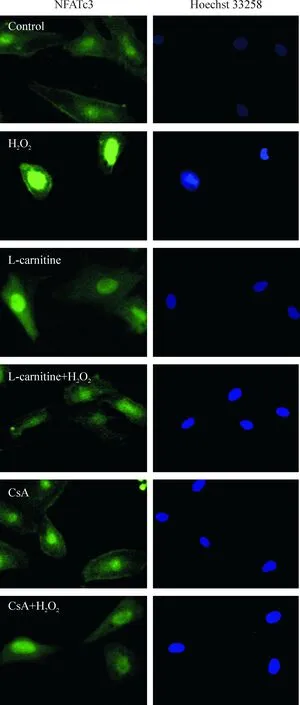
Figure 3. Effect of L-carnitine and CsA on NFATc3 nuclear translocation in rat cardiac myocytes under H2O2 stimulation (×400).
制剂CsA可显著抑制H2O2诱发的NFATc3核转位。提示该现象是CaN依赖的。既然左卡尼汀可抑制CaN的表达[5],那么左卡尼汀抑制NFATc3核转位很可能是其抑制CaN表达的结果。
综上所述,左卡尼汀对H2O2诱发的NFATc3的细胞核转位呈现明显的抑制作用。左卡尼汀发挥其抗氧化应激损伤可能与此有关。
[参 考 文 献]
[1]Arrigoni-MartelliE,CasoV.Carnitineprotectsmitochondriaandremovestoxicacylsfromxenobiotics[J].DrugsExpClinRes, 2001, 27(1): 27-49.
[2] Lysiak W, Lilly K, DiLisa F, et al. Quantitation of the effect of L-carnitine on the levels of acid-soluble short-chain acyl-CoA and CoASH in rat heart and liver mitochondria[J]. J Biol Chem, 1988, 263(3): 1151-1156.
[3]ReboucheCJ,SeimH.Carnitinemetabolismanditsregulationinmicroorganismsandmammals[J].AnnuRevNutr, 1998, 18: 39-61.
[4] Chao HH, Liu JC, Hong HJ, et al. L-carnitine reduces doxorubicin-induced apoptosis through a prostacyclin-mediated pathway in neonatal rat cardiomyocytes[J]. Int J Cardiol, 2011, 146(2): 145-152.
[5] 贾桂枝,王洪新,李 红, 等. 左卡尼汀调控钙调神经磷酸酶表达抑制过氧化氢诱导心肌细胞凋亡作用[J]. 中国药理学通报, 2014, 30(3): 425-428.
[6] 戴红良,贾桂枝,刘 堃, 等. 左卡尼汀通过抑制钙/钙调素依赖蛋白激酶Ⅱ信号通路抑制过氧化氢诱导的大鼠心肌细胞凋亡[J].中国病理生理杂志, 2013, 29(7):1250-1254.
[7]ChouHC,ChanHL. 5-Methoxytryptophan-dependentprotectionofcardiomyocytesfromheartischemiareperfusioninjury[J].ArchBiochemBiophys, 2014, 543:15-22.
[8] Sun X, Chen RC, Yang ZH, et al. Taxifolin prevents diabetic cardiomyopathyinvivoandinvitroby inhibition of oxidative stress and cell apoptosis[J]. Food Chem Toxicol, 2014, 63:221-232.
[9]PurnomoY,PiccartY,CoenenT,etal.Oxidativestressandtransforminggrowthfactor-β1-inducedcardiacfibrosis[J].CardiovascHematolDisordDrugTargets, 2013, 13(2):165-172.
[10] Wang R, Miura T, Harada N, et al. Pleiotropic effects of the beta-adrenoceptor blocker carvedilol on calcium regulation during oxidative stress-induced apoptosis in cardiomyocytes[J]. J Pharmacol Exp Ther, 2006, 318(1):45-52.
[11]ErmakG,DaviesKJ.Calciumandoxidativestress:fromcellsignalingtocelldeath[J].MolImmunol, 2002, 38(10):713-721.
[12] 冯 星, 金明华, 刘晓梅, 等. CaN抑制剂对H2O2诱导的大鼠H9c2心肌细胞凋亡的影响[J]. 吉林大学学报:医学版, 2009, 35(2): 249-253.
[13]ZhuH,GaoW,JiangH,etal.CalcineurinmediatesacetylcholinesteraseexpressionduringcalciumionophoreA23187-inducedHeLacellapoptosis[J].BiochimBiophysActa, 2007, 1773(4): 593-602.
[14] Guo J, Gan XT, Haist JV, et al. Ginseng inhibits cardiomyocyte hypertrophy and heart failure via NHE-1 inhibition and attenuation of calcineurin activation[J]. Circ Heart Fail, 2011, 4(1):79-88.
[15]TanX,LiJ,WangX,etal.TanshinoneIIAprotectsagainstcardiachypertrophyviainhibitingcalcineurin/NFATc3pathway[J].IntJBiolSci, 2011, 7(3):383-389.

