罗氏Cobas8000 c701全自动生化分析仪模块性能验证
冯 磊,徐文波,张大莲,张兴锋,代艳娟,毛星星,罗曼玲
(玉溪市人民医院 检验科,云南玉溪653100)
罗氏Cobas8000 c701全自动生化分析仪模块性能验证
冯 磊,徐文波,张大莲,张兴锋,代艳娟,毛星星,罗曼玲
(玉溪市人民医院 检验科,云南玉溪653100)
目的:对罗氏Cobas8000 c701全自动生化分析仪模块进行仪器性能验证。方法:依照YY/T 0654-2008标准,对杂散光、吸光度线性范围、吸光度准确性、吸光度稳定性、吸光度重复性、吸光度零点漂移、样品针携带污染率、加样系统准确性与重复性、孵育池温度准确性及波动、临床项目的批内精密度、试剂仓温度共计十一项性能进行验证。结果:罗氏Cobas8000 c701全自动生化分析仪模块各项性能指标与YY/T 0654-2008标准及厂商规定的分析性能基本一致,符合质量目标要求。结论:验证方案可操作性和实用性强,除可用于实验室管理机构的相关认证及认可工作,还可为仪器故障的诊断及处理提供依据。
全自动生化分析仪;性能验证;质量
为配合实验室ISO15189质量体系建设,同时也为了验证新购入罗氏Cobas8000 c701全自动生化分析仪模块是否满足国家食品药品监督管理局2008年颁布的中华人民共和国医药行业标准(YY/T 0654-2008)中关于全自动生化分析仪的性能要求,于2013年11月8日与罗氏诊断产品(上海)有限公司工程师共同对实验室罗氏Cobas8000 c701全自动生化分析仪模块按照YY/T 0654-2008标准进行仪器性能验证。
1 材料和方法
1.1 仪器设备
德国罗氏诊断公司生产Cobas8000 c701全自动生化分析仪模块、经过标定的温度计及加样器各一支。
1.2 试剂
1.2.1 罗氏原装ALT、Urea、TP试剂、校准品cfas 、PCCC1质控品(批号:168331)、PCCC2质控品(批号:168411)、罗氏原装配套离子补偿液、罗氏原装配套check试剂。
1.2.2 其他试剂:50g/L亚硝酸钠溶液一套、国家一级线性标准物质(C1-C5共5个浓度)一套、吸光度值为5000±5%的标准物质溶液(准物质1)和吸光度值为10000±5%的标准物质溶液(准物质2)各一套、色素溶液Orange G原液一瓶。以上试剂购自中国计量科学院北京分院,均为安培包装一次性使用现成商品试剂。加样系统准确性与重复性检定所用sample solution(特定吸光度的Orange G)与Instrument check试剂有罗氏公司提供。
1.3 方法
性能验证检测工作开始前需更换新的比色杯及光源灯,检测工作环境温度(15~32℃)、相对湿度(45%~85% RH)、水质(<1 μS/cm)、电压(220V)达标, UPS工作正常,确保孵育池已执行换水,且温度已达到37℃,光源灯已稳定30min以上,并确认仪器设备各组成机构工作正常。
(1)杂散光检测。以蒸馏水为参比,340nm波长测50g/L亚硝酸钠溶液吸光度,要求吸光度不小于23000。
(2)吸光度线性范围检测。测定505nm波长处线性范围。以国家一级线性标准物质C1-C5为色素液分别在各模块上测定吸光度,D模块应测定内圈和外圈,每个浓度测定5次,计算算术平均数及线性相关系数,要求相关系数大于0.995。
(3)吸光度准确性检测。以蒸馏水为参比,340nm波长分别测定标准物质1和标准物质2溶液吸光度,重复5次,计算算术平均数与标准值之差,要求标准物质1和标准物质2溶液吸光度的允许误差分别为±250 、±700,即4870±250、9750±700。
(4)吸光度稳定性检测。340nm波长测定标准物质1,10min内连续测定20个读数,测定间隔为仪器读数间隔,要求最大值与最小值之差小于100。
(5)吸光度重复性检测。340nm波长测定标准物质2,10min内连续测定20个读数,测定间隔为仪器读数间隔,最小反应体积为180μL,计算20个测定值的CV,要求CV<1.5%。
(6)吸光度零点漂移检测。执行Cell Blank后,检查后续比色杯和第一个比色杯的吸光度值,最大差值不大于±800。
(7)样品针携带污染率检测。以蒸馏水为试剂,色素溶液Orange G原液与蒸馏水为样品,反应体积为仪器规定最大(380μL),按照原液、原液、原液、蒸馏水、蒸馏水、蒸馏水的顺序为一组,测定吸光度,共测定5组。要求携带污染率不大于0.5%。携带污染率计算公式如下:
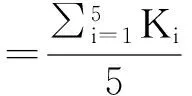
其中,Vs:样品加入量,Vr:试剂加入量。
(8)加样系统准确性与重复性检测。运用罗氏公司提供的专用程序Instrument Check,对样品针A/B、试剂针A/B加样的准确性及重复性进行检定,采用sample solution与蒸馏水为样本,instrument check为试剂,进行Instrument Check 检测。其中每根加样系统针加样21次,抛弃第一次结果计算后20次吸光度值的均值、SD及CV。要求样品针、试剂1针和试剂2针吸光度均值位于仪器规定范围内,即:278~326、694~767、351~387,CV值应分别小于1.5%、0.5%、1%。
(9)孵育池温度准确性及波动检测。将经过标定的精度为0.1℃的温度检测仪探头放入孵育池中,在温度显示稳定后,每隔30s测温一次,检测10min。要求温度值在37±0.3℃内,波动度不大于±0.2℃。
(10)试剂仓温度检测。将经过标定的精度为0.1℃的温度检测仪探头放入试剂仓中,在温度显示稳定后,每隔1min测温一次,检测10min。要求温度值在4~15±0.3℃内,波动度不大于±0.2℃。
(11)临床项目批内精密度检测。使用罗氏配套试剂、校准品及相应测定程序,定标通过后以PCCC1、PCCC2为标本重复进行20次测定,测定项目为ALT、Urea、TP,计算CV值,要求ALT、Urea、TP三个项目CV值应分别≤5%、≤2.5%、≤2.5%。
(12)电解质项目精密度检测。使用电解质配套试剂、校准品及相应测定程序,定标通过后对PCCC1、PCCC2分别进行20次重复测定,计算均值及测定值与靶值的偏差,要求电解质三个项目偏差均≤3.0%。
以上各检测内容以YY/T 0654-2008标准设计,出具的检测报告可用于实验室管理机构对实验室进行的相关认证及认可工作(如ISO15189和CAP认证等)。
2 结果
(1)杂散光:吸光度结果为46089,符合要求(>23000)。
(2)吸光度线性范围:相关系数为1,符合要求(>0.9950)。
(3)吸光度准确性:检测结果见表1。均在规定范围内。

表1 吸光度准确性检测结果
(4)吸光度稳定性:最大值(4790)与最小值(4762)之差为28,小于100。
(5)吸光度重复性: CV值为0.303%,小于1.5%。
(6)吸光度零点漂移:最大值(7820)与最小值(7710)之差为110,小于800。
(7)样品针携带污染率:样品针A和样品针B的5次平均样品携带污染率分别为0.46%、0.28%,均小于0.5%。
(8)加样系统准确性与重复性:检测结果见表2。按照标准均符合要求。
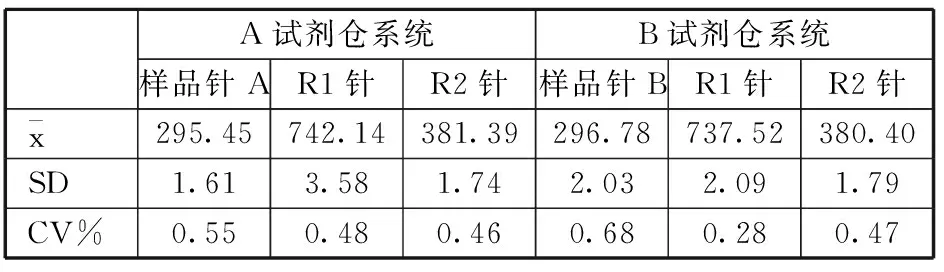
表2 加样系统准确性与重复性检测结果
(9)孵育池温度准确性及波动:所有时间位点温度测定值均为37.0℃,均符合规定要求。
(10)试剂仓温度检测:所有时间位点温度测定值均符合规定要求。
(11)临床项目的批内精密度:检测结果见表3,ALT、TP和Urea测定结果单位分别为U/L、g/L和mmol/L。按照标准均符合要求。
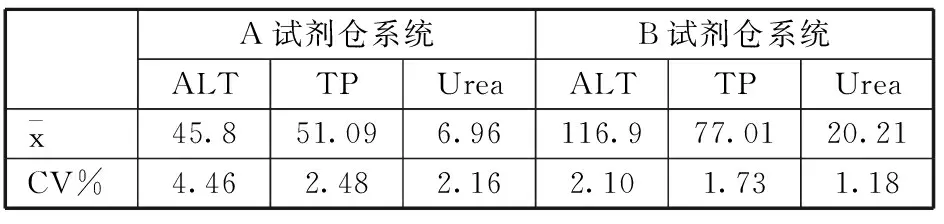
表3 临床项目批内精密度检测结果
(12)电解质项目精密度检测:结果见表4,K+、Na+、Cl-测定结果单位均为mmol/L。按照标准均符合要求。
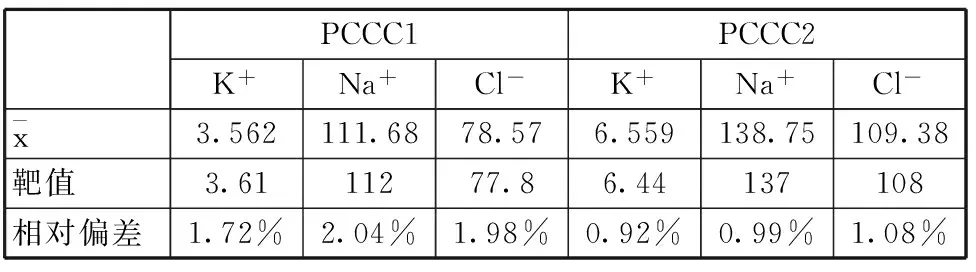
表4 电解质项目精密度检测结果
3 讨论
医学实验室认可是目前检验医学界讨论和关注的热点。《医学实验室质量和能力的专用要求》(ISO 15189)和美国病理家学会(CAP)要求参加其认可的实验室,在开展某一检测项目前,需提供并保留相关的方法学验证实验数据。但在进行检测项目性能验证之前需了解检测仪器的各项性能指标是否达到要求,只有检测仪器达标了,其所检测的项目才有可能达标,也才能达到实验室管理的最终目标,即:为临床提供准确可靠的检验结果。但如何合理选择、系统设计检测系统性能验证方案,检测系统的分析性能达到什么样的标准才能满足临床要求,国内报道甚少,是一个急需解决的现实问题。国家食品药品监督管理局2008年4月25日颁布2009年6月1日开始实施的中华人民共和国医药行业标准(YY/T 0654-2008)中对全自动生化分析仪的性能要求及验证方法做了全面规范,使各实验室有了可依照的标准,但该规范存在某些方法可操作性不强、某些评价内容不全及评价标准偏低的现象。故本实验室在依照该标准的同时,参考已通过ISO 15189实验室认可实验室的经验并结合仪器实际性能,探讨并制定了该套针对罗氏全自动生化分析仪仪器性能验证方案,供同行参考。
该验证方案主要有以下几点与YY/T 0654-2008稍有出入或改进,说明如下:(1)验证中所用试剂如50g/L亚硝酸钠溶液、C1-C5共5个浓度的国家一级线性标准物质、吸光度值为5000和10000的标准物质溶液、色素溶液Orange G原液等,无须自己配制,可自中国计量科学院北京分院购买,为安培包装一次性使用现成商品试剂,既保证质量又方便使用。(2)吸光度线性范围验证方法中,使用国家一级线性标准物质C1-C5共5个浓度梯度的物质为色素液,而非如标准上所说用Orange G自配11个浓度梯度色素液。同时,改用相关系数大于0.995为评价标准,而非标准规定的相对偏倚在±5%范围内的最大吸光度应不小于20000。通过以上改进,既避免了手工配制色素液时带来的误差,又避免了计算相对偏倚的繁琐,使评价更加简单易行且有效。(3)在加样系统准确性与重复性验证中,本方案使用罗氏公司提供的专用试剂sample solution 和instrument check运用专门编制的Instrument Check程序进行验证,与标准所推荐的比色法在方法学上是一样的,但避免了推荐方法中手工配制色素液的繁杂与误差。另外,在评价标准上对CV值的要求也严于标准规定的2%,对仪器的性能要求更高。(4)除了标准规定项目外,本方案还增加了电解质项目精密度检测,对仪器各部件性能的验证更全面。
验证结果显示本实验室罗氏Cobas8000 c701全自动生化分析仪模块各项性能指标与YY/T 0654-2008标准及厂商规定的分析性能基本一致,符合质量目标要求。本研究选用的验证方案可操作性和实用性较强,能够满足ISO 15189相关要求,为全自动生化分析仪性能验证提供了一套较标准的方案,对临床实验室的标准化和认可具有重要意义,可用于实验室管理机构的相关认证及认可工作中。另外,该验证方案还可用于全自动生化分析仪日常运行情况性能检测,如遇到原因不明的仪器故障、对仪器进行全面维护保养后、对仪器主要部件进行维修或更换后等情况,相关检测结果可为仪器故障的诊断及处理提供依据。如杂散光检测不达标,提示可能存在冲洗站工作不正常、光源老化、光路脏或光度计和电路连接不良等,为故障确定提供了线索,意义显著。
[1]丛玉隆,邓新立.实验室ISO 15189认可对学科建设的几点启示[J].中华检验医学杂志, 2007, 30(2):128-131.
[2] 毕波,吕元.定量检测方法学性能验证的系统设计[J].中华检验医学杂志, 2007, 30(2):143-145.
[3] 冯磊,年士艳,徐文波,等. 罗氏全自动生化分析仪Modular DPP模块性能验证[J]. 医疗装备,2011,24(12):10-12.
2014-05-14
TH773
A
1002-2376(2014)09-0005-03

