碳酸镧治疗维持性透析患者并发高磷血症疗效观察
陈晓霞,卢媛,楼季庄
论著·临床
碳酸镧治疗维持性透析患者并发高磷血症疗效观察
陈晓霞,卢媛,楼季庄
目的评价碳酸镧治疗维持性透析患者高磷血症的有效性。方法根据是否服用碳酸镧将患者分为观察组和对照组。碳酸镧观察组16例,均服用碳酸镧,每次500 mg,2~3次/d;对照组23例,口服碳酸钙,0.75 g/次,每天2次。结果与治疗前比较,治疗1、2、6个月后,观察组血磷水平均下降(P<0.01),对照组下降不明显(P>0.05),且观察组较对照组各时点血磷下降明显[(1.80±0.25)mmol/L vs. (2.21±0.33)mmol/L、(1.56±0.19)mmol/L vs.(2.28±0.26)mmol/L、(1.51±0.17)mmol/L vs. (2.29±0.25)mmol/L](P<0.01)。2组血钙下降均不明显(P>0.05);治疗6个月后,观察组PTH较对照组下降更明显[(614.8±178.38)pg/ml vs. (982.63±716.34)pg/ml](P<0.05)。结论碳酸镧治疗维持性透析患者高磷血症较传统降磷方法治疗有效。
高磷血症;碳酸镧;透析,维持性
慢性肾脏病(chronic kidney disease,CKD)尤其是终末期肾脏病(ESRD)患者普遍伴随着钙磷代谢紊乱,长期高磷血症除了引发继发性甲状旁腺功能亢进、肾性骨病、维生素D代谢障碍,还会加重血管钙化,进而引起严重心脑血管事件,是终末期肾脏病患者心脑血管疾病发生率和病死率逐年增高的重要因素。目前我国透析患者中,矿物质和骨代谢异常(MBD)普遍存在,据大型横断面研究显示,80%透析患者伴有高磷血症[1]。高磷血症是心血管疾病死亡和全因死亡的独立危险因素。本文通过了解我院血液净化中心透析患者的血磷管理情况,有效提高CKD-MBD管理水平。同时加强血清磷水平的管理对减少CKD疾病负担,提高患者生活质量有积极意义。
1 资料与方法
1.1 临床资料 2001年5月—2013年5月在我院血液净化中心规律透析3个月以上,血磷水平>1.78 mmol/L的患者39例,纳入标准:(1)近3周未使用磷结合剂的透析高磷血症患者;(2)正在服用含钙的磷结合剂的透析高磷血症患者。排除标准:(1)对磷结合剂过敏者;(2)肠梗阻、粪便嵌塞者;(3)急性消化道溃疡、溃疡性结肠炎、克罗恩病患者;(4)妊娠期或哺乳期妇女;(5)医师认为不适合磷结合剂患者。其中腹膜透析4例,血液透析35例;原发病为慢性肾小球肾炎14例,糖尿病肾病14例,高血压肾病5例,药物性肾损害1例,多囊肾1例,血管炎1例,梗阻性肾病1例,慢性肾盂肾炎1例,痛风肾病l例。参照K/DOQI慢性肾脏病及透析的临床实践指南,所有患者均接受个体化的抗高血压、纠正贫血、钙磷代谢和骨代谢紊乱的治疗,治疗目标值:透析前血压<140/90 mm Hg,血红蛋白(Hb)110~120 g/L,血清校正钙2.10~2.37 mmol/L,血磷1.13~1.78 mmol/L,钙磷乘积<13.75 mmol/L;血清全段甲状旁腺激素(PTH)150~300 pg/ml。所有透析患者要求低磷饮食,按是否服用碳酸澜分为2组,服用碳酸镧者为观察组16例,男6例,女10例,年龄22~71(53±13)岁,治疗前血钙2.08~2.72(2.37±0.19)mmol/L,血磷2.04~3.19(2.47±0.32)mmol/L,血PTH 27.7~2 338(997.31±231.48)ng/L。未服用碳酸镧者为对照组23例,男15例,女8例,年龄为38~76(55±14)岁,治疗前血钙2.00~2.63(2.40±0.21)mmol/L,血磷1.9~2.94(2.32±0.39)mmol/L,血PTH 37.2~2 500(902.92±652.92)ng/L。2组患者性别、年龄、血钙、血磷、血PTH水平比较差异均无统计学意义(P>0.05),具有可比性。2组患者均签署知情同意书。
1.2 治疗方法 所有入选血透患者规律血液透析每周3次,每次透析4 h,采用金宝AK96或Fresenius透析机,聚砜膜透析器,膜面积1.3~1.5 m2,血流量200~280 ml/min,透析液流量500 ml/min,均使用海德诺医用透析A液,透析液钙浓度1.5 mmol/L,若监测结果出现高钙血症,则使用低钙透析液,钙浓度为1.25 mmol/L,B液为碳酸氢盐透析液。腹膜透析患者均采用持续性不卧床腹膜透析(CAPD),4 h交换腹透液,夜间留腹,使用美国Baxter公司生产的乳酸盐透析液,钙浓度为1.25 mmol/L。高磷血症患者待血磷下降至正常水平后使用骨化三醇治疗甲状旁腺功能亢进。观察组患者入组时根据血磷水平服用碳酸镧500 mg,每天2~3次,后根据血磷水平及患者经济承受能力调整碳酸镧维持用量。对照组根据血钙水平服用碳酸钙降血磷,0.75 g/次,每天2次,若血钙水平超过正常值高限,停用碳酸钙,嘱其限磷饮食,低钙透析液进行血液透析。
1.3 观测指标 2组在基线及用药第1、2、6个月末访视血磷、血钙、血甲状旁腺素(PTH)指标变化。
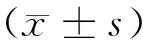
2 结 果
2.1 血磷变化 与治疗前比较,观察组患者服用碳酸镧治疗后1、2、6个月血磷均下降,差异有统计学意义(P<0.01)。对照组患者血磷与治疗前比较差异无统计学意义(P>0.05)。2组比较,观察组服用碳酸镧后血磷下降更明显(P<0.01)。见表1。
2.2 血钙变化 与治疗前比较,治疗后1、2、6个月2组患者血钙下降不明显(P>0.05)。2组间比较血钙水平差异亦无统计学意义(P>0.05)。见表1。
2.3 血PTH变化 与治疗前比较,治疗后6个月治疗组患者下降明显(P<0.05),对照组下降不明显(P>0.05)。2组比较差异有统计学意义(P<0.05)。见表1。

表1 2组治疗前后指标比较
注:与治疗前比较,*P<0.01;与对照组治疗后各时点比较,#P<0.05,△P<0.01
3 讨 论
随着肾功能的逐渐下降、ESRD患者的血磷排泄逐渐减少,常常出现高磷血症。而高磷血症可导致严重的并发症,如肾性骨病、甲状旁腺功能亢进等,且其与心血管疾病的发病率和病死率相关[2,3]。有研究显示,在ESRD患者中,持续的高磷血症及钙磷乘积升高与患者的病死率呈正相关[3]。所以控制高磷血症对改善ESRD患者生活质量和预后有重要意义。
控制高磷血症的主要措施包括限制饮食中磷摄入、充分透析、使用磷结合剂及切除甲状旁腺等。K/DOQI指南建议对CKD 5期伴高磷血症者,每天磷摄入量为800~1 000 mg;但饮食中的磷含量很难精确计算,大多数患者仅靠控制饮食中磷的摄入难以达到治疗目的,而且过度饮食控制会造成蛋白质摄入不足导致营养不良。常规血液透析约每周清除磷1 000 mg,远远低于饮食摄入的磷;腹膜透析每周磷的清除量高于血液透析,也不足以维持血磷平衡。虽然应用自动腹膜透析机行日间短时加夜间缓慢腹膜透析能够增加磷清除,但价格昂贵难以在全社会广泛应用。残余肾功能对血磷的清除起重要作用,当残余肾功能丧失后,血液透析和持续性非卧床腹膜透析患者的血磷明显升高。因此,90%以上透析患者需口服磷结合剂来控制血磷。
目前,传统磷结合剂主要为含铝或含钙的磷结合剂,但长期使用含铝的磷结合剂可导致铝在体内潴留,引起贫血、骨病和中枢神经系统损害等严重的不良反应,故只适合短期用于其他药物不能有效控制的高磷血症[4]。而含钙的磷结合剂可导致高钙血症,有增加钙磷乘积以及导致转移性钙化和心血管疾病的危险[5~7],故传统的磷结合剂并非治疗高磷血症的理想药物[8]。
碳酸镧作为一种新型非钙非铝磷结合剂已在西方国家、日本及中国台湾等地区得以广泛应用。2008年美国医疗处方保险计划(Medicare Part D)中,碳酸镧的年处方费用为4 882万美元,居透析患者用药第5位[9]。它含有的三价阳离子镧与磷有高度的亲和力,与磷结合后生成不易溶解、不易被消化吸收的磷酸镧,该复合物水溶性低,几乎不被肠道吸收,极少量被吸收的镧可通过胆汁及肠壁分泌排入肠道内,可通过粪便排出体外,从而达到降低血磷的作用[10],但受限于价格等因素在我国大陆地区尚未普及。
很多随机、对照临床研究均证实了碳酸镧在ESRD患者中降低血磷水平的有效性。在短期研究中,与安慰剂相比,每天1 350~3 000 mg的碳酸镧可显著降低血磷水平,每天2 250 mg的碳酸镧使血磷水平在第1周就显著下降,在第2周使血磷水平降低到正常范围,并在后续治疗中,持续使血磷水平维持在目标范围[11]。多项研究显示,碳酸镧治疗组的血磷达标率显著高于安慰剂组,同时碳酸镧治疗显著降低了钙磷乘积和PTH水平[12~14]。本研究结果显示,观察组患者服用碳酸镧降磷治疗后血磷下降明显,其下降幅度与对照组差异有统计学意义。经碳酸镧治疗的患者,其高PTH水平亦下降明显,原因可能是与传统磷结合剂,尤其是含钙的磷结合剂相比,其可以将患者血钙水平维持在较低的水平,间接减少对甲状旁腺的刺激作用;其次观察组患者血磷水平大多数下降在K/DOQI指南建议的范围内,即0.81~1.78 mmol/L,可使用活性维生素D 冲击治疗甲状旁腺功能亢进症。维生素D制剂的主要不良反应是促进肠道钙磷的吸收,引起血钙、血磷的升高,因此用药过程中应监测血钙磷水平,及时调整药物治疗;同时应夜间睡眠服药,减少不良反应的发生。而碳酸镧不含钙,不增加胃肠道的钙负荷,即使加用活性维生素D也不会引起明显的血钙升高。对照组患者入组时为高磷血症,且大多数血钙水平维持在正常高值,血钙磷乘积均大于13.75 mmol/L,大多数患者降磷治疗只能依靠饮食控制及低钙透析,故治疗后血钙、血磷下降不明显,不符合使用活性维生素D治疗甲状旁腺功能亢进症的指征,故血PTH水平在观察前后无差异。
高磷血症是CKD尤其是ESRD患者的重要问题,发生率高,控制不理想。各种磷结合剂已成为治疗高磷血症的主要措施。含钙的磷结合剂是我国自20世纪80年代至今广泛使用的药物,易导致钙负荷增加,在部分患者中不宜使用。近10余年来,不含钙、铝的新型磷结合剂已在欧美等国广泛使用,大量循证医学证据证实其对于CKD-MBD治疗的有效性,且不良反应远低于传统磷结合剂。其中,碳酸镧在各种磷结合剂之中,显示出很好的前景:磷结合力高,且在整个消化道内均能发挥良好的降磷效果,不良反应较少、性价比及临床依从性好,是迄今为止较为理想的磷结合剂[15]。
1 张训. 慢性肾脏病继发性甲状旁腺功能亢进的新认识[J]. 中国中西医结合肾病杂志,2010,11(4):283-285.
2 Sprague SM, Evenepoel P, Curzi MP, et al. Simultaneous control of PTH and Ca P Is sustained over three years of treatment with cinacalcet HCI[J]. Clin J Am Soc Nephrol, 2009, 4(9):1465-1476.
3 Finn WF.Lanthanum carbonate versus standard therapy for the treatment of hyperphosphatemia:safety and efficacy in chronic maintenance hemodialysis patients[J].Clinical Nephrology,2006,65(3):191-202.
4 Kates DM, Andress DL.Control of hyperphosphatemia in renal failure: role of aluminum[J]. Semin Dial,1996, 9:301-315.
5 Nitsch D,Mylne A,Rodefiek PJ,et a1.Chronic kidney disease and hip fraetrue related mortality in older people in the UK[J].Nephrol Dial Transplant, 2009, 24(5):1539-1544.
6 Goodman WG, Goldin J, Kuizon BD, et a1. Coronary artery calcification in young adults with end-stage renal disease who are undergoing dialysis[J].N Engl J Med, 2000, 42(485):1478-1483.7 Covic A,Kanbay M,Voroneanu L,et a1.Vascular calcification in chronic kidney disease[J].Clin Sci, 2010, 119(3):111-121.
8 高玉春, 李孜, 唐晓红. 碳酸镧治疗维持性血液透析患者高磷血症有效性和安全性的系统评价[J]. 中国循证医学杂志, 2006, 6(10): 727-731.
9 National Institutes of Health, National Institute of Diabetes and Digestive and Kidney Disease. U.S. Renal Data System[J]. USRDS 2011 Annual Data Report: Atlas of Chronic Kidney Disease and End-Stage Renal Disease in the United States,2011[R/OL]. [2010-06-28].
10 Loeatelli F, D’Amico M, Pontoriero G. Lanthanum carbonate (Shire)[J].Drugs,2003,9(6):688-695.
11 Finn WF, Joy MS,Hladik G, et al. Efficacy and safety of lanthanum carbonate for reduction of serum phosphorus in patients with chronic renal failure receiving hemodialysis[J]. Clin Nephrol, 2004, 62(3):193-201.
12 AI-Baaj F, Speake M, Hutchison AJ. Control of serum phosphate by oral lanthanum carbonate in patients undergoing haemodialysis and continuous ambulatory peritoneal dialysis in a short-term, placebo-controlled study[J]. Nephrol Dial Transplant, 2005, 20(4):775-782.
13 Chlang SS, Chen JB, Yang WC. Lanthanum carbonate (Fosrenol) efficacy and tolerability in the treatment of hyperphosphatemic patients with end-stage renal disease[J]. Clin Nephrol. 2005, 63(6):461-470.
14 Takashi S.Multicenter prospective randomized,double blind comparative study between lanthanum carbonate and calcium carbonate as phosphate binders in Japanese hemodialysis patients with hyperphosphatemia[J]. Clin Nephrol, 2008, 70(6):401-410.
15 陈楠, 史浩. 慢性肾脏病高磷血症治疗: 新型磷结合剂碳酸镧研究进展[J].中华内科杂志,2012, 9(51): 742-744.
Lanthanumcarbonatetreatmentofmaintenancehemodialysispatientswithhyperphosphatemia
CHENXiaoxia,LUYuan,LOUJizhuang.
BloodPurificationCenter,NanjingHospitalAffiliatedtoNanjingMedicalUniversity/FirstHospitalofNanjingCity,Nanjing210029,China
LOUJizhuang,E-mail:dyyyxts200@126.com
ObjectiveTo evaluate the effectivenes of lanthanum carbonate for hyperphosphatemia in patients undergoing maintenance hemodialysis.MethodsAccording to whether taking lanthanum carbonate or not, patients were divided into observation group and control group. Lanthanum carbonate observation group of 16 cases, were treated with lanthanum carbonate, every time 500 mg, 2-3 times/d; 23 cases in the control group, oral calcium carbonate.0.75 g,twice aday.ResultsCompared with before treatment, treatment for 1, 2, 6 months later, the observation group serum phosphorus levels were decreased (P<0.01), the control group decreased not obviously (P>0.05), and the observation group serum phosphorus decreased significantly [(1.80±0.25 )mmol/L vs. (2.21±0.33) mmol/L, (1.56±0.19) mmol/L vs. (2.28±0.26) mmol/L, (1.51±0.17) mmol/L vs. (2.29±0.25) mmol/L](P<0.01) than those in the control group. The 2 groups of calcium decreased not significantly(P>0.05); after 6 months of treatment, compared with the control group, the observation group PPTH decreased more significantly [(614.80±178.38) pg/ml vs. (982.63±716.34) pg/ml] (P<0.05).ConclusionLanthanum carbonate treatment of maintenance hemodialysis patients with hyperphosphatemia is better than the traditional method is effective in the treatment of phosphorus reduction.
Hyperphosphatemia; Lanthanum carbonate;Hemodialysis,maintenance
210029 南京医科大学附属南京医院/南京市第一医院血液净化中心
楼季庄,E-mail: dyyyxts200@126.com
10.3969/j.issn.1671-6450.2014.06.018
2014-03-12)

