离子色谱法测定乳品中硫氰酸钠含量
陈基耘
(广东省珠海市质量计量监督检测所,广州珠海 519002)
离子色谱法测定乳品中硫氰酸钠含量
陈基耘
(广东省珠海市质量计量监督检测所,广州珠海 519002)
采用离子色谱法测定乳品中硫氰酸钠的含量。样品用5 mL乙腈沉淀蛋白质,上清液过C18柱净化,所得的产物采用离子色谱法测定,外标法定量。结果表明,通过流动相以及前处理方法的改进,硫氰酸钠质量浓度在0.10~4.00 mg/L范围内与色谱峰面积呈良好的线性,相关系数r2=1,方法的检出限为0.01 mg/L。在牛奶样品中加入硫氰酸钠标准溶液进行回收试验,测得回收率为95.0%~101.0%,测定结果的相对标准准偏差为1.8%~2.8%(n=7)。该方法操作简便,能有效避免假阳性的发生,测定结果准确,适合于乳品中硫氰酸钠的检测。
离子色谱;乳品;硫氰酸钠
在GB 2760-2007 《食品添加剂使用卫生标准》出台前,硫氰酸钠(Sodium Thiocyanat)一直被我国作为生鲜牛乳的保鲜剂,它在牛奶中的主要作用是抑菌,从而达到保鲜的目的。然而硫氰酸钠是一种具有毒性的化学物质,即使少量摄入也可能会对人体尤其是胎儿、婴儿的神经和智力发育产生危害[1]。随着我国在储运鲜乳技术方面的发展以及对食品安全方面工作力度的加大,保鲜技术逐步完善,因此GB 2760-2007中硫氰酸钠作为生鲜牛乳保鲜剂的内容已被删除。另外,2008年卫生部发布了《食品中可能违法添加的非食用物质和易滥用的食品添加剂名单(第一批)》,明确规定硫氰酸钠属于违法添加的非食用物质。2009年,卫生部发布《全国打击违法添加非食用物质和滥用食品添加剂专项整治抽检工作指导原则和方案的通知》(以下简称“通知”),其中推荐了牛奶中硫氰酸钠的检测方法,指定检验方法1:离子色谱法测定牛奶中硫氰酸根。
近年来,文献报道的乳品中硫氰酸钠的检测方法主要有分光光度法[2-3]、离子色谱法[4-5]以及液相色谱法[6],但到目前为止尚无标准方法。笔者在“通知”指定的检验方法1的基础上,改用AS19阴离子交换柱进行离子色谱分离,并调整了流动相比例,得到的色谱图可将复杂样品中的干扰离子更有效地分开。另外,针对用乙腈作为沉淀剂净化部分牛乳样品时出现蛋白质沉淀不完全的情况,采用了滴加少量乙酸溶液或冷藏试样溶液的方法进行改善,这样得到的试样溶液更澄清,更适合于离子色谱进样分析。通过比较方法调整前后的离子色谱图发现,方法改进后简便易行,检测结果准确可靠。
1 实验部分
1.1 主要仪器与试剂
离子色谱仪:ICS-1500型,配电导检测器,阴离子抑制器,KOH自动淋洗液系统,戴安中国有限公司;
分析天平:HA202M型,0.01 mg,日本A&D公司;
水相滤膜:0.22 µm,上海安谱科学仪器有限公司;
超声波仪:KJ-50型,无锡市科洁超声电子设备有限公司;
甲醇、乙腈、乙酸乙脂:色谱纯,广州化学试剂厂;冰乙酸:分析纯,广州化学试剂厂;
硫氰酸钠标准品:纯度不低于99.99%,美国Aldrich化学试剂公司;
乙酸溶液:体积分数1%,吸取冰乙酸1 mL,加水溶解,稀释至100 mL;
硫氰酸钠标准溶液:100 mg/L,准确称取硫氰酸钠标准品0.0100 g,用超纯水溶解并定容至100 mL;
实验用水为超纯水(电阻率为18.2 MΩ·cm)。
1.2 离子色谱条件
分析柱:AS19阴离子交换柱(4.0 mm×250 mm);保护柱:IonPac AS19柱(4.0 mm×50 mm);柱温:30℃;进样体积:25 µL;淋洗系统:KOH溶液自动淋洗,流速为1.0 mL/min;抑制器电流:200 mA;外标法定量;KOH溶液梯度程序1(“通知”中指定检测方法1中KOH溶液梯度程序):45 mmol/L (0~13 min)→70 mmol/L (13.1~18 min)→45 mmol/L (18.1~23 min);KOH溶液梯度程序2(本方法KOH溶液梯度程序):35 mmol/L (0~23 min)→70 mmol/L (23.1~32 min)→35 mmol/L(32.1~40 min)。
1.3 实验方法
计算机教学中多媒体电子教室教学软件应用尤为重要,对于学生更好的了解计算机知识学习概念具有一定的实际帮助,同时使学生计算机知识教学更为有效,提高学生总体知识学习效益。计算机教学的多媒体电子教室软件应用主体应用知识涵盖内容更为广泛,使学生计算机知识体系结构更为完善,帮助学生实现对计算机知识的合理化应用,提高学生计算机知识的实际操作能力,通过多媒体电子教室的软件应用,使教师的计算机知识教学不仅停留在理论知识方面,在综合实践方面也能够有效的发挥出良好的教学效益
1.3.1 硫氰酸钠的提取
称取4 mL液体乳品试样(固体乳粉试样称取1 g,加水稀释振摇均匀形成4 mL乳品试样),加入5 mL乙腈沉淀蛋白,过滤后取5 mL上清溶液置于50 mL容量瓶中,加水定容至刻度,得到样品溶液,备用。
1.3.2 硫氰酸钠的净化
将1.3.1中得到的样品溶液注入C18小柱(使用前用5 mL甲醇和10 mL水活化30 min),以小于3 mL/min的流速通过C18小柱,弃去前2 mL滤液,收集10 mL滤液,待测。
2 结果与讨论
2.1 蛋白质沉淀溶液的选择
牛奶样品不但成分复杂,其蛋白质和脂肪含量均较高,因此在硫氰酸钠的检测过程中,样品的净化是难点。试验比较了加入乙醇、丙酮、乙腈作为沉淀剂时对乳品试样的沉淀效果。结果表明,加入乙腈时沉淀效果较好。另外,部分牛乳样品在加入5 mL乙腈沉淀蛋白后得到的上清液还有轻微白色,置于4℃冰箱中冷藏1 h或者加入1 mL1%乙酸溶液后得到了更好的沉淀效果。加入1 mL 1%乙酸溶液前后的色谱图,分别见图1、图2。由图1、图2可知,乙酸的出峰时间靠前,少量乙酸的加入,不会影响硫氰酸根的出峰及计算。

图1 未加入乙酸溶液时的色谱图
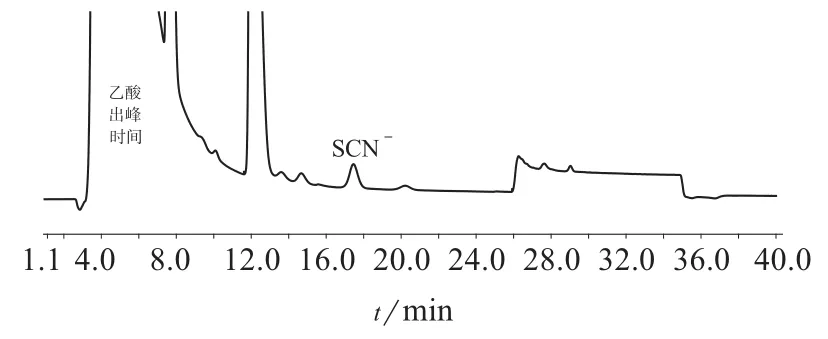
图2 加入乙酸溶液时的色谱图
2.2 淋洗液比例的选择
由实验可知,硫氰酸根在AS19柱中的保留时间较长,即出峰时间较晚。淋洗液中KOH浓度的选择,不仅要调高浓度使非测定离子在硫氰酸根出峰前迅速洗脱出来,又要控制浓度使硫氰酸根和其它离子的出峰时间有更长的时间差,避免其它离子的干扰。
按照1.2中洗脱程序1得到的图谱见图3,按照洗脱程序2得到的色谱图见图4。比较图3、图4可知,洗脱程序1由于洗脱浓度较高,有部分干扰离子和硫氰酸根一起洗脱出来,造成了检测结果的假阳性;程序2洗脱浓度合适,硫氰酸跟和干扰离子能很好分开。

图3 KOH浓度梯度洗脱程序1得到的色谱图

图4 KOH浓度梯度洗脱程序2得到的色谱图
2.3 标准曲线方程及检出限
用超纯水将硫氰酸钠逐级稀释成质量浓度为0.10,0.50,1.00,2.00,4.00 mg/L的系列标准工作溶液,依次进样分析。以色谱峰面积(y)为纵坐标,以硫氰酸根的质量浓度c(mg/L)为横坐标,绘制标准曲线,得线性回归方程为y=1.228 1c-0.005,线性相关系数r²=1,线性范围为0.10~4.00 mg/L。
向空白样品中添加硫氰酸钠标准溶液,根据仪器给出的信噪比参数,以3倍信噪比(S/N=3)确定方法的检出限,硫氰酸根的检出限为0.01 mg/L。
2.4 精密度及回收试验
在同一纯牛奶样品中加入硫氰酸钠标准溶液进行加标回收试验,加标浓度分别为0.20,0.50,2.00 mg/L,试验结果见表1。由表1可知,回收率在95.0%~101.0%之间,相对标准偏差为1.8%~2.8%。由此可见,该法的精密度和准确度较高,能有效地对牛乳中硫氰酸钠含量进行监督检测。
2.5 样品测定
采用所建方法对珠海市售的5款牛奶样品进行硫氰酸钠含量的检测,结果见表2。由表2可知,硫氰酸钠含量分布在3.5~6.2 mg/L之间。根据研究表明,牛奶中硫氰酸钠的浓度要达到15 mg/kg才能有效杀菌[7]。表2中检测数据均明显小于该值,所以可以排除人为添加的可能。由于硫氰酸盐广泛存在于动物组织和分泌物中(如乳腺、肾脏等),因此所测得的微量硫氰酸钠,可能是在自然条件下存在的结果[7]。

表1 回收试验结果(n=7)

表2 牛乳样品中硫氰酸钠含量测定结果
3 结语
利用离子色谱法对硫氰酸钠进行检测,通过样品前处理方法的改善,降低了复杂样品中其它离子对待测离子的干扰,从而降低了硫氰酸钠检测中假阳性情况的发生,可以有效地对牛乳中硫氰酸钠含量进行监督检测。
[1]顾欣,黄士新,李丹妮,等.乳中硫氰酸盐对人类健康的风险评估[J].中国兽药杂志,2010,44(9): 45-49.
[2]苏婷婷,续莺,顾洪涛.乳制品中硫氰酸钠含量的测定——分光光度法[J].中国乳业,2013,134(2): 48-49.
[3]张遴,王文瑞,蔡砚,等.分光光度法测定婴幼儿食品中硫氰酸钠[J].理化检验:化学分册,2013,49(6): 717-719.
[4]杨一刚.离子色谱测定乳制品中硫氰酸钠含量[J].食品工程,2012,123(2): 55-57.
[5]李滢倩,王潇,王岩,等.离子色谱法测定液体乳中硫氰酸根[J].轻工科技,2014,182(1): 3-4.
[6]董云香.牛奶中硫氰酸钠的检测方法研究[J].轻工科技,2012,160(3): 9-21.
[7]李晰晖,赵越,任国谱.原料乳中硫氰酸钠质量分数的调查与分析[J].食品工业,2013,34(11): 248-251.
Determination of Sodium Thiocyanate Content in Milk by Ion Chromatography
Chen Jiyun
(Guangdong Zhuhai Supervision Testing Institute of Quality and Metrology, Zhuhai 519002, China)
Ion chromatography was applied to the determination of sodium thiocyanate content in milk. The sample was purified by protein precipitation and the C18extraction column. Then the product was tested by ion chromatography and the concentration was quantified by external standard method. Through the improment of mobile phase and pretreatment method,the concentration of sodium thiocyanate was linear with peak area in the range of 0.10-4.00 mg/L, and the correlation coefficient was r2=1. The detection limit determination of the method was 0.01 mg/L. Test recovery experiment was made by standard addition method,and the recovery was 95.0%-101.0%. The relative standard deviation of the determination results was 1.8%-2.8% (n=7). This method has the advantages of simple operation, it can effectively avoid the occurrence of false positive so it is suitable for detection of sodium thiocyanate in milk.
ion chromatography; milk; sodium thiocyanat
O657.3
A
1008-6145(2014)04-0042-03
10.3969/j.issn.1008-6145.2014.04.012
联系人:陈基耘;E-mail: jacquichen@126.com
2014-04-29

