重度肥胖合并2型糖尿病胃旁路术后低血糖营养干预1例
钮丹叶,刘燕萍,朱慧娟
中国医学科学院 北京协和医学院 北京协和医院 1营养科 2内分泌科, 北京 100730
·病例报告·
重度肥胖合并2型糖尿病胃旁路术后低血糖营养干预1例
钮丹叶1,刘燕萍1,朱慧娟2
中国医学科学院 北京协和医学院 北京协和医院1营养科2内分泌科, 北京 100730
低血糖; 重度肥胖; 胃旁路手术; 营养干预
近年来,重度肥胖合并糖尿病的外科治疗在我国发展迅速,腹腔镜胃旁路手术(laparoscopic Roux-en-Y gastric bypass,LRYGB)被认为是临床疗效最肯定的术式。然而,由于重度肥胖合并2型糖尿病患者存在糖、脂代谢异常,胃旁路手术后易出现与其相关的并发症,低血糖是其中较难处理的一种并发症,发生机制复杂多样,既与幽门缺如、胃肠短路后排空过快有关,也与患者高胰岛素血症或异常的胃肠激素-胰岛素反馈机制有关。营养干预是LRYGB术后低血糖干预的首要与基础步骤。本文报告1例重度肥胖合并2型糖尿病LRYGB术后频发低血糖患者的营养干预策略。
临床资料
病例摘要
患者男,27岁,自幼肥胖,22岁诊为“2型糖尿病”,予不规则降糖治疗,25岁(2011年11月)因肥胖行LRYGB手术,术后2个月内体重由135 kg下降至96 kg。术后3个月开始患者在空腹、夜间或餐后1~3 h反复发作心慌、手抖、出汗、头晕症状,有饥饿感,症状发作时静脉血糖2.1 mmol/L,进食后上述症状缓解,进食碳水化合物较蛋白质更易诱发餐后低血糖反应。曾先后行伏格列波糖、阿卡波糖、生长抑素类似物(奥曲肽)、二甲双胍+吡格列酮治疗,发作次数有所减少。频发低血糖以来,患者进食次数及食量较术后早期明显增加,体重反弹。术后1.5年因“发作性心慌、手抖、出汗、头晕1年”于2013年5月3日入住北京协和医院内分泌科诊治。
查体:身高178 cm,体重113 kg,体重指数35.7 kg/m2,腰围124 cm,腹型肥胖,颈部、腋窝可见黑棘皮。
实验室检查:口服葡萄糖耐量试验及胰岛素检查示2 h血糖低,服糖后胰岛素异常升高(表1);动态血糖监测(连续67.5 h):空腹血糖平均3.9 mmol/L,早餐后2 h平均血糖5.6 mmol/L,午餐后2 h平均血糖4.9 mmol/L,晚餐后2 h平均血糖5.3 mmol/L;空腹最低血糖2.7 mmol/L,餐后最低血糖约3 mmol/L。C肽(空腹)0.1 nmol/L(3.0 ng/ml)。
腹部增强CT:胰腺未见明确占位病变。
营养干预
入院后予以经典倾倒综合征饮食,即低碳水化合物、低血糖生成指数、低脂糖尿病饮食5020.8 kJ/d(1200 kcal/d)。一日三餐,早餐主食50 g、鸡蛋60 g;午、晚餐为混合膳食,主食35 g,绿叶蔬菜200 g,瘦肉50 g;干稀分食,即在餐前及餐后0.5~1 h内不用液体;细嚼慢咽;进餐时采用半卧位,餐后平卧20~30 min;除发生低血糖外禁用高血糖生成指数食物。同时继续予二甲双胍0.5 g随餐口服以改善血糖与胰岛素抵抗。患者遵医嘱执行后仍有明显饥饿感。3 d内低血糖发作4次,主要出现在早餐后、午餐前及睡前,血糖峰值为6.7 mmol/L,血糖谷值为3.1 mmol/L。遂在餐前添加膳食纤维7 g(其中含燕麦β-葡聚糖粉3 g),应用3 d内低血糖发作1次,餐后2 h血糖最高为5.9 mmol/L,最低为3.8 mmol/L(表2)。

表 1 口服葡萄糖耐量试验及胰岛素检查结果(术后10个月)
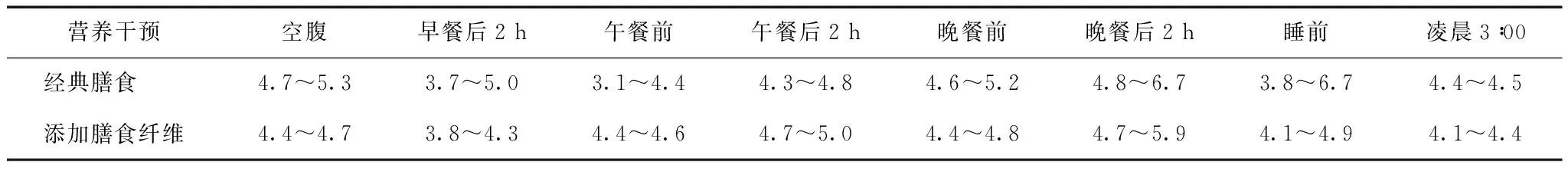
表 2 经典膳食与添加膳食纤维后患者血糖水平(mmol/L)
应用可溶性膳食纤维后,患者午餐前、晚餐前及夜间血糖趋于平稳,饱腹感明显而饥饿感基本消失,可耐受低能量饮食。2个月后随访患者进食规律,一日三餐,餐前服用膳食纤维,体重下降3 kg,无低血糖发生,无明显不良反应。
讨 论
术后低血糖是LRYGB后发生率较少,但较难处理的并发症之一,究其成因,与胃肠道生理结构改变有直接关系,也与患者糖代谢状况及胰岛功能变化有密切关系,临床上常将其归诊为倾倒综合征(dumping syndrome)[1]。
术后低血糖病因诊断
在LRYGB后出现低血糖,并伴有消化道或血管舒张反应症状,不能除外倾倒综合征。根据临床症状出现距离进餐时间的早晚,倾倒综合征分早期和晚期,前者可见腹胀、腹痛、恶心等消化道不适,以及心悸、出汗、血压下降、面色潮红等血管舒缩症状,一般发生在进餐后0.5 h内;晚期主要表现为低血糖,常发生于进餐后1~3 h[2- 4]。有学者认为激惹诊断试验有助于区分早期或晚期倾倒综合征,即在禁食12 h后测定血糖、心率、血压、红细胞压积,进行口服葡萄糖耐量试验(饮用75 g无水葡萄糖),测定30 min、1 h、2 h、3 h血糖、心率、血压、红细胞压积,如30 min时红细胞压积较前升高≥3%或1 h时心率增加>10次/min,诊断为早期倾倒综合征;如2 h血糖<2.5 mmol/L,则诊断为晚期倾倒综合征[1]。区别倾倒综合征的分期有助于明确病因,采取有针对性的营养干预。不伴有消化道及血管舒缩症状的术后低血糖,如C肽<0.6 ng/ml应考虑与药物使用有关,C肽>0.6 ng/ml则应进一步检测胰岛素原水平;如胰岛素原>5 pmol/L,考虑为胰岛素瘤,如胰岛素原<5 pmol/L则考虑为胰岛细胞增殖症[1]。
本例患者有LRYGB手术史,起病初期出现心悸、出汗、头晕等血管舒缩症状,发病时血糖低于2.5 mmol/L,口服葡萄糖耐量试验提示,服糖后2 h血糖为2.3 mmol/L,故可确立晚期倾倒综合征诊断。值得注意的是,该患者亦常表现为无症状性低血糖,结合其空腹C肽0.1 nmol/L(3.0 ng/ml),虽腹部CT未见胰腺占位,但不能除外胰岛素瘤或胰岛细胞增殖症可能,应进一步行胰岛素原等检查。
倾倒综合征发病机制与营养干预
目前认为,晚期倾倒综合征的病理生理学机制是胃切除术后胃容积减少、幽门缺如及胃空肠吻合术后十二指肠反馈性抑制胃排空功能丧失等导致胃排空加速,使食物中碳水化合物快速进入小肠,引起胰高血糖素样肽- 1等胃肠激素水平升高,刺激胰岛素过度分泌,从而引起反应性低血糖。此外,LRYGB后患者出现餐后低血糖,可能与胰岛细胞增生、胰岛功能亢进、胰岛细胞增殖症有关[2- 5]。也有学者认为,倾倒综合征和胰岛细胞增殖症可能是胃旁路手术后同一病理生理异常的不同阶段。结合本例患者为LRYGB后,胃容积缩减,口服葡萄糖耐量试验显示基础胰岛素水平正常,服糖后胰岛素水平迅速升高,CT检查未见胰腺占位,考虑其发病机制主要与胃排空过快导致胰岛素分泌迅速增加有关。该患者术前即诊断为2型糖尿病,其病理生理基础为肥胖所致高胰岛素血症及胰岛素抵抗。低血糖症状出现在术后2个月体重快速减轻后,考虑与胰岛素抵抗缓解,胰岛素敏感性增强有关。如能限制进食后胃排空及碳水化合物的快速入肠与吸收入血,可延缓或避免出现胰岛细胞增殖与难治性低血糖。
晚期倾倒综合征所致低血糖的治疗首先应考虑饮食调整,其次可给予α-糖苷酶抑制剂、生长抑素类似物等药物治疗,难治患者还可考虑再次手术和持续性肠道喂养等治疗。在各种治疗方法中,饮食治疗是基础[2,6]。
本例患者入院后按照倾倒综合征经典饮食干预方法严格执行后仍有饥饿感,低血糖症状无明显改善,且以早餐后及午餐前低血糖更为明显。究其原因,考虑如下:(1)早餐主要为馒头+鸡蛋,相较午晚餐混合膳食,血糖指数与血糖负荷更高,更容易引起胰岛素反应性升高,从而引起低血糖;(2)患者LRYGB后,幽门丧失,虽予半卧位进食,餐后平躺等措施,但仍存在胃排空过快。三餐前加用含燕麦β-葡聚糖膳食纤维后症状得到改善,体重减轻,这是由于可溶性膳食纤维可增加食物黏稠度,减缓食物中单糖类成分的排空速度,从而阻止了肠腔内渗透压的迅速升高[2, 7- 8];同时高膳食纤维饮食具有低血糖指数、饱腹感强等特点,因此既有助于预防早期倾倒综合征,亦有助于帮助预防以低血糖为主要特征的晚期倾倒综合征,并能起到限制食欲的作用。
以LRYGB为代表的减重暨糖尿病手术治疗正在蓬勃开展,术前评估患者的胰岛功能,术后及早采取预防倾倒综合征饮食管理措施,采用低能量、低碳水化合物、低血糖指数膳食,并提高可溶性膳食纤维用量,有效控制食物排空,方有助于患者术后长期坚持限能量饮食,预防胰岛细胞增殖等并发症,实现减重的目标。
[1]Ceppa EP, Ceppa DP, Omotosho PA, et al. Algorithm to diagnose etiology of hypoglycemia after Roux-en-Y gastric bypass for morbid obesity: case series and review of the literature[J]. Surg Obes Relat Dis, 2012, 8: 641- 647.
[2]Tack J,Arts J, Caenepeel P, et al. Pathophysiology, diagnosis and management of postoperative dumping syndrome[J]. Nat Rev Gastroenterol Hepatol, 2009, 6: 583- 590.
[3]Stefater MA, Kohli R, Inge TH. Advances in the surgical treatment of morbid obesity[J]. Mol Aspects Med, 2013, 34: 84- 94.
[4]Ritz P, Hanaire H. Post-bypass hypoglycaemia: a review of current findings[J]. Diabetes Metab, 2011, 37: 274- 281.
[5]Hammer HF. Medical complications of bariatric surgery: focus on malabsorption and dumping syndrome[J]. Dig Dis, 2012, 30:182- 186.
[6]刘兴振, 邹大进.胃肠减肥术围手术期管理要点[J].中国实用内科, 2012,32:754- 756.
[7]Harju E, Heikkila J, Larmi TK. Effect of guar gum on gastric emptying after gastric resection[J]. JPEN J Parenter Enteral Nutr, 1984, 8: 18- 20.
[8]Aleixandre A, Miguel M. Dietary fiber in the prevention and treatment of metabolic syndrome: a review[J]. Crit Rev Food Sci Nutr, 2008,48:905- 912.
刘燕萍 电话:010-69159081,E-mail:liuyp1227@vip.sina.com
R459.3;R587.1;R619
B
1674-9081(2014)04-0472-03
10.3969/j.issn.1674-9081.2014.04.025
2013- 11- 15)

