乙内酰脲类化合物药理作用研究进展
颜翔鹏,梁庆模
·综述·
乙内酰脲类化合物药理作用研究进展
颜翔鹏,梁庆模*
乙内酰脲类化合物是一类包含多种取代基团的五元杂环类化合物。可天然提取和人工合成,由于取代基团种类繁多且有较大的反应活性,使得乙内酰脲类化合物及其衍生物具有多种药理学作用,在医药卫生、渔业、化工业等领域有着广泛的应用价值。本文就乙内酰脲类化合物的药理作用进行综述。
乙内酰脲;药理作用;抑制剂;化合物
0 引言
乙内酰脲(Hydantoin)又名海因,妥因,化学名称为2,4-咪唑啉二酮,其结构通式如图1所示,其中R1、R2可为多种烯基、烷基、芳基;R3、R4为羟烷基、氰烷基、缩水甘油基、胺烷基等。1861年Baeyer用尿酸降解物尿囊素通过加氢首次获得乙内酰脲,虽然乙内酰脲制备方法已经问世150余年,但真正对此物进行深入研究还是20世纪60年代之后。目前,乙内酰脲及其化合物可从中药独角莲、蛤蟆油、某些海洋生物及菌类等物质中进行生物提取[1-3],也可以根据结构式使用多种方法进行人工合成。由于乙内酰脲的取代部位和取代基团各异,且取代的基团又各具生物活性,基团与基团之间相互作用,导致乙内酰脲类化合物具有多种药理作用。乙内酰脲结构通式见图1。
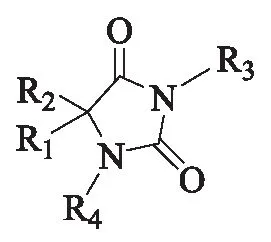
图1 乙内酰脲结构通式
乙内酰脲类化合物药理作用广泛,涉及到神经肌肉系统、呼吸系统、心血管系统、免疫系统、内分泌等系统,具有抗痉挛、抗菌消炎、止咳平喘、降低血糖、抗心律失常、抗肿瘤等药理作用,在治疗炎症、类风湿性关节炎等自身免疫性系统性疾病、慢性阻塞性肺疾病、糖尿病、高血压、肿瘤、惊厥、癫疒间症等疾病方面,乙内酰脲类化合物都有很好的应用前景和研究价值。目前,除卤代乙内酰脲类化合物广泛应用于消毒杀菌和苯基乙内酰脲类化合物用于抗惊厥和心律失常外,大部分乙内酰脲类化合物的药理作用还处于研究阶段。以下将乙内酰脲类化合物的药理作用进行分述。
1 乙内酰脲类化合物抗惊厥、抗心律失常作用
苯妥英钠,化学名5,5-二苯基-2,4-咪唑烷二酮钠盐,又名二苯乙内酰脲,是乙内酰脲化合物的一种,作为控制癫疒间大发作的首选药物,广泛应用于临床,其作用机制可能与增加细胞钠离子外流,减少钠离子内流,而使神经细胞膜稳定,提高兴奋阈,减少病灶高频放电的扩散有关[4]。还有其衍生物美芬妥因、美替妥英、乙苯妥英、磷苯妥英等都是被熟知的抗惊厥药物。除了已经应用于临床的这些药物之外,还有许多种乙内酰脲类化合物正处于研究状态,在利用最大电休克发作(Maximal electroshock seizure MES)试验和皮下戊四唑(Subcutaneous pentylenetetrazole scPTZ)试验评估乙内酰脲类化合物抗惊厥活性的动物实验中,发现五号位取代的环丙基乙内酰脲化合物能更好地保护MES试验,与苯妥英钠相比,5b、5d、5e、5g、5j的效果更突出;在scPTZ试验中,5j与标准药物丙戊酸钠在20 mg/kg和40 mg/kg剂量时,具有均等的药效[5]。其他的5-取代乙内酰脲化合物,如5,5-联吡啶乙内酰脲、硫乙内酰脲等也具有抗惊厥作用[6]。
同时,苯妥英钠通过缩短动作电位间期及有效不应期,还可抑制钙离子内流,降低心肌自律性,抑制交感中枢,对心房、心室的异位节律点有抑制作用,提高房颤与室颤阈值,起到抗心律失常的作用。熟知的阿奇利特就是乙内酰脲化合物中的一种。在二苯基乙内酰脲衍生物的体内实验中发现,含有二甲氧基苯基哌嗪的水溶性乙内酰脲化合物(11a,19a)在肾上腺素导致的心律不齐模型中具有强效的抗心律不齐作用,另一种乙内酰脲类化合物(9a)在氯化氮所致的心律失常模型中具有最高效的拮抗作用[7]。
2 乙内酰脲类化合物抗病原微生物作用
细菌的多药耐药性(Multidrug resistance MDR) 是药物治疗细菌感染失败的重要原因,其主要机制是细菌通过药物输出泵排出药物,使药物不能进入病原体,不能发挥作用。研究显示,乙内酰脲类化合物通过抑制细菌的药物输出泵系统从而发挥抗菌作用[8-10]。Dymek等[8]的研究中,用16种新型乙内酰脲化合物和苯唑西林钠作用于ATTC 25923型金黄色葡萄球菌和HPV-107型金黄色葡萄球菌属,通过减少或者抑制金黄色葡萄球菌对苯唑西林钠的抵抗情况来评估这些乙内酰脲类化合物的抗菌能力,结果显示,乙内酰脲化合物PI8a 明显地降低了苯唑西林钠对HPV-107型金黄色葡萄球菌属的最低抑菌浓度,对金葡菌感染有强力的疗效。这和Handzlik等[9]应用萘啶酸抗肠杆菌 ATCC-13048 型及 CM-64 型的研究一致,都是通过降低了药物的最低抑菌浓度达到抗菌效果。Machado等[10]的研究中用荧光测定法检测细胞内溴化乙锭的积聚,来检测23种乙内酰脲化合物对肠炎沙门氏菌血清型NCTC 13349 的抑菌效果,结果显示,乙内酰脲化合物SZ7是一种无毒且能有效治疗肠炎沙门氏菌血清型NCTC 13349感染物质。1,3-二溴-5,5-二甲基乙内酰脲是一类新型广谱消毒杀菌剂,通过在水中能形成次溴酸,进而释放出活化溴,与含氮的物质作用生成溴化胺,从而杀灭病原体,可以杀灭嗜肺军团菌、金黄色葡萄球菌、大肠菌杆菌、枯草杆菌黑色变种芽孢等多种细菌芽胞及繁殖体,特别是对嗜肺军团菌的作用最强[11-12]。脂质A是细菌脂多糖的重要组成部分,脂质A合成的核心酶是脱乙酰基酶,乙内酰脲衍生物能抑制脱乙酰基酶的活性,从而达到抗菌作用[13]。Rajic等[13-14]在对3,5-双取代基乙内酰脲衍生物5a-h的研究中发现,5a-h对牛痘病毒有选择性抑制效果。有研究显示,一些乙内酰脲类化合物对人类免疫缺陷病毒(HIV)、单纯疱疹病毒1、2型(HSV-1、HSV-2)均有抗病毒效果[15-16]。
3 乙内酰脲类化合物抗肿瘤作用
乙内酰脲类化合物通过多种机制发挥抗肿瘤作用。在对非小细胞肺癌A549型细胞的研究中发现,5-苯亚甲基-乙内酰脲化合物UPR1024能够抑制表皮生长因子受体(Epidermal growth factor receptor)络氨酸激酶的活性,使细胞积聚在细胞周期的S期,还能导致DNA损伤、DNA突变,同时还能增强p53、p21蛋白表达,从而发挥抗肿瘤作用[17]。Shah等[18]在对前列腺癌-3M细胞的研究中发现,苯基-亚甲基-乙内酰脲化合物(Phenyl-methylene hydantoin,PMH)能够通过增加细胞与细胞之间的粘附作用,抑制降钙素对交联化合物的降解,明显降低前列腺原位癌的生长,并且能抑制在裸鼠远处器官形成微小转移,对自发肿瘤也有抑制生长的作用。另有研究显示,PMH通过抑制CD44表达,从而达到抗前列腺癌的作用[19]。多药耐药性也是肿瘤药物治疗失败的重要原因,通过增加表达ATP依赖的药物输出泵,最主要的是ABC药物转运P-糖蛋白,也就是ABCB1,从而减少抗肿瘤药物在细胞内的聚集[20]。在对淋巴瘤细胞、结肠癌细胞等的多项研究中显示,乙内酰脲通过抑制药物输出泵系统特别是抑制ABCB1,减少有效药物被排出,协同其他抗肿瘤药物发挥抗肿瘤作用[21-23]。乙内酰脲化合物还通过细胞毒作用发挥抗肿瘤作用,Kavitha等[24]的研究中发现,乙内酰脲化合物DFH、DCH的细胞毒作用在人白血病细胞中具有时间和剂量依赖性,并能抑制DNA复制,使细胞处于G1期,促使白血病细胞凋亡。乙内酰脲类化合物还具有抗宫颈癌、乳腺癌、胰腺癌等肿瘤的作用[13]。
4 乙内酰脲类化合物治疗慢性阻塞性肺疾病、止咳作用
金属蛋白酶12(Matrix metalloproteinases12,MMP12)优先表达与活化的巨噬细胞,可由吸烟者的巨噬细胞产生,在用香烟导致慢性阻塞性肺疾病(Chronic obstructive pulmonary diseases,COPD)的大鼠模型中,野生型的大鼠发生了肺气肿,而MMP12基因被敲除的大鼠没有发生肺气肿,表明MMP12是COPD发病的重要酶。金属蛋白酶9参与多种生理和病理过程,也参与多种炎症反应,能够促进炎症细胞从脉管向组织迁移。乙内酰脲类化合物及其衍生物能够有效抑制MMP12和MMP9等多种金属蛋白酶的活性,对治疗COPD具有重要作用,且对哮喘也有疗效[25]。在运用1-甲基乙内酰脲类化合物检测其止咳效能的动物实验中发现,7a、7c和7d 三种化合物的止咳性能优于可待因[26]。
5 乙内酰脲类化合物抑制黑色素形成作用
酪氨酸酶是黑色素生成的核心酶,它能催化酪氨酸生成黑色素,许多皮肤病就是由于黑色素生成异常造成。在运用1H 和13C 标记的核磁共振和光谱分析中发现,5-苯亚甲基乙内酰脲类化合物2e在B16细胞中能抑制酪氨酸酶的活性,从而抑制黑色素的生成,对治疗色素沉着有很好效果[27]。
6 乙内酰脲类化合物抗炎作用
肿瘤坏死因子-a(Tumor necrosis factor-a,TNF-a)是人体内的一种重要的细胞因子,在炎症、发热、急性反应等过程中起重要作用,但是过量的TNF-a却有致死的作用。肿瘤坏死因子转化酶(TNF-a converting enzyme,TACE),能促进TNF-a的释放,对炎症的发生产生重要影响。乙内酰脲衍生物能够抑制TACE的活性,从而抑制TNF-a的产生,能改善内风湿性关节炎、非胰岛素依赖的糖尿病及克罗恩病病人的症状[28]。前列腺素(Prostaglandins,PG)在炎症的发生过程中扮演主要角色,许多非甾体抗炎药都是通过抑制环氧化物酶(cyclooxygenase,COX)的活性减少PG的产生而达到抗炎效果。乙内酰脲衍生物能够高效、高选择性抑制COX-2,抑制炎症的发展[29]。在1-甲基乙内酰脲衍生物7a的实验中对比发现其抗炎效果是布洛芬的2倍[26]。
7 乙内酰脲类化合物其他药理作用
环磷酸腺苷(cyclic adenosine 3′,5′-monophosphate,cAMP)和环磷酸鸟苷(cyclic guano 3′,5′-monophosphate,cGMP)是体内重要的第二信使,是细胞内信号传导的重要物质,磷酸二酯酶(phosphodiesterases,PDEs)能够水解cAMP及cGMP,降低信号传导,致使疾病发生。乙内酰脲衍生物能够抑制PDE5,发挥广泛的药理学作用。在海绵体组织能治疗男性性功能不全,在脉管系统中可以用于治疗高血压疾病,还能促进肿瘤细胞凋亡[30]。乙内酰脲类化合物作为金属蛋白酶抑制剂,能抑制多种金属蛋白酶的活性,对多种疾病都有疗效。如各种炎症性和变态反应性疾病(关节炎、胃肠炎、皮肤炎、角膜溃疡等),各种组织损伤的修复,慢性肾病,阿尔兹海默病,动脉粥样硬化狭窄,鼻炎等疾病[25]。 乙内酰脲类化合物及其衍生物具有广泛的药理作用,基本涉及了人体的各个系统、器官、组织,其抗惊厥和心律失常的作用已经在临床广泛使用。同时,乙内酰脲类化合物及其衍生物可用于预防和治疗人类多种疾病,也为人类战胜疾病提供了新的药物选择。在治疗肿瘤、感染性疾病、慢性阻塞性肺疾病、糖尿病、慢性肾病、肾功能不全、尿毒症、类风湿性关节炎等免疫性疾病方面都有很好的应用前景,故乙内酰脲类化合物及其衍生物具有广阔的市场前景。
[1] Mudit M,Khanfar M,Muralidharan A,et al.Discovery,design,and synthesis of anti-metastatic lead phenylmethylene hydantoins inspired by marine natural products[J].Bioorganic & Medicinal Chemistry,2009,17(4):1731-1738.
[2] Chen Guangying,Lin Yongcheng,Wen Lu,et al.Two new metabolites of a marine endophytic fungus (No.1893)from an estuarine mangrove on the South China Sea coast[J].Tetrahedron,2003,59(26):4907-4909.
[3] 陈光英,朱峰,林永成,等.南海红树内生真菌1947号次级代谢产物的研究[J].化学研究与应用,2007,19(1):98-99.
[5] Zhu Q,Pan Y,Xu Z,et al.Synthesis and potential anticonvulsant activity of new N-3-substituted 5,5-cyclopropanespirohydantoins[J].European Journal of Medicinal Chemistry,2009,44(1):296-302.
[6] Malawska B.New anticonvulsant agentst[J].Current Topics in Medicinal Chemistry,2005,5(1):69-85.
[7] Zygmunt M,Handzlik J,Bednarski M,et al.Synthesis and evaluation of in vivo activity of diphenylhydantoin basic derivatives[J].European Journal of Medicinal Chemistry,2004, 39(12):1013-1027.
[8] Dymek A,Armada A,Handzlik J,et al.The activity of 16 new hydantoin compounds on the intrinsic and overexpressed efflux pump system of Staphylococcus aureus[J].In Vivo,2012,26(2):223-229.
[9] Handzlik J,Szyma E,Chevalier J,et al.Amine-alkyl derivatives of hydantoin:New tool to combat resistant bacteria[J].Eur J Med Chen,2011,46(12):5807-5816.
[10]Machado L,Spengler G,Evaristo M,et al.Biological activity of twenty-three hydantoin derivatives on intrinsic efflux pump system of Salmonella enterica serovar Enteritidis NCTC 13349[J].In Vivo,2011,25(5):769-772.
[11]陈春田,张顺合,常琳.二溴海因消杀片消毒相关性能的实验观察[J].中国消毒学杂志, 2010,27(1):38-40.
[12]陈越英,吴晓,松孙俊,等.二溴海因对嗜肺军团菌杀灭效果及其影响因素的实验研究[J].中国消毒学杂志,2009,26(2):121-123.
[13]Rajic Z,Zorc B,Raic-Malic S,et al.Hydantoin derivatives of L-and D-amino acids:synthesis and evaluation of their antiviral and antitumoral activity [J].Molecules,2006,11(11):837-848.
[14]Mansoor UF,Reddy PAP,Siddiqui MA,et al.Hydantoin derivatives useful as antibacterial agents:US,7998961B2[P].2011-08-16.
[15]Khodair AI,El-Subbagh HI,El-Emam AA,et al.Synthesis of certain 5-substituted 2-thiohydantoin derivatives as potential cytotoxic and antiviral agents[J].Boll Chim Farm,1997,136(8):561-567.
[16]El-Barbary AA,Khodair AI,Pedersen EB,et al.S-Glucosylated hydantoins as new antiviral agents[J].Medicinal Chemistry,1994,37(1):73-77.
[17]Cavazzoni A,Alfieri RR,Carmi C,et al.Dual mechanisms of action of the 5-benzylidene-hydantoin UPR1024 on lung cancer cell lines[J].Molecular Cancer Therapeutics,2008,7(2):361-370.
[18]Shah GV,Muralidharan A,Thomas S,et al.Identification of a small molecule class to enhance cell-cell adhesion and attenuate prostate tumor growth and metastasis[J].Molecular Cancer Therapeutics,2009,8(3):509-520.
[19]Yang K,Tang Y,Iczkowski KA.Phenyl-methylene hydantoins alter CD44-specific ligand binding of benign and malignant prostate cells and suppress CD44 isoform expression[J].Am J Transl Res,2010,2(1):88-94.
[20]Lee CA,Cook JA,Reyner EL,et al.P-glycoprotein related drug interactions:clinical importance and a consideration of disease states[J].Expert Opinion Drug Metabolism & Toxicology,2010,6(5):603-619.
[21]Spengler G,Evaristo M,Handzlik J,et al.Biological activity of hydantoin derivatives on P-Glycoprotein (ABCB1) of mouse lymphoma cells[J].Anticancer Res,2010,30(12):4867-4871.
[22]Martins A,Dymek A,Handzlik J,et al.Activity of fourteen new hydantoin compounds on the human ABCB1 Efflux Pump[J].In Vivo,2012,26(2):293-297.
[23]Spengler G,Handzlik J,Ocsovszki I,et al.Modulation of multidrug efflux pump activity by new hydantoin derivatives on colon adenocarcinoma cells without inducing apoptosis[J].Anticancer Research,2011,31(10):3285-3288.
[24]Kavitha CV,Nambiar M,Ananda Kumar CS,et al.Novel derivatives of spirohydantoin induce growth inhibition followed by apoptosis in leukemia cells[J].Biochemical Pharmacology,2009,77(3):348-363.
[25]Gabos B,Ripa L,Stenvall K,et al.Hydantoin derivatives for the treatment of obstructive airway diseases:US,7989620B2[P].2011-08-02.
[26]Lu H,Kong D,Wu B,et al.Synthesis and evaluation of anti-inflammatory and antitussive activity of hydantoin derivatives[J].Letters in Drug Design & Discovery,2012,9(6):638-642.
[27]Ha YM,Kim JA,Park YJ,et al.Analogs of 5-(substituted benzylidene)hydantoin as inhibitors of tyrosinase and melanin formation[J].Biochimica et Biophysica Acta General Subjects,2011,1810(6):612-619.
[28]Sheppeck JE,Duan J,Xue CB,et al.Hydantoins and related heterocycles as Inhibitors of matrix metalloproteinases and/or TNF-a converting enzyme(TACE):US,7482372B2[P].2009-01-27.
[29]Zarghi A,Javid FS,Ghodsi R,et al.Design,synthesis and biological evaluation of new 5,5-diarylhydantoin derivatives as selective cyclooxygenase-2 inhibitors[J].Scientia Pharmaceutica,2011,79(3):449-460.
[30]Abadi AH,Lehmann J,Piazza GA,et al.Synthesis,molecular modeling,and biological evaluation of novel tetrahydro-β-carboline hydantoin and tetrahydro-β-carboline thiohydantoin derivatives as phosphodiesterase 5 inhibitors[J].International Journal of Medicinal Chemistry,2011,32(3):461-470.
Research advance of hydantoin compounds pharmacological
YAN Xiang-peng,LIANG Qing-mo*
(The Affiliated Nanhua Hospital of University of South China,Hengyang 421001,China)
Hydantoin compounds are a kind of heterocyclic compounds which contain a variety of replacing groups.They can be extracted from natural and synthetic.Because of containing so many types of replacing groups and large reactivities,hydantoin compounds and its derivatives have many kinds of pharmacological effects and a broad application value in medicine and health care,fisheries,industrial and other fields.This article will expound pharmacological of hydantoin compounds.
Hydantoin compounds;Pharmacological;Inhibitor;Compounds
2013-11-07
南华大学附属南华医院,湖南 衡阳 421001
湖南省自然科学省市联合基金(No.12JJ9030)
*通信作者

