纳洛酮用于弥漫性轴索损伤患者的有效性和安全性的系统评价
李文涛,张斌飞,宋锦宁,马旭东,刘尊伟,顾 华
(西安交通大学医学院第一附属医院神经外科,陕西西安 710061)
◇专题研究◇
纳洛酮用于弥漫性轴索损伤患者的有效性和安全性的系统评价
李文涛,张斌飞,宋锦宁,马旭东,刘尊伟,顾 华
(西安交通大学医学院第一附属医院神经外科,陕西西安 710061)
目的 纳洛酮用于弥漫性轴索损伤(DAI)的疗效仍存在疑虑,本研究通过meta分析评价其有效性和安全性。方法 计算机检索各数据库,筛选纳洛酮与对照组比较治疗DAI的随机对照研究(RCT)。由研究者独立评价纳入研究的方法学并提取研究数据,采用STATA 12.0软件进行统计分析。结果 共纳入12个低质量RCT,包括964例DAI患者。Meta分析结果显示:纳洛酮可以降低DAI患者病死率(RR=0.56,95%CI:0.46~0.68,P<0.001);改善格拉斯哥预后评分(RR=1.56,95%CI:1.14~2.12,P=0.005);并且能缩短患者昏迷时间(WMD=-9.47,95%CI:-13.84~-5.10,P<0.001)。结论 由于缺乏高质量的随机双盲对照试验,纳入研究中纳洛酮使用剂量、疗程等存在差异,故纳洛酮改善DAI患者预后的证据尚不充分,其疗效和安全性尚需进一步评价。
纳洛酮;弥漫性轴索损伤;系统评价;meta分析
弥漫性轴索损伤(diffuse axonal injury, DAI)是以广泛性的神经轴索伴毛细血管破损为特征的原发性脑损伤,占所有脑外伤的28%~42%,病死率高达42%~62%,重残及植物生存约30%~40%[1],因此它是决定颅脑损伤患者转归和预后的一个重要因素[2],但是目前没有特别有效的治疗手段[3]。
近年来,纳洛酮作为人工合成的阿片受体拮抗剂,被越来越多地应用到DAI的救治上。其主要依据为脑损伤后颅内阿片类、兴奋性氨基酸等神经递质增多,而纳洛酮能够竞争性抑制阿片肽的神经毒性作用,使其成为DAI治疗的一项选择[4-5]。但是纳洛酮的真实疗效尚不清楚,因此本研究应用循证医学的方法,系统评价纳洛酮治疗DAI有效性和安全性的问题。
1 资料与方法
1.1 纳入标准 研究类型:随机对照研究(randomized controlled trial, RCT)。研究对象:DAI患者,通过临床表现和影像学检查诊断,格拉斯哥昏迷评分(glasgow coma scale, GCS)3~15分。干预措施:DAI患者急诊入院后随机分为纳洛酮组和对照组,前者给予纳洛酮治疗,后者可为安慰剂或者空白对照。在两组的救治过程中,均辅以降颅压、促神经损伤修复等治疗。结局指标:早期病死率、格拉斯哥预后(glasgow outcome score, GOS)评分、苏醒时间、并发症情况。
1.2 检索策略 按主题词对应自由词的方式,以“naloxone, diffuse axonal injury, diffuse axonal injury [Mesh/Emtree]”检索Pubmed, Embase, Cochrane Library;以“纳洛酮、弥漫性轴索损伤、脑外伤、脑损伤”为检索词,检索中国知网、万方、维普、中国生物医学文献数据库,均从建库时间到2014年6月,检索过程未做任何限定。为避免漏检,辅以google学术等资源查找相关文献。
1.3 资料提取与质量评价 2位评价员各自按照标准筛选文献,对于符合的文献阅读全文,以表格形式提取研究设计的具体方法和感兴趣指标,并做交叉核对确保数据的准确性。纳入研究的质量评价依据改良Jadad评分量表进行,主要为:随机序列的产生、隐藏分组、施盲、撤出与退出4个方面,分数依次为2、2、2、1,总分1~3分为低质量,4~7分为高质量。
1.4 统计分析 病死率和GOS评分的二分类资料使用相对危险度(relative risk, RR)计算,苏醒时间用权重均数差(weighted mean difference, WMD)计算,RR、WMD都以95%可信区间(95% confidence interval, 95%CI)表示。各研究之间的统计学异质性采用I2检验评估,当统计学异质性较小时(P>0.1,I2<50%),采用固定效应模型分析;当统计学异质性较大(P<0.1,I2>50%),分析可能的异质性来源,采用随机效应模型进行分析[6]。统计分析采用STATA 12.0软件(StataCorp, College Station, TX),以P≤0.05为差异有统计学意义。
2 结 果
2.1 文献检索流程及结果 初步检索各数据库总计247篇,按标题摘要内容排除重复、综述、对照试验及其他不符合纳入标准的研究216篇,纳入的31篇通读全文后排除19篇未涉及感兴趣指标、多篇重复发表的文献后,最终纳入RCT 12篇[7-18],均为中文文献。
2.2 纳入研究的一般情况 12篇研究[7-18]共计964例DAI患者,其中纳洛酮组478例,对照组486例。各研究均粗略给出了患者的基线资料,其中9项研究[7,9-10,12-17]纳入GCS≤8患者,2项研究[8,18]纳入GCS>8的轻型DAI患者,1项[11]没有具体报道GCS评分。有2项研究[11,17]未记录受伤到接受治疗的时间,其余研究集中在16 h以内。不同研究给患者的纳洛酮剂量有较大差异,持续时间从10 d到 20 d 不等,见表1。
2.3 质量评价 12篇RCT[7-18]质量低下,存在很大程度的方法学偏倚:没有全面报道RCT必备因素的高质量文献,研究仅仅描述为随机分配,也没有涉及隐藏分配和施盲的信息,其中有2个研究[9,12]的分配方案采用了单双日入组的半随机法,其余仅描述为随机分配。所以总体上研究质量低、可信度差,这对结果的真实性存在和很大影响。
2.4 Meta分析结果
2.4.1 病死率 12个研究报道了病死率(1项[10]报道两组均无病死患者):研究间统计学异质性较小(P=0.995,I2=0.0%),固定效应模型分析后显示:纳洛酮组DAI患者总体病死率低于对照组(RR=0.56,95%CI:0.46~0.68,P<0.001),见图1。做敏感性分析发现:采用随机效应模型后(RR=0.57,95%CI:0.47~0.69,P<0.001)或者去掉权重最大的研究[15]后(RR=0.56,95%CI:0.45~0.71,P<0.001),与之前结果保持一致。由于有2项研究[8,18]纳入了GCS>8的患者,1项[11]没有报道GCS评分,将3篇去除之后结果依然显示纳洛酮组的病死率低于对照组(RR=0.55,95%CI:0.44~0.69,P<0.001)。另外,排除5个样本量偏低(N≤60)的研究[10-11,13-14,17]后,结果提示纳洛酮组的病死率仍低于对照组(RR=0.57,95%CI:0.47~0.71,P<0.001)。以上结果均提示:纳洛酮治疗可以降低DAI后的病死率。
表1 纳入研究的基线信息
Tab.1 The baseline information of the included studies
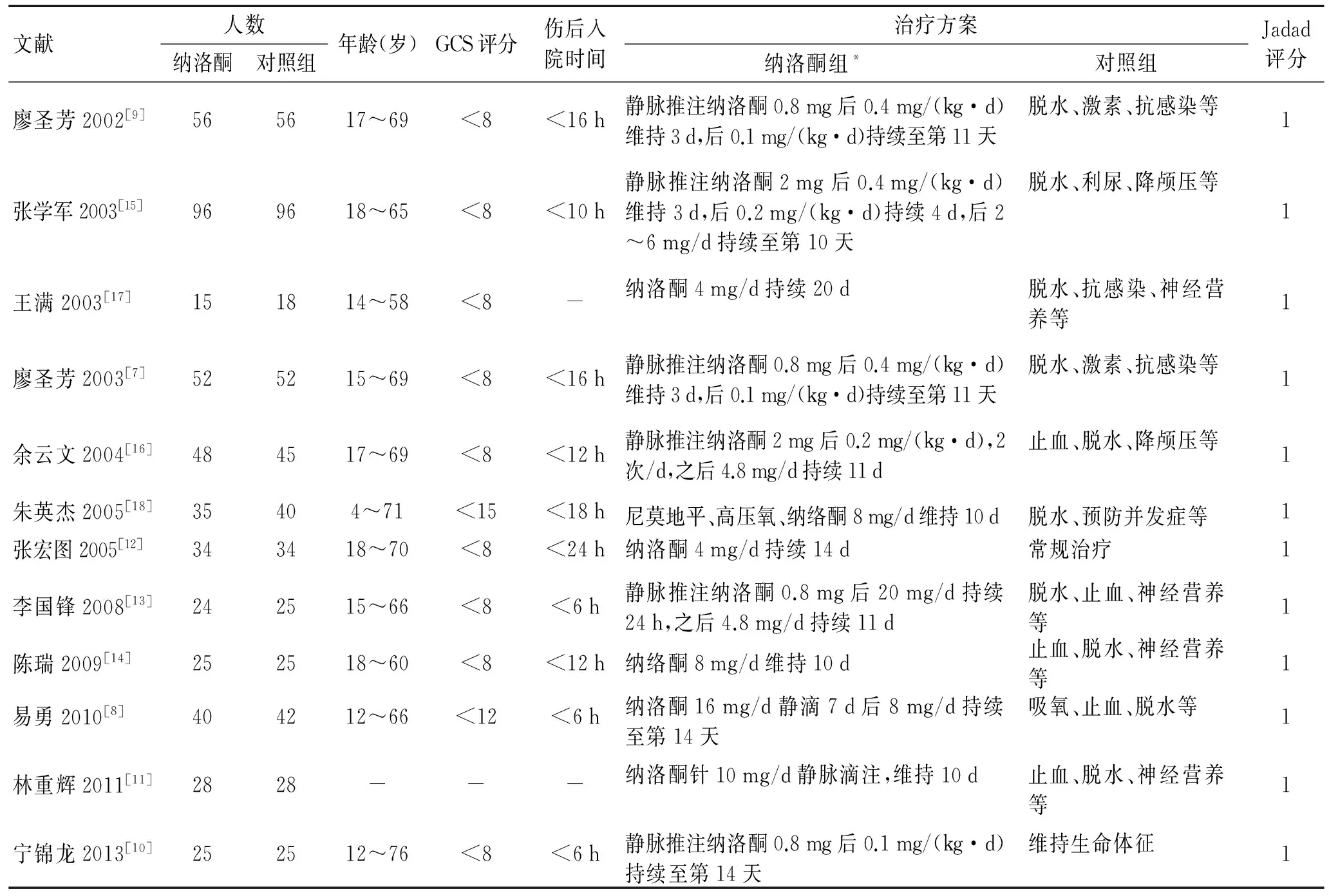
文献人数纳洛酮对照组年龄(岁)GCS评分伤后入院时间治疗方案纳洛酮组*对照组Jadad评分廖圣芳2002[9]565617~69<8<16h静脉推注纳洛酮0.8mg后0.4mg/(kg·d)维持3d,后0.1mg/(kg·d)持续至第11天脱水、激素、抗感染等1张学军2003[15]969618~65<8<10h静脉推注纳洛酮2mg后0.4mg/(kg·d)维持3d,后0.2mg/(kg·d)持续4d,后2~6mg/d持续至第10天脱水、利尿、降颅压等1王满2003[17]151814~58<8-纳洛酮4mg/d持续20d脱水、抗感染、神经营养等1廖圣芳2003[7]525215~69<8<16h静脉推注纳洛酮0.8mg后0.4mg/(kg·d)维持3d,后0.1mg/(kg·d)持续至第11天脱水、激素、抗感染等1余云文2004[16]484517~69<8<12h静脉推注纳洛酮2mg后0.2mg/(kg·d),2次/d,之后4.8mg/d持续11d止血、脱水、降颅压等1朱英杰2005[18]35404~71<15<18h尼莫地平、高压氧、纳络酮8mg/d维持10d脱水、预防并发症等1张宏图2005[12]343418~70<8<24h纳洛酮4mg/d持续14d常规治疗1李国锋2008[13]242515~66<8<6h静脉推注纳洛酮0.8mg后20mg/d持续24h,之后4.8mg/d持续11d脱水、止血、神经营养等1陈瑞2009[14]252518~60<8<12h纳络酮8mg/d维持10d止血、脱水、神经营养等1易勇2010[8]404212~66<12<6h纳洛酮16mg/d静滴7d后8mg/d持续至第14天吸氧、止血、脱水等1林重辉2011[11]2828---纳洛酮针10mg/d静脉滴注,维持10d止血、脱水、神经营养等1宁锦龙2013[10]252512~76<8<6h静脉推注纳洛酮0.8mg后0.1mg/(kg·d)持续至第14天维持生命体征1
注:*纳洛酮组的治疗方案在对照组基础上进行。
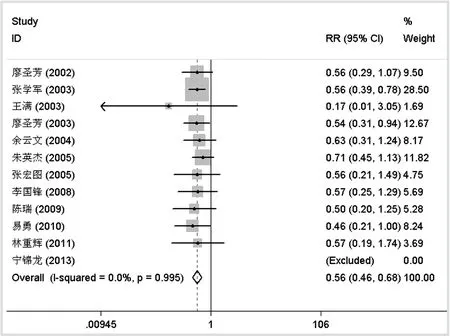
图1 纳洛酮组与对照组病死率比较的森林图
Fig.1 The forest plot of naloxone versus control on fatality
2.4.2 GOS预后 GOS评分在4~5为良好预后,统计后发现3 m GOS 4~5统计学异质性较大(P<0.001,I2=73.7%),采用随机效应模型分析结果提示纳洛酮组患者的预后优于对照(RR=1.56,95%CI:1.14~2.12,P=0.005),见图2。通过逐一排除,发现异质性来源主要为宁锦龙2013[10],去除该研究后异质性下降(P=0.111,I2=36.0%),效应量为(RR=1.64,95%CI:1.36~1.99,P<0.001),其可能原因为该研究报道DAI患者中部分人群接受依达拉奉干预,但是具体治疗信息匮乏。排除5个样本量偏低(N≤60)的研究[10-11,13-14,17]后(RR=1.62,95%CI:1.12~2.33,P<0.001)或者排除2个[8,18]GCS>8和1项[11]未报道GCS的研究后(RR=1.74,95%CI:1.10~2.74,P<0.001),结果仍提示纳洛酮组的预后优于对照组。
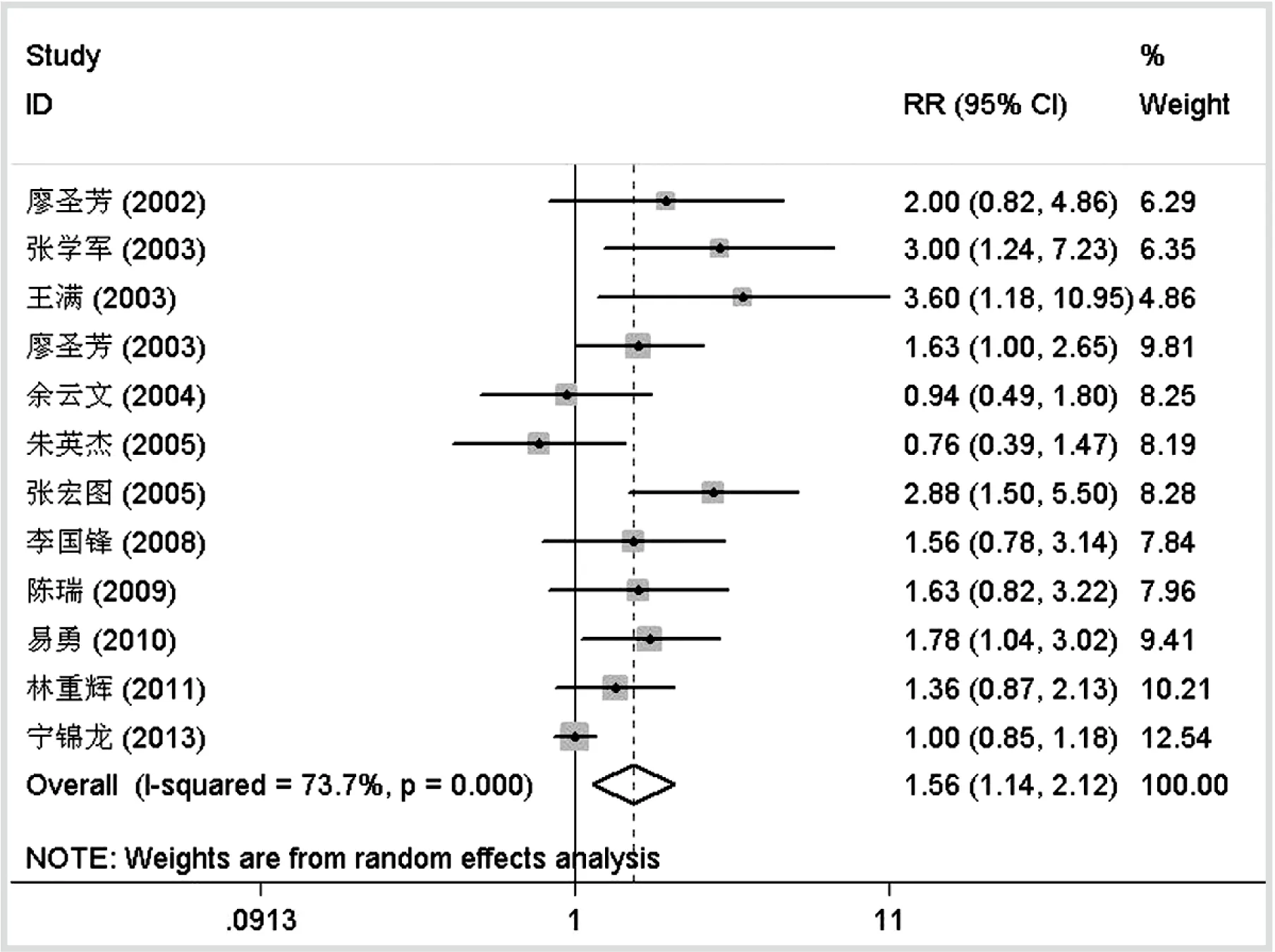
图2 纳洛酮组与对照组GOS比较的森林图
Fig.2 The forest plot of naloxone versus control on GOS
2.4.3 昏迷时间 有7个研究[7-11,13,15]报道了纳洛酮治疗后昏迷时间的变化,由于统计学异质性较大(P<0.001,I2=91.0%),采用随机效应模型分析。结果提示:纳洛酮组患者昏迷时间短于对照(WMD=-9.47,95%CI:-13.84~-5.10,P<0.001),见图3。去掉小样本量研究(N≤60)[10-11,13]后(WMD=-9.66,95%CI:-16.32~-3.00,P<0.001)或排除1个[8]GCS>8和1项[11]未报道GCS的研究后(WMD=-6.93,95%CI:-9.61~-4.24,P<0.001),结果也提示纳洛酮组的昏迷时间短于对照组。
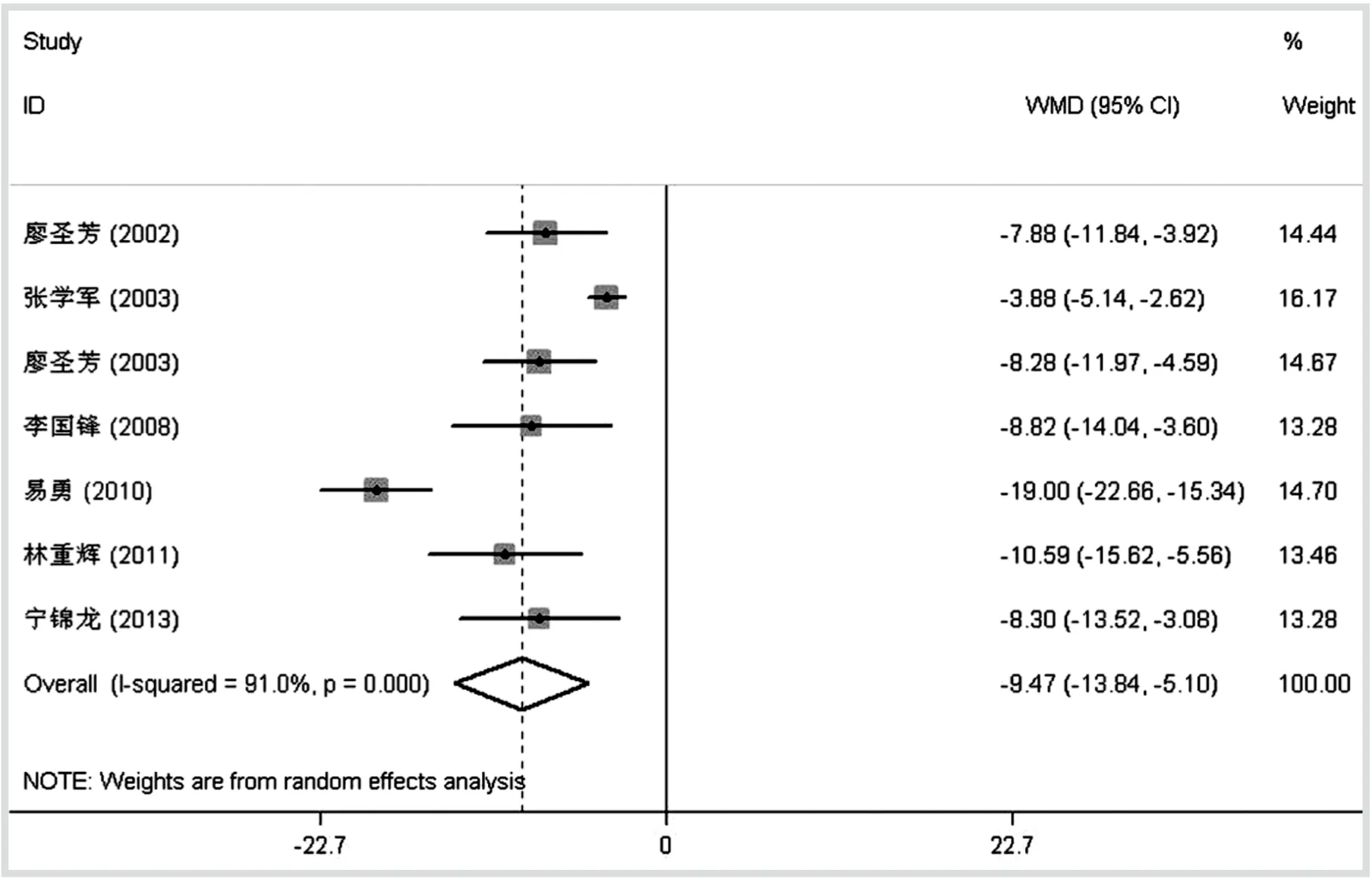
图3 纳洛酮组与对照组昏迷时间比较的森林图
Fig.3 The forest plot of naloxone versus control on duration of coma
2.4.4 并发症和不良反应事件 1个研究[15]报道了两组患者的并发症情况:肺部感染、电解质紊乱、应激性溃疡、肝肾功能不全在组间均无差别。另有5个研究[7,9-10,13-14]报道纳洛酮组未见任何毒副作用。
2.4.5 发表偏倚 本系统评价纳入了12个研究,我们以病死率为指标绘制了漏斗图,见图4。Begg’s检验Z=0.31,P=0.775(连续性校正后)和Egger’s检验P=0.207,姑且认为不存在发表偏倚。
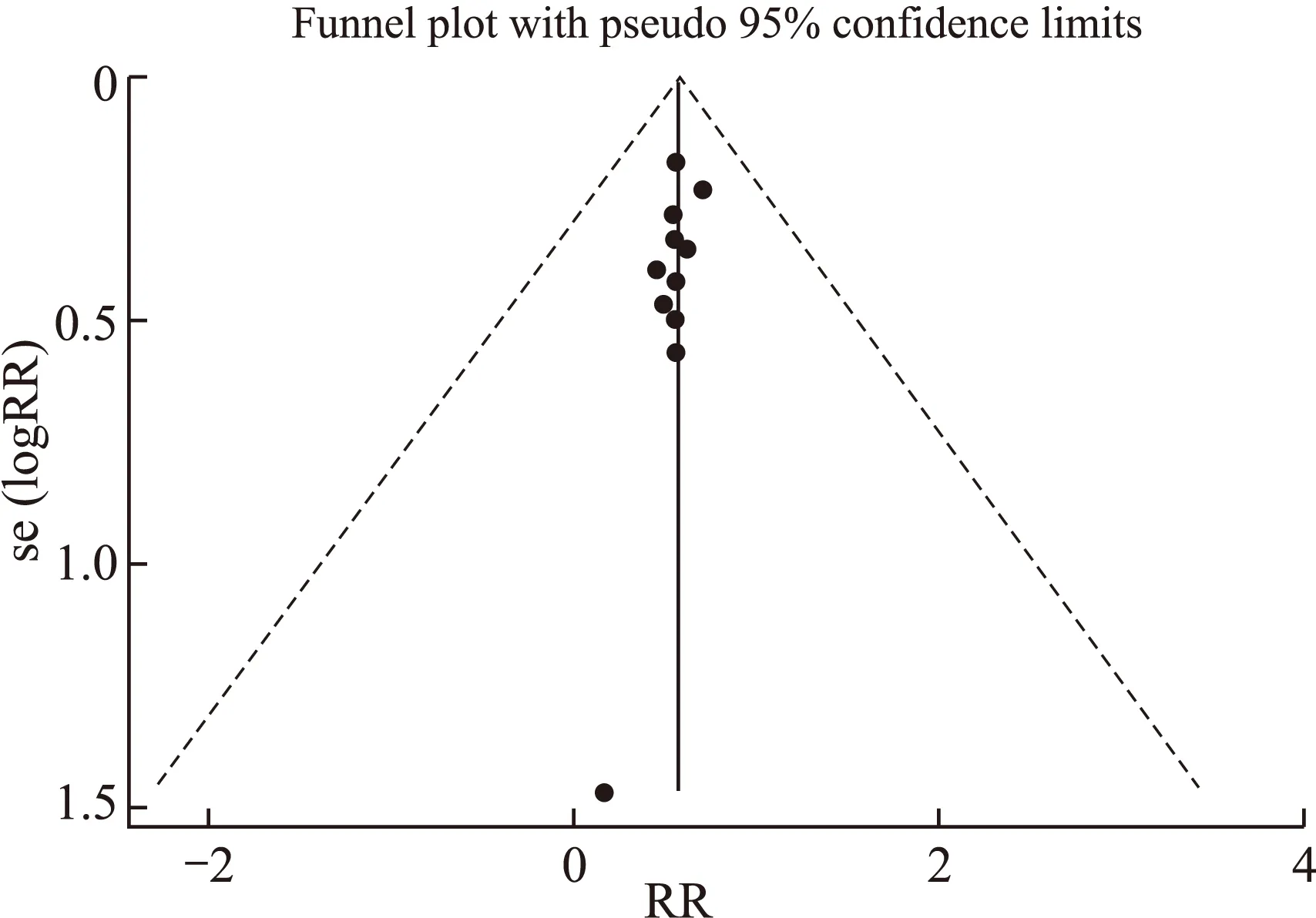
图4 Meta分析的漏斗图
Fig.4 The funnel plot of meta-analysis
3 讨 论
颅脑损伤以后体内阿片类递质急剧增多[5],阿片受体拮抗剂有减缓受体激活的作用,被认为可有效降低病死率,改善预后,且无并发症[19]。但是Cochrane外伤协作组于2013年通过了纳洛酮能否降低颅脑损伤病死率和改善预后的系统评价计划书[20],明确指出纳洛酮的治疗作用值得进一步探讨,因此进行了该研究。但我们发现:国外主要是将纳洛酮用于急性中毒、各种休克、心肺脑复苏等,而应用于颅脑损伤、特别是单纯DAI患者的研究较少,未见大规模应用于临床的文献报道。因此,针对纳洛酮救治DAI的研究主要集中在国内,这使得该结果具有地域局限性。
在cochrane图书馆和国外其他关于DAI的系统评价中,随访期末(至少3个月)时DAI患者病死率、GOS预后结局是主要疗效判定指标。本系统评价对DAI患者早期病死率、3月GOS预后及昏迷患者苏醒时间等主要疗效指标的初步分析结果显示:常规治疗方案联合纳洛酮可以改善患者预后。对于DAI病死率的结果,我们通过敏感性分析排除可能的影响因素仍发现统计学差异,这一结果相对稳定。在预后判断上,GOS评分提示治疗3月后纳洛酮组患者神经系统功能明显改善;而且纳洛酮对于昏迷患者有较强的促醒作用,但是统计学异质性偏大,我们采用meta回归试图探索其中的异质性来源,但是限于研究提供的信息缺乏,并没有发现相关因素。我们怀疑异质性可能与医师对残疾程度和苏醒评价的主观性有关,本系统评价只根据原作者提供的数据,没有按照预先制定的标准对数据进行调整,影响到试验结果的可信度。
同时,对于纳洛酮的冲击疗法,心血管反应是主要观察指标。虽然个别研究简单说明未见不良反应,这可能与昏迷患者的低反应状态有关,因此无法对不良反应的指标进行综合评价。总体上研究者对药物的不良反应缺乏足够重视,因此本系统评价尚不能就纳洛酮用于DAI的安全性得出确切结论。另外,所有纳入研究的方法学均存在严重的方法学缺陷:没有1个研究详细且正确地报道随机分配的方法,也未说明是否进行分配隐藏,这可能导致患者的选择偏倚;纳入研究均未报告盲法,这可能导致实施偏倚和测量偏倚。故在选择、实施和测量等各阶段产生偏倚的可能性极大。由于存在上述质量问题,对本系统评价的结果应保持谨慎态度。
综上,国内外均缺乏高质量的随机双盲对照试验,纳入研究中纳洛酮使用剂量、疗程等存在差异,故纳洛酮改善DAI患者预后的证据尚不充分,其疗效和安全性尚需进一步评价。
[1] 刘晓斌,宋锦宁. 脑弥漫性轴索损伤[J]. 医学综述, 2006, 12(12):742-745.
[2] 宋锦宁,刘守勋. 脑弥漫性轴索损伤的特点及临床诊断[J]. 中国神经精神疾病杂志, 1997, 23(3):141-144.
[3] SMITH DH, HICKS R, POVLISHOCK JT. Therapy development for diffuse axonal injury[J]. J Neurotrauma, 2013, 30(5):307-323.
[4] MCINTOSH TK, HEAD VA, FADEN AI. Alterations in regional concentrations of endogenous opioids following traumatic brain injury in the cat[J]. Brain Res, 1987, 425(2):225-233.
[5] HAYES RL, LYETH BG, JENKINS LW, et al. Possible protective effect of endogenous opioids in traumatic brain injury[J]. J Neurosurg, 1990, 72(2):252-261.
[6] ARMITAGE P, BERRY G, MATTHEWS JNS. Analysing Means and Proportions. Statistical Methods in Medical Research[M]. Blackwell Science Ltd, 2008: 83-146.
[7] 廖圣芳,陈汉民,王玉差,等. 大剂量纳洛酮治疗弥漫性轴索损伤的临床研究[J]. 中国现代医学杂志, 2003, 13(12):63-65.
[8] 易勇,淡冰,陈犇. 亚低温冬眠疗法联合纳洛酮治疗弥漫性轴索损伤的分析[J]. 当代医学, 2010, 16(21):27-28.
[9] 廖圣芳,陈汉民,王玉差,等. 大剂量纳洛酮在治疗弥漫性轴索损伤中的应用[J]. 实用医学杂志, 2002, 18(11):1179-1180.
[10] 宁锦龙,钟向球. 依达拉奉联合纳洛酮治疗弥漫性轴索损伤[J]. 中国实用医刊, 2013, 40(15):117-118.
[11] 林重辉,黄雪钦,徐声亮,等. 高压氧加纳洛酮治疗弥漫性轴索损伤[J]. 中国伤残医学, 2011, 19(5):6-7.
[12] 张宏图. 纳洛酮治疗弥漫性轴索损伤疗效观察[J]. 实用医药杂志, 2005, 22(6):504-505.
[13] 李国锋. 早期大剂量纳洛酮治疗弥漫性轴索损伤的临床观察[J]. 现代医院, 2008, 8(3):23-24.
[14] 陈瑞. 早期纳洛酮治疗弥漫性轴索损伤的临床观察[J]. 中国医学创新, 2009, 6(36):106-107.
[15] 张学军. 盐酸纳洛酮治疗弥漫性轴索损伤96例临床观察[J]. 医学临床研究, 2003, 20(8):628-629.
[16] 余云文. 弥漫性轴索伤早期应用大剂量纳洛酮治疗的体会[J]. 浙江创伤外科, 2004, 9(4):217-218.
[17] 王满,马树成. 纳络酮治疗弥漫性轴索损伤[J]. 中国新药与临床杂志, 2003, 22(1):30-37.
[18] 朱英杰,杨加友,向昌华, 等. 75 例弥漫性轴索损伤的疗效分析[J]. 吉首大学学报:自然科学版, 2005, 26(1):95-96,117.
[19] 金尔伦全国多中心双盲临床研究课题组. 金尔伦(盐酸纳洛酮)治疗急性颅脑损伤病人随机双盲多中心前瞻性临床研究[J]. 中华神经外科杂志, 2001, 17(3):135-139.
[20] LEI J, GAO G, JIANG J. Naloxone for improving mortality and neurological outcomes following acute traumatic brain injury (Protocol)[J]. Cochrane Database Syst Rev, 2013, 7: CD010679. DOI: 10.1002/14651858.CD010679.
(编辑 卓选鹏)
Efficacy and safety of naloxone on patients with diffuseaxonal injury: a systematic review
LI Wen-tao, ZHANG Bin-fei, SONG Jin-ning, MA Xu-dong, LIU Zun-wei, GU Hua
(Department of Neurosurgery, the First Affiliated Hospital, Medical School of Xi’an Jiaotong University, Xi’an 710061, China)
Objective The role of naloxone in diffuse axonal injury (DAI) remains in doubt. This meta-analysis is to evaluate the efficacy and safety of naloxone. Methods A systematic electronic literature search was conducted to identify from Databases randomized controlled trials (RCTs) comparing the use of naloxone with control group in patients with DAI. Data extraction and quality evaluation of studies were performed by investigators independently. A meta-analysis was performed by STATA 12.0. Results Totally 12 studies involving 964 patients met our inclusion criteria. Meta-analysis showed naloxone could decrease the mortality (RR=0.56,95%CI:0.46-0.68,P<0.001), increase Glasgow outcome scale (RR=1.56,95%CI:1.14-2.12,P=0.005), and shorten duration of coma (WMD=-9.47,95%CI:-13.84~-5.10,P<0.001), compared to control group. Conclusion Due to the lack of high-quality randomized double-blind controlled trials, and variation in dose and duration of naloxone, the evidence that naloxone can improve the prognosis of DAI is insufficient. The efficacy and safety of naloxone on DAI need to be further evaluated.
naloxone; diffuse axonal injury; systematic review; meta-analysis
2014-07-09
2014-09-25
国家自然科学基金资助项目(No.30471774);教育部新世纪优秀人才支持计划资助项目(No.NCET-05-0831);陕西省自然科学基金资助项目(No.2003C1-16) Supported by the National Natural Science Foundation of China (No.30471774), the New-Century Excellent Talents Program of Ministry of Education(No.NCET-05-0831) and the Natural Science Foundation of Shaanxi Province (No.2003C1-16)
宋锦宁,博士,教授,主任医师,博士生导师. Email: jinnings@126.com
李文涛(1968-),男(汉族),在职硕士研究生. 研究方向:立体定向放射外科、颅脑损伤基础与临床. E-mail: liwentao616@163.com
时间:2014-10-15 16∶39 网络出版地址:http://www.cnki.net/kcms/detail/61.1399.R.20141015.1639.002.html
R651.1
A
10.7652/jdyxb201406011

