基于β-环糊精稳定的Pickering乳液微观结构与流变性质研究
袁继凤, 徐化能, 王周平
(江南大学食品学院,江苏 无锡 214122)
乳液是由两种互不相溶的液体相所组成的分散体系,在食品、化工、农业以及医药等领域有着广泛的应用。乳液为一种多尺度、复杂的热力学不稳定体系,通常需要加入乳化剂来予以稳定。常用乳化剂包括表面活性剂、聚合物和固体颗粒,其中以固体颗粒稳定的乳液被称为Pickering乳液[1]。与传统乳液相比,Pickering乳液具有更好的聚结稳定性、经济性和环境友好性。目前,公认的Pickering乳液的稳定机理主要为固体颗粒吸附于油/水界面并形成固体颗粒单层/多层膜,从而稳定乳液[2]。
环糊精(cyclodextrins,CDs)是一类环状低聚糖,常见的有 α-、β-和 γ-环糊精,聚合度分别为 6、7和8。环糊精具有空腔结构,可以掩蔽特殊气味和缓释有效成分,因此被广泛应用于食品、医药和日用化学品工业中[3]。近年来,环糊精开始被应用于Pickering乳液的制备和研究中。研究结果表明,β-环糊精与油相分子的部分结构包合形成络合物,这种络合物可在油水界面形成一种稳定的膜,因此可将其界定为Pickering乳液[4-6]。乳状液的稳定性主要取决于体系中颗粒与颗粒之间、颗粒与液滴之间形成的三维网络结构。Inoue等[7]在研究中发现β-环糊精与油相形成的乳剂随着β-环糊精的加入量的增加,成乳范围增加,乳液液滴粒径减小。
尽管以往研究考察了环糊精在油水分散体系的特性及其稳定乳液的能力,而对其与常规表面活性剂分散体系性质及其稳定乳液能力的差异尚未进行比较。通过测定β-环糊精稳定的乳液的微观结构和剪切粘度等特性,考察β-环糊精浓度、油水体积比等对乳液稳定性的影响,并比较其与非离子表面活性剂吐温-80稳定乳液能力的差异,进而阐明两者对乳液的不同稳定机理。
1 材料与方法
1.1 实验材料与试剂
β-环糊精、吐温-80:均为化学纯,购于上海国药集团化学试剂有限公司;大豆油:购于中粮福临门公司;实验用水为去离子水。
1.2 实验仪器
IKA T8高剪切分散乳化机:德国IKA公司产品;AR-G2流变仪:美国TA公司产品;BX51光学显微镜:日本Olympus公司产品。
1.3 实验方法
1.3.1 乳液的制备 油水体积比1∶9乳液:离心管中分别加 入 0.1、0.2、0.3、0.5、0.8、1.0 g β-环糊精(吐温-80),缓慢加入18 mL去离子水和2 mL大豆油,使用IKA T8高剪切分散乳化机在25℃、10 000 r/min下高速搅拌2 min[8],配制成乳化剂质量浓度为 0.5、1.0、1.5、2.5、4.0、5.0 g/dL 的乳液。
不同油水比乳液:离心管中加入0.5 g β-环糊精,分别缓慢加入 18、16、14、12、10 mL 去离子水和2、4、6、8、10 mL 大豆油, 按上述方式制得油水比分别为 1∶9、2∶8、3∶7、4∶6、5∶5 的乳液。
1.3.2 乳液乳化系数的测定 将制备好的乳液平行样品密封,静置于25℃环境中。不同β-环糊精添加量的乳液静置3 d后,外观形态呈现出明显的不同。乳液底部会析出半透明液体,顶部白色部分为乳液层。分别测量乳液层高度与样品的总高度,计算乳化系数。
乳化系数(CreamingIndex,CI)按公式(1)计算[9-11]:
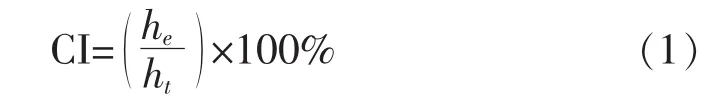
其中,he为静置3 d后乳液层的高度,ht为样品的总高度。
1.3.3 乳液液滴微观形态 取稳定乳液层制片,通过光学显微镜进行观察。光学显微镜照片通过连接在显微镜上的图像采集装置采集,根据对象不同大小,选择合适放大倍数的光镜,然后根据放大倍数设定标尺。
1.3.4 乳液粘度测定 乳液的表观粘度采用ARG2流变仪表征,夹具直径为40 mm,测试温度为25℃。将样品置于平行板之间,间隙设为1 mm,测试温度为25℃,剪切速率变化范围为1~100 s-1。
2 结果与讨论
2.1 不同β-环糊精/吐温-80质量浓度对乳液性质的影响
2.1.1 乳化系数 乳液分层指油水相的分离,是一种乳液不稳定性的现象。乳化系数越大,表明乳液层占总样品体积的百分比越大,乳液越稳定。静置3 d后,两种乳化剂制备所得乳液,在静置过程中均没有油相析出,仅有一定体积的水相从乳液底部析出。其乳化系数如表1所示。
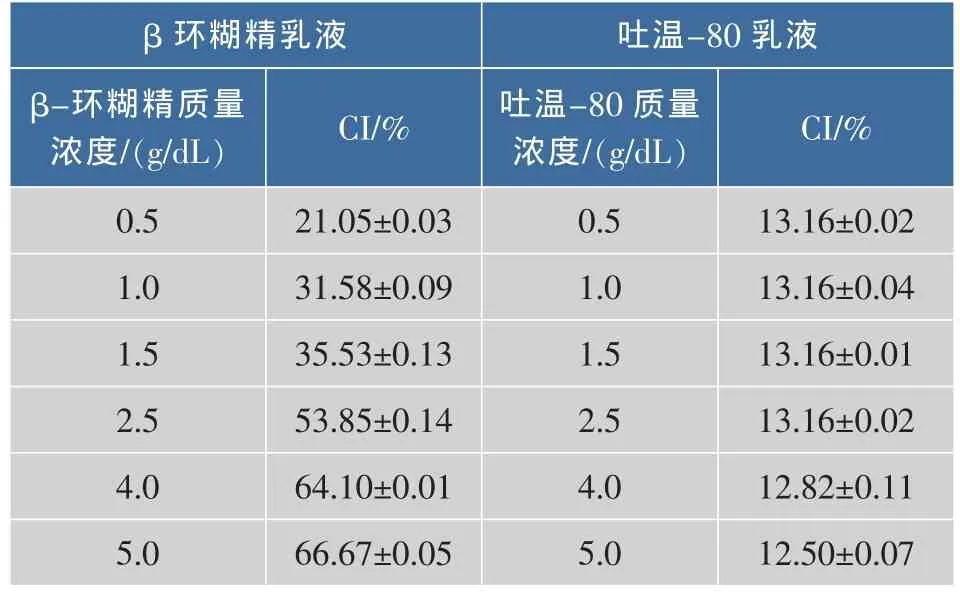
表1 不同质量浓度β-环糊精和吐温-80的乳化系数Table 1 Creaming index of the emulsions prepared with differentconcentration ofβ-Cyclodextrin/Tween-80
表1表明,β-环糊精和吐温-80的乳化系数呈现出明显的差异。当β-环糊精质量浓度从0.5 g/dL增加到5 g/dL时,乳化系数值从21.5%增加到66.67%;而吐温-80稳定乳液的能力较差,其乳化系数基本维持在13.16%左右,且吐温-80质量浓度对乳化系数值影响很小。乳化系数随环糊精浓度的增大而增大,可能与环糊精与油的络合物吸附在油水界面处形成连续的网络结构有关,当这种结构的强度足够高时能阻止乳液液滴之间的聚并[5],从而抑制乳液的分层。环糊精浓度的增加意味着在油-水混合体系中能形成更多的络合物,乳液液滴间形成高覆盖度的油-水界面层的可能性增加,这有利于提高乳液的稳定性。
2.1.2 乳液微观结构 环糊精乳液光学显微镜图见图1(a)。乳液液滴的粒径随着β-环糊精质量浓度的增加而逐渐减小,这意味着β-环糊精稳定乳液的能力逐渐增强。这可能因为,当β-环糊精质量浓度增加时,越来越多的环糊精/油的络合物颗粒吸附于油/水界面而使相界面膜更加致密,有效阻止了液滴的聚并,进而导致乳液滴粒径降低。当质量浓度增至4.0 g/dL时,继续增加β-环糊精浓度,乳液液滴粒径基本不变,说明β-环糊精稳定乳液的能力趋于恒定。吐温-80乳液光学显微镜图见图1(b),使用吐温-80制备的乳液,液滴相对均匀,吐温-80浓度的增加对乳液粒径无显著影响。环糊精与吐温-80乳液微观结构差异可能与两者稳定乳液机理不同有关:表面活性剂吐温-80的加入,能造成体系的界面张力降低,使得乳液液滴分散得细密均匀;而β-环糊精能与油形成络合物,吸附在油水界面膜上,在液滴周围形成一层致密的颗粒膜,使得乳液液滴间彼此不容易发生聚结。
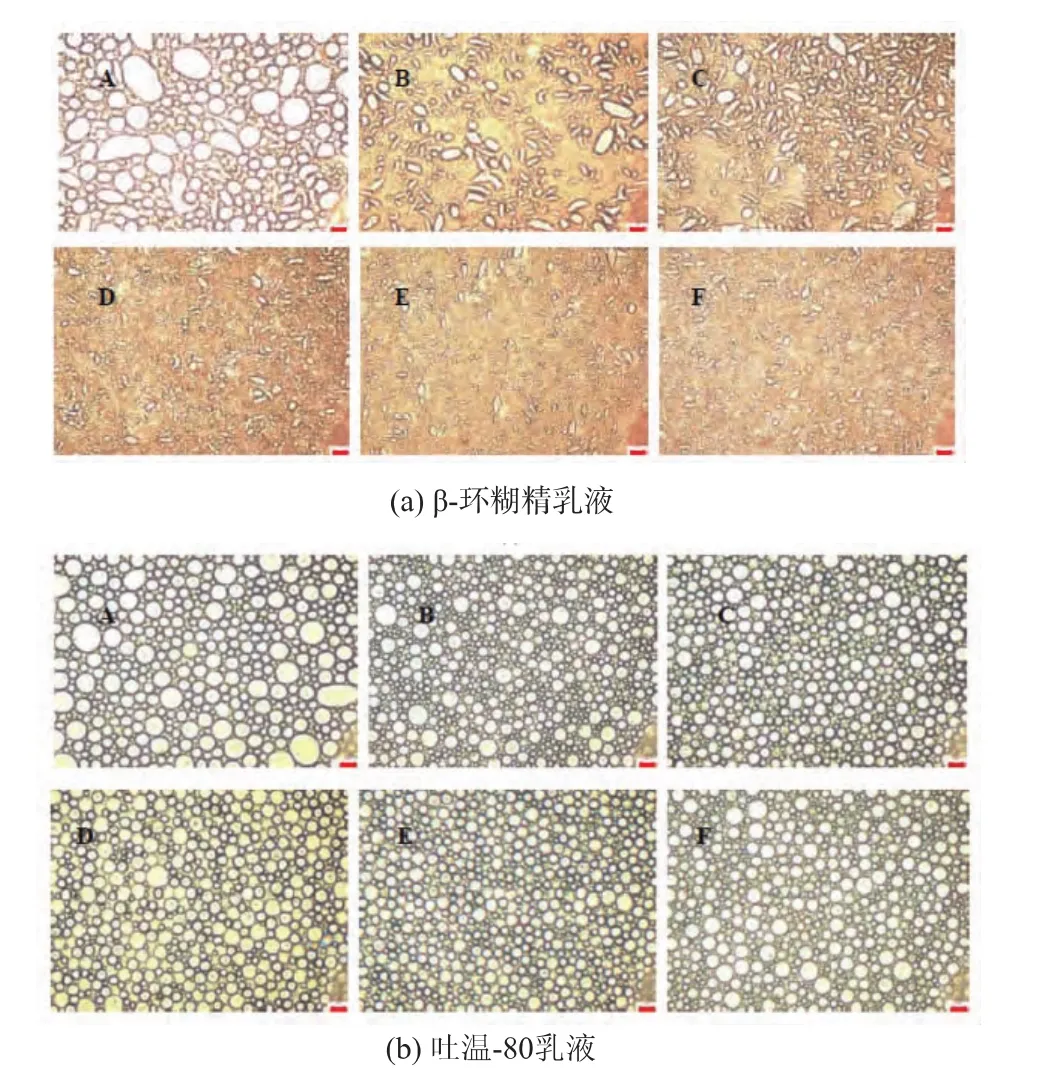
图1 乳液光学显微镜图Fig.1 Microscope images for the droplets of the emulsions prepared with β-CD(a)or Tween-80(b)
从乳液液滴形态角度分析,吐温-80乳液呈现为圆球形而β环糊精乳液呈现为不规则形态。这可能因为,吐温-80分子形成的界面膜强度远小于环糊精/油络合物颗粒形成的界面膜,表现为:制片过程中,吐温-80界面膜重新排布,形成圆球形乳液颗粒;环糊精/油络合物界面膜无法重新排布而发生形变,乳液液滴呈现不规则形态。
在作者研究的β-环糊精浓度范围内,环糊精浓度的增加既可以降低水油界面张力[4],又能显著提高界面膜的刚度和强度,从而提高乳液的稳定性;而在吐温-80质量浓度范围内,界面张力变化不大,因此,乳液液滴粒径基本不变。
2.1.3 乳液粘度 如图2所示,在设定的剪切速率范围内(1~100 s-1),随着剪切速率的增加,β-环糊精乳液的黏度均呈下降趋势,即呈现出剪切变稀行为;而吐温-80乳液的粘度均呈上升趋势,即呈现出剪切变稠行为。在任何一个剪切速率下,β-环糊精乳液的黏度都显著大于吐温-80乳液的黏度。这是由于环糊精络合物在油水界面形成致密的颗粒膜,乳液的流动在质点附近将受到干扰,需要消耗额外的能量,因此乳液的剪切粘度较高;相反,吐温-80具有表面活性,表面能降低,因而乳液在流动时克服的阻力小,剪切粘度较低。
为了更形象地描述乳液的非牛顿流变行为,可采用幂律方程对实验结果进行拟合[12]:
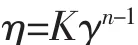
式中,η为乳液的黏度;K为稠度系数;γ为剪切速率;n为流动指数(根据n值可以推测剪切对乳液体系的作用,n<1为剪切变稀,n=1为牛顿流体,n>1 为剪切变稠)。

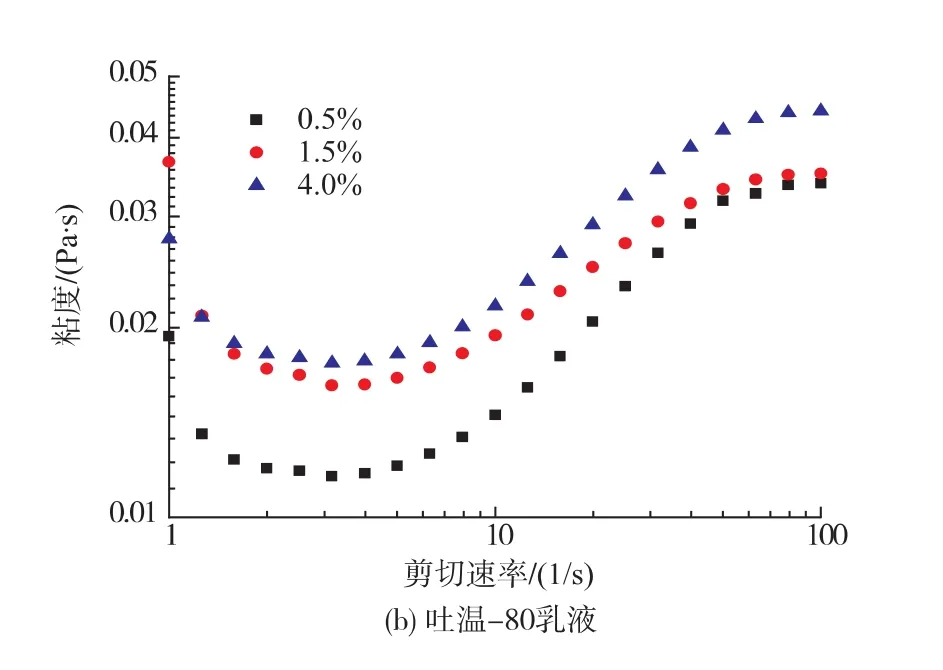
图2 不同β-环糊精/吐温-80质量浓度下的乳液的剪切黏度Fig.2 Viscosity of the emulsions prepared with β-CD(a)or Tween-80(b)
表2列出了不同乳化剂乳液的K与n的拟合结果。结果表明:β-环糊精质量浓度为0.5 g/dL的乳液流动指数n较小,说明该质量浓度下乳液中形成的络合物含量较少,不能形成强度较高的界面膜,因此表现出乳化系数值最低,乳液粒径最大。当β-环糊精质量浓度增至1.5 g/dL和4 g/dL时,乳液之间流动指数n差别减小,但稠度系数K相差较大,说明不同β-环糊精浓度的乳液,其剪切变稀的程度相似,但粘度存在较大的差异。对于吐温-80,其粘度显著小于β-环糊精乳液的粘度,因此其稠度系数K远小于β-环糊精乳液。
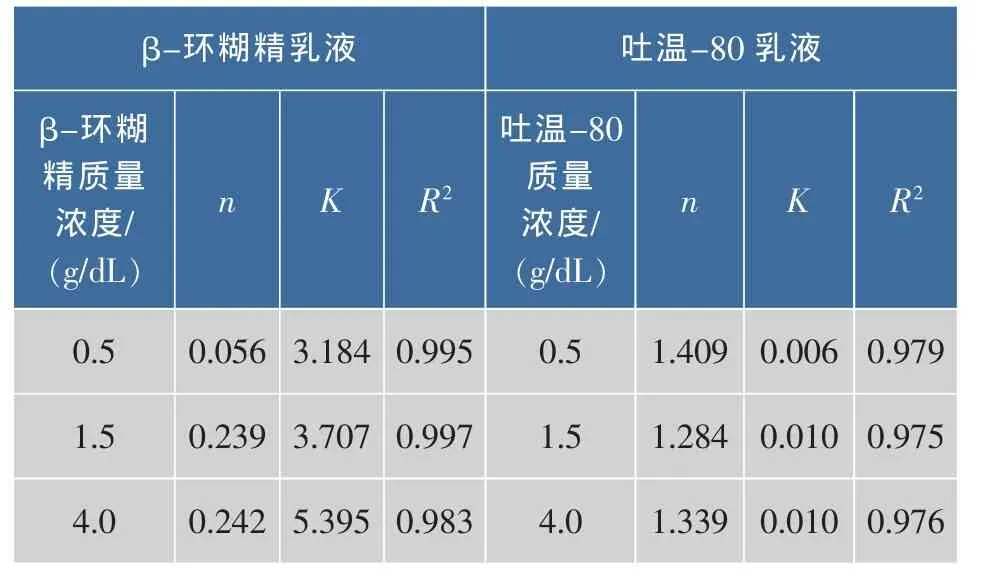
表2 不同β-环糊精/吐温-80质量浓度时乳液幂率方程拟合参数表Table 2 Power law model parameters of the emulsions prepared with β-CD or Tween-80
2.2 不同油水体积比对乳液性质的影响
2.2.1 乳化系数 图3显示,β-环糊精质量浓度为2.5 g/dL时,随着油水体积比的增加,乳液层的体积不断增大。结合表3可知,当油水体积比从1∶9增加到5∶5时,乳化系数值从53.85%增加到92.29%。

图3 不同油水体积比下β-环糊精乳液的稳定性Fig.5 Stability of the emulsions stabilized with β-CD at the concentration of 2.5 g/dL
β-环糊精浓度相同,生成环糊精/油络合物量相同,即能够形成的界面膜面积相同。随着油水体积比增大,界面膜强度减低,颗粒发生聚并,形成较大粒径的乳液液滴,导致乳液相体积增大,乳化系数值增大。
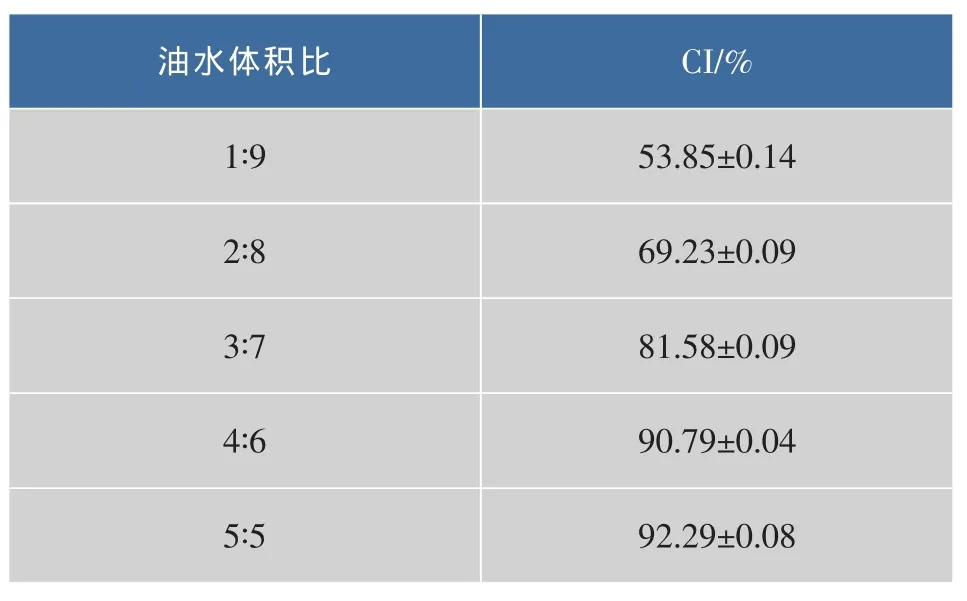
表3 不同油水体积比时β-环糊精的乳化系数Table 3 Creaming index of the emulsions prepared with different oil/water volume ratio
2.2.2 乳液微观结构 图4表明,乳液液滴的粒径随着油水体积比的增加而逐渐增加,可能是因为随着油水体积比例的增加,乳液油滴之间空间减小,液滴间作用力明显增强,导致液滴间相互碰撞并融合的可能性增加,因此乳液粒径增大。
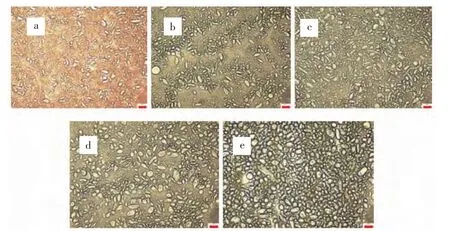
图4 不同油水体积比时β-环糊精乳液的光学显微镜图Fig.4 Microscope images for the droplets of the emulsions prepared with β-CD at the concentration of 2.5 g/dL
2.2.3 乳液黏度 如图5所示,不同油水体积比的β-环糊精乳液,随着剪切速率的增加其粘度均呈下降趋势,即呈现出剪切变稀行为;在同一剪切速率下,随着油相体积比的增加,β-环糊精乳液的粘度逐渐增加。油相体积的增加,乳液液滴间作用力明显增强,导致乳液粘度增大。将图5数据进行拟合,参数如表4所示。随着油水体积比的增加,乳液之间流动指数n差别较小,而稠度系数K相差较大,表明不同油水体积比的β-环糊精乳液,其剪切变稀的程度相似,但粘度存在较大的差异。
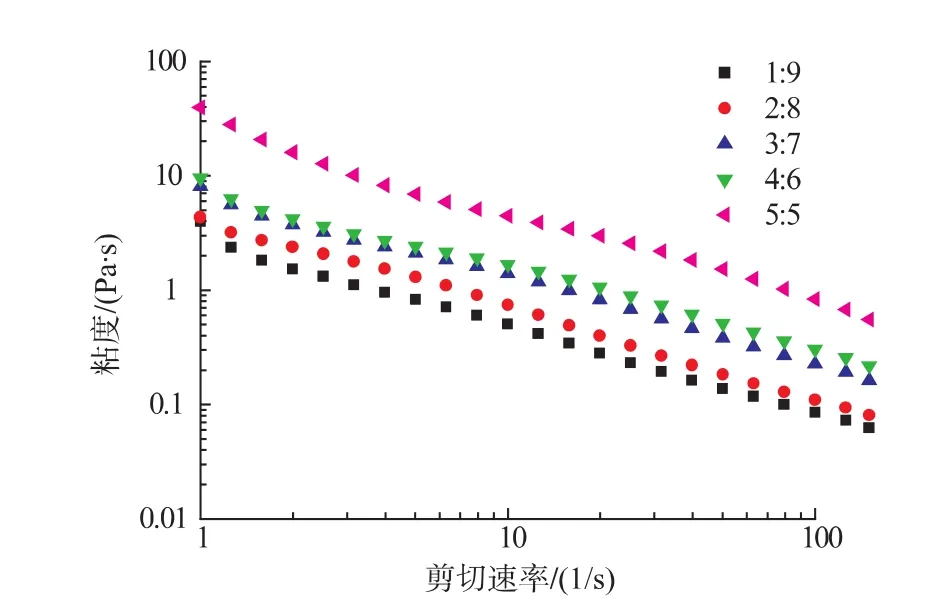
图5 不同油水体积时β-环糊精乳液的剪切黏度Fig.5 Viscosity of the emulsions prepared with different oil/water volume ratios
3 结语
β-环糊精稳定的乳液的稳定性显著高于吐温-80;β-环糊精乳化系数随环糊精质量浓度的增大而增大,而吐温-80质量浓度对乳化系数值影响很小;乳液液滴的粒径随着β-环糊精质量浓度的增加而逐渐减小,随着油水体积比的增加而增加;β-环糊精乳液粘度呈现典型的剪切变稀行为,而吐温-80乳液呈现剪切变稠行为。环糊精/油的络合物颗粒能吸附于油/水界面形成颗粒膜结构,其结构强度随环糊精含量的增加而提高,从而起到阻止液滴聚并、稳定乳液的作用。
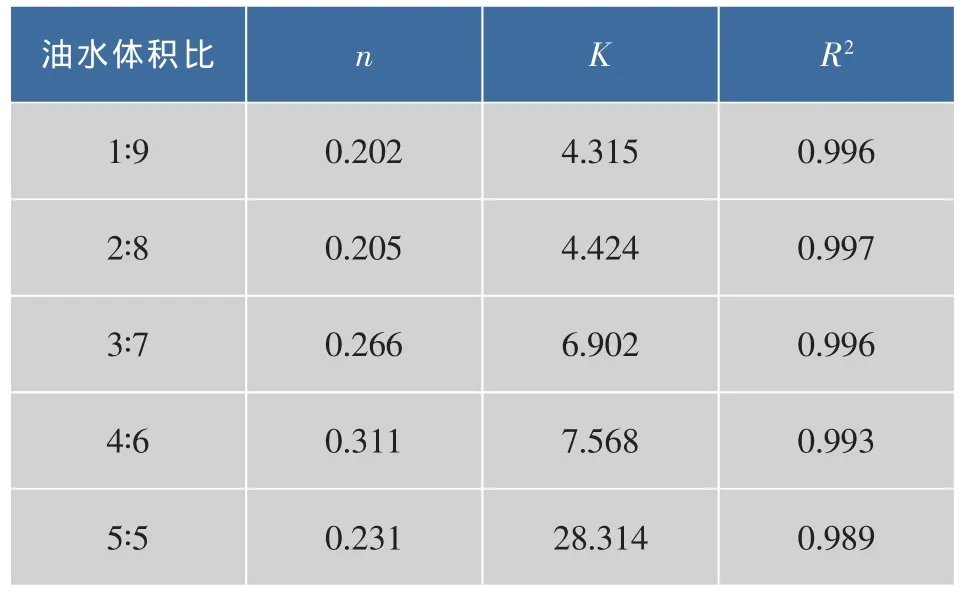
表4 不同油水体积时乳液幂率方程拟合参数表Table 4 Power law model parameters of the emulsions prepared with different oil/water volume ratios
[1]杨飞,王君,蓝强,等.Pickering 乳状液的研究进展[J].化学进展,2009,21(7-8):1418-1426.Yang fei,Wang jun,Lan qiang,et al.Research progress on pickering emulsions[J].Progress in Chemistry,2009,21 (7-8):1418-1426.
[2]易成林,杨逸群,江金强,等.颗粒乳化剂的研究及应用[J].化学进展,2011,23(1):65-79.Yi cheng-lin,Yang yi-qun,Jiang jin-qiang,et al.Research and Application of Particle Emulsifiers [J].Progress in Chemistry,2011,23(1):65-79.
[3]金征宇,徐学明,陈寒青,等.环糊精化学-制备与应用[M].北京:化学工业出版社,2009.
[4]Baghali G.M.Self-assembly of cyclodextrin – oil inclusion complexes at the oil-water interface:a route to surfactant-free emulsions[J].Journal of Materials Chemistry A,2013,1:10836-10846.
[5]Leila D.Formation of oil-in-water (O/W)pickering emulsions via complexation between β-cyclodextrin and selected organic solvents[J].Starch-St?rke,2012,64(11):898-913.
[6]Motoki I.Emulsion preparation using β-cyclodextrin and its derivatives acting as an emulsifier[J].Chemical and Pharmaceutical Bulletin,2008,56(9):1335-1337.
[7]Hashizaki K,Kageyama T,Inoue M,et al.Preparation and characterization of cycloalkanol/water emulsion using α-cyclodextrin as an emulsifier[J].Journal of Dispersion Science and Technology,2009,30(6):852-856.
[8]Sunsanee U.Rheological properties and stability of oil-in-water emulsions containing tapioca maltodextrin in the aqueous phase[J].Journal of Food Engineering,2013,116(1):170–175.
[9]Maryam K,Khorshid F.Investigation into the potential ability of Pickering emulsions (food-grade particles)to enhance the oxidative stability of oil-in-water emulsions[J].Journal of Colloid and Interface Science,2012,366(1):209–215.
[10]Supratim G,Tu T.Comparison of pickering and network stabilization in water-in-oil emulsions[J].Langmuir,2011,27(11):6589–6597.
[11]孙平,杨惠娟,王雅琦,等.麦芽糊精硬脂酸酯的酶法合成及其乳化性的研究[J].食品与生物技术学报,2013,32(1):9-14.Sun ping,Yang hui-juan,Wang ya-qi,et al.Lipase-Catalyzed Synthesis and Emulsification of Dextrin Ester[J].Journal of Food Science and Biotechnology,2013,32(1):9-14.
[12]Pablo B,Elizabeth T.Rheological and microstructural characterization of WPI-stabilized O/W emulsions exhibiting timedependent flow behavior[J].Food Science and Technology,2012,46(2):375-381.

