颈椎前路桥式自锁定聚醚醚酮椎间融合器治疗颈椎病的临床疗效分析
曹盛生,秦育宏,饶敏杰,罗 彤,聂少平,肖保卫,张功恒
颈椎前路减压椎间植骨融合术是治疗颈椎疾病的常规手术方法,植骨融合是手术关键步骤之一,而融合材料和融合方式的选择对融合率起着重要作用[1]。传统的颈椎前路手术是在髂骨上取三面皮质骨进行椎间植骨融合,存在手术创面大、术后髂骨供骨区疼痛等并发症;此外,三面皮质骨植骨易产生术后植骨块松动、移位,甚至椎体间隙塌陷[2]。近年来,颈椎椎间融合技术得到了飞速发展,不断更新的设计和理念使之更为完善。本研究旨在通过分析颈椎前路椎间盘切除减压后应用桥式自锁定聚醚醚酮(PEEK)椎间融合器治疗颈椎病的临床疗效,以期为今后临床治疗颈椎病提供参考依据。
1 资料与方法
1.1 一般资料 选择2011年6月—2012年9月宜春市人民医院骨科采用颈椎前路椎间盘切除减压并应用桥式自锁定PEEK椎间融合器植骨融合治疗的颈椎病患者23例,其中男15例,女8例;年龄40~75岁,平均51.5岁;脊髓型颈椎病21例,神经根型颈椎病2例;融合节段中单节段病变10例,双节段病变11例,三节段病变2例;共植入38枚PEEK融合器,其中C3~44枚,C4~515枚,C5~613枚,C6~76枚;病程6~35个月,平均13.5个月。患者均以颈脊髓受压表现为主,四肢麻木、乏力,躯干束带感,步态不稳,抽搐,大小便功能障碍,四肢腱反射亢进,部分伴上肢剧烈根性疼痛。患者术前均行常规颈椎正侧位及过屈、过伸位X线片、CT矢状位二维重建及MRI检查,其中25个节段椎体后缘有骨赘形成,3个节段存在局灶性后纵韧带骨化(不需行椎体次全切除);4例存在受累节段不稳。入选患者均满足以下标准:(1)均有颈脊髓受压临床表现,保守治疗效果不佳;(2)影像学上有颈脊髓受压改变,即有MRI T2加权像信号增高的脊髓受损改变,病变节段与患者临床表现一致。排除发育性椎管狭窄、黄韧带明显肥厚、病变节段在3节以上者。
1.2 手术方法 全麻后患者取仰卧位,肩背部垫高,头稍后仰,取右侧横弧形切口,沿颈血管鞘与气管食管内脏鞘之间钝性分离,直达椎体前缘。静脉滴注甲泼尼龙80 mg,C型臂X线机透视下定位,显露病变椎体间隙及相邻上、下各半个椎体,切开前纵韧带,病变椎间盘上下位椎体各置入一枚撑开螺钉,撑开器撑开椎体间隙,在两侧颈长肌范围内减压,宽度16~18 mm。仔细摘除病变椎间盘,注意清除侧方突出的椎间盘,刮除椎体后缘的增生骨赘,减压槽的上、下边缘应行扩大减压,以彻底解除脊髓压迫,根据情况决定是否处理后纵韧带。刮除病变间隙上下终板软骨板,使之粗糙化。试模后选择合适的锁定PEEK融合器型号。于髂嵴前1/3段开小骨窗,刮勺刮取适量松质骨填满PEEK融合器中空部分,开窗皮质骨原位覆盖骨窗。将融合器满意植入椎体间隙,取锁定钛夹插片通过融合器嵌入上下位椎体中桥式锁定固定。
1.3 术后处理 术后脱水、预防感染,有神经损害症状者加用神经营养药物,颈围保护3个月,并对患者进行定期随访。术后1周X线片观察颈椎正侧位,术后每3个月X线片观察颈椎正侧位及过屈、过伸位,直至达到椎间融合满意,并可行CT矢状位二维重建进一步观察椎间融合情况。
1.4 主要观察指标
1.4.1 临床评价指标 (1)记录手术时间及出血量,分别统计单节段、双节段、三节段平均手术时间及出血量。(2)记录手术并发症发生情况。(3)采用日本骨科学会疼痛JOA评分标准评估患者术后神经功能恢复情况[3]:JOA改善率=(术后评分-术前评分)/(17-术前评分)×100%,若改善率>75%为优,50%~74%为良,25%~49%为一般,<25%为差。
1.4.2 影像学评价指标 (1)测量椎体间隙高度变化:在颈椎侧位X线片上测量病变椎体间隙的上下椎体前、中、后缘高度,其平均值即为椎体间隙高度。(2)测量颈椎生理曲度:于齿状突后上缘至第7颈椎椎体后下缘作一直线,C4后缘中点与该直线的垂直距离即为颈椎生理曲度。(3)X线片评价植骨融合[4]:①骨小梁穿过两边界面和椎体前后缘骨桥形成;②椎体与椎间融合器之间无透亮线;③过屈、过伸位X线椎体间相对角度位移≤2°;④有足够的椎体间隙高度,无塌陷和侧弯。部分患者采用颈椎CT评价植骨融合情况,当椎间融合器与邻近终板之间有连续骨小梁通过时即认为达到骨性融合。(4)采用UCLA系统评价植骨融合后邻近节段退变情况[5]。所有影像学数据测量与评估均在GEAW 4.0软件上进行。
1.5 统计学方法 采用SPSS 15.0统计软件包对数据进行处理,术前、末次随访JOA评分、椎体间隙高度及颈椎生理曲度的比较采用配对t检验,以P<0.05为差异有统计学意义。
2 结果
2.1 临床疗效结果 23例患者中22例获得随访,1例因联系方式更改而失访。随访时间为10~23个月,平均18.0个月。手术时间(82.1±36.1) min,其中单节段病变(66.1±20.1) min,双节段病变(96.3±9.1) min,三节段病变(108.2±10.0) min。术中出血量120~260 ml,平均(170.0±43.0) ml。末次随访所有患者四肢麻木、躯干束带感等症状有不同程度减轻,行走功能得到明显改善。术前JOA评分为(9.2±2.2)分,低于末次随访的(15.1±3.3)分,差异有统计学意义(t=6.28,P<0.05);JOA改善率为75.8%;优16例(72.7%),良3例(13.6%),一般3例(13.6%),差0例。所有患者无喉上神经及喉返神经损伤、气管食管瘘、脑脊液漏、颈部及取骨区血肿、伤口感染等并发症发生,无融合器松动、脱出等内固定并发症发生,仅1例患者髂骨供区轻度疼痛,但不影响日常生活。
2.2 影像学结果 按照UCLA评价系统,至末次随访患者均无植骨融合后邻近节段椎间盘退变进展表现。术前椎体间隙高度为(5.80±1.50) mm,低于末次随访的(8.60±2.11) mm,差异有统计学意义(t=4.81,P<0.05)。术前颈椎生理曲度为(3.92±0.48) mm,低于末次随访的(7.85±0.93) mm,差异有统计学意义(t=9.16,P<0.05)。术后9个月随访38个椎体间隙均获得完全骨性融合,融合率为100%,融合时间为3~6个月,平均4.0个月。患者影像学资料详见图1。
3 讨论
自1988年Bagby和Kuslish将钛合金多孔螺纹状椎间融合器(BAK)成功应用于人类腰椎间融合术后,颈椎间融合器的研究和临床应用也开始有了相继报道,并取得了较好的临床效果,进而得到广泛应用。但是孤立的融合器可向前移位压迫刺激食管、气管,向后移位再次压迫脊髓,易出现诸多手术相关并发症[6]。联合颈椎前路钢板系统的使用能明显减低融合器的移位,减少假关节的形成,但是使用钢板螺钉固定不但扩大了手术暴露的范围、手术创伤大,还增加了脊髓损伤的风险,也存在内固定相关并发症:(1)内固定松动、断裂、移位;(2)内固定刺激周围组织、器官(神经、食管),产生发音困难、吞咽困难;(3)钉板边缘易诱发骨化,造成相邻节段椎体退变、骨赘形成,有时产生食管瘘等严重并发症[7-8]。因此,为了寻找更加理想的融合材料和方法,使其既能实现植入后的即时稳定,又能促进融合并很好地重建或维持椎体间隙高度和颈椎生理曲度,国内外学者不断地进行着探索。
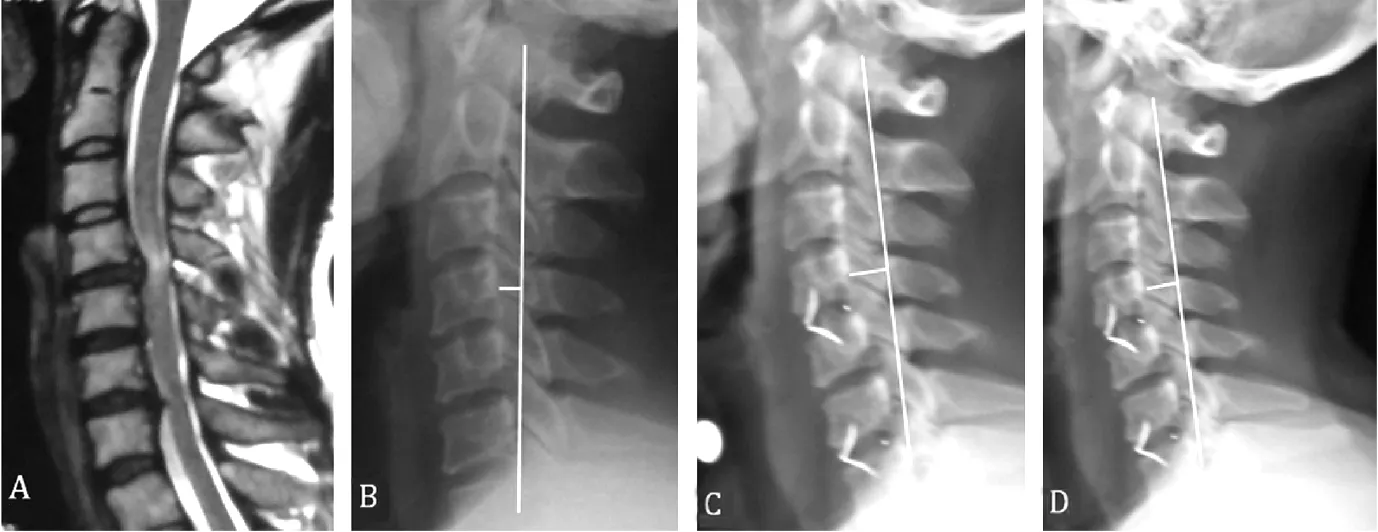
注:患者,男,46岁,脊髓型颈椎病。图A 为术前颈椎MRI示C4~5、C6~7椎间盘突出,颈脊髓受压;图B为术前颈椎侧位X线片示C4~5、C6~7椎体间隙高度及颈椎生理曲度减小;图C为术后颈椎侧位X线片示椎体间隙高度及颈椎生理曲度恢复正常;图D为末次随访颈椎侧位X线片示椎体间隙高度及颈椎生理曲度得到有效维持
图1 患者影像学资料
Figure1 Imaging data of patient
桥式自锁定PEEK椎间融合器由一种独立的生物材料PEEK椎间融合器和自锁定钛夹(MC)固定嵌片组成。PEEK是一种全芳香半结晶性高聚物,具有多种优良的综合性能,如对氧高度稳定,具有坚韧、高强度、高刚性和耐蠕变的特点。PEEK具有以下优点:(1)生物相容性好。有研究表明PEEK复合材料具有良好的生物相容性,植入骨组织后可与之良好接合,并引导新骨生长[9]。(2)弹性模量与人体骨组织非常接近,强度与皮质骨相当,从而避免了应力遮挡和应力集中。(3)材料具有可透光性,在X线下即可清晰观察骨生长融合情况,评价植骨融合疗效,且不妨碍CT、MRI检查,这是金属材料内置物无法比拟的。(4)上下两端开口的环状设计加大了椎间融合器的横截面积,使植骨与椎体间有足够大的接触面积,可促进融合,以获得满意的融合率。(5)稳定性好。椎间融合器表面为锯齿状凸面,通过配套插片加以固定,可提供术中即刻稳定及术后长期稳定,避免了术后内固定相关并发症的发生。(6)手术操作简便,无需联合钢板内固定,暴露范围少,对机体组织损伤小,缩短手术时间,可微创植入,减少了过度牵拉导致的喉上、喉返神经损伤及食管瘘的发生。(7)减少了植骨量。只需在髂骨开一小骨窗刮取少量松质骨,避免了取三面皮质骨对所取髂骨块塑形要求较高的缺陷,也减少了大切口取骨产生的血肿、术后供骨区疼痛、股外侧麻木等并发症的发生。鉴于上述诸多优点,近年来桥式自锁定PEEK椎间融合器得到了广泛的应用。
应用桥式自锁定PEEK椎间融合器需具有以下指征[10]:(1)症状性颈椎退变患者(如颈椎不稳、脊髓型颈椎病)、神经根型颈椎病、局灶性后纵韧带骨化伴明显相应症状者。(2)急性椎间盘突出伴症状明显者。(3)无椎体骨折的不稳定性颈椎创伤者。由于椎间融合器是由外部结构将椎体撑开而恢复椎体间隙高度,并通过“撑开-压缩”张力带效应促进植骨融合,骨质疏松症患者因椎体界面承受压力的能力较差,术后易出现融合器下沉,故禁用于严重骨质疏松症患者。对于不稳定的颈椎椎体骨折患者,因维持运动的单位韧带和骨性结构缺如,不能发挥“撑开-压缩”机制,融合器植入后无法重建损伤节段的稳定性。此外,对3个节段以上病变需行后路手术或长段后纵韧带骨化需行椎体次全切除者不适用。
应用桥式自锁定PEEK椎间融合器需注意以下几点:(1)该技术主要适用于脊髓压迫来自前方且位于椎体间隙平面患者,对连续型后纵韧带骨化、骨性颈椎管狭窄、黄韧带肥厚所导致的脊髓受压者不宜使用;(2)术中需选择大小合适的椎间融合器,以确保内置物的稳定性,增强其牢固性;(3)彻底解除脊髓及神经根的压迫是手术获得良好疗效的前提,因此,术中必须彻底切除椎间盘及椎体后缘增生骨赘,两侧松解至钩椎关节,必要时可切除后纵韧带。(3)刮匙处理终板,使之在保持完整的前提下有血液渗出,以提供良好的植骨床。
本研究发现,末次随访患者神经功能均有不同程度的改善,术前JOA评分低于末次随访,JOA改善率为75.8%,且无手术并发症发生;术后影像学检查证实融合节段均获得骨性融合,椎体间隙高度和颈椎生理曲度均高于术前。表明应用桥式自锁定PEEK椎间融合器治疗颈椎病的临床疗效肯定。
Chu等[11]报道有10%~20%的患者因椎间融合后相邻椎间盘代偿性活动增加,引起退变不稳而发生了相邻节段椎间盘退变并出现相应的临床症状需再次手术治疗。本研究患者未发现该并发症,可能与以下原因有关:(1)桥式自锁定PEEK椎间融合器不同于传统融合器,其解剖外形特点及固定片的设计增加了内置物的稳定性,可有效避免过度撑开椎体间隙导致的术后邻近节段椎间盘退变[12]。(2)桥式自锁定PEEK椎间融合器的形状设计符合颈椎结构解剖特点,可减缓因颈椎生理曲度变小引起的颈椎生物力学异常而导致的邻近节段椎间盘退变[13]。(3)与传统钢板固定相比,其刚度较低,减少了对邻近节段的力学影响,减缓了相邻节段椎间盘的退变。(4)本研究只随访了22例患者,数量较少。(5)本研究平均随访时间为18.0个月,随访时间相对较短。
综上所述,颈椎前路椎间盘切除减压后应用桥式自锁定PEEK融合器植骨融合,操作简单,手术创伤小,植骨融合率高,能有效恢复椎体间隙高度及颈椎生理曲度,临床效果满意,为治疗颈椎病较好的方法之一。但本研究还存在以下不足:(1)采用JOA评分对患者术前及末次随访进行比较和分析,只能反映脊髓及神经损伤的严重程度和术中减压是否彻底,并不能说明不同融合方式的优劣;(2)随访时间较短,不能完整评价其对相邻节段退变的影响;(3)本研究未将传统钢板螺钉固定手术方式作为对照组,使本研究结果说服力有限。因此,今后还有待于进行更深入的研究。
1 Yamazaki T,Yasuda S,Uemura K,et al.New instrument for creating bone graft cavities for anterior cervical decompression and fusion:the anterior fusion spinal fork[J].Neurol Med Chir (Tokyo),2012,52(9):691-694.
2 Song KJ,Taghavi CE,Hsu MS,et al.Plate augmentation in anterior cervical discectomy and fusion with cage for degenerative cervical spinal disorders[J].Eur Spine J,2010,19(10):1677-1683.
3 Emery SE,Bohlman HH,Bolesta MJ,et al.Anterior cervical decompression and arthrodesis for the treatment of cervical spondylotic myelopathy.Two to seventeen-year follow-up[J].J Bone Joint Surg Am,1998,80(7):941-951.
4 Lin CN,Wu YC,Wang NP,et al.Preliminary experience with anterior interbody titanium cage fusion for treatment of cervical disc disease[J].Kaohsiung J Med Sci,2003,19(5):208-216.
5 Yang JY,Lee JK,Song HS.The ifmpact of adjacent segment degeneration on the clinical outcome after lumbar spinal fusion[J].Spine (Phila Pa 1976),2008,33(5):503-507.
6 Wu WJ,Jiang LS,Liang Y,et al.Cage subsidence does not,but cervical lordosis improvement does affect the long-term results of anterior cervical fusion with stand-alone cage for degenerative cervical disc disease:a retrospective study[J].Eur Spine J,2012,21(7):1374-1382.
7 Ahn JS,Lee JK,Kim JH.Comparative study of clinical outcomes of anterior cervical discectomy and fusion using autobone graft or cage with bone substitute[J].Asian Spine J,2011,5(3):169-175.
8 Joo YH,Lee JW,Kwon KY,et al.Comparison of fusion with cage alone and plate instrumentation in two-level cervical degenerative disease[J].J Korean Neurosurg Soc,2010,48(4):342-346.
9 Wilkinson JS,Mann SA,Stoneham GW,et al.Comparison of post-operative lordosis with the PEEK cage and the cervical plate[J].Can J Neurol Sci,2011,38(1):72-77.
10 Zhou J,Li X,Dong J,et al.Three-level anterior cervical discectomy and fusion with self-locking stand-alone polyetheretherketone cages[J].J Clin Neurosci,2011,18(11):1505-1509.
11 Chu CW,Kung SS,Tsai TH,et al.Anterior discectomies and interbody cage fusion without plate fixation for 5-level cervical degenerative disc disease:a 5-year follow-up[J].Kaohsiung J Med Sci,2011,27(11):524-527.
12 Yang JJ,Yu CH,Chang BS,et al.Subsidence and nonunion after anterior cervical interbody fusion using a stand-alone polyetheretherketone (PEEK) cage[J].Clin Orthop Surg,2011,3(1):16-23.
13 Lied B,Roenning PA,Sundseth J,et al.Anterior cervical discectomy with fusion in patients with cervical disc degeneration:a prospective outcome study of 258 patients (181 fused with autologous bone graft and 77 fused with a PEEK cage)[J].BMC Surg,2010,10(1):10.
本文链接
颈椎病又称颈椎综合征,是颈椎骨关节炎、增生性颈椎炎、颈神经根综合征、颈椎间盘脱出症的总称,是一种以退行性病理改变为基础的疾患。主要由于颈椎长期劳损、骨质增生,或椎间盘脱出、韧带增厚,致使颈椎脊髓、神经根或椎动脉受压,出现一系列功能障碍的临床综合征。表现为颈椎间盘退变本身及其继发性的一系列病理改变,如椎节失稳、松动;髓核突出或脱出;骨刺形成;韧带肥厚和继发的椎管狭窄等,刺激或压迫了邻近的神经根、脊髓、椎动脉及颈部交感神经等组织,引起一系列症状和体征。颈椎病可分为:颈型颈椎病、神经根型颈椎病、脊髓型颈椎病、椎动脉型颈椎病、交感神经型颈椎病、食管压迫型颈椎病。

