胃癌根治术后患者预后的多因素分析
张军喜 李发中 李宗辉 柴健 马颖辉 董玮
胃癌是最常见的恶性肿瘤之一,多数患者胃癌被确诊时已到中、晚期,其高发病率和病死率严重威胁着人们的身体健康。目前,根治性手术仍是胃癌的主要治疗方式之一,然而,患者术后远期疗效不甚理想。很多学者对影响胃癌患者预后的因素进行了探讨,报道不尽一致[1-2]。本文对289例胃癌根治术后患者的生存情况及其影响因素进行分析,旨在了解影响胃癌根治术患者预后的相关因素,为临床判断预后及选择合理治疗方案提供参考,现报道如下。
1 资料与方法
1.1 一般资料 收集2006年1月-2009年1月在洛阳市中心医院接受胃癌根治术的患者完整的病历资料,共347例,所有患者均经病理诊断证实。289例获得随访结果,其中男221例,女68例;年龄34~80岁,中位年龄60.25岁;根据国际抗癌联盟(UICC)TNM分期标准:Ⅰ、Ⅱ、Ⅲ、Ⅳ期分别为41例、81例、115例、52例。
1.2 方法 通过病历资料提供的信息进行电话和信件随访,随访截止日期2014年1月1日,参考文献[3-4]初步拟定纳入分析的因素是:年龄、性别、瘤体部位、瘤体大小、病理类型、浸润深度、组织分化、手术方式、TNM分期、淋巴转移、综合治疗等。
1.3 统计学处理 采用SPSS 17.0统计学软件对数据进行处理,生存时间、生存率的计算采用寿命表法,影响胃癌根治术预后的风险因素分析采用COX比例风险回归模型,以P<0.05表示差异有统计学意义。
2 结果
2.1 一般情况 本研究观察终点为术后5年,有随访结果的289例胃癌患者中,截至随访终点,死亡85例,中位生存时间(45.23±7.58)个月,1、3和5年生存率分别是77.98%、53.64%和41.26%。
2.2 影响预后的单因素分析 全变量模型:病理类型、浸润深度、组织分化、TNM分期、淋巴转移、综合治疗等是影响胃癌根治术预后的主要因素(P<0.05),性别、年龄、瘤体部位、瘤体大小、手术方式等与胃癌根治术预后无关(P>0.05),见表1。
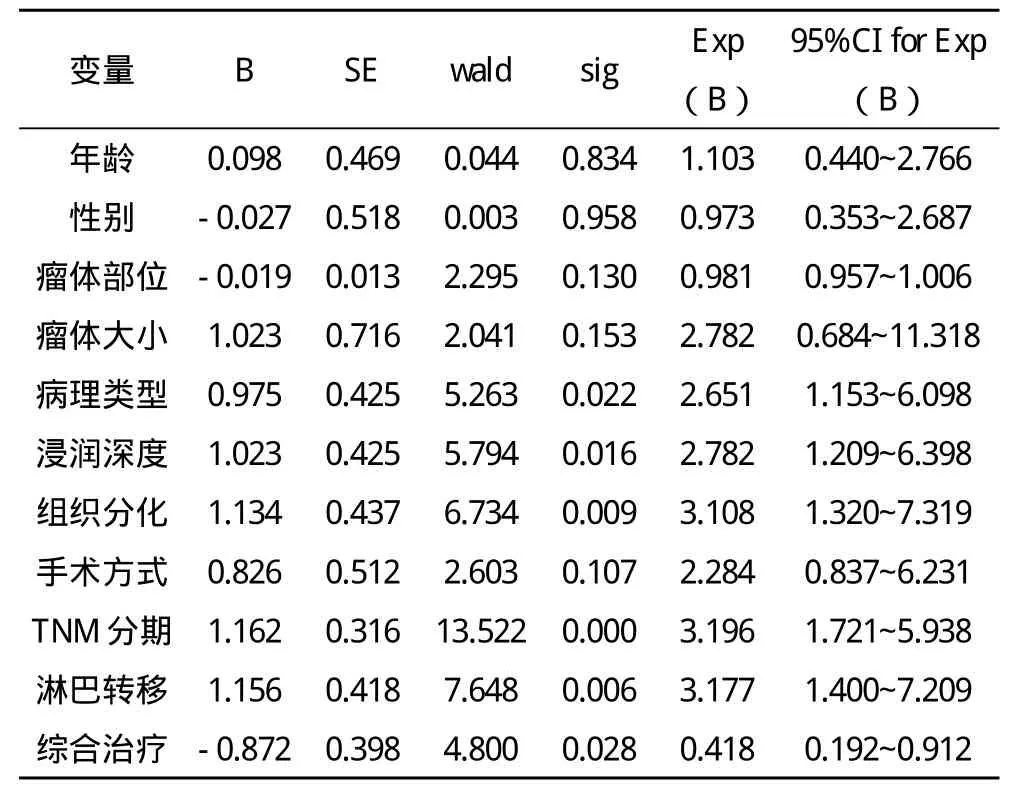
表1 影响胃癌根治术预后生存的单因素分析
2.3 影响预后的多因素分析 用逐步回归模型(变量进入模型,P≤0.05;变量剔除模型,P>0.05):最终保留在模型的因素有:淋巴转移(RR=3.284)、组织分化(RR=3.168)、浸润深度(RR=3.174)和TNM分期(RR=3.152),TNM分期Ⅰ期、Ⅱ期、Ⅲ期和Ⅳ期5年生存率分别是76.12%、54.36%、40.18%和29.26%,见表2。
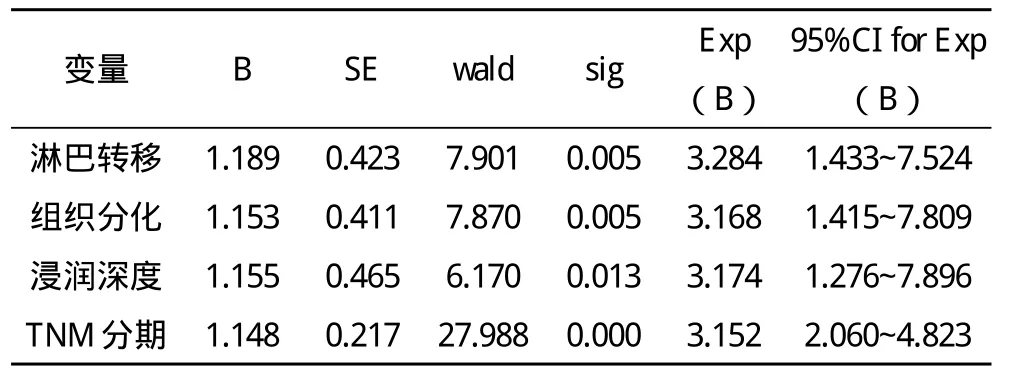
表2 影响胃癌根治术后多因素分析
3 讨论
胃癌的诊治水平虽然有了很大的提高,但胃癌起病隐匿,出现临床症状时肿瘤已发展到中、晚期,且易通过淋巴系统转移及术后易复发,预后较差,文献报道5年生存率在20%~50%[5],与本研究结果一致。临床工作者先后对影响胃癌根治术预后的因素进行了探讨,报道不尽一致,现将本研究结果进行一讨论。
淋巴结转移与胃癌预后有密切关系[6]。本研究单因素和多因素分析显示:有无淋巴结转移(局部淋巴结转移、远处转移),与无淋巴结转移比较,有淋巴结转移患者死亡的风险增加3.28倍,提示局部淋巴结转移是胃癌患者的独立预后因素。标注在行胃癌根治术时应尽可能扩大淋巴结清扫范围,必要时对哨兵淋巴结进行活检,以期提高胃癌患者的生存率。肿瘤组织学分化越低预后越差,即胃癌根治术预后与组织分化程度呈正相关。本研究发现胃癌组织分化分级(按高、中、低顺序)每增加一级,患者死亡的风险增加3.168倍(95%CI: 1.415~7.809),与国外研究结果一致[3]。有研究表明,肿瘤浸润深度与胃癌预后显著相关[7]。意大利学者Marchet等[8]对1853例胃癌根治术后资料分析认为肿瘤浸润深度是影响胃癌预后的独立因素。本研究单因素分析显示,随着瘤体浸润深度的增加,5年生存率逐渐降低,多因素分析结果与意大利学者研究结果一致。可能的原因是胃壁全层均含有丰富的血管和淋巴管,随着肿瘤浸润深度的增加,肿瘤细胞通过血管和淋巴管向全身转移的机会越多,肿瘤种植转移的几率也会增加。按照第UICC/AJCC(TNM)分期标准,肿瘤的TNM分期主要是以肿瘤的浸润深度和淋巴结转移度为依据,可以反映肿瘤的生长和转移特点,随着肿瘤的浸润深度的增加,患者的预后也会愈差[7]。本研究结果表明:TNM分期Ⅰ期、Ⅱ期、Ⅲ期和Ⅳ期5年生存率分别是76.12%、54.36%、40.18%和29.26%。多因素分析显示TNM分期每增加1级,患者死亡的风险增加3.152倍(95%CI:2.060~4.823)。提示胃癌患者的预后在很大程度上取决于治疗时所处的TNM分期。因此,在TNMⅠ期、Ⅱ期进行根治手术可有效提高患者的生存率。
本组资料中,年龄、性别、瘤体部位、瘤体大小、病理类型、手术方式、综合治疗等与患者预后无关,与其他学者观点不尽一致。潘原等[9]进行多因素分析表明近端胃癌根治术后5年生存率低于远端胃癌,胃贲门癌是影响预后的独立因素。Radoslaw等[10]认为大体分型也是影响胃癌术后生存的独立因素。还有研究认为印戒细胞癌预后显著差于其他病理类型(P<0.05)[11]。Pacelli等[12]发现辅助化疗对总体预后无明显改善。这些不同结果的产生,可能与研究对象来自不同人种、地区或是样本数不同以及预后因素之间的相互影响有关,还有待于进一步研究。单因素分析时病理类型、术后综合治疗是影响预后的因素,多因素分析时与预后的相关性未得到统计学支持,但并不表明这些因素的作用不重要。由于某些因素在组间的分布不均衡及各因素间的相互关联,往往不能得出可靠的、独立的预后因素。样本量少、因素间的多重共性均是导致不能入选模型的原因,另外,一些肿瘤相关因子、基因表达等也是预后因素。但本研究并未有涉及。此还需要进一步扩大病例数量或改变分析方法继续探讨。
总之,胃癌根治术后远期生存不理想,淋巴转移、组织分化、浸润深度和TNM分期是预后的独立危险因素。在临床工作中,结合患者临床表现及利用胃镜进行病理学诊断,尽早发现早期胃癌方为上策。
[1]张立志,马德青.影响胃癌术后患者预后的相关因素分析[J].齐齐哈尔医学院学报,2012,3(7):919-921.
[2]王峰,高阳,张力,等.胃癌术后预后因素的COX比例风险回归[J].青岛医药卫生,2010,42(4):252-255.
[3]Hu X,Tian D Y,Cao L,et al.Progression and prognosis of gastric stump cancer[J].J Surg Oncol,2009,100(6):472-476.
[4]马海波,王爽,魏克飞.胃癌根治术后生存状态的5年随访[J].世界华人消化杂志,2010,18(27):2920-2924.
[5]Paoletti X,Obak K,Burzykowski T, et al.Benefit of adjuvant chemotherapy for resectable gastric cancer: a meta analysis[J].JAMA,2010,303(17):1729-1737.
[6]Wu A W,Ji J F, Yang H.Long-term outcome of a large series of gastric cancer patients in China[J].Chinese J Cancer Res,2010,22(3):167-175.
[7]施伟,王建,张梅玲,等.1340例胃癌根治术后患者预后的多因素分析[J].南京医科大学学报(自然科学版),2011,31(9):1310-1315.
[8]Marchet A,Mocellin S,Ambrosi A,et al.The prognostic value of N-ratio in patients with gastric cancer:validation in a large,multicenter series[J].Eur J Surg Oncol,2008,34(2):159-165.
[9]潘原,薛强,梁寒,等.320例胃癌根治术后预后因素的回顾性分析[J].中国肿瘤临床,2008,35(13):739-743.
[10]Radoslaw J,Elfriede B,Arnulf H.Prognostic relevance of demographics and surgical practice for patients with gastric cancer in two centers: in Poland versus Germany[J].Gastric Cancer,2011,14(3):234-241.
[11]Piessen G,Messager M,Leteurtre E,et al.Signet ring cell histology is an independent predictor of poor prognosis in gastric adenocarcinoma regardless of tumoral clinical presentation[J].Ann Surg,2009,250(6):878-887.
[12]Pacelli F,Sanchez A M,Covino M,et al.Improved outcomes for rectal cancer in the era of preoperative chemoradiation and tailored mesorectal excision: a series of 338 consecutive cases[J].Am Surg,2013,79(2):151-161.

