表面活性剂对腈纶碱法水解的影响
李 慧,李青松,朱 林,周 超,朱新生
(苏州大学纺织与服装工程学院,江苏苏州215021)
腈纶废丝及废弃腈纶织物的水解回收利用具有重要的现实意义。腈纶中的大量的活性基团腈基会水解形成羧基、酰胺基等,可用于制备油田钻井液的处理剂、高吸水性树脂、铸造粘合剂等。腈纶水解方法主要有酸法水解[1]、酶水解、加压水解[2-3]和碱法水解等[4-5]。但这些方法中,存在酸碱浓度偏高、水解产物结构多变性、水解效率低等缺点,陈兆文等[5]尝试用乙醇和水混合溶剂调整聚丙烯腈(PAN)水解作用,发现36%的腈基转化为羧基。作者在腈纶碱法水解过程中加入表面活性剂,研究了表面活性剂对其水解反应的影响。
1 实验
1.1 原料及仪器
腈纶浆粕:上海兰邦工业纤维有限公司产;腈纶短纤维:常熟绣珀纤维有限公司提供;氢氧化钠:分析纯,国药集团化学试剂有限公司产;36% ~38%盐酸:分析纯,常州市武卫试剂有限公司产;醋酸钠(NaAc):分析纯,天津市恒兴化学试剂制造有限公司产;十二烷基苯磺酸钠:化学纯,上海凌峰化学试剂有限公司产;吐温80:分析纯,市售;阳离子表面活性剂1427:南京栖霞山印染助剂厂;聚丙烯酸钠(PAAS)增稠剂:市售。
电子天平:奥豪斯仪器有限公司制;HP500型水浴振荡器:南通宏大实验仪器有限公司制;NDJ-8S数字式黏度计:上海尼润智能科技有限公司制;Nicolet 5700型红外光谱仪:美国热电公司制;DDB-303A型电导率仪:上海雷磁仪器制造厂制。
1.2 实验步骤
称取定量的PAN浆粕或者腈纶短纤维,将氢氧化钠及一定量的表面活性剂溶于水后加入到250 mL的锥形瓶中,将纤维加入到锥形瓶中,恒温振荡器温度控制指定温度,加热水解处理2 h,取出、用稀盐酸中和滴定、电导率法判断滴定终点,并对清洗干燥处理后的纤维进行表征。
1.3 分析测试
电导率:用1.2 mol/L稀盐酸滴定水解产物及电导率仪测定水解产物的电导率,作出曲线图。
吸湿性:将水解产物水洗至pH值为8左右,在烘箱中干燥后拿出,置于干燥器中冷却称重,然后在室温下进行吸湿实验,称重,计算吸湿率。
黏度:采用数字式黏度计在标准状态下测定反应体系黏度。
红外光谱:将水解产物干燥后剪成碎片,接近固体粉末,用红外光谱仪在标准状态下测定。
元素分析:采用1108型自动元素分析仪测定水解产物中C,N,H的含量,并采用Eager 200软件进行分析。
转化率:根据电导率和盐酸滴定量绘制曲线,计算腈纶水解腈基转化为羧基的转化率。
2 结果与讨论
2.1 表面活性剂对水解反应的影响
由图1可看出,PAN浆粕中,2 244 cm-1对应于C≡N的伸缩振动吸收峰,1 741,1 240,1 050 cm-13个峰则来自于共聚单元丙烯酸酯吸收峰,而1 376 cm-1对应于甲基弯曲变形吸收峰,1 454 cm-1对应于主链亚甲基弯曲变形吸收峰。水解处理后的PAN浆粕的红外光谱可看出,一方面,浆粕中的共聚单元丙烯酸甲酯全部转化为羧基;另一方面,3种处理后的浆粕的腈基转化为极性的羧基(1 410 cm-1和 1 575 cm-1)和酰胺基(1 650 cm-1)。但是,基于红外光谱图较难定量分析表面活性剂对水解的促进作用。
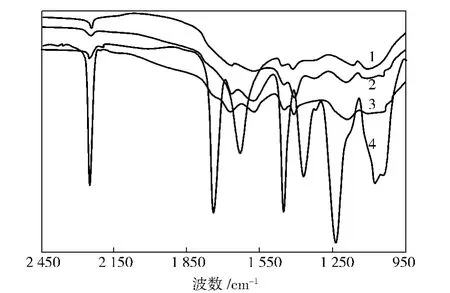
图1 不同条件下水解的PAN浆粕红外光谱Fig.1 IR spectra of PAN pulp under different hydrolysis condtions
由表1看出,在阳离子表面活性剂存在下所得水解纤维吸湿性最大,表明更多的腈基转化为极性的羧基、酰胺基。当浆粕水解物亲水性增大后,其水溶性也增加。根据Stokes-Einstein黏度方程可得,水解处理后浆粕的水溶液粘度会降低。同样也发现阳离子表面活性剂加快了PAN浆粕的水解作用。
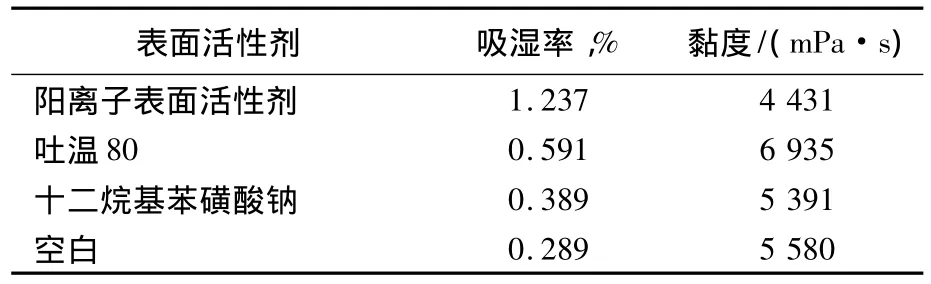
表1 不同表面活性剂对PAN浆粕水解反应的影响Tab.1 Effect of surfactants on hydrolysis of PAN pulp
2.2 阳离子表面活性剂作用
由图2可见,当PAN水解液中不含有阳离子表面活性剂时,对水解产物滴定时,盐酸用量约11 mL,与理论用量非常接近(用于0.5 g氢氧化钠滴定的量),即PAN中的腈基几乎没有转变为羧基。而当添加阳离子表面活性剂后,滴定时盐酸用量约为8 mL,意味着生成的羧基消耗了部分氢氧化钠而使盐酸用量降低。
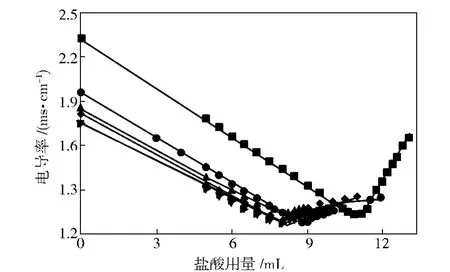
图2 不同的阳离子表面活性剂用量时腈纶水解物盐酸滴定曲线Fig.2 Hydrochloric acid titration curves of PAN hydrolysate while using different amounts of cationic surfactants
由图2还可见,盐酸用量减少后,电导率经由最低点而继续上升时,其斜率与无阳离子表面活性剂时不同,斜率减小,说明表面活性剂的加入,确实减少了盐酸的用量,但减少的盐酸用量与表面活性剂用量没有直接关系,且盐酸减少量与阳离子活性剂用量无关。电导率从最低点回升时,加入阳离子表面活性剂的滴定曲线的斜率相同,表明阳离子表面活性剂加入也没有改变回升曲线的斜率。阳离子表面活性剂加快了PAN的水解作用,且较小斜率回升曲线意味着PPAS形成。
由于阳离子表面活性剂存在加快水解作用,设计一个4因子3水平的实验,按照正交表的选择原则选择正交表L9(34),进行实验,以确定其用量与其他水解参数之间的关系,结果见表2。
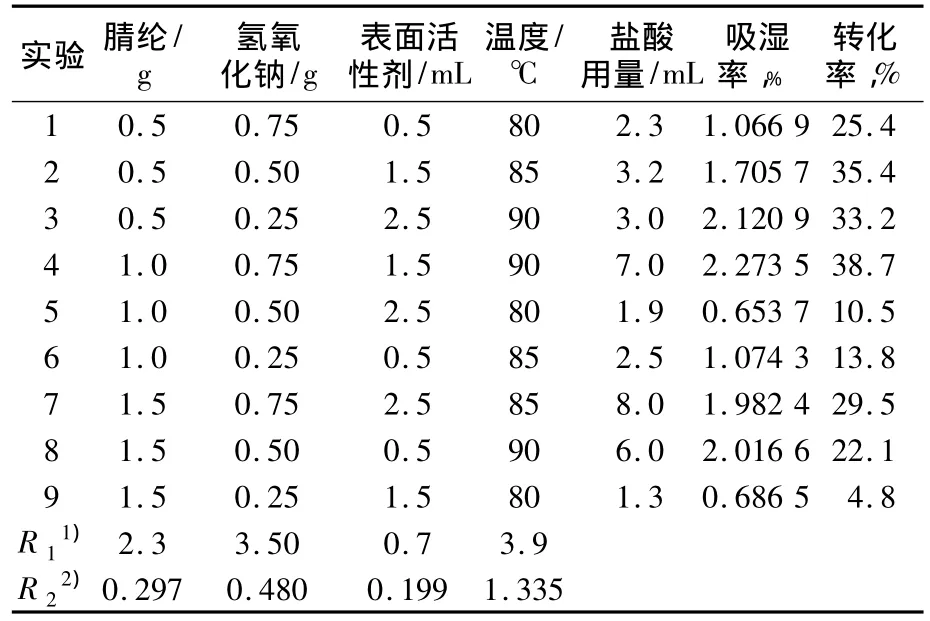
表2 实验方案和结果分析Tab.2 Experimental scheme and result analysis
由表2可见,温度变化时,水解液滴定时盐酸用量和所得水解物的吸湿性差异最大,即反应温度是最重要因素,其次是氢氧化钠用量,再次是腈纶用量,而阳离子表面活性剂的影响较小。吸湿性与盐酸用量显示出的一致性。盐酸用量越多,形成的羧基量越多,吸湿性越强。基于盐酸用量,选出最优的水平组合是 PAN 1.5 g,NaOH 0.75 g,阳离子表面活性剂2.5 mL,实验温度90℃。
从表3可以看出,水解产物各元素组分的比例发生了较大改变,其中实验4号所得水解物的氮含量仅为16.40%,而原始腈纶中的氮含量为23.57%,转化很明显。若当腈基转变为酰胺基团时,N/C比值变化较小;而当腈基转变为羧基时,N/C比值急剧降低。实验3和4中,会有较大量的腈基转变为羧基。
表3 腈纶水解产物中各元素的组成Tab.3 Element composition of PAN hydrolysate
2.3 定量确定羧基含量
由图3可以看出,0.5 g氢氧化钠需大约1.2 mol盐酸11 mL中和,这与理论值比较接近。继续滴定盐酸时,溶液的电导率急剧上升。

图3 不同浓度醋酸钠和氢氧化钠的混合溶液的滴定曲线Fig.3 Titration curves of sodium acetate and sodium hydroxide blend solution with different blend ratio
当醋酸钠存在时,出现低斜率的曲线部分,然后再次出现斜率激增的曲线部分,且激增的斜率与纯氢氧化钠溶液类似。这说明斜率较小的曲线部分意味着羧酸钠存在,即使羧酸钠转变为羧酸的过程。羧酸钠用量增加,滴定用的盐酸量越多。
从图4可见,盐酸滴定增稠剂和氢氧化钠的混合溶液的滴定曲线形状及变化趋势与羧酸钠情况非常一致,斜率较小的曲线意味着羧基钠转变为羧酸。电导率最低转变点前移和下移是由于氢氧化钠用量减少所造成的。
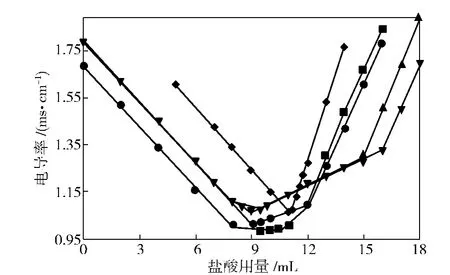
图4 不同浓度的PAAS和NaOH的混合溶液的滴定曲线Fig.4 Titration curves of PAAS and NaOH blend solution with different blend ratio
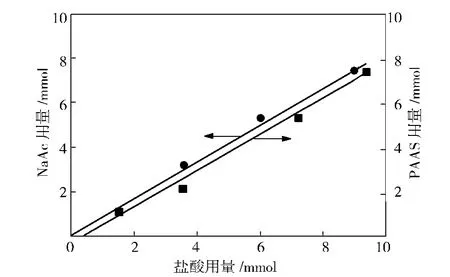
图5 盐酸用量与PAAS和NaAc含量关系Fig.5 Relationship between hydrochloric acid amount and PAAS and NaAc contents
从图5可见,盐酸用量与羧基含量之间的关系曲线。NaAc拟合曲线方程为:
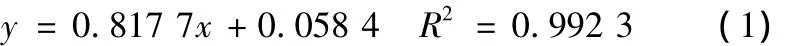
PAAS拟合曲线议程为:
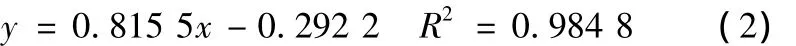
两种化合物拟合曲线趋势线近似平行,即PAAS与NaAc拟合曲线的斜率非常接近。比较PAAS与NaAc滴定结果发现,可以根据盐酸的用量直接计算腈纶水解后的羧酸钠的生成量,进而计算产物的转化率(以摩尔计),见表2。
从表2可以看出,不同条件下腈纶水解的程度不同,其中正交实验 4(即 1 g PAN,0.75 g NaOH,1.5 mL阳离子表面活性剂,90℃,时间2 h)腈基转化为羧基的转化率高达38.7%,实际达到 6.85 mmol/g。
3 结论
a.腈纶水解过程中,表面活性剂加速腈基的水解,其中以阳离子表面活性剂最为明显。
b.最佳的碱性水解条件为腈纶短纤维1 g,NaOH 0.75 g,阳离子表面活性剂1427 1.5 mL,温度90℃,时间2 h,腈基转化为羧基的转化率(以摩尔计)为38.7%。
[1]Krentsel L B,Kudryavtsev Y V,Rebrov A I,et al.Acidic hydrolysis of polyacrylonitrile:effect of neighboring groups[J].Macromolecules,2001,34(16):5607 -5610.
[2]Dietrich G.Reaction products of polyacrylonitrile with dicyandiamide[J].Die Angew Makromol Chem,1981,41(1):57 -67.
[3]王杰,宋宏陛,崔书文.聚丙烯腈废料的催化加压水解[J].化学工程,1989,19(3):20-22.
[4]钟玉莲,安树林,何立刚.聚丙烯腈系高吸水纤维的制备及性能表征[J].天津工业大学学报,2009,28(1):16-17.
[5]陈兆文,徐文国.PAN纤维部分水解法制备离子交换纤维[J].北京理工大学学报,2008,28(2):177-180.

