硅溶胶-纳米金修饰金电极电化学发光法测定苦参碱的研究
罗 应,李利军,邓春燕,程 昊,孙 科,李彦青
(广西工学院 生物与化学工程系,广西 柳州 545006)
苦参碱(Matrine,MT,结构式见图1)是从豆科槐属植物苦豆子(Sophora alopecuroides L)的干燥根、植株、果实中提取的一种具有广泛生物活性的生物碱,具有镇咳、护肝、保肝、镇痛、消炎抗菌、清热利尿、抗肿瘤、抗过敏、抗心率失常等多种药理作用[1]。目前,关于苦参碱的测定方法有高效液相色谱法[2-3]、毛细管电泳法[4-5]、直接电化学法[6]、气相色谱法[7]、液相色谱质谱联用法[8]等。但这些方法或操作繁琐,或涉及有毒试剂,或使用的仪器设备贵重以及需专业的技术人员。与之相比,电化学发光法的选择性好、灵敏度高、操作简单。因此,研究和建立简单、快速、灵敏的苦参碱电化学发光分析新方法具有重要的理论意义和潜在的应用价值。
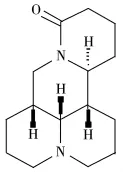
图1 苦参碱的分子结构Fig.1 Molecular structure of matrine
传统的电化学发光(ECL)研究仅限于在裸电极/电解液界面上,而电极表面的分子剪裁、微结构的设计及其潜在应用价值的研究,提高了电化学发光的灵敏度,将其应用推进到一个新的阶段。化学修饰电极在提高选择性和灵敏度方面具有独特的优越性,修饰电极表面上的微结构可提供多种能利用的势场,使待测物能够进行有效的分离富集,基于控制电极点位还可进一步提高其选择性[9]。目前,有关修饰电极的研究已有报道。郭志慧等[10]用Nafion膜修饰电极,周谷珍等[11]用Self-Assembling(SA)膜法修饰电极,Bard等[12]用Langmuir-Blodget(LB)膜法修饰电极。但这些方法都存在不足之处,如Nafion膜的传质过程较慢[13],自组装膜在反复的电压扫描时不稳定;LB膜易被有机溶剂破坏而剥离电极等。本文采用溶胶-凝胶法对电极进行了修饰。
硅溶胶是二氧化硅胶体微粒在水中均匀扩散形成的乳白色半透明胶体溶液,可形成三维网络结构,具有较好的生物相容性、物理刚性、化学惰性、热稳定性及在水中几乎不溶胀等性质[14]。硅溶胶具有成膜溶解的特性,但在成膜时收缩较大、易龟裂,为克服这个缺点,可添加水溶性乳液作为辅助成膜物,如聚乙烯醇(PVA)。纳米金具有高比表面积、高表面活性及良好的导电性等特性[15],因其可提高电极与表面修饰物之间的电子传递,增加电极表面的反应位点,而被广泛应用于修饰电极。但将硅溶胶与纳米金制成混合液修饰金电极用于联吡啶钌体系中的报道较少。本文将硅溶胶、聚乙烯醇(PVA)、L-半胱氨酸按比例混合制成复合物溶液,再将纳米金与复合物溶液超声混合后作为电极修饰材料,实验结果表明此修饰电极对联吡啶钌具有很好的电化学和电化学发光特性。据此建立了电化学发光测定苦参碱的新方法,并将其成功应用于药片中苦参碱含量的测定。
1 实验部分
1.1 仪器与试剂
MPI-E型电致化学发光分析系统(西安瑞迈电子科技有限公司);DL-60D型超声波清洗器(上海之信仪器有限公司);XW-80A型旋涡混合器(上海精科实业有限公司);EF20 pH计(梅特勒-托利多仪器上海有限公司)。电化学实验采用三电极系统:硅溶胶-纳米金修饰的金电极作为工作电极,Pt丝电极为对电极,Ag/AgCl(饱和KCl溶液)为参比电极。
1.5×10-4mol/L苦参碱标准储备液:准确称取0.003 7g苦参碱(中国药品生物制品检定所),用水定容于100 mL的棕色容量瓶中,超声脱气后冷藏于冰箱中(4℃)备用;1.0×10-3mol/L联吡啶钌储备液:准确称取六水合三(2,2-联吡啶)氯化钌(购于Aldrich公司)0.018 7 g,用水定容于25 mL的棕色容量瓶中,用超声波除气后放入冰箱中(4℃)冷藏;氯金酸(上海科兴实验室设备有限公司);柠檬酸三钠(台山市粤侨试剂塑料有限公司);PVA4000(广州化学试剂厂);L-半胱氨酸(上海晶纯试剂有限公司);硅溶胶、磷酸氢二钠、磷酸二氢钠、硼酸、四硼酸钠(西陇化工股份有限公司),所用试剂除苦参碱、联吡啶钌为优级纯外,其它均为分析纯。实验用水均为二次石英亚沸水。
1.2 修饰电极的制备
1.2.1 金电极的预处理 修饰前用金相砂纸小心打磨金丝电极(d=1 mm),并在鹿皮上用Al2O3粉(d50=20~50 nm)抛光至镜面,用水冲洗后,依次用水、无水乙醇-水(1∶1,体积比)、水超声清洗,晾干。将其置于0.10 mol/L H2SO4溶液中进行循环伏安扫描,直至得到稳定的循环伏安(CV)曲线,晾干待用。
1.2.2 纳米金的制备 纳米金的制备方法与文献[16]相似。将氯金酸溶液置于数显测速恒温磁力搅拌器上,在600 r/min转速下搅拌加热至沸腾,再加入一定量的柠檬酸三钠,使液体颜色稳定并持续加热一段时间后,停止加热,冷却至室温,得纳米金溶胶。
1.2.3 硅溶胶-纳米金混合溶液的制备 将0.3 mL硅溶胶、0.15 mL L-半胱氨酸(10 mmol/L)、0.2 mL 0.05%的PVA混合,制成硅溶胶混合溶液,再向其中加入0.2 mL纳米金制成硅溶胶-纳米金混合溶液。
1.2.4 硅溶胶修饰金电极与硅溶胶-纳米金修饰金电极的制备 将经过预处理的金电极浸入0.65 mL硅溶胶混合液中,约30 s后取出,在4℃下放置12 h后得硅溶胶修饰金电极;将经过预处理的金电极浸入0.85 mL硅溶胶-纳米金混合液中,约30 s后取出,在4℃下放置12 h后得到硅溶胶-纳米金修饰金电极。
1.3 实验方法
实验在室温下进行,测定发光强度前溶液用超声波除气5 min,所有电位值均相对于参比电极。由MPI-E型电致化学发光工作站分别记录Ru(bpy发光强度I0和Ru(bpy与苦参碱的发光强度I,以相对强度(I-I0)绘制相对峰高强度与苦参碱浓度的校正曲线。工作电极采用硅溶胶-纳米金修饰的金电极,支持电解质为0.1 mol/L磷酸缓冲液(pH 9.0),光电倍增管负高压为800 V,循环伏安扫描速率为100 mV/s。电化学发光检测池如图2所示。
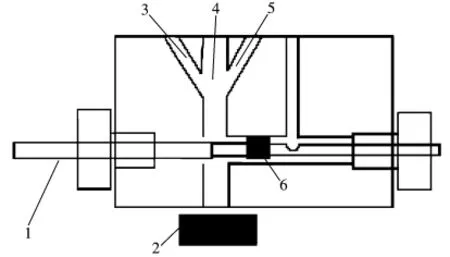
图2 电化学发光检测示意图Fig.2 Schematic diagram of the ECL detection cell
2 结果与讨论
2.1 苦参碱在不同电极上的电化学与电化学发光行为
考察了苦参碱在不同电极上的电化学和电化学发光行为。图3A为苦参碱在硅溶胶-纳米金修饰的金电极(a)、硅溶胶修饰的金电极(b)和裸金电极(c)上的CV图。由图3A可以看出,在相同条件下,硅溶胶-纳米金修饰金电极比硅溶胶修饰金电极对联吡啶钌的增敏效果好,氧化峰电流由8.1 μA增至16.2 μA,增大了2倍。同时,修饰电极与裸电极相比,充电电流明显增大,这是因为硅溶胶、纳米金的加入增加了电极的比表面积和电极表面的反应位点。因此,最终采用硅溶胶-纳米金修饰的金电极作为工作电极。
由图3B可以观察到苦参碱在硅溶胶-纳米金修饰的金电极(a)、硅溶胶修饰的金电极(b)和裸金电极(c)上的发光强度分别为1 549、896和230,硅溶胶-纳米金修饰的金电极上的发光强度大大增加,是裸电极的6.7倍。这表明硅溶胶、纳米金的加入增加了电极的比表面积和电极表面的反应位点,与图3A的结论一致。
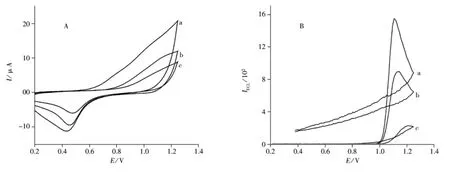
图3 苦参碱在不同电极上的循环伏安图(A)和循环伏安发光图(B)Fig.3 CVs(A)and ECL curves(B)of different electrodes in 1.50×10-5mol/L matrine
2.2 苦参碱对Ru(bpy)电化学与电化学发光行为的增敏作用
实验于0.2~1.25 V的电位范围,考察了Ru(bpy苦参碱与Ru(bpy共存体系在硅溶胶-纳米金修饰金电极上的电化学行为和电化学发光行为(见图4)。从图4A的循环伏安图可以观察到Ru(bpy在0.95~1.15 V左右出现一氧化峰(曲线a),当加入苦参碱后,氧化峰电流升高,峰电位仍在0.95~1.15 V左右(曲线b),该现象表明苦参碱对Ru(bp的电化学反应有明显的增敏作用。同时可以观察到共存体系中仅在1.1 V左右出现1个特征氧化峰,说明苦参碱和Ru(bpy发生电化学共反应前并未被氧化,1.1 V处的电流为Ru(bp氧化所致。
从图4B的电化学发光图观察到,当加入一定浓度的苦参碱时,Ru(bpyECL强度从380(曲线a)增加到12 582(曲线b),在1.0 V开始出现发光信号,到1.1V达到最大值,这与图4A中在1.1 V处氧化峰电流达到最大相符。可见,在相同的条件下,加入苦参碱后,Ru(bpy的发光强度增加约25倍,说明苦参碱对Ru(bp的ECL强度具有显著增强作用。
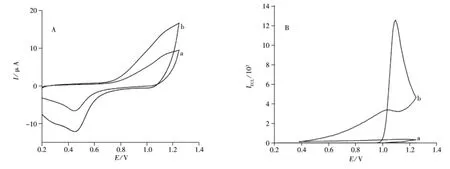
图4 苦参碱对Ru(bpy循环伏安图(A)及电化学发光图(B)的增敏作用Fig.4 CVs(A)and ECL curves(B)of matrine on silica sol-nano-gold modified gold
2.3 缓冲体系以及pH值的选择
缓冲体系及pH值对生物碱类药物与Ru(bpy)2+3的反应有重要影响。本实验考察了0.2 mol/L H3BO3-0.05 mol/L Na2B4O7·10H2O缓冲体系和0.1 mol/L Na2HPO4-0.1 mol/L NaH2PO4缓冲体系对联吡啶钌-苦参碱体系ECL强度和稳定性的影响(见图5)。结果表明,PBS缓冲体系的电化学发光强度明显优于硼酸体系,在酸性环境或碱性过高的情况下ECL强度较低,在pH 9.0时达到最大值,可能是由于溶液中过多的OH-参与电极上的竞争反应造成高价态联吡啶钌(Ⅲ)减少。综合考虑,实验选择pH 9.0的PBS缓冲体系作为最佳介质。
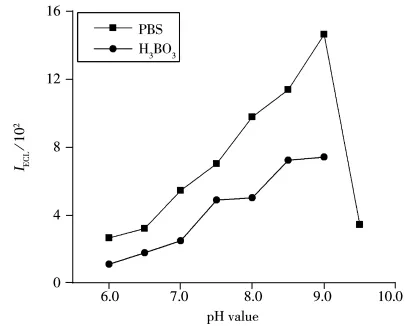
图5 缓冲溶液pH值对电化学发光强度的影响Fig.5 Effect of pH value on ECL intensity
2.4 修饰剂配比的选择
纳米金的浓度不但影响联吡啶钌的ECL强度,而且也影响膜的电子传递及机械强度。实验结果显示,在硅溶胶中不断增加纳米金量的过程中,电极表面的催化活性位点不断增加,其氧化电流增大,ECL强度也随之增强;但当纳米金与硅溶胶的体积比超过1∶3时,过多的纳米金易发生团聚而使电极重复性变差,信噪比降低。因此实验选择纳米金与硅溶胶的体积比1∶3作为修饰剂的最佳配比。
2.5 仪器参数的优化选择
光电倍增管负高压影响仪器检测的灵敏度及稳定性,考察了不同负高压对电化学发光强度的影响,结果表明:随着负高压的增大,发光强度和噪声均增大,为了得到足够的灵敏度和较低的噪音,选择800 V作为本实验的负高压。考察了不同扫描速率(10~100 mV/s)对ECL发光强度的影响,结果表明:随着扫描速率的增大发光强度增大,当达到100 mV/s后基本趋于平衡,这可能是由于较大的扫描速率可以保证在电极表面产生足够的高价联吡啶钌(Ⅲ),同时有限的电极表面积使产生的高价联吡啶钌(Ⅲ)的量达到一定的平衡,因此发光强度值基本不变,但过高的扫描速率会影响仪器的使用寿命。综合考虑,选择100 mV/s作为本实验的最佳扫描速率。
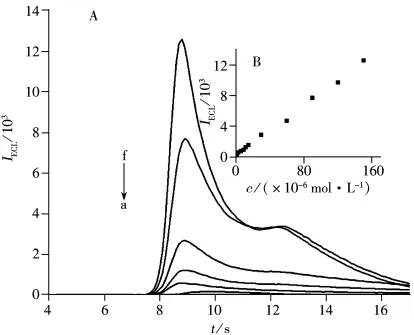
图6 不同浓度苦参碱的电致化学发光曲线Fig.6 ECL curves of different concentrations of matrine cmatrine(a- f):0.15,3.0,12.0,30.0,90.0,150.0 μmol/L;insert:calibration curve of ECL intensity vs.matrine concentration
2.6 方法的评价
在最佳实验条件下,通过电致化学发光工作站记录了不同浓度苦参碱标准溶液的发光强度响应曲线(图6A),以相对峰高对其浓度进行线性回归。苦参碱浓度在1.5×10-7~1.5×10-4mol/L 范围内呈线性关系(r2=0.998 4)(图6B),其线性回归方程为:I=81.023×106c+228.26,检出限(S/N=3)为7.3×10-9mol/L,连续 8次测定 1.5×10-5mol/L的苦参碱,发光强度值的RSD为1.4%。
2.7 样品的分析
取1枚苦参碱栓50 mg(武汉人福药业有限责任公司),溶于5 mL 0.1 mol/L盐酸,过滤后用水定容至200 mL棕色容量瓶中,稀释后其标示浓度为1.00×10-5mol/L,在最佳实验条件下对该样品平行测定5次,其RSD为2.4%,表明此方法的重现性好。
在样品中加入标准溶液进行回收率实验,测得回收率为98%~102%,平均回收率为100%,RSD为1.8%,表明方法具有较好的灵敏度和重现性,可有效用于实际样品的分析。
3 结论
建立了以硅溶胶-纳米金修饰的金电极作为工作电极电化学发光测定苦参碱的方法,充分利用硅溶胶、纳米金的高灵敏电催化作用,提高了电极的电流响应,拓展了线性范围。该修饰电极结合了硅溶胶和纳米金的优点,具有灵敏度高、稳定性好和操作简便等特点,拓宽了联吡啶钌电化学发光体系的应用范围,若将此方法应用于传感器的制备将具有重要意义。
[1]Ren C C,Gao Z N.Chin.J.Anal.Lab.(任超超,高作宁.分析试验室),2009,28(8):47-50.
[2]Liang Y M.Chem.Ind.Technol.Dev.(梁燕明.化工技术与开发),2006,35(7):27-28.
[3]Zhang L,Xu L,Tan X J,Liao Q F,Guo W,Chen X H,Bi K S.Chromatographia,2007,66:115 -120.
[4]Chen Q H,Li P,Cheng F J,Li B,Wu S C,He J.Chromatographia,2009,69:11 -12.
[5]Li L J,Hu D C,Gao W Y,Li Y Q,Kong H X.J.Instrum.Anal.(李利军,胡大春,高文燕,李彦青,孔红星.分析测试学报),2011,30(6):678-682.
[6]Yao H Q,Gao Z N,Han X X,Yu J Q,Du Y.J.Ningxia Univ.:Nat.Sci.Ed.(姚慧琴,高作宁,韩小霞,余建强,杜盐.宁夏大学学报:自然科学版),2004,25(4):346-348.
[7]Jiang L,Wang H X.Anal.Instrum.Newslett.(江林,王海霞.分析测试仪器通讯),1997,7(4):222-227.
[8]Wu Y J,Chen J J,Cheng Y Y.Anal.Bioanal.Chem.,2005,382:1595 -1600.
[9]Dong S J,Che G L,Xie Y W.Chemically Modified Electrodes.Beijing:Science Press(董绍俊,车广礼,谢远武.化学修饰电极.北京:科学出版社),2003:1-10.
[10]Guo Z H,Tang L J,Zhang Z J.Chin.J.Anal.Chem.(郭志慧,唐隆健,章竹君.分析化学),2009,37(1):13-18.
[11]Zhou G Z,Zheng L Y,Li L H,Sun Y X.J.Hunan Univ.Arts Sci.:Nat.Sci.Ed.(周谷珍,郑丽英,李莉花,孙元喜.湖南文理学院学报:自然科学版),2008,20(3):38-41.
[12]Zhang X,Bard A.J.Phys.Chem.,1988,92:5566-5569.
[13]Wang H Y,Xu G B,Dong S J.Analyst,2001,126:1095 -1099.
[14]Gao Y S,Wang Y,Di J W.J.Appl.Chem.(高盐生,王媛,狄俊伟.应用化学),2010,27(3):363-366.
[15]Du Y,Luo X L,Xu J J,Chen H Y.Bioelectrochemistry,2007,70(2):342-347.
[16]Frens G.Nat.Phys.Sci.,1973,241:20 -22.

